2025年中考化学题型专题复习 题型六 科学探究题课件(25页ppt)
文档属性
| 名称 | 2025年中考化学题型专题复习 题型六 科学探究题课件(25页ppt) |  | |
| 格式 | pptx | ||
| 文件大小 | 996.2KB | ||
| 资源类型 | 试卷 | ||
| 版本资源 | 通用版 | ||
| 科目 | 化学 | ||
| 更新时间 | 2025-02-17 14:14:09 | ||
图片预览






文档简介
(共25张PPT)
七年级上册
题型六 科学探究题
2025年中考化学题型专题复习
类型1 酸碱盐综合反应后物质成分的探究
【典例1】
某化学兴趣小组进行了如下实验探究,请你参与。
如图1,向碳酸钠和硫酸钠的混合溶液中加入氢氧化钡溶液,充分反应后静置。
类型1 酸碱盐综合反应后物质成分的探究
【典例1】
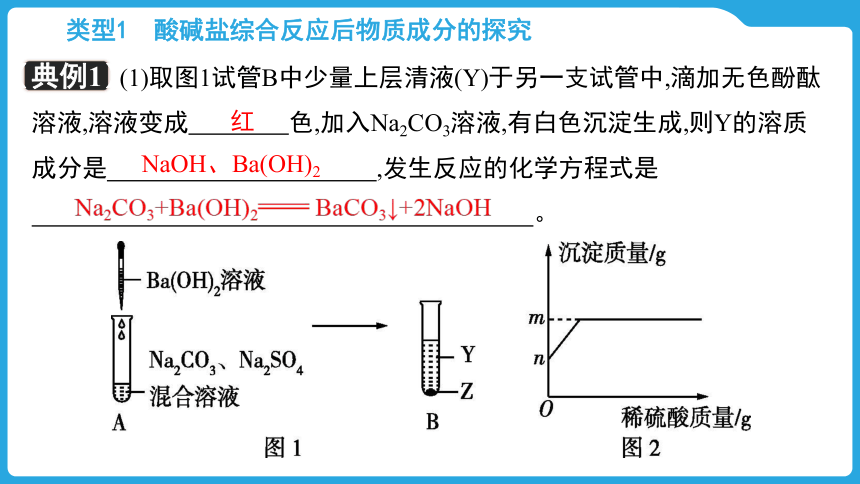
(1)取图1试管B中少量上层清液(Y)于另一支试管中,滴加无色酚酞溶液,溶液变成 色,加入Na2CO3溶液,有白色沉淀生成,则Y的溶质成分是 ,发生反应的化学方程式是
。
红
NaOH、Ba(OH)2
Na2CO3+Ba(OH)2 BaCO3↓+2NaOH
类型1 酸碱盐综合反应后物质成分的探究
【典例1】
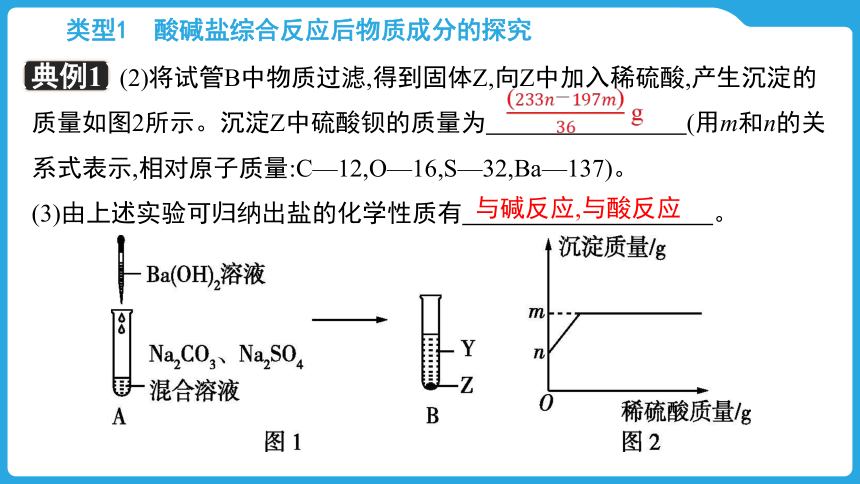
(2)将试管B中物质过滤,得到固体Z,向Z中加入稀硫酸,产生沉淀的质量如图2所示。沉淀Z中硫酸钡的质量为 (用m和n的关系式表示,相对原子质量:C—12,O—16,S—32,Ba—137)。
(3)由上述实验可归纳出盐的化学性质有 。
g
与碱反应,与酸反应
类型1 酸碱盐综合反应后物质成分的探究
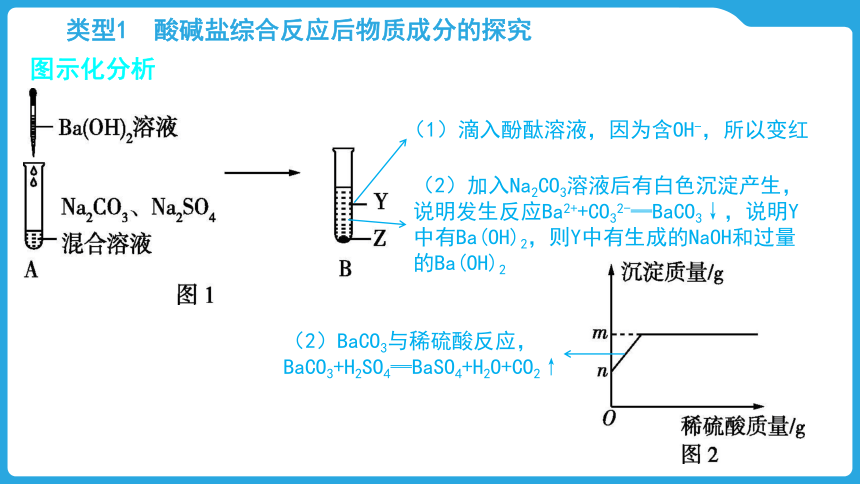
图示化分析
(1)滴入酚酞溶液,因为含OH-,所以变红
(2)加入Na2CO3溶液后有白色沉淀产生,说明发生反应Ba2++CO32-═BaCO3↓,说明Y中有Ba(OH)2,则Y中有生成的NaOH和过量的Ba(OH)2
(2)BaCO3与稀硫酸反应,BaCO3+H2SO4═BaSO4+H2O+CO2↑
类型1 酸碱盐综合反应后物质成分的探究
图示化分析
定量分析数据:
(m-n) g为BaCO3和H2SO4反应生成BaSO4的质量与BaCO3的质量差,设沉淀Z中BaCO3的质量为x:
BaCO3+H2SO4 BaSO4+H2O+CO2↑ Δm
197 233 36
x (m-n) g
x=
所以Z中BaSO4的质量=n g- g= g。
类型1 酸碱盐综合反应后物质成分的探究
(1)Y中一定含OH-,滴入酚酞溶液会变红。加入Na2CO3溶液,有白色沉淀生成,说明一定有Ba(OH)2溶液,则Y的溶质有NaOH、Ba(OH)2,涉及的化学方程式为Na2CO3+Ba(OH)2 BaCO3↓+2NaOH。
(2)沉淀Z的成分为BaCO3、BaSO4,向Z中加入稀硫酸,发生反应:BaCO3+H2SO4 BaSO4+H2O+CO2↑。n~m段的质量差即为生成的BaSO4的质量与Z中原有的BaCO3的质量差,设沉淀Z中BaCO3的质量为x,
类型1 酸碱盐综合反应后物质成分的探究
BaCO3~BaSO4 Δm
197 233 36
x (m-n) g
x=
则沉淀Z中BaSO4的质量为n g- g= g。
(3)结合题目可获取盐的化学性质:与碱反应,与酸反应。
类型2 溶解度与酸碱盐综合
【典例2】
我国化学家侯德榜发明的侯氏制碱法,开创了世界制碱工业的新纪元。制碱工艺中的关键反应为NaCl+CO2+NH3+H2O NaHCO3↓+NH4Cl。室温(20 ℃)下,某兴趣小组在实验室利用如图装置模拟该反应。
类型2 溶解度与酸碱盐综合
【典例2】
已知:①20 ℃时,几种盐的溶解度如下表;
②氨气极易溶于饱和食盐水,形成的溶液呈碱性。
(1)为配制饱和食盐水,应向100 g水中至少加入 g NaCl固体。
(2)仪器a的名称是 ,装置D的作用是 。
(3)装置A制取的CO2中会混有HCl,用饱和NaHCO3溶液吸收HCl的化学方程式为 。
36.0
试管
产生氨气
NaHCO3+HCl NaCl+H2O+CO2↑
物质 NaCl NaHCO3 NH4Cl
溶解度/g 36.0 9.6 37.2
类型2 溶解度与酸碱盐综合
(4)为使CO2在装置C中能充分吸收,可采取的措施是 。
充分反应后,装置C中有晶体析出。为分析晶体产生的原因,兴趣小组继续开展探究。
查阅资料:一定条件下,可溶性物质的溶解存在限度,当相应离子浓度过大时,可溶性物质会部分结晶析出。
(5)装置C中析出的晶体主要成分是NaHCO3而不是NH4Cl,原因是 。
向装置C中通入NH3后,再通入CO2(合理即可)
反应生成的NaHCO3质量较大,且在20 ℃时,NaHCO3溶解度较小
【典例2】
类型2 溶解度与酸碱盐综合
(6)装置C中的物质过滤后得到的滤液在工业上称为母液。侯氏制碱法通过向母液中加入食盐,使NH4Cl结晶析出,析出晶体的原因是 。
母液中含有大量N和少量Na+,加入NaCl,溶液中Cl-浓度增大,使NH4Cl结晶析出(合理即可)
【典例2】
类型2 溶解度与酸碱盐综合
思路分析
类型2 溶解度与酸碱盐综合
(1)根据20 ℃时几种盐的溶解度可知,20 ℃时NaCl的溶解度是36.0 g,所以为配制饱和食盐水,应向100 g水中至少加入36.0 g NaCl固体。
(4)由于氨气极易溶于饱和食盐水,形成的溶液呈碱性,碱性溶液能充分吸收二氧化碳,所以为使CO2在装置C中被充分吸收,可采取的措施是向装置C中通入NH3后,再通入CO2。
类型2 溶解度与酸碱盐综合
(5)装置C中发生的总反应的化学方程式及质量关系为:
NaCl+CO2+NH3+H2O NaHCO3↓+NH4Cl
84 53.5
反应生成的NaHCO3质量较大,且在20 ℃时,NaHCO3溶解度较小,所以装置C
中析出的晶体主要成分是NaHCO3而不是NH4Cl。
(6)一定条件下,可溶性物质的溶解存在限度,当相应离子浓度过大时,可溶性物质会部分结晶析出。母液中含有大量N和少量Na+,当加入NaCl,溶液中Cl-浓度增大,使氯化铵结晶析出。
类型3 物质变化相关的项目式探究
【典例3】
[2024湖南中考]2024年5月1日,我国利用船舶加装的碳捕捉系统回收的首罐液态二氧化碳卸船,标志着远洋航行船舶从燃油消耗到二氧化碳回收利用形成闭环。同学们对“二氧化碳回收利用形成闭环”非常感兴趣,开展有关二氧化碳的项目式学习。
任务一:调查空气中二氧化碳含量增加的原因
同学们调查到空气中二氧化碳含量增加的原因有很多,你认为有
(写一种即可)。
化石燃料的燃烧(或人和动植物的呼吸作用等,合理即可)
类型3 物质变化相关的项目式探究
【典例3】
任务二:讨论使空气中二氧化碳含量减少的方法
同学们讨论了使空气中二氧化碳含量减少的方法,知道低碳生活方式可以减少二氧化碳排放,你的一种低碳生活方式是 。
有同学想到二氧化碳能使澄清石灰水 (填实验现象),补充了可以利用碱溶液或水吸收二氧化碳。
任务三:探究实验室中不同试剂吸收二氧化碳的效果
实验室提供4种试剂:水、饱和石灰水、质量分数为0.165%的NaOH溶液、质量分数为40%的NaOH溶液。
节能出行(合理即可)
变浑浊
类型3 物质变化相关的项目式探究
【典例3】
【提出问题】上述4种试剂吸收二氧化碳的效果如何
【查阅资料】①室温下,饱和石灰水中氢氧化钙的质量分数约为0.165%;
②利用压强传感器及信息处理终端可将实验数据进行记录、呈现和分析。
【进行实验】
步骤1:各装置气密性良好(夹持装置已省略),同学们用4只250 mL烧瓶集满纯净的二氧化碳气体。
步骤2:用4支注射器分别取60 mL上述提供的4种试剂,将烧瓶分别连接压强传感器和注射器(如图1所示)。
类型3 物质变化相关的项目式探究
【典例3】
步骤3:待烧瓶内气压平稳后,迅速将4支注射器内试剂分别全部注入相对应的烧瓶中,关闭止水夹,观察压强变化。一段时间后,振荡烧瓶,继续观察压强变化。小组合作完成实验,并展示烧瓶内压强随时间变化的曲线图(如图2所示)。
类型3 物质变化相关的项目式探究
【典例3】
【分析讨论】根据40%NaOH溶液对应的曲线,分析t1~t3 s时间段曲线变化的原因是 。
【得出结论】结合图2数据,从压强和吸收效果两个角度对比分析,得到的结论是 。
t1~t2 s时间段NaOH溶液与CO2气体反应(吸收CO2),导致压强减小,t2 s时振荡烧瓶,反应速率加快,压强减小更快
同一种物质的溶液,浓度越大,吸收效果越好,压强减小越快(合理即可)
类型3 物质变化相关的项目式探究
【典例3】
任务四:形成二氧化碳闭环的意识
在老师指导下,知道上述实验中40%NaOH溶液吸收二氧化碳后,氢氧化钠有剩余。为了达到零碳排放和对环境无污染,形成二氧化碳
闭环的意识。现处理上述实验中40%NaOH溶液吸收二氧化碳后的液体,你设计的实验方案是 。 师生对其他烧瓶中的物质也进行了科学处理。
【拓展思维】我国已经实现了利用二氧化碳合成淀粉、甲醇和负碳纤维等,“二氧化碳回收利用形成闭环”是未来碳科学和技术发展的探索方向。
先向溶液中加入适量的氯化钙(或其他可溶性钙盐),使碳酸钠与钙离子反应生成碳酸钙沉淀,通过过滤将沉淀分离,然后向滤液中滴加适量稀盐酸,实现对碳酸钠与氢氧化钠的去除,从而不产生CO2排放
类型3 物质变化相关的项目式探究
思路分析
类型3 物质变化相关的项目式探究
思路分析
相同条件下,水的吸收能力最差
定量分析:相同条件下,等溶度等体积的氢氧化钠和氢氧化钙溶液吸收二氧化碳时,氢氧化钠溶液的吸收能力稍强
相同条件下,40%的NaOH溶液吸收二氧化碳能力最强
类型3 物质变化相关的项目式探究
思路分析
类型3 物质变化相关的项目式探究
任务三:
【分析讨论】二氧化碳能溶于水,能与氢氧化钠反应生成碳酸钠和水,导致气体减少,瓶内压强明显减小,振荡后反应更充分,压强减小程度更明显,因此t2~t3 s时间段压强明显减小。
【得出结论】分析图像信息可知,使用40%氢氧化钠溶液压强下降到最低,因此吸收二氧化碳效果最好。
任务四:氢氧化钠与二氧化碳反应生成碳酸钠和水,实验中剩余液体为氢氧化钠、碳酸钠的混合溶液,可先加入氯化钙溶液,与碳酸钠反应生成碳酸钙沉淀,过滤后再向滤液中加入稀盐酸,除去氢氧化钠,过程中可用酚酞溶液指示反应终点。
七年级上册
题型六 科学探究题
2025年中考化学题型专题复习
类型1 酸碱盐综合反应后物质成分的探究
【典例1】
某化学兴趣小组进行了如下实验探究,请你参与。
如图1,向碳酸钠和硫酸钠的混合溶液中加入氢氧化钡溶液,充分反应后静置。
类型1 酸碱盐综合反应后物质成分的探究
【典例1】
(1)取图1试管B中少量上层清液(Y)于另一支试管中,滴加无色酚酞溶液,溶液变成 色,加入Na2CO3溶液,有白色沉淀生成,则Y的溶质成分是 ,发生反应的化学方程式是
。
红
NaOH、Ba(OH)2
Na2CO3+Ba(OH)2 BaCO3↓+2NaOH
类型1 酸碱盐综合反应后物质成分的探究
【典例1】
(2)将试管B中物质过滤,得到固体Z,向Z中加入稀硫酸,产生沉淀的质量如图2所示。沉淀Z中硫酸钡的质量为 (用m和n的关系式表示,相对原子质量:C—12,O—16,S—32,Ba—137)。
(3)由上述实验可归纳出盐的化学性质有 。
g
与碱反应,与酸反应
类型1 酸碱盐综合反应后物质成分的探究
图示化分析
(1)滴入酚酞溶液,因为含OH-,所以变红
(2)加入Na2CO3溶液后有白色沉淀产生,说明发生反应Ba2++CO32-═BaCO3↓,说明Y中有Ba(OH)2,则Y中有生成的NaOH和过量的Ba(OH)2
(2)BaCO3与稀硫酸反应,BaCO3+H2SO4═BaSO4+H2O+CO2↑
类型1 酸碱盐综合反应后物质成分的探究
图示化分析
定量分析数据:
(m-n) g为BaCO3和H2SO4反应生成BaSO4的质量与BaCO3的质量差,设沉淀Z中BaCO3的质量为x:
BaCO3+H2SO4 BaSO4+H2O+CO2↑ Δm
197 233 36
x (m-n) g
x=
所以Z中BaSO4的质量=n g- g= g。
类型1 酸碱盐综合反应后物质成分的探究
(1)Y中一定含OH-,滴入酚酞溶液会变红。加入Na2CO3溶液,有白色沉淀生成,说明一定有Ba(OH)2溶液,则Y的溶质有NaOH、Ba(OH)2,涉及的化学方程式为Na2CO3+Ba(OH)2 BaCO3↓+2NaOH。
(2)沉淀Z的成分为BaCO3、BaSO4,向Z中加入稀硫酸,发生反应:BaCO3+H2SO4 BaSO4+H2O+CO2↑。n~m段的质量差即为生成的BaSO4的质量与Z中原有的BaCO3的质量差,设沉淀Z中BaCO3的质量为x,
类型1 酸碱盐综合反应后物质成分的探究
BaCO3~BaSO4 Δm
197 233 36
x (m-n) g
x=
则沉淀Z中BaSO4的质量为n g- g= g。
(3)结合题目可获取盐的化学性质:与碱反应,与酸反应。
类型2 溶解度与酸碱盐综合
【典例2】
我国化学家侯德榜发明的侯氏制碱法,开创了世界制碱工业的新纪元。制碱工艺中的关键反应为NaCl+CO2+NH3+H2O NaHCO3↓+NH4Cl。室温(20 ℃)下,某兴趣小组在实验室利用如图装置模拟该反应。
类型2 溶解度与酸碱盐综合
【典例2】
已知:①20 ℃时,几种盐的溶解度如下表;
②氨气极易溶于饱和食盐水,形成的溶液呈碱性。
(1)为配制饱和食盐水,应向100 g水中至少加入 g NaCl固体。
(2)仪器a的名称是 ,装置D的作用是 。
(3)装置A制取的CO2中会混有HCl,用饱和NaHCO3溶液吸收HCl的化学方程式为 。
36.0
试管
产生氨气
NaHCO3+HCl NaCl+H2O+CO2↑
物质 NaCl NaHCO3 NH4Cl
溶解度/g 36.0 9.6 37.2
类型2 溶解度与酸碱盐综合
(4)为使CO2在装置C中能充分吸收,可采取的措施是 。
充分反应后,装置C中有晶体析出。为分析晶体产生的原因,兴趣小组继续开展探究。
查阅资料:一定条件下,可溶性物质的溶解存在限度,当相应离子浓度过大时,可溶性物质会部分结晶析出。
(5)装置C中析出的晶体主要成分是NaHCO3而不是NH4Cl,原因是 。
向装置C中通入NH3后,再通入CO2(合理即可)
反应生成的NaHCO3质量较大,且在20 ℃时,NaHCO3溶解度较小
【典例2】
类型2 溶解度与酸碱盐综合
(6)装置C中的物质过滤后得到的滤液在工业上称为母液。侯氏制碱法通过向母液中加入食盐,使NH4Cl结晶析出,析出晶体的原因是 。
母液中含有大量N和少量Na+,加入NaCl,溶液中Cl-浓度增大,使NH4Cl结晶析出(合理即可)
【典例2】
类型2 溶解度与酸碱盐综合
思路分析
类型2 溶解度与酸碱盐综合
(1)根据20 ℃时几种盐的溶解度可知,20 ℃时NaCl的溶解度是36.0 g,所以为配制饱和食盐水,应向100 g水中至少加入36.0 g NaCl固体。
(4)由于氨气极易溶于饱和食盐水,形成的溶液呈碱性,碱性溶液能充分吸收二氧化碳,所以为使CO2在装置C中被充分吸收,可采取的措施是向装置C中通入NH3后,再通入CO2。
类型2 溶解度与酸碱盐综合
(5)装置C中发生的总反应的化学方程式及质量关系为:
NaCl+CO2+NH3+H2O NaHCO3↓+NH4Cl
84 53.5
反应生成的NaHCO3质量较大,且在20 ℃时,NaHCO3溶解度较小,所以装置C
中析出的晶体主要成分是NaHCO3而不是NH4Cl。
(6)一定条件下,可溶性物质的溶解存在限度,当相应离子浓度过大时,可溶性物质会部分结晶析出。母液中含有大量N和少量Na+,当加入NaCl,溶液中Cl-浓度增大,使氯化铵结晶析出。
类型3 物质变化相关的项目式探究
【典例3】
[2024湖南中考]2024年5月1日,我国利用船舶加装的碳捕捉系统回收的首罐液态二氧化碳卸船,标志着远洋航行船舶从燃油消耗到二氧化碳回收利用形成闭环。同学们对“二氧化碳回收利用形成闭环”非常感兴趣,开展有关二氧化碳的项目式学习。
任务一:调查空气中二氧化碳含量增加的原因
同学们调查到空气中二氧化碳含量增加的原因有很多,你认为有
(写一种即可)。
化石燃料的燃烧(或人和动植物的呼吸作用等,合理即可)
类型3 物质变化相关的项目式探究
【典例3】
任务二:讨论使空气中二氧化碳含量减少的方法
同学们讨论了使空气中二氧化碳含量减少的方法,知道低碳生活方式可以减少二氧化碳排放,你的一种低碳生活方式是 。
有同学想到二氧化碳能使澄清石灰水 (填实验现象),补充了可以利用碱溶液或水吸收二氧化碳。
任务三:探究实验室中不同试剂吸收二氧化碳的效果
实验室提供4种试剂:水、饱和石灰水、质量分数为0.165%的NaOH溶液、质量分数为40%的NaOH溶液。
节能出行(合理即可)
变浑浊
类型3 物质变化相关的项目式探究
【典例3】
【提出问题】上述4种试剂吸收二氧化碳的效果如何
【查阅资料】①室温下,饱和石灰水中氢氧化钙的质量分数约为0.165%;
②利用压强传感器及信息处理终端可将实验数据进行记录、呈现和分析。
【进行实验】
步骤1:各装置气密性良好(夹持装置已省略),同学们用4只250 mL烧瓶集满纯净的二氧化碳气体。
步骤2:用4支注射器分别取60 mL上述提供的4种试剂,将烧瓶分别连接压强传感器和注射器(如图1所示)。
类型3 物质变化相关的项目式探究
【典例3】
步骤3:待烧瓶内气压平稳后,迅速将4支注射器内试剂分别全部注入相对应的烧瓶中,关闭止水夹,观察压强变化。一段时间后,振荡烧瓶,继续观察压强变化。小组合作完成实验,并展示烧瓶内压强随时间变化的曲线图(如图2所示)。
类型3 物质变化相关的项目式探究
【典例3】
【分析讨论】根据40%NaOH溶液对应的曲线,分析t1~t3 s时间段曲线变化的原因是 。
【得出结论】结合图2数据,从压强和吸收效果两个角度对比分析,得到的结论是 。
t1~t2 s时间段NaOH溶液与CO2气体反应(吸收CO2),导致压强减小,t2 s时振荡烧瓶,反应速率加快,压强减小更快
同一种物质的溶液,浓度越大,吸收效果越好,压强减小越快(合理即可)
类型3 物质变化相关的项目式探究
【典例3】
任务四:形成二氧化碳闭环的意识
在老师指导下,知道上述实验中40%NaOH溶液吸收二氧化碳后,氢氧化钠有剩余。为了达到零碳排放和对环境无污染,形成二氧化碳
闭环的意识。现处理上述实验中40%NaOH溶液吸收二氧化碳后的液体,你设计的实验方案是 。 师生对其他烧瓶中的物质也进行了科学处理。
【拓展思维】我国已经实现了利用二氧化碳合成淀粉、甲醇和负碳纤维等,“二氧化碳回收利用形成闭环”是未来碳科学和技术发展的探索方向。
先向溶液中加入适量的氯化钙(或其他可溶性钙盐),使碳酸钠与钙离子反应生成碳酸钙沉淀,通过过滤将沉淀分离,然后向滤液中滴加适量稀盐酸,实现对碳酸钠与氢氧化钠的去除,从而不产生CO2排放
类型3 物质变化相关的项目式探究
思路分析
类型3 物质变化相关的项目式探究
思路分析
相同条件下,水的吸收能力最差
定量分析:相同条件下,等溶度等体积的氢氧化钠和氢氧化钙溶液吸收二氧化碳时,氢氧化钠溶液的吸收能力稍强
相同条件下,40%的NaOH溶液吸收二氧化碳能力最强
类型3 物质变化相关的项目式探究
思路分析
类型3 物质变化相关的项目式探究
任务三:
【分析讨论】二氧化碳能溶于水,能与氢氧化钠反应生成碳酸钠和水,导致气体减少,瓶内压强明显减小,振荡后反应更充分,压强减小程度更明显,因此t2~t3 s时间段压强明显减小。
【得出结论】分析图像信息可知,使用40%氢氧化钠溶液压强下降到最低,因此吸收二氧化碳效果最好。
任务四:氢氧化钠与二氧化碳反应生成碳酸钠和水,实验中剩余液体为氢氧化钠、碳酸钠的混合溶液,可先加入氯化钙溶液,与碳酸钠反应生成碳酸钙沉淀,过滤后再向滤液中加入稀盐酸,除去氢氧化钠,过程中可用酚酞溶液指示反应终点。
同课章节目录
