6.2 第2课时 金属活动性 置换反应课件(共16张PPT) 2024-2025学年初中化学科粤版九年下册
文档属性
| 名称 | 6.2 第2课时 金属活动性 置换反应课件(共16张PPT) 2024-2025学年初中化学科粤版九年下册 |

|
|
| 格式 | pptx | ||
| 文件大小 | 578.5KB | ||
| 资源类型 | 教案 | ||
| 版本资源 | 科粤版 | ||
| 科目 | 化学 | ||
| 更新时间 | 2024-12-19 00:00:00 | ||
图片预览





文档简介
(共16张PPT)
第六单元 金 属 和 金 属 材 料
6.2 第2课时 金属活动性 置换反应
新知导学
新知导入
运动会上小明夺得了百米赛跑的铜牌,他在化学实验室中经过一番加工,把自己的铜牌变成了“银牌”,小明是如何把运动会上获得的铜牌变成“银牌”的呢
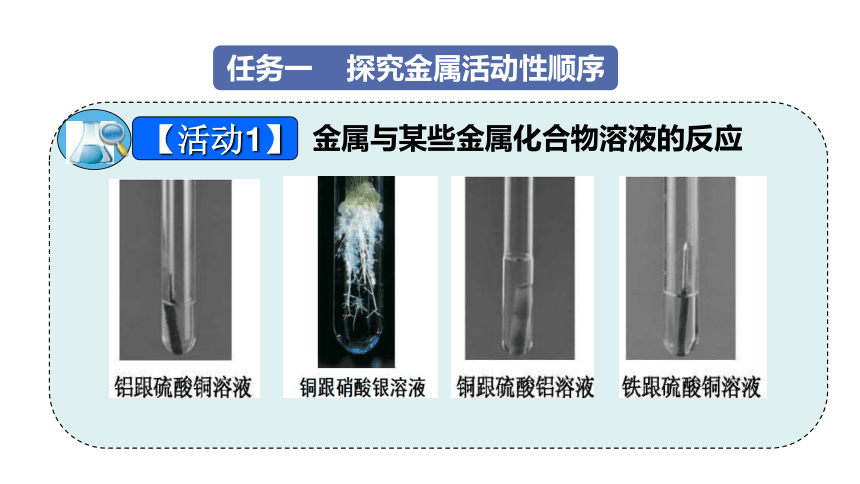
任务一 探究金属活动性顺序
金属与某些金属化合物溶液的反应
【活动1】
任务一 探究金属活动性顺序
金属与某些金属化合物溶液的反应
【活动1】
实验 现象 反应的化学方程式
铝丝浸入硫酸铜溶液中
铜丝浸入硝酸银溶液中
铜丝浸入硫酸铝溶液中
铁丝浸入硫酸铜溶液中
【归纳】
铝、铁能与硫酸铜溶液反应,说明铝、铁比铜活泼;
金属与某些金属化合物溶液的反应
任务一 探究金属活动性顺序
铜能与硝酸银溶液反应,不能与硫酸铝溶液反应,说明铜比银活泼,不如铝活泼。
得出金属活动性顺序是铝、铁>铜>银。
【归纳】
任务一 探究金属活动性顺序
金属活动性顺序
任务二 思考金属活动性顺序的作用
【活动2】
金属活动性顺序的应用
金属活动性顺序在工农业生产和科学研究中有重要作用,有以下判断依据:
1.在金属活动性顺序里,金属的位置越靠前,它的活动性就越强。
2.在金属活动性顺序里,位于氢前面的金属能置换出稀盐酸、稀硫酸一类稀酸中的氢。
3.在金属活动性顺序里,排在前面活动性较强的金属能把排在后面活动性较弱的金属从其化合物溶液中置换出来。
任务三 利用金属活动性进行判断
【活动3】
判断置换反应能否发生
课堂练习:下列物质能否发生反应 写出能发生反应的化学方程式,并判断它们是不是置换反应。
(1)银与稀盐酸
(2)锌与硫酸铜溶液
(3)铜与硫酸锌溶液
(4)铝与硝酸银溶液
任务四 利用金属活动性设计实验
【活动4】
分组设计实验,试剂自选
设计实验探究铁和铜的活动性顺序
思考:
任务四 利用金属活动性设计实验
【活动5】
分组设计实验,试剂自选
设计实验探究锌、铁和铜的活动性顺序
思考:
【归纳】
两种金属可利用金属和另一金属化合物溶液能否反应,比较两者的活动性顺序;
三种金属的活动性顺序常利用“中间原则”:两金夹一液,或两液夹一金。
任务四 利用金属活动性设计实验
课堂小结
课堂小结
课堂小结
课堂练习
1.若金属锰(Mn在金属化合物中显+2价)在金属活动性顺序中位于铝和锌之间,则下列反应不正确的是 ( )
A.Mn+H2SO4 ==MnSO4+H2↑
B.Mg+MnSO4 ==MgSO4+Mn
C.Fe+MnSO4 ==FeSO4+Mn
D.Mn+CuSO4 ==MnSO4+Cu
C
课堂小结
课堂练习
2.有A、B、C、D四种金属,分别把它们加入稀盐酸中,A、B、D表面有气体放出,C无明显现象,再把A、D加入B的化合物溶液中,D表面有B析出,而A没有,则四种金属的活动性顺序为 ( )
A.A>B>D>C B.B>D>A>C
C.D>A>B>C D.D>B>A>C
D
课堂小结
课堂练习
3.判断下列物质能否发生反应,若能,写出相关化学方程式。
(1)银与稀硫酸
(2)锌与氯化铜溶液
(3)银与氯化铜溶液
(4)镁与硫酸亚铁溶液
不能
不能
Zn+CuCl2==ZnCl2+Cu
Mg+FeSO4==MgSO4+Fe
谢 谢 观 看
第六单元 金 属 和 金 属 材 料
6.2 第2课时 金属活动性 置换反应
新知导学
新知导入
运动会上小明夺得了百米赛跑的铜牌,他在化学实验室中经过一番加工,把自己的铜牌变成了“银牌”,小明是如何把运动会上获得的铜牌变成“银牌”的呢
任务一 探究金属活动性顺序
金属与某些金属化合物溶液的反应
【活动1】
任务一 探究金属活动性顺序
金属与某些金属化合物溶液的反应
【活动1】
实验 现象 反应的化学方程式
铝丝浸入硫酸铜溶液中
铜丝浸入硝酸银溶液中
铜丝浸入硫酸铝溶液中
铁丝浸入硫酸铜溶液中
【归纳】
铝、铁能与硫酸铜溶液反应,说明铝、铁比铜活泼;
金属与某些金属化合物溶液的反应
任务一 探究金属活动性顺序
铜能与硝酸银溶液反应,不能与硫酸铝溶液反应,说明铜比银活泼,不如铝活泼。
得出金属活动性顺序是铝、铁>铜>银。
【归纳】
任务一 探究金属活动性顺序
金属活动性顺序
任务二 思考金属活动性顺序的作用
【活动2】
金属活动性顺序的应用
金属活动性顺序在工农业生产和科学研究中有重要作用,有以下判断依据:
1.在金属活动性顺序里,金属的位置越靠前,它的活动性就越强。
2.在金属活动性顺序里,位于氢前面的金属能置换出稀盐酸、稀硫酸一类稀酸中的氢。
3.在金属活动性顺序里,排在前面活动性较强的金属能把排在后面活动性较弱的金属从其化合物溶液中置换出来。
任务三 利用金属活动性进行判断
【活动3】
判断置换反应能否发生
课堂练习:下列物质能否发生反应 写出能发生反应的化学方程式,并判断它们是不是置换反应。
(1)银与稀盐酸
(2)锌与硫酸铜溶液
(3)铜与硫酸锌溶液
(4)铝与硝酸银溶液
任务四 利用金属活动性设计实验
【活动4】
分组设计实验,试剂自选
设计实验探究铁和铜的活动性顺序
思考:
任务四 利用金属活动性设计实验
【活动5】
分组设计实验,试剂自选
设计实验探究锌、铁和铜的活动性顺序
思考:
【归纳】
两种金属可利用金属和另一金属化合物溶液能否反应,比较两者的活动性顺序;
三种金属的活动性顺序常利用“中间原则”:两金夹一液,或两液夹一金。
任务四 利用金属活动性设计实验
课堂小结
课堂小结
课堂小结
课堂练习
1.若金属锰(Mn在金属化合物中显+2价)在金属活动性顺序中位于铝和锌之间,则下列反应不正确的是 ( )
A.Mn+H2SO4 ==MnSO4+H2↑
B.Mg+MnSO4 ==MgSO4+Mn
C.Fe+MnSO4 ==FeSO4+Mn
D.Mn+CuSO4 ==MnSO4+Cu
C
课堂小结
课堂练习
2.有A、B、C、D四种金属,分别把它们加入稀盐酸中,A、B、D表面有气体放出,C无明显现象,再把A、D加入B的化合物溶液中,D表面有B析出,而A没有,则四种金属的活动性顺序为 ( )
A.A>B>D>C B.B>D>A>C
C.D>A>B>C D.D>B>A>C
D
课堂小结
课堂练习
3.判断下列物质能否发生反应,若能,写出相关化学方程式。
(1)银与稀硫酸
(2)锌与氯化铜溶液
(3)银与氯化铜溶液
(4)镁与硫酸亚铁溶液
不能
不能
Zn+CuCl2==ZnCl2+Cu
Mg+FeSO4==MgSO4+Fe
谢 谢 观 看
