3.3 第3课时 依据化学式的计算 课件(共14张PPT) 2024-2025学年化学沪教版九年级上册
文档属性
| 名称 | 3.3 第3课时 依据化学式的计算 课件(共14张PPT) 2024-2025学年化学沪教版九年级上册 |

|
|
| 格式 | pptx | ||
| 文件大小 | 423.0KB | ||
| 资源类型 | 教案 | ||
| 版本资源 | 沪教版 | ||
| 科目 | 化学 | ||
| 更新时间 | 2024-12-20 00:00:00 | ||
图片预览






文档简介
(共14张PPT)
第3章 物质构成的奥秘
第3节 第3课时 依据化学式的计算
我们已经知道,化合物的化学式不仅表示组成物质的各种元素,而且清楚地显示出其中所含元素的原子数之比。那么,化学式能否告诉我们有关组成元素之间的质量关系的信息呢?
农业技术人员在研究氮肥的肥效时,首先必须知道所施氮肥的含氮量;化工生产中某些产品质量的分析,也要设法测出其中某种元素的含量。在这些实践活动中,人们常常根据物质的化学式来确定组成物质的元素之间的质量关系。
新知导学
观察思考
计算水中氢、氧两种元素的质量比。
1.查出H、O元素的相对原子质量:H为1,O为16
2.明确H2O中原子的个数比:氢原子数:氧原子数=2:1
3.计算H、O元素的质量比:
(1×2):16=1:8
参照左边的例子,计算CO2中碳、氧元素的质量比。
计算CO2中碳、氧两种元素的质量比。
1._________________________
__________________________;
2. ________________________
__________________________;
3. ________________________
_____________________ 。
C、O元素的相对原子质量:
C为12,O为16
CO2中原子的个数比:
碳原子数:氧原子数=1:2
C、O元素的质量比:
12:(16×2)=3:8
新知导学
1.二氧化硫中各元素的质量比。
2.氢氧化钙中各元素间的质量比。
3.碳酸氢铵中各元素间的质量比。
4.碱式碳酸铜中各元素间的质量比。
计算下列物质中各元素的质量比。
SO2中S、O元素的质量比:32:(16×2)=1:1
Ca(OH)2中Ca、O、H元素的质量比:40:(16×2):(1×2)=20:16:1
NH4HCO3中N、H、C、O元素的质量比:14:(1×5):12:(16×3)=14:5:12:48
Cu2(OH)2CO3中Cu、O、H、C元素的质量比:(64×2):(16×5):(1×2):12=64:40:1:6
新知导学
交流讨论
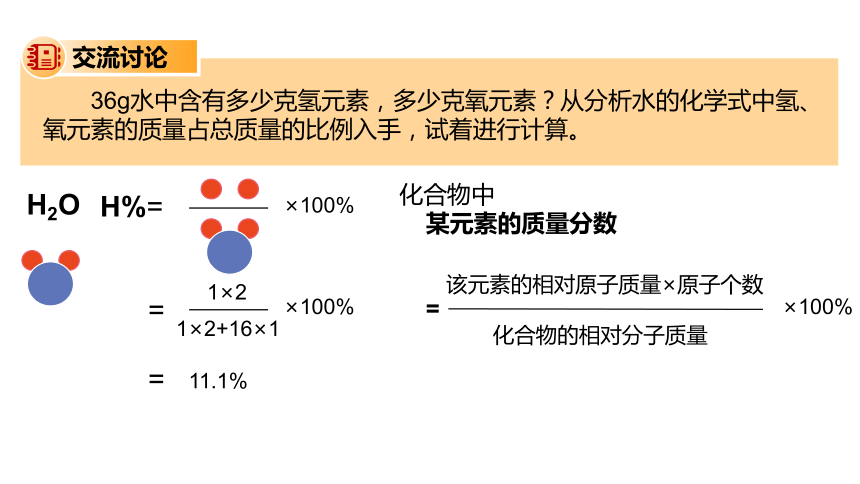
36g水中含有多少克氢元素,多少克氧元素?从分析水的化学式中氢、氧元素的质量占总质量的比例入手,试着进行计算。
H2O
H%=
=
=
×100%
×100%
1×2
1×2+16×1
11.1%
化合物中
某元素的质量分数
=
该元素的相对原子质量×原子个数
化合物的相对分子质量
×100%
新知导学
1.计算碳酸氢铵中氮元素的质量分数。
2.计算(NH4)2SO4 中氮元素的质量分数。
根据化学式求下列物质中某种元素的质量分数。
新知导学
计算36g水中氢元素的质量。
1.计算水中氢元素的质量分数:H%=11.1%
2.计算36g水中氢元素的质量:m(H)=36g×11.1%=4g
参照左边的例子,计算36g水中氧元素的质量。
计算36g水中氧元素的质量。
1. _________________________
__________________________;
2.__________________________
__________________________。
水中氧元素的质量分数:O%=89%
36g水中氧元素的质量:
m(O)=36g×89%=32g
新知导学
1.计算152克硫酸亚铁中含铁元素多少克?
2.多少克硫酸亚铁中含有 28g 铁元素?
3.多少克碳酸氢铵的含氮量与16g硝酸铵的含氮量相等?
4.多少克高锰酸钾中含有的氧元素与34g过氧化氢中含的氧元素质量相等?
根据化学式求物质中某元素的质量
解:尿素中氮元素的质量分数为 ×100%≈46.7%。
43.5%<46.7%,说明含有杂质,属于混合物
新知导学
尿素是一种肥效高、土壤适应性好的常用氮肥,其化学式为CO(NH2)2。现有一尿素样品,测得其中氮元素的质量分数为43.5%,试通过计算说明该尿素样品是纯净物还是混合物。
14×2
12+16+14×2+1×4
有关化学式的计算
一、计算组成物质的各元素的原子个数比
二、计算化合物中各元素的质量比
三、计算化合物中某元素的质量分数
某元素的质量分数=
课堂小结
该原子的相对原子质量(Ar)×原子个数
化合物的相对分子质量(Mr)
×100%
课堂巩固
1.蓝莓中含有丰富的花青素(C15H11O6)。下列有关叙述中错误的是( )
A.花青素的相对分子质量为287
B.花青素中碳、氢、氧三种原子的个数比为15:11:6
C.花青素中氧元素的质量分数最小
D.57.4g花青素中含有36g碳元素
C
课堂巩固
2.α-丙氨酸是组成人体蛋白质的氨基酸之一,其化学式为C3H7NO2。
(1)α-丙氨酸的相对分子质量为 。
(2)α-丙氨酸中,碳、氧元素的质量比为 。
(3)α-丙氨酸中氮元素的质量分数为 (精确到0.1%)。
(4)89gα-丙氨酸中氮元素质量为 g。
89
9:8
15.7%
14
课堂巩固
3.如图是某品牌鲜牛奶包装袋上的产品说明(部分)。
(1)该袋装鲜牛奶属于 (填“纯净物”或“混合物”)。
(2)这一袋牛奶至少含钙 g(精确到0.01g)。
(3)该牛奶中钙元素的质量分数至少为 。
混合物
0.53
0.106%
谢 谢 观 看
第3章 物质构成的奥秘
第3节 第3课时 依据化学式的计算
我们已经知道,化合物的化学式不仅表示组成物质的各种元素,而且清楚地显示出其中所含元素的原子数之比。那么,化学式能否告诉我们有关组成元素之间的质量关系的信息呢?
农业技术人员在研究氮肥的肥效时,首先必须知道所施氮肥的含氮量;化工生产中某些产品质量的分析,也要设法测出其中某种元素的含量。在这些实践活动中,人们常常根据物质的化学式来确定组成物质的元素之间的质量关系。
新知导学
观察思考
计算水中氢、氧两种元素的质量比。
1.查出H、O元素的相对原子质量:H为1,O为16
2.明确H2O中原子的个数比:氢原子数:氧原子数=2:1
3.计算H、O元素的质量比:
(1×2):16=1:8
参照左边的例子,计算CO2中碳、氧元素的质量比。
计算CO2中碳、氧两种元素的质量比。
1._________________________
__________________________;
2. ________________________
__________________________;
3. ________________________
_____________________ 。
C、O元素的相对原子质量:
C为12,O为16
CO2中原子的个数比:
碳原子数:氧原子数=1:2
C、O元素的质量比:
12:(16×2)=3:8
新知导学
1.二氧化硫中各元素的质量比。
2.氢氧化钙中各元素间的质量比。
3.碳酸氢铵中各元素间的质量比。
4.碱式碳酸铜中各元素间的质量比。
计算下列物质中各元素的质量比。
SO2中S、O元素的质量比:32:(16×2)=1:1
Ca(OH)2中Ca、O、H元素的质量比:40:(16×2):(1×2)=20:16:1
NH4HCO3中N、H、C、O元素的质量比:14:(1×5):12:(16×3)=14:5:12:48
Cu2(OH)2CO3中Cu、O、H、C元素的质量比:(64×2):(16×5):(1×2):12=64:40:1:6
新知导学
交流讨论
36g水中含有多少克氢元素,多少克氧元素?从分析水的化学式中氢、氧元素的质量占总质量的比例入手,试着进行计算。
H2O
H%=
=
=
×100%
×100%
1×2
1×2+16×1
11.1%
化合物中
某元素的质量分数
=
该元素的相对原子质量×原子个数
化合物的相对分子质量
×100%
新知导学
1.计算碳酸氢铵中氮元素的质量分数。
2.计算(NH4)2SO4 中氮元素的质量分数。
根据化学式求下列物质中某种元素的质量分数。
新知导学
计算36g水中氢元素的质量。
1.计算水中氢元素的质量分数:H%=11.1%
2.计算36g水中氢元素的质量:m(H)=36g×11.1%=4g
参照左边的例子,计算36g水中氧元素的质量。
计算36g水中氧元素的质量。
1. _________________________
__________________________;
2.__________________________
__________________________。
水中氧元素的质量分数:O%=89%
36g水中氧元素的质量:
m(O)=36g×89%=32g
新知导学
1.计算152克硫酸亚铁中含铁元素多少克?
2.多少克硫酸亚铁中含有 28g 铁元素?
3.多少克碳酸氢铵的含氮量与16g硝酸铵的含氮量相等?
4.多少克高锰酸钾中含有的氧元素与34g过氧化氢中含的氧元素质量相等?
根据化学式求物质中某元素的质量
解:尿素中氮元素的质量分数为 ×100%≈46.7%。
43.5%<46.7%,说明含有杂质,属于混合物
新知导学
尿素是一种肥效高、土壤适应性好的常用氮肥,其化学式为CO(NH2)2。现有一尿素样品,测得其中氮元素的质量分数为43.5%,试通过计算说明该尿素样品是纯净物还是混合物。
14×2
12+16+14×2+1×4
有关化学式的计算
一、计算组成物质的各元素的原子个数比
二、计算化合物中各元素的质量比
三、计算化合物中某元素的质量分数
某元素的质量分数=
课堂小结
该原子的相对原子质量(Ar)×原子个数
化合物的相对分子质量(Mr)
×100%
课堂巩固
1.蓝莓中含有丰富的花青素(C15H11O6)。下列有关叙述中错误的是( )
A.花青素的相对分子质量为287
B.花青素中碳、氢、氧三种原子的个数比为15:11:6
C.花青素中氧元素的质量分数最小
D.57.4g花青素中含有36g碳元素
C
课堂巩固
2.α-丙氨酸是组成人体蛋白质的氨基酸之一,其化学式为C3H7NO2。
(1)α-丙氨酸的相对分子质量为 。
(2)α-丙氨酸中,碳、氧元素的质量比为 。
(3)α-丙氨酸中氮元素的质量分数为 (精确到0.1%)。
(4)89gα-丙氨酸中氮元素质量为 g。
89
9:8
15.7%
14
课堂巩固
3.如图是某品牌鲜牛奶包装袋上的产品说明(部分)。
(1)该袋装鲜牛奶属于 (填“纯净物”或“混合物”)。
(2)这一袋牛奶至少含钙 g(精确到0.01g)。
(3)该牛奶中钙元素的质量分数至少为 。
混合物
0.53
0.106%
谢 谢 观 看
同课章节目录
