湖南省2014年学业水平考试试卷讲评及分析
文档属性
| 名称 | 湖南省2014年学业水平考试试卷讲评及分析 |  | |
| 格式 | zip | ||
| 文件大小 | 223.7KB | ||
| 资源类型 | 教案 | ||
| 版本资源 | 人教版(新课程标准) | ||
| 科目 | 化学 | ||
| 更新时间 | 2016-04-08 07:04:17 | ||
图片预览



文档简介
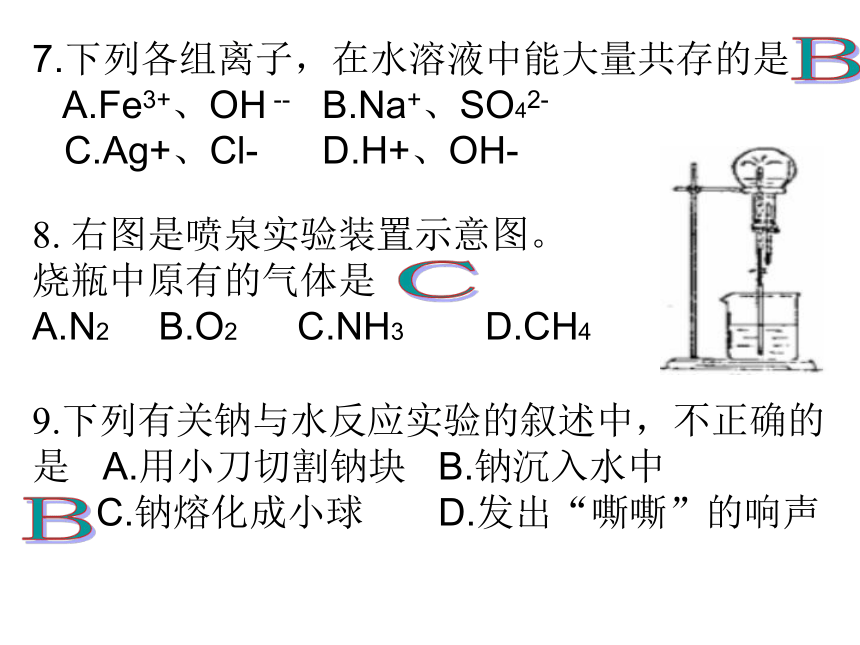
课件26张PPT。第二次学考成绩分析一、选择题参考答案(共22题,44分)此卷为2014年湖南省学考真题1.以下是一些常用的危险品标志,在烟花爆竹包装箱上应贴上 :2.当光束通过下列分散系时,能产生丁达尔效应的是 : A.CuSO4溶液 B.Na2CO3溶液
C.Fe(OH)3胶体 D.Ba(OH)2溶液 3.下列化合物中,属于盐的是 :
A.H2O B.H2SO4 C.KOH D.KNO3DCD4.下列气体中,可用向下排空气法收集的是
A.Cl2 B.SO2 C.CO2 D.H2DAA7.下列各组离子,在水溶液中能大量共存的是
A.Fe3+、OH -- B.Na+、SO42-
C.Ag+、Cl- D.H+、OH-9.下列有关钠与水反应实验的叙述中,不正确的是 A.用小刀切割钠块 B.钠沉入水中
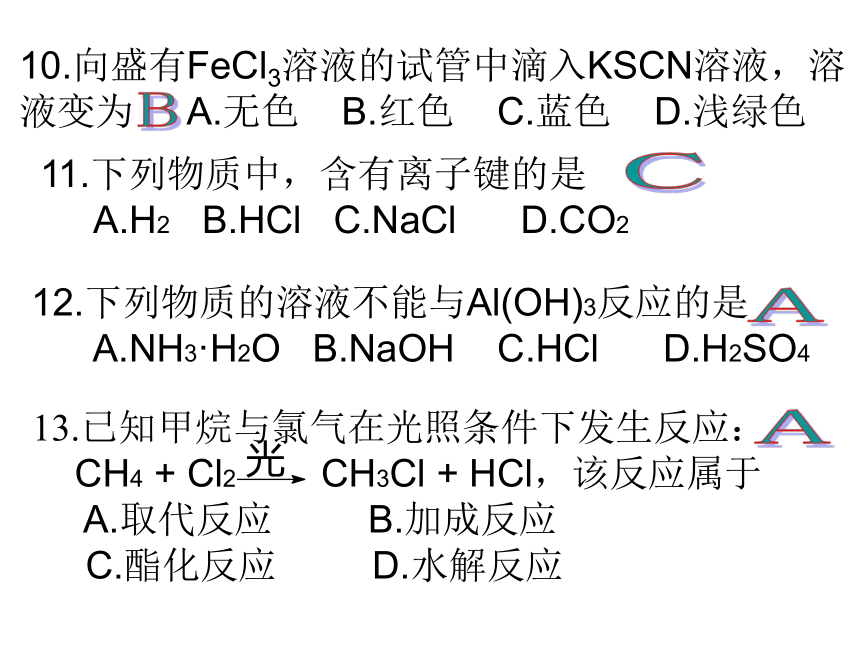
C.钠熔化成小球 D.发出“嘶嘶”的响声CBB11.下列物质中,含有离子键的是
A.H2 B.HCl C.NaCl D.CO212.下列物质的溶液不能与Al(OH)3反应的是
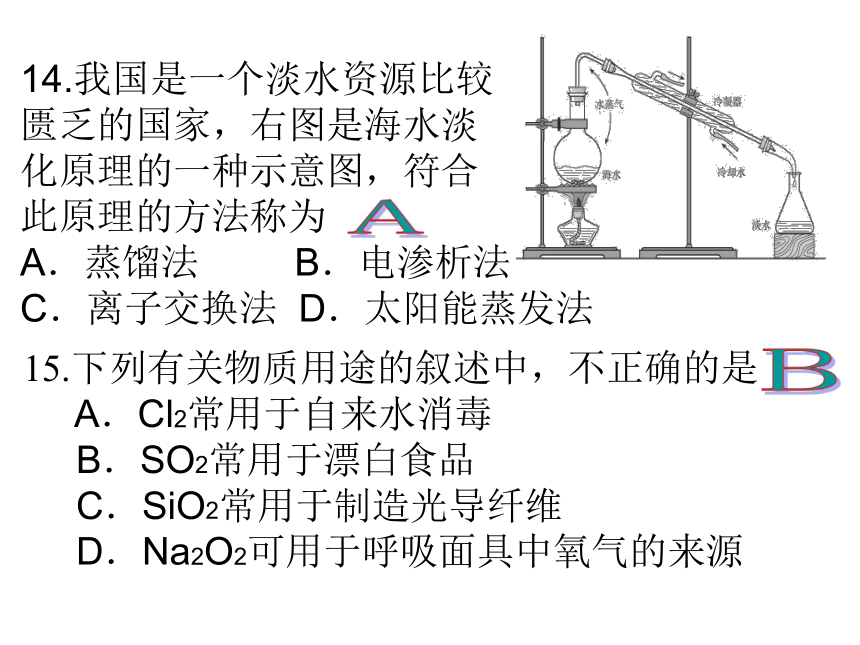
A.NH3·H2O B.NaOH C.HCl D.H2SO4 10.向盛有FeCl3溶液的试管中滴入KSCN溶液,溶液变为 A.无色 B.红色 C.蓝色 D.浅绿色CBAA15.下列有关物质用途的叙述中,不正确的是
A.Cl2常用于自来水消毒
B.SO2常用于漂白食品
C.SiO2常用于制造光导纤维
D.Na2O2可用于呼吸面具中氧气的来源BA18.下列有关1molH2的说法中,不正确的是(NA表示阿伏加德罗常数)A.质量为2g B.含氢原子数为NA
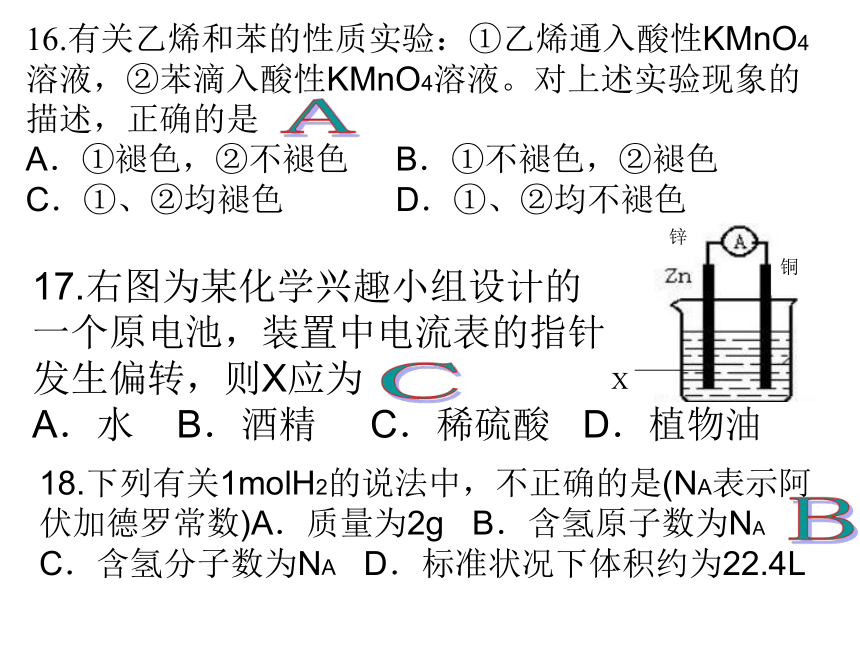
C.含氢分子数为NA D.标准状况下体积约为22.4L16.有关乙烯和苯的性质实验:①乙烯通入酸性KMnO4溶液,②苯滴入酸性KMnO4溶液。对上述实验现象的描述,正确的是
A.①褪色,②不褪色 B.①不褪色,②褪色
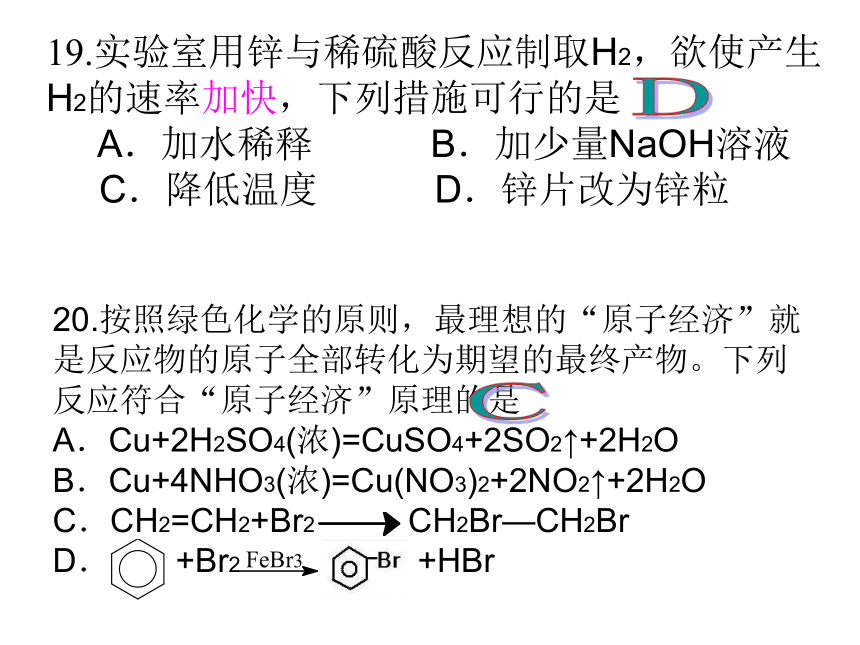
C.①、②均褪色 D.①、②均不褪色CBA 19.实验室用锌与稀硫酸反应制取H2,欲使产生H2的速率加快,下列措施可行的是
A.加水稀释 B.加少量NaOH溶液
C.降低温度 D.锌片改为锌粒DC21.将一小段镁带投入到盛有稀盐酸的试管中,发生剧烈反应。一段时间后,用手触摸试管外壁感觉烫手。这个实验事实说明该反应
A.为放热反应 B.为吸热反应
C.过程中热能转化为化学能
D.反应物的总能量低于生成物的总能量 DA二、填空题(本题包括4小题,每空2分,共26分) 23.(6分)钠、铝和铁是中学化学常见的三种重要金属。请回答下列问题:
(1)钠在空气中燃烧生成淡黄色的 (填“Na2O”或“Na2O2”);
(2)Al2O3能溶于酸或强碱溶液生成盐和水,则是一种 (填“酸性”、“碱性”或“两性”)氧化物;
(3)Fe(OH)3不溶于水,但能溶于酸,请写出Fe(OH)3与盐酸反应的化学方程式:
。Na2O2两性Fe(OH)3+3HCl=FeCl3 + 3H2O 24.(6分)氮、硫的化合物与人类生活和生产有着密切的联系。请回答下列问题:
(1)在空气质量报告的各项指标中,有SO2和NO2的指数,SO2是一种无色有毒气体,NO2是一种 (填“无色”或“红棕色”) 有毒气体;
(2)氨气极易溶于水,其水溶液显 (填“酸”、“碱”或“中”)性;
(3) 加热时,浓硫酸可与碳发生反应:C+2H2SO4(浓)=CO2↑+2SO2↑+2H2O。在该反应中,浓H2SO4表现出 (填“吸水”、“脱水”或“氧化”)性。 红棕色碱氧化性25.(6分)乙醇和乙酸是生活中两种常见的有机物。请回答下列问题:
(1)乙醇的结构简式为CH3CH2OH,乙醇分子含有的官能团为 ;
(2)生活中常用食醋除去暖瓶内的水垢(主要成分是CaCO3),反应的化学方程式为2CH3COOH+CaCO3=(CH3COO)2Ca+CO2↑+H2O。通过这个事实,你得出醋酸与碳酸的酸性强弱关系是:醋酸 碳酸(填“>”或“<”);
(3)在浓硫酸的催化作用下,加热乙酸和乙醇的混合溶液,可发生酯化反应。请完成化学方程式:CH3COOH +CH3CH2OH
CH3COO CH2CH3+ 。>羟基H2O26. (8分)下表是元素周期表的一部分,除标出的元素外,表中的每个编号代表一种元素,请根据要求回答问题:
N②<⑥③>⑤Mg+2H+ ==Mg2+ + H2↑三、实验题(本题包括1小题,每空2分,共10分)容量瓶27.(10分)实验室需配置100mL2.00mol/LNaCl溶液,请你参与实验过程,并完成相关实验报告(填写表格中横线上数字序号所示内容)。 实验步骤
(1)计算:溶质NaCl固体的质量为 ② g。
(2)称量:用托盘天平称取所需NaCl固体。
(3)溶解:将称好的NaCl固体放入烧杯中,用适量蒸馏水溶解。
(4)转移、洗涤:将烧杯中的溶液注入仪器①中,并用少量蒸馏水洗涤烧杯内壁2~3次,洗涤液也都注入仪器①中。
(5) ③ :将蒸馏水注入仪器至液面离刻度线1~2cm时,改用胶头滴管滴加蒸馏水至液面与刻度线相切。
(6)摇匀:盖好瓶塞 ,反复上下颠倒,然后静置。117定容思考与探究
(1)实验步骤(3)、(4)中都要用到玻璃棒,其作用分别是搅拌、 。
(2)某同学在实验步骤(6)后,发现凹液面低于刻度线,于是再向容器中滴加蒸馏水至刻度线,该同学所配置溶液是浓度 ⑤ (填“>”、“=”或“<”)2.00mol/L。引流<第二部分 选做题(20分)28.本题为《化学与生活(选修1)》选做题,每空2分,共20分。请根据题意,选择恰当的选项用字母代号填空。
(1)均衡营养和正确使用药物是保证身心健康的重要
方面,现有下列四种物质:
A.葡萄糖 B.氨基酸
C.麻黄碱 D.阿司匹林
①蛋白质水解的最终产物是 ;
②人体内最重要的供能物质是 ;
③具有解热镇痛作用,用于治疗感冒的是 ;
④对支气管哮喘症有明显疗效的是 。CBAD(2)材料是人类赖以生存和发展的重要物质基础。
①试管、烧杯和烧瓶等化学仪器的主要材质
是 ;A.玻璃 B.陶瓷
②钢铁是目前用量最大的铁合金。钢铁接触海水发
生电化学腐蚀,其负极反应式为 ;
A.O2+2H2O + 4e- = 4OH-
B.Fe - 2e-= Fe2+
因此,为防止轮船船体被腐蚀,可在船体上安装一定量的 。A.锌块 B.铜块AAB⑶当前,环境治理已成为重要的民生工程。
①2014年1月,教育部规定在学校公共场所禁止吸烟。下列有关说法中,不正确的是 ;
A.吸烟会对室内和公共场所造成污染
B.吸入焦油、尼古丁及颗粒物可导致多种病变
C.N2、CO2、CO和尼古丁都属于室内空气污染物C ②下列做法可能会加重“雾霾”的是 ;
A.大量焚烧秸秆
B.在汽车尾气系统装置催化转化器
C.发展煤的气化和液化等洁净煤技术
③下列处理垃圾的方法中,不正确的是 。
A.回收利用废纸 B.回收利用易拉罐 C.填埋废旧电池 CA29.本题为《化学反应原理(选修4)》选做题,每空2分,共20分。⑴合成氨是人类科技发展史上的一项重大突破。已知:25℃时,合成氨反应的热化学为:N2(g)+3H2(g) 2NH3(g) ΔH=-92.4kJ/mol
请回答下列问题:
①其他条件不变时,升高温度,化学反应速率 (填“增大”或“减小”);
②25℃时,取1mol N2和3mol H2置于2L的密闭容器中,在催化剂存在下进行反应,达到平衡时放出的热量 ,
A.大于92.4 kJ B.等于92.4 kJ C.小于92.4 kJ 增大C③一定条件下,上述反应达到化学平衡状态的标志是 ;
A.N2、H2、NH3的浓度相等;
B.容器内压强不再变化;
C.单位时间内消耗amol N2,同时生成2amol
NH3;
④25℃时,上述反应平衡常数的表达式为:
K= 。 B(2)右图是电解NaCl溶液的 示意图。请回答下列问题: ①石墨电极上的反应式 为 ; ②电解一段时间后,溶液的 PH (填“增大”、 “减小”或“不变”)。增大2Cl-- -- 2e-- ==Cl2↑(3)水溶液中的离子平衡是化学反应原理的重要内容。请回答下列问题:
①常温下,0.1mol/LCH3COONa溶液呈 (填“酸”、“碱”或“中”)性,
溶液中c(Na+) c(CH3COO-)(填“>”、“<”或“=”);碱>②常温下,在浓度均为0.1mol/L的盐酸和NH4Cl溶液中,水的电离程度大小关系是:0.1mol/L盐酸 0.1mol/LNH4Cl溶液(填“>”、“<”或“=”);
③已知:20℃时,Ksp(AgCl)=1.1×10-10,Ksp(AgBr)=2.0×10-13。将AgCl和AgBr的饱和溶液等体积混合,再逐滴加入足量浓AgNO3溶液,充分反应后,生成沉淀量的关系是:m(AgCl) m(AgBr)(填“>”、“<”或“=”)。<
C.Fe(OH)3胶体 D.Ba(OH)2溶液 3.下列化合物中,属于盐的是 :
A.H2O B.H2SO4 C.KOH D.KNO3DCD4.下列气体中,可用向下排空气法收集的是
A.Cl2 B.SO2 C.CO2 D.H2DAA7.下列各组离子,在水溶液中能大量共存的是
A.Fe3+、OH -- B.Na+、SO42-
C.Ag+、Cl- D.H+、OH-9.下列有关钠与水反应实验的叙述中,不正确的是 A.用小刀切割钠块 B.钠沉入水中
C.钠熔化成小球 D.发出“嘶嘶”的响声CBB11.下列物质中,含有离子键的是
A.H2 B.HCl C.NaCl D.CO212.下列物质的溶液不能与Al(OH)3反应的是
A.NH3·H2O B.NaOH C.HCl D.H2SO4 10.向盛有FeCl3溶液的试管中滴入KSCN溶液,溶液变为 A.无色 B.红色 C.蓝色 D.浅绿色CBAA15.下列有关物质用途的叙述中,不正确的是
A.Cl2常用于自来水消毒
B.SO2常用于漂白食品
C.SiO2常用于制造光导纤维
D.Na2O2可用于呼吸面具中氧气的来源BA18.下列有关1molH2的说法中,不正确的是(NA表示阿伏加德罗常数)A.质量为2g B.含氢原子数为NA
C.含氢分子数为NA D.标准状况下体积约为22.4L16.有关乙烯和苯的性质实验:①乙烯通入酸性KMnO4溶液,②苯滴入酸性KMnO4溶液。对上述实验现象的描述,正确的是
A.①褪色,②不褪色 B.①不褪色,②褪色
C.①、②均褪色 D.①、②均不褪色CBA 19.实验室用锌与稀硫酸反应制取H2,欲使产生H2的速率加快,下列措施可行的是
A.加水稀释 B.加少量NaOH溶液
C.降低温度 D.锌片改为锌粒DC21.将一小段镁带投入到盛有稀盐酸的试管中,发生剧烈反应。一段时间后,用手触摸试管外壁感觉烫手。这个实验事实说明该反应
A.为放热反应 B.为吸热反应
C.过程中热能转化为化学能
D.反应物的总能量低于生成物的总能量 DA二、填空题(本题包括4小题,每空2分,共26分) 23.(6分)钠、铝和铁是中学化学常见的三种重要金属。请回答下列问题:
(1)钠在空气中燃烧生成淡黄色的 (填“Na2O”或“Na2O2”);
(2)Al2O3能溶于酸或强碱溶液生成盐和水,则是一种 (填“酸性”、“碱性”或“两性”)氧化物;
(3)Fe(OH)3不溶于水,但能溶于酸,请写出Fe(OH)3与盐酸反应的化学方程式:
。Na2O2两性Fe(OH)3+3HCl=FeCl3 + 3H2O 24.(6分)氮、硫的化合物与人类生活和生产有着密切的联系。请回答下列问题:
(1)在空气质量报告的各项指标中,有SO2和NO2的指数,SO2是一种无色有毒气体,NO2是一种 (填“无色”或“红棕色”) 有毒气体;
(2)氨气极易溶于水,其水溶液显 (填“酸”、“碱”或“中”)性;
(3) 加热时,浓硫酸可与碳发生反应:C+2H2SO4(浓)=CO2↑+2SO2↑+2H2O。在该反应中,浓H2SO4表现出 (填“吸水”、“脱水”或“氧化”)性。 红棕色碱氧化性25.(6分)乙醇和乙酸是生活中两种常见的有机物。请回答下列问题:
(1)乙醇的结构简式为CH3CH2OH,乙醇分子含有的官能团为 ;
(2)生活中常用食醋除去暖瓶内的水垢(主要成分是CaCO3),反应的化学方程式为2CH3COOH+CaCO3=(CH3COO)2Ca+CO2↑+H2O。通过这个事实,你得出醋酸与碳酸的酸性强弱关系是:醋酸 碳酸(填“>”或“<”);
(3)在浓硫酸的催化作用下,加热乙酸和乙醇的混合溶液,可发生酯化反应。请完成化学方程式:CH3COOH +CH3CH2OH
CH3COO CH2CH3+ 。>羟基H2O26. (8分)下表是元素周期表的一部分,除标出的元素外,表中的每个编号代表一种元素,请根据要求回答问题:
N②<⑥③>⑤Mg+2H+ ==Mg2+ + H2↑三、实验题(本题包括1小题,每空2分,共10分)容量瓶27.(10分)实验室需配置100mL2.00mol/LNaCl溶液,请你参与实验过程,并完成相关实验报告(填写表格中横线上数字序号所示内容)。 实验步骤
(1)计算:溶质NaCl固体的质量为 ② g。
(2)称量:用托盘天平称取所需NaCl固体。
(3)溶解:将称好的NaCl固体放入烧杯中,用适量蒸馏水溶解。
(4)转移、洗涤:将烧杯中的溶液注入仪器①中,并用少量蒸馏水洗涤烧杯内壁2~3次,洗涤液也都注入仪器①中。
(5) ③ :将蒸馏水注入仪器至液面离刻度线1~2cm时,改用胶头滴管滴加蒸馏水至液面与刻度线相切。
(6)摇匀:盖好瓶塞 ,反复上下颠倒,然后静置。117定容思考与探究
(1)实验步骤(3)、(4)中都要用到玻璃棒,其作用分别是搅拌、 。
(2)某同学在实验步骤(6)后,发现凹液面低于刻度线,于是再向容器中滴加蒸馏水至刻度线,该同学所配置溶液是浓度 ⑤ (填“>”、“=”或“<”)2.00mol/L。引流<第二部分 选做题(20分)28.本题为《化学与生活(选修1)》选做题,每空2分,共20分。请根据题意,选择恰当的选项用字母代号填空。
(1)均衡营养和正确使用药物是保证身心健康的重要
方面,现有下列四种物质:
A.葡萄糖 B.氨基酸
C.麻黄碱 D.阿司匹林
①蛋白质水解的最终产物是 ;
②人体内最重要的供能物质是 ;
③具有解热镇痛作用,用于治疗感冒的是 ;
④对支气管哮喘症有明显疗效的是 。CBAD(2)材料是人类赖以生存和发展的重要物质基础。
①试管、烧杯和烧瓶等化学仪器的主要材质
是 ;A.玻璃 B.陶瓷
②钢铁是目前用量最大的铁合金。钢铁接触海水发
生电化学腐蚀,其负极反应式为 ;
A.O2+2H2O + 4e- = 4OH-
B.Fe - 2e-= Fe2+
因此,为防止轮船船体被腐蚀,可在船体上安装一定量的 。A.锌块 B.铜块AAB⑶当前,环境治理已成为重要的民生工程。
①2014年1月,教育部规定在学校公共场所禁止吸烟。下列有关说法中,不正确的是 ;
A.吸烟会对室内和公共场所造成污染
B.吸入焦油、尼古丁及颗粒物可导致多种病变
C.N2、CO2、CO和尼古丁都属于室内空气污染物C ②下列做法可能会加重“雾霾”的是 ;
A.大量焚烧秸秆
B.在汽车尾气系统装置催化转化器
C.发展煤的气化和液化等洁净煤技术
③下列处理垃圾的方法中,不正确的是 。
A.回收利用废纸 B.回收利用易拉罐 C.填埋废旧电池 CA29.本题为《化学反应原理(选修4)》选做题,每空2分,共20分。⑴合成氨是人类科技发展史上的一项重大突破。已知:25℃时,合成氨反应的热化学为:N2(g)+3H2(g) 2NH3(g) ΔH=-92.4kJ/mol
请回答下列问题:
①其他条件不变时,升高温度,化学反应速率 (填“增大”或“减小”);
②25℃时,取1mol N2和3mol H2置于2L的密闭容器中,在催化剂存在下进行反应,达到平衡时放出的热量 ,
A.大于92.4 kJ B.等于92.4 kJ C.小于92.4 kJ 增大C③一定条件下,上述反应达到化学平衡状态的标志是 ;
A.N2、H2、NH3的浓度相等;
B.容器内压强不再变化;
C.单位时间内消耗amol N2,同时生成2amol
NH3;
④25℃时,上述反应平衡常数的表达式为:
K= 。 B(2)右图是电解NaCl溶液的 示意图。请回答下列问题: ①石墨电极上的反应式 为 ; ②电解一段时间后,溶液的 PH (填“增大”、 “减小”或“不变”)。增大2Cl-- -- 2e-- ==Cl2↑(3)水溶液中的离子平衡是化学反应原理的重要内容。请回答下列问题:
①常温下,0.1mol/LCH3COONa溶液呈 (填“酸”、“碱”或“中”)性,
溶液中c(Na+) c(CH3COO-)(填“>”、“<”或“=”);碱>②常温下,在浓度均为0.1mol/L的盐酸和NH4Cl溶液中,水的电离程度大小关系是:0.1mol/L盐酸 0.1mol/LNH4Cl溶液(填“>”、“<”或“=”);
③已知:20℃时,Ksp(AgCl)=1.1×10-10,Ksp(AgBr)=2.0×10-13。将AgCl和AgBr的饱和溶液等体积混合,再逐滴加入足量浓AgNO3溶液,充分反应后,生成沉淀量的关系是:m(AgCl) m(AgBr)(填“>”、“<”或“=”)。<
