江苏省南京市2024-2025学年度九年级第一学期期末化学练习卷(含答案)
文档属性
| 名称 | 江苏省南京市2024-2025学年度九年级第一学期期末化学练习卷(含答案) |

|
|
| 格式 | docx | ||
| 文件大小 | 1.2MB | ||
| 资源类型 | 教案 | ||
| 版本资源 | 人教版 | ||
| 科目 | 化学 | ||
| 更新时间 | 2024-12-24 00:00:00 | ||
图片预览

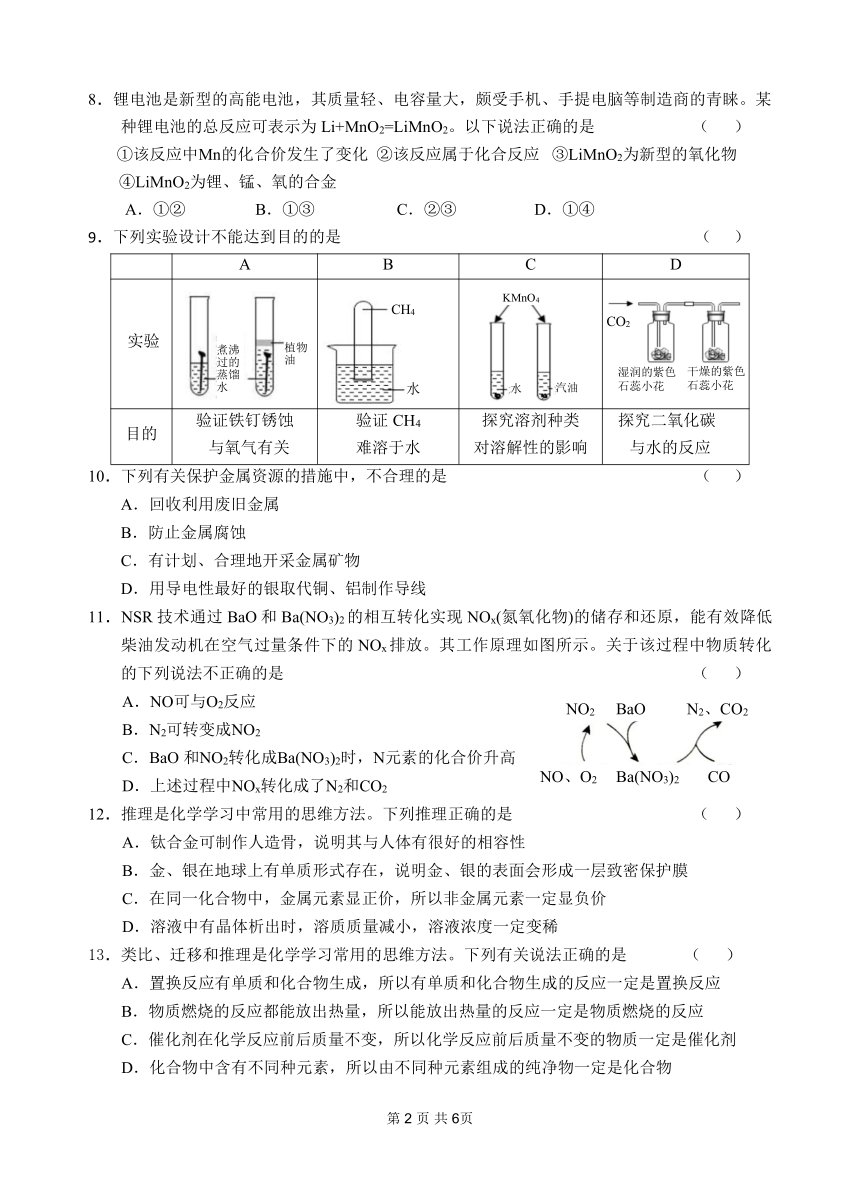
文档简介
2025届第一学期期末练习卷
九年级化学
可能用到的相对原子质量: C-12 H-1 O-16 Cu-64
一、选择题(本题包括 15 小题,每小题只有一个选项符合题意。每小题 2 分,共 30 分)
1.下列变化属于化学变化的是 ( )
A.弯曲铁丝 B.酒精挥发 C.冰雪融化 D.铁片生锈
2.下列物质由分子构成的是 ( )
A.铝 B.硫酸铜 C.金刚石 D.C60
3.下列化学用语书写不正确的是 ( )
A.2个氢原子:2H B.氢气中氢元素的化合价:H2
C.2个氢分子:2H2 D.2个氢离子:2H+
4.下列物质中都具有可燃性的一组是 ( )
A.CO、O2 、CH4 B.N2 、CO2、H2
C.H2、CO、C D.O2 、CO2、CO
5.下列有关做法或说法,不符合安全要求的是 ( )
A.油锅着火,可倒入蔬菜灭火 B.加油站严禁烟火
C.煤矿井下应保持通风良好 D.夜间闻到“燃气”气味,应开灯及时查明漏点
6.航天科技测得三氧化二碳(C2O3)是金星大气层的成分之一。据实验分析得出,C2O3与CO的化学性质相似。根据你所学知识推测下列关于三氧化二碳的认识不正确的是 ( )
三氧化二碳中碳元素的质量分数约为33.3%
B.三氧化二碳由2个碳原子和3个氧原子构成
C.三氧化二碳充分燃烧后的产物是CO2
D.三氧化二碳中C、O元素质量比为1∶2
7.某两种物质在光照条件下能发生化学反应(微观示意图如下,其中一种小球代表一种原子),下列说法正确的是 ( )
A.图示中共有四种分子 B.图示中的反应物都是单质
C.该反应属于置换反应 D.该图示不符合质量守恒定律
8.锂电池是新型的高能电池,其质量轻、电容量大,颇受手机、手提电脑等制造商的青睐。某种锂电池的总反应可表示为Li+MnO2=LiMnO2。以下说法正确的是 ( )
①该反应中Mn的化合价发生了变化 ②该反应属于化合反应 ③LiMnO2为新型的氧化物
④LiMnO2为锂、锰、氧的合金
A.①② B.①③ C.②③ D.①④
9.下列实验设计不能达到目的的是 ( )
A B C D
实验 (
煮沸过的蒸馏水
) (
C
H
4
水
) (
KMnO
4
)
目的 验证铁钉锈蚀 与氧气有关 验证CH4 难溶于水 探究溶剂种类 对溶解性的影响 探究二氧化碳 与水的反应
10.下列有关保护金属资源的措施中,不合理的是 ( )
A.回收利用废旧金属
B.防止金属腐蚀
C.有计划、合理地开采金属矿物
D.用导电性最好的银取代铜、铝制作导线
11.NSR技术通过BaO和Ba(NO3)2的相互转化实现NOx(氮氧化物)的储存和还原,能有效降低柴油发动机在空气过量条件下的NOx排放。其工作原理如图所示。关于该过程中物质转化的下列说法不正确的是 ( )
A.NO可与O2反应
B.N2可转变成NO2
C.BaO 和NO2转化成Ba(NO3)2时,N元素的化合价升高
D.上述过程中NOx转化成了N2和CO2
12.推理是化学学习中常用的思维方法。下列推理正确的是 ( )
A.钛合金可制作人造骨,说明其与人体有很好的相容性
B.金、银在地球上有单质形式存在,说明金、银的表面会形成一层致密保护膜
C.在同一化合物中,金属元素显正价,所以非金属元素一定显负价
D.溶液中有晶体析出时,溶质质量减小,溶液浓度一定变稀
13.类比、迁移和推理是化学学习常用的思维方法。下列有关说法正确的是 ( )
A.置换反应有单质和化合物生成,所以有单质和化合物生成的反应一定是置换反应
B.物质燃烧的反应都能放出热量,所以能放出热量的反应一定是物质燃烧的反应
C.催化剂在化学反应前后质量不变,所以化学反应前后质量不变的物质一定是催化剂
D.化合物中含有不同种元素,所以由不同种元素组成的纯净物一定是化合物
14.除去下列物质中混有的少量杂质(括号内为杂质),拟定的实验方案可行的是 ( )
A.N2(O2)——通过灼热的氧化铜
B.FeSO4溶液(CuSO4)——加入过量的铁粉,过滤
C.Zn(Cu)——加入足量的稀盐酸,过滤、洗涤、干燥
D.CaO(CaCO3)——加水溶解、过滤
15.用等质量相同表面积的镁条、等体积不同浓度的稀盐酸在一定条件下反应,实验结果如图所示。下列结论正确的是 ( )
①镁与盐酸的反应是放热反应
②b曲线对应的盐酸浓度较大
③盐酸浓度越大,反应速率越快
④单位时间内放出热量越多,反应速率越快
⑤装置内氢气的质量先增大,后减小
⑥两种情况最终产生氢气的质量可能相同
A.①②③④ B.①③④⑤ C.①③④⑥ D.③④⑤⑥
二、(本题包括 2 小题,共 21分)
16.(10分)化学是一门以实验为基础的科学。
(1)下图是初中化学制取气体的常见装置图。
①仪器a的名称 。
②实验室选择制取O2、CO2、H2等气体的反应原理时,不属于考虑的范畴是 (填字母)。
A.原料的来源和成本 B.气体的纯度和环保
C.反应的快慢和操作性 D.气体的密度和溶解性
③实验室用石灰石和稀盐酸制取二氧化碳的化学方程式为 。
④实验室用高锰酸钾制取并收集氧气,可选用的装置为 (填字母)。
⑤下列各组气体中,可用排水法、向上排气法、向下排法中的同一种方法收集的一组气体是
(填字母)。
A.O2 、CO2 B.CO2、H2 C.H2、O2
(2)右图装置是对(1)中A装置的优化。
①此装置通过注射器控制液体的量,从而控制反应的速率。若用此装置制取氧气,则其化学方程式为 。
②此装置也适用于实验室用锌与稀硫酸反应制取氢气,但制得的氢气在点燃前一定要验纯。此装置排出气体不纯的原因及验纯的目的是
。
③用下列制取氢气装置可控制反应发生与停止的是 (填字母)。
17.(11分)化学变化总伴随着能量的变化。
(1)燃料的燃烧是人类获取能量的重要途径,目前,三大化石能源包括煤、石油和 。使燃料充分燃烧要考虑:燃烧时要有足够的空气(氧气)和 ,等等。
(2)碳与二氧化碳的反应为吸热反应,其化学方程式为 。
(3)火箭推进器中用联氨(N2H4)和四氧化二氮(N2O4)作推进剂,当它们混合时产生大量的水蒸气和一种单质,并提供能量,其化学方程式为 ;选联氨作推进器中燃料,除了热值高外,另一个很大优点是 。
(4)酒精是实验室中常用的燃料,实验中充分燃烧69g酒精,理论上最多可产生CO2的质量是多少?(利用化学方程式进行计算,写出计算过程)
三、(本题包括 2 小题,共 14分)
18.(8分)人类的生产生活离不开金属。
(1)铁是年产量最高的金属,以赤铁矿为例,用化学方程式表示工业炼铁原理
;
(2)下列金属的用途与其化学性质相关的是 (填字母)。
A.镁粉用于制作烟花 B.铜作导线 C.铁用于制作炊具 D.铝可制成铝箔
(3)氯化铁能腐蚀铜,工业上常用此原理生产印刷线路板。以下是印刷线路板的生产及废液的处理过程:
请回答下列问题:
①步骤Ⅱ中发生了两个反应:2FeCl3+Fe=3FeCl2 和 。
②滤渣的成分有 ,步骤Ⅲ中发生反应的化学方程式是 。
19.(6分)溶液在生命活动和生产、生活中都起到十分重要的作用。
(1)将少量下列厨房物质分别加入水中,可形成溶液的是 (填字母)。
A.食盐 B.蔗糖 C.味精 D.芝麻油
(2)如右图装置,向试管中加入下列物质后,气球会变大的是 (填字母)。
A.NaCl B.NH4NO3 C.NaOH D.CaO
(3)如图为硝酸钾和氯化钠的溶解度曲线。
① 10℃时,硝酸钾的溶解度为20.9g。这句话的含义是
。
② 20℃时,将40g硝酸钾加入到100g水中,充分搅拌,形
成 溶液(填“饱和”或“不饱和”);
③50℃时,将等质量的硝酸钾和氯化钠分别配成饱和溶液,
所需水的质量:硝酸钾 氯化钠(填“大于”
“等于”或“小于”)。
④将60℃时硝酸钾、氯化钠的饱和溶液分别降温到20℃,
则析出硝酸钾与氯化钠晶体的质量关系为 (填
“大于”“小于”或“不确定”)。
四、(本题包括 1 小题,共 5分)
20.右图中A~E为初中化学常见的物质。其中A、B、E为氧化物,C、D为单质,且A与B反应、 B与C反应均生成一种红色单质。图中“-”表示两端的物质间能发生化学反应;“ → ”表示物质间存在转化关系;部分反应物、生成物或反应条件已略去。
(1)E的化学式为 ;
(2)A与D反应的化学方程式: ;
(3)B与C反应的化学方程式: 。
五、(本题包括1小题,共10分)
21.(10分)木炭用于金属冶炼在我国已有几千年的历史。
【实验探究】右图是实验室用木炭还原CuO的实验装置图。
木炭与氧化铜反应实验的现象为
。
实验时要先将块状木炭研细,再与CuO粉末混合均匀
后使用。这样处理的目的是 。
(3)写出使澄清石灰水变浑浊的化学方程式 。
【实验反思1】该实验中可能有多种因素产生CO2气体:
(1)C与氧化铜反应生成的CO2;
(2)C与生成的CO2气体反应生成CO,CO再与CuO反应生成的CO2;
(3) (请再写出一种可能)。
【实验反思2】木炭与氧化铜的反应中有CO产生吗?
(1)查阅资料:当木炭较多、温度较高时,该反应产生的气体中可能含有CO和CO2,于是小组的同学们在老师指导下设计实验进行了验证。已知:碱石灰是NaOH和CaO的混合物,可以吸收CO2和水。
①D中玻璃管盛装的试剂为CuO,E中盛装的试剂为澄清的石灰水。若A装置产物中确有CO,则应观察到的现象有 。
②将1.44 g碳和16.0g CuO混合于A中,先打开K,通一会N2后关闭K,若在高温下二者正好完全反应成单质Cu,理论上则可生成 g CO。
(2)木炭与CuO的比例及反应时的温度也影响其固体生成物,可能会有Cu2O生成,Cu2O也为红色固体,难溶于水,可与稀硫酸反应生成Cu和CuSO4。
请设计简单实验验证CuO和足量木炭反应后所得的红色固体中是否有Cu2O。
操作 现象 结论
九年级化学练习卷参考答案
一、选择题(本题共15小题,每小题2分,共30分)
题号 1 2 3 4 5 6 7 8 9 10 11 12 13 14 15
答案 A D B C D B A A D D B A C B C
化学方程式:化学式正确得一半分,其它有错总扣一半分
二、(本题包括2小题,共21分)
16.(10分)(1)①长颈漏斗 ② D ③CaCO3+2HCl = CaCl2+CO2↑+ H2O ④BD或BE
⑤AC (2)① 2H2O22H2O+ O2↑ ②原装置内有空气,会与生成的氢气混合,致使氢气中混有氧气;验纯的目的是判断装置氧气是否排尽,防止点然使装置发生爆炸③ACDE
(11分)(1)天然气 燃料要与空气要有尽够大的接触面积 (2)C+CO22CO
(3)2N2H4+N2O4=3N2↑+4H2O↑ 生成物对环境无污染
(4)解:设最多可产生CO2的质量为x。
C2H5OH+3O22CO2 +3H2O
46 88
69g x
答:最多可产生132g二氧化碳。
三、(本题包括2小题,共14分)
18.(8分)(1)3CO+Fe2O3 2Fe+3CO2 (2)A
(3)①Fe + CuCl2 = FeCl2 + Cu ②Fe、Cu Fe + 2HCl = FeCl2 +H2↑
19.(6分)(1) AB (2)B (3)①表示10℃时,100g水中最多能溶解20.9g硝酸钾
②饱和③小于④不确定
四、(本题包括1小题,共5分)
20.(5分)(1)CO2(2)CO+CuOCu+CO2
(3)C + 2CuO2Cu + CO2↑
五、(本题包括1小题,共10分)
21.(10分)【实验探究】
D中黑色固体变为红色,E中澄清石灰水变浑浊
增大固体的接触面积
Ca(OH)2 + CO2 CaCO3↓+ H2O
【实验反思】(3)C与试管内O2反应生成CO2、CO与试管内O2反应生成CO2(合理答案给分)
【查阅资料】(1)②D中固体变红,E中澄清石灰水变浑浊③1.12
取少量红色固体与试管中,加入少量稀H2SO4,振荡 若溶液颜色变蓝 若溶液仍为无色 则固体中有Cu2O 则固体中无Cu2O
(2)
九年级化学
可能用到的相对原子质量: C-12 H-1 O-16 Cu-64
一、选择题(本题包括 15 小题,每小题只有一个选项符合题意。每小题 2 分,共 30 分)
1.下列变化属于化学变化的是 ( )
A.弯曲铁丝 B.酒精挥发 C.冰雪融化 D.铁片生锈
2.下列物质由分子构成的是 ( )
A.铝 B.硫酸铜 C.金刚石 D.C60
3.下列化学用语书写不正确的是 ( )
A.2个氢原子:2H B.氢气中氢元素的化合价:H2
C.2个氢分子:2H2 D.2个氢离子:2H+
4.下列物质中都具有可燃性的一组是 ( )
A.CO、O2 、CH4 B.N2 、CO2、H2
C.H2、CO、C D.O2 、CO2、CO
5.下列有关做法或说法,不符合安全要求的是 ( )
A.油锅着火,可倒入蔬菜灭火 B.加油站严禁烟火
C.煤矿井下应保持通风良好 D.夜间闻到“燃气”气味,应开灯及时查明漏点
6.航天科技测得三氧化二碳(C2O3)是金星大气层的成分之一。据实验分析得出,C2O3与CO的化学性质相似。根据你所学知识推测下列关于三氧化二碳的认识不正确的是 ( )
三氧化二碳中碳元素的质量分数约为33.3%
B.三氧化二碳由2个碳原子和3个氧原子构成
C.三氧化二碳充分燃烧后的产物是CO2
D.三氧化二碳中C、O元素质量比为1∶2
7.某两种物质在光照条件下能发生化学反应(微观示意图如下,其中一种小球代表一种原子),下列说法正确的是 ( )
A.图示中共有四种分子 B.图示中的反应物都是单质
C.该反应属于置换反应 D.该图示不符合质量守恒定律
8.锂电池是新型的高能电池,其质量轻、电容量大,颇受手机、手提电脑等制造商的青睐。某种锂电池的总反应可表示为Li+MnO2=LiMnO2。以下说法正确的是 ( )
①该反应中Mn的化合价发生了变化 ②该反应属于化合反应 ③LiMnO2为新型的氧化物
④LiMnO2为锂、锰、氧的合金
A.①② B.①③ C.②③ D.①④
9.下列实验设计不能达到目的的是 ( )
A B C D
实验 (
煮沸过的蒸馏水
) (
C
H
4
水
) (
KMnO
4
)
目的 验证铁钉锈蚀 与氧气有关 验证CH4 难溶于水 探究溶剂种类 对溶解性的影响 探究二氧化碳 与水的反应
10.下列有关保护金属资源的措施中,不合理的是 ( )
A.回收利用废旧金属
B.防止金属腐蚀
C.有计划、合理地开采金属矿物
D.用导电性最好的银取代铜、铝制作导线
11.NSR技术通过BaO和Ba(NO3)2的相互转化实现NOx(氮氧化物)的储存和还原,能有效降低柴油发动机在空气过量条件下的NOx排放。其工作原理如图所示。关于该过程中物质转化的下列说法不正确的是 ( )
A.NO可与O2反应
B.N2可转变成NO2
C.BaO 和NO2转化成Ba(NO3)2时,N元素的化合价升高
D.上述过程中NOx转化成了N2和CO2
12.推理是化学学习中常用的思维方法。下列推理正确的是 ( )
A.钛合金可制作人造骨,说明其与人体有很好的相容性
B.金、银在地球上有单质形式存在,说明金、银的表面会形成一层致密保护膜
C.在同一化合物中,金属元素显正价,所以非金属元素一定显负价
D.溶液中有晶体析出时,溶质质量减小,溶液浓度一定变稀
13.类比、迁移和推理是化学学习常用的思维方法。下列有关说法正确的是 ( )
A.置换反应有单质和化合物生成,所以有单质和化合物生成的反应一定是置换反应
B.物质燃烧的反应都能放出热量,所以能放出热量的反应一定是物质燃烧的反应
C.催化剂在化学反应前后质量不变,所以化学反应前后质量不变的物质一定是催化剂
D.化合物中含有不同种元素,所以由不同种元素组成的纯净物一定是化合物
14.除去下列物质中混有的少量杂质(括号内为杂质),拟定的实验方案可行的是 ( )
A.N2(O2)——通过灼热的氧化铜
B.FeSO4溶液(CuSO4)——加入过量的铁粉,过滤
C.Zn(Cu)——加入足量的稀盐酸,过滤、洗涤、干燥
D.CaO(CaCO3)——加水溶解、过滤
15.用等质量相同表面积的镁条、等体积不同浓度的稀盐酸在一定条件下反应,实验结果如图所示。下列结论正确的是 ( )
①镁与盐酸的反应是放热反应
②b曲线对应的盐酸浓度较大
③盐酸浓度越大,反应速率越快
④单位时间内放出热量越多,反应速率越快
⑤装置内氢气的质量先增大,后减小
⑥两种情况最终产生氢气的质量可能相同
A.①②③④ B.①③④⑤ C.①③④⑥ D.③④⑤⑥
二、(本题包括 2 小题,共 21分)
16.(10分)化学是一门以实验为基础的科学。
(1)下图是初中化学制取气体的常见装置图。
①仪器a的名称 。
②实验室选择制取O2、CO2、H2等气体的反应原理时,不属于考虑的范畴是 (填字母)。
A.原料的来源和成本 B.气体的纯度和环保
C.反应的快慢和操作性 D.气体的密度和溶解性
③实验室用石灰石和稀盐酸制取二氧化碳的化学方程式为 。
④实验室用高锰酸钾制取并收集氧气,可选用的装置为 (填字母)。
⑤下列各组气体中,可用排水法、向上排气法、向下排法中的同一种方法收集的一组气体是
(填字母)。
A.O2 、CO2 B.CO2、H2 C.H2、O2
(2)右图装置是对(1)中A装置的优化。
①此装置通过注射器控制液体的量,从而控制反应的速率。若用此装置制取氧气,则其化学方程式为 。
②此装置也适用于实验室用锌与稀硫酸反应制取氢气,但制得的氢气在点燃前一定要验纯。此装置排出气体不纯的原因及验纯的目的是
。
③用下列制取氢气装置可控制反应发生与停止的是 (填字母)。
17.(11分)化学变化总伴随着能量的变化。
(1)燃料的燃烧是人类获取能量的重要途径,目前,三大化石能源包括煤、石油和 。使燃料充分燃烧要考虑:燃烧时要有足够的空气(氧气)和 ,等等。
(2)碳与二氧化碳的反应为吸热反应,其化学方程式为 。
(3)火箭推进器中用联氨(N2H4)和四氧化二氮(N2O4)作推进剂,当它们混合时产生大量的水蒸气和一种单质,并提供能量,其化学方程式为 ;选联氨作推进器中燃料,除了热值高外,另一个很大优点是 。
(4)酒精是实验室中常用的燃料,实验中充分燃烧69g酒精,理论上最多可产生CO2的质量是多少?(利用化学方程式进行计算,写出计算过程)
三、(本题包括 2 小题,共 14分)
18.(8分)人类的生产生活离不开金属。
(1)铁是年产量最高的金属,以赤铁矿为例,用化学方程式表示工业炼铁原理
;
(2)下列金属的用途与其化学性质相关的是 (填字母)。
A.镁粉用于制作烟花 B.铜作导线 C.铁用于制作炊具 D.铝可制成铝箔
(3)氯化铁能腐蚀铜,工业上常用此原理生产印刷线路板。以下是印刷线路板的生产及废液的处理过程:
请回答下列问题:
①步骤Ⅱ中发生了两个反应:2FeCl3+Fe=3FeCl2 和 。
②滤渣的成分有 ,步骤Ⅲ中发生反应的化学方程式是 。
19.(6分)溶液在生命活动和生产、生活中都起到十分重要的作用。
(1)将少量下列厨房物质分别加入水中,可形成溶液的是 (填字母)。
A.食盐 B.蔗糖 C.味精 D.芝麻油
(2)如右图装置,向试管中加入下列物质后,气球会变大的是 (填字母)。
A.NaCl B.NH4NO3 C.NaOH D.CaO
(3)如图为硝酸钾和氯化钠的溶解度曲线。
① 10℃时,硝酸钾的溶解度为20.9g。这句话的含义是
。
② 20℃时,将40g硝酸钾加入到100g水中,充分搅拌,形
成 溶液(填“饱和”或“不饱和”);
③50℃时,将等质量的硝酸钾和氯化钠分别配成饱和溶液,
所需水的质量:硝酸钾 氯化钠(填“大于”
“等于”或“小于”)。
④将60℃时硝酸钾、氯化钠的饱和溶液分别降温到20℃,
则析出硝酸钾与氯化钠晶体的质量关系为 (填
“大于”“小于”或“不确定”)。
四、(本题包括 1 小题,共 5分)
20.右图中A~E为初中化学常见的物质。其中A、B、E为氧化物,C、D为单质,且A与B反应、 B与C反应均生成一种红色单质。图中“-”表示两端的物质间能发生化学反应;“ → ”表示物质间存在转化关系;部分反应物、生成物或反应条件已略去。
(1)E的化学式为 ;
(2)A与D反应的化学方程式: ;
(3)B与C反应的化学方程式: 。
五、(本题包括1小题,共10分)
21.(10分)木炭用于金属冶炼在我国已有几千年的历史。
【实验探究】右图是实验室用木炭还原CuO的实验装置图。
木炭与氧化铜反应实验的现象为
。
实验时要先将块状木炭研细,再与CuO粉末混合均匀
后使用。这样处理的目的是 。
(3)写出使澄清石灰水变浑浊的化学方程式 。
【实验反思1】该实验中可能有多种因素产生CO2气体:
(1)C与氧化铜反应生成的CO2;
(2)C与生成的CO2气体反应生成CO,CO再与CuO反应生成的CO2;
(3) (请再写出一种可能)。
【实验反思2】木炭与氧化铜的反应中有CO产生吗?
(1)查阅资料:当木炭较多、温度较高时,该反应产生的气体中可能含有CO和CO2,于是小组的同学们在老师指导下设计实验进行了验证。已知:碱石灰是NaOH和CaO的混合物,可以吸收CO2和水。
①D中玻璃管盛装的试剂为CuO,E中盛装的试剂为澄清的石灰水。若A装置产物中确有CO,则应观察到的现象有 。
②将1.44 g碳和16.0g CuO混合于A中,先打开K,通一会N2后关闭K,若在高温下二者正好完全反应成单质Cu,理论上则可生成 g CO。
(2)木炭与CuO的比例及反应时的温度也影响其固体生成物,可能会有Cu2O生成,Cu2O也为红色固体,难溶于水,可与稀硫酸反应生成Cu和CuSO4。
请设计简单实验验证CuO和足量木炭反应后所得的红色固体中是否有Cu2O。
操作 现象 结论
九年级化学练习卷参考答案
一、选择题(本题共15小题,每小题2分,共30分)
题号 1 2 3 4 5 6 7 8 9 10 11 12 13 14 15
答案 A D B C D B A A D D B A C B C
化学方程式:化学式正确得一半分,其它有错总扣一半分
二、(本题包括2小题,共21分)
16.(10分)(1)①长颈漏斗 ② D ③CaCO3+2HCl = CaCl2+CO2↑+ H2O ④BD或BE
⑤AC (2)① 2H2O22H2O+ O2↑ ②原装置内有空气,会与生成的氢气混合,致使氢气中混有氧气;验纯的目的是判断装置氧气是否排尽,防止点然使装置发生爆炸③ACDE
(11分)(1)天然气 燃料要与空气要有尽够大的接触面积 (2)C+CO22CO
(3)2N2H4+N2O4=3N2↑+4H2O↑ 生成物对环境无污染
(4)解:设最多可产生CO2的质量为x。
C2H5OH+3O22CO2 +3H2O
46 88
69g x
答:最多可产生132g二氧化碳。
三、(本题包括2小题,共14分)
18.(8分)(1)3CO+Fe2O3 2Fe+3CO2 (2)A
(3)①Fe + CuCl2 = FeCl2 + Cu ②Fe、Cu Fe + 2HCl = FeCl2 +H2↑
19.(6分)(1) AB (2)B (3)①表示10℃时,100g水中最多能溶解20.9g硝酸钾
②饱和③小于④不确定
四、(本题包括1小题,共5分)
20.(5分)(1)CO2(2)CO+CuOCu+CO2
(3)C + 2CuO2Cu + CO2↑
五、(本题包括1小题,共10分)
21.(10分)【实验探究】
D中黑色固体变为红色,E中澄清石灰水变浑浊
增大固体的接触面积
Ca(OH)2 + CO2 CaCO3↓+ H2O
【实验反思】(3)C与试管内O2反应生成CO2、CO与试管内O2反应生成CO2(合理答案给分)
【查阅资料】(1)②D中固体变红,E中澄清石灰水变浑浊③1.12
取少量红色固体与试管中,加入少量稀H2SO4,振荡 若溶液颜色变蓝 若溶液仍为无色 则固体中有Cu2O 则固体中无Cu2O
(2)
同课章节目录
