2025年九年级中考化学专题复习 计算应用题 课件(共36张PPT)
文档属性
| 名称 | 2025年九年级中考化学专题复习 计算应用题 课件(共36张PPT) |

|
|
| 格式 | pptx | ||
| 文件大小 | 1.0MB | ||
| 资源类型 | 教案 | ||
| 版本资源 | 通用版 | ||
| 科目 | 化学 | ||
| 更新时间 | 2024-12-25 00:00:00 | ||
图片预览










文档简介
(共36张PPT)
计算应用题
专题六 计算应用题
计算应用题是河北中考必考题型,解题思路一般固定,均以实验为背景,第一问一般都是根据质量守恒定律求某一物质的质量,数据易得,难度小;第二问一般为计算某溶质的溶质质量分数或混合物中某物质的质量分数。 预计 2025 年河北中考计算题仍将以化学方程式与溶质质量分数或混合物中某物质的质量分数的综合计算为主,计算题的整体难度不会增加,试题将更加灵活,更加注重联系实验操作过程或解决生活和生产实际中的具体问题。
■类型一 文字叙述类
1.[2024·威海改编]某品牌“发热鞋垫”中发热剂的主要成分为铁粉、 活 性炭和氯化钠等。 为测定其中铁粉的含量,小明同学进行如下实验: 取 5 g 发热剂样品于烧杯中,逐滴加入稀硫酸至不再产生气泡,测得加入稀硫酸的质量为 23.4 g,反应后烧杯内剩余物的总质量为 28.3 g。
(1)反应生成氢气的质量是 ______。
(2)计算发热剂中铁粉的质量分数。(假设其他成分不与酸反应)
专题六 计算应用题
0.1 g
解:设参加反应的铁的质量为x。
发热剂中铁粉的质量分数为
答:发热剂中铁粉的质量分数为56%。
专题六 计算应用题
2.[2024·长沙]某小苏打包装袋上标注的碳酸氢钠含量为 99%,小丽同学对此产生质疑。她取 9 g 该小苏打样品于烧杯中,向其中加入50 g 稀硫酸,恰好完全反应后,称得烧杯中剩余物质的质量为 54.6 g。(已知:2NaHCO3+H2SO4=Na2SO4+2CO2↑+2H2O,其他成分不与稀硫酸反应)
(1)计算反应中产生 CO2 的质量为 ______ g。
(2)请计算该小苏打样品中碳酸氢钠的质量分数,并判断包装袋上碳酸氢钠含量的标注是否准确。(计算结果百分号前保留一位小数)
4.4
专题六 计算应用题
解:设该小苏打样品中碳酸氢钠的质量为 x。
则该小苏打样品中碳酸氢钠的质量分数为 ,93.3%<99%
答:该小苏打样品中碳酸氢钠的质量分数为 99%,包装袋上碳酸氢钠含量的标注不准确。
专题六 计算应用题
3. 某氯化钠溶液中含有少量氯化钡(BaCl2),学习小组为测定其中氯化钡的质量分数,在50.0 g 该溶液中加入 50.0 g 硫酸钠溶液恰好完全反应,经测定生成沉淀的质量为 4.66 g。请回答下列问题。
(1)反应后溶液的质量为 ______ g。
(2)原氯化钠溶液中氯化钡的质量分数。
95.34
专题六 计算应用题
解:设参加反应的氯化钡的质量为 x。
原氯化钠溶液中氯化钡的质量分数为
答:原氯化钠溶液中氯化钡的质量分数为 8.32%。
专题六 计算应用题
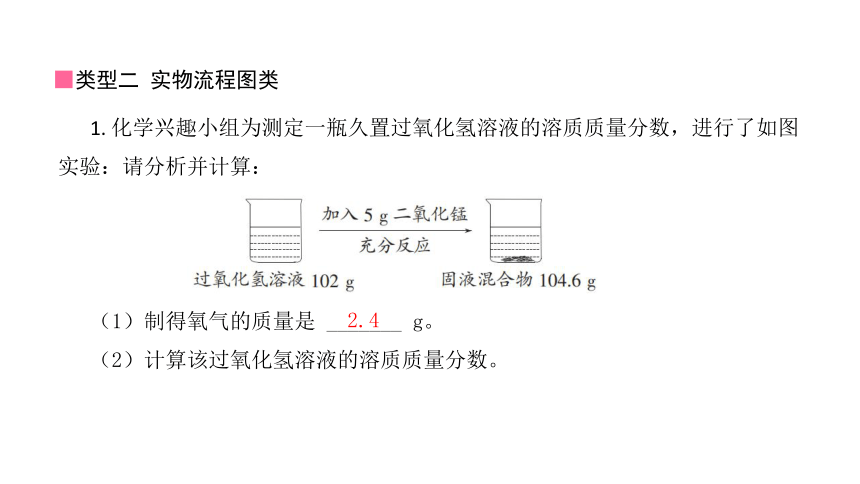
■类型二 实物流程图类
1. 化学兴趣小组为测定一瓶久置过氧化氢溶液的溶质质量分数,进行了如图实验:请分析并计算:
(1)制得氧气的质量是 _______ g。
(2)计算该过氧化氢溶液的溶质质量分数。
2.4
专题六 计算应用题
解:设参加反应的 H2O2 的质量为 x。
该过氧化氢溶液的溶质质量分数为
答:该过氧化氢溶液的溶质质量分数为 5%。
专题六 计算应用题
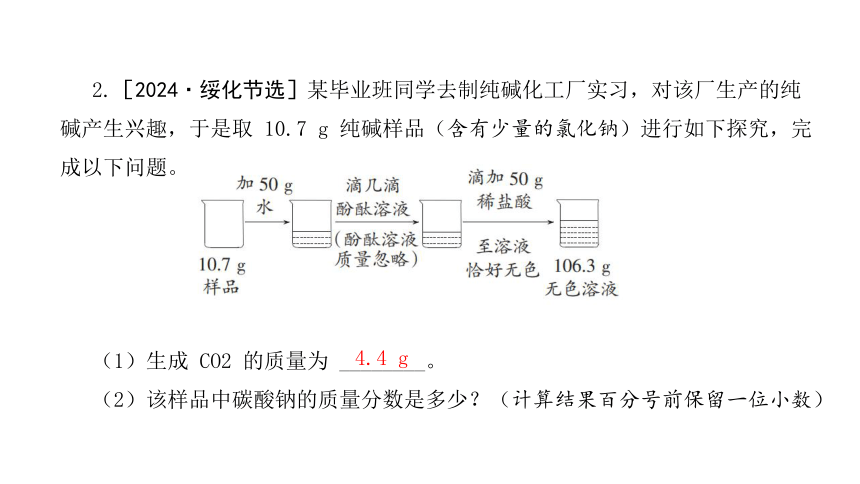
2.[2024·绥化节选]某毕业班同学去制纯碱化工厂实习,对该厂生产的纯碱产生兴趣,于是取 10.7 g 纯碱样品(含有少量的氯化钠)进行如下探究,完成以下问题。
(1)生成 CO2 的质量为 ________。
(2)该样品中碳酸钠的质量分数是多少?(计算结果百分号前保留一位小数)
4.4 g
专题六 计算应用题
专题六 计算应用题
解::设参加反应的 Na2CO3 的质量为 x。
样品中碳酸钠的质量分数为
答:该样品中碳酸钠的质量分数是99.1%。
3. 某补钙剂的有效成分是碳酸钙,其他成分不含钙且不与稀盐酸反应。 学习小组的同学进行如图所示实验。
(1)产生气体的质量为 _______ g。
(2)计算补钙剂中碳酸钙的质量分数。
1.1
专题六 计算应用题
专题六 计算应用题
解:设 5 g 补钙剂中碳酸钙的质量为 x。
补钙剂中碳酸钙的质量分数为
答:补钙剂中碳酸钙的质量分数为50%。
4.[2024·保定莲池区一模]金属涂层光纤是在光纤的表面涂布 Cu-Al 合金层的光纤。 为测定 Cu-Al 合金样品中铝的质量分数,小明取一定质量的样品放入烧杯中,分 2 次加入质量分数相同的稀硫酸,实验过程如图所示。请计算:
(1)生成氢气的总质量为 _______ g。
(2)Cu-Al 合金样品中铝的质量分数。
0.6
专题六 计算应用题
专题六 计算应用题
解:设 Cu-Al 合金样品中铝的质量为 x。
Cu-Al 合金样品中铝的质量分数为
答:Cu-Al 合金样品中铝的质量分数为 54%
■类型三 表格数据分析类
1.[2024·兰州]兴趣小组同学得知鸡蛋壳的主要成分是碳酸钙,就用它来测定某瓶标签破损的稀盐酸中溶质的质量分数。 称取 5.5 g干燥的鸡蛋壳(杂质不参加反应)于烧杯中,再将 75 g 该稀盐酸分 3 次加入,充分反应后得到实验数据如下:
请计算:
(1)鸡蛋壳中碳酸钙的质量为 _______ g。
5
专题六 计算应用题
解:由题中表格数据分析可知,25 g 稀盐酸能与 2.5 g 碳酸钙恰好完全反应。
设 25 g 稀盐酸中溶质的质量为 x。
该稀盐酸中溶质的质量分数是
答:该稀盐酸中溶质的质量分数是7.3%。
(2)该稀盐酸中溶质的质量分数是多少?
专题六 计算应用题
2. 实验室有一瓶含杂质的高锰酸钾。 某校课外兴趣小组用该试剂加热制取氧气(杂质不参加反应)。 反应过程中固体质量随时间变化的数据见表:
请计算:
(1)反应过程中共制得气体的质量 _____。
(2)该试剂中所含高锰酸钾的质量分数。
6.4 g
专题六 计算应用题
解:设参加反应的高锰酸钾的质量为x。
该药品中所含高锰酸钾的质量分数为
答:该药品中所含高锰酸钾的质量分数为 80%。
专题六 计算应用题
3.[2024·潍坊改编]“金粉”(Cu-Zn 合金)是一种金属颜料,可用于文物修复。 某化学兴趣小组通过实验测定“金粉”中铜的含量:称取25 g“金粉”样品放入锥形瓶中,将 100 g 稀硫酸分 5 次加入,记录每次反应后锥形瓶内物质的总质量。 实验过程和数据如表。
回答下列问题。
专题六 计算应用题
解:根据质量守恒定律,生成氢气的总质量为 25 g+100 g-124.8 g=0.2 g。
设参加反应锌的质量为 x。
故样品中铜的质量分数为
答:样品中铜的质量分数为 74%。
(1)a 的数值为 _____。
(2)计算样品中铜的质量分数。
专题六 计算应用题
104.8
1. 工业上,煅烧石灰石可制生石灰和二氧化碳。某化学兴趣小组在实验室煅烧 25 g 石灰石样品(样品中杂质不反应),在煅烧过程中,剩余固体的质量随时间的变化如图所示。 求:
(1)石灰石完全分解产生的二氧化碳的质量
是 _______ g。
(2)计算 25 g 石灰石样品中碳酸钙的质
量分数。
8.8
专题六 计算应用题
■类型四 坐标曲线类
专题六 计算应用题
解:设 25 g 样品中碳酸钙的质量为 x。
样品中碳酸钙的质量分数为
答:样品中碳酸钙的质量分数为80%。
2.[2024·自贡]实验室现有一瓶失去标签的氢氧化钠溶液,某化学课外活动小组为测定该溶液溶质的质量分数。 取该氢氧化钠溶液20 g,向其中滴加质量分数为 7.3%的稀盐酸,同时测得其 pH 变化与加入稀盐酸的质量关系如图所示。
(1)图中 a 点时所得溶液中溶质为 ________
(填化学式)。
(2)试计算该氢氧化钠溶液溶质的质量分数。
NaCl
专题六 计算应用题
专题六 计算应用题
解:设该氢氧化钠溶液溶质的质量为 x。
该氢氧化钠溶液溶质的质量分数为
答:该氢氧化钠溶液溶质的质量分数为 4%。
3. 学校环保小组检测发现实验室的某酸性废液中含有 CuSO4。 该小组取 100 g 废液,为了测定废液中 CuSO4 的质量分数,逐滴加入KOH 溶 液 至 过 量 。测得生成沉淀(无其他沉淀)的质量与所加 KOH 溶液的质量关系如图所示:
(1)反应结束后生成沉淀质量是 _______ g。
(2)计算废液中 CuSO4 的质量分数。
9.8
专题六 计算应用题
专题六 计算应用题
解:设参加反应的 CuSO4 的质量为 x。
废液中 CuSO4 的质量分数为
答:废液中 CuSO4的质量分数为16%。
4. 将一定质量分数的稀盐酸加入放有一块已生锈铁片的烧杯中,充分反应后,测得生成H2 的质量与稀盐酸的质量关系如图所示(假设铁片除有 Fe2O3 外不含其他杂质)。请回答下列问题。
(1)生成氢气的质量为 _______ g。
(2)计算所用的稀盐酸的溶质质量分数。
0.4
专题六 计算应用题
专题六 计算应用题
解:设与铁反应消耗稀盐酸的溶质质量为 x。
所用稀盐酸的溶质质量分数为
答:所用的稀盐酸的溶质质量分数为 14.6%。
1. 小明为了测定某硫酸溶液中溶质的质量分数,如图甲,向 60 g 硫酸溶液中缓缓注入质量分数为 10%的氢氧化钠溶液,测得溶液的pH 与氢氧化钠溶液的质量对应关系如图乙。 请回答下列问题。
专题六 计算应用题
■类型五 组合类
(1)图乙中 a 点溶液含有的溶质是 ____________________。
(2)请计算硫酸溶液中溶质的质量分数。(计算结果百分号前保留一位小数)
专题六 计算应用题
解:设参加反应的硫酸的质量为 x。
硫酸溶液中溶质的质量分数为
答:硫酸溶液中溶质的质量分数为 4.1%。
氢氧化钠、硫酸钠
2. 航天员王亚平在天和核心舱开展科普实验:将泡腾片塞入一个蓝色水球里,泡腾片逐渐溶解并不断冒泡,水球变成“气泡球”。某兴趣小组为了测定某泡腾片中 NaHCO3 的含量(该泡腾片成分如图所示),先将装有水的烧杯放在电子天平上,再将 10.00 g 该泡腾片投入水中并搅拌,当质量不再变化时,为确保 NaHCO3 完全反应,他又向烧杯中分次加入 10%的稀硫酸,每次加 2.00 g,总质量变化如表所示:
专题六 计算应用题
专题六 计算应用题
【提示】泡腾片中的柠檬酸(用 H3R 表示)溶于水后,与 NaHCO3 反应生成的盐为 Na3R。
(1)泡腾片中的 NaHCO3 在表中 ____(填序号)时已反应完全。
(2)计算这种泡腾片中 NaHCO3 的质量分数。
专题六 计算应用题
③
专题六 计算应用题
解:生成二氧化碳的质量为40.00 g-39.56 g=0.44 g。
设 10.00 g 该泡腾片中NaHCO3 的质量为 x。
则这种泡腾片中 NaHCO3 的质量分数为
答:这种泡腾片中 NaHCO3 的质量分数为 8.4%。
计算应用题
专题六 计算应用题
计算应用题是河北中考必考题型,解题思路一般固定,均以实验为背景,第一问一般都是根据质量守恒定律求某一物质的质量,数据易得,难度小;第二问一般为计算某溶质的溶质质量分数或混合物中某物质的质量分数。 预计 2025 年河北中考计算题仍将以化学方程式与溶质质量分数或混合物中某物质的质量分数的综合计算为主,计算题的整体难度不会增加,试题将更加灵活,更加注重联系实验操作过程或解决生活和生产实际中的具体问题。
■类型一 文字叙述类
1.[2024·威海改编]某品牌“发热鞋垫”中发热剂的主要成分为铁粉、 活 性炭和氯化钠等。 为测定其中铁粉的含量,小明同学进行如下实验: 取 5 g 发热剂样品于烧杯中,逐滴加入稀硫酸至不再产生气泡,测得加入稀硫酸的质量为 23.4 g,反应后烧杯内剩余物的总质量为 28.3 g。
(1)反应生成氢气的质量是 ______。
(2)计算发热剂中铁粉的质量分数。(假设其他成分不与酸反应)
专题六 计算应用题
0.1 g
解:设参加反应的铁的质量为x。
发热剂中铁粉的质量分数为
答:发热剂中铁粉的质量分数为56%。
专题六 计算应用题
2.[2024·长沙]某小苏打包装袋上标注的碳酸氢钠含量为 99%,小丽同学对此产生质疑。她取 9 g 该小苏打样品于烧杯中,向其中加入50 g 稀硫酸,恰好完全反应后,称得烧杯中剩余物质的质量为 54.6 g。(已知:2NaHCO3+H2SO4=Na2SO4+2CO2↑+2H2O,其他成分不与稀硫酸反应)
(1)计算反应中产生 CO2 的质量为 ______ g。
(2)请计算该小苏打样品中碳酸氢钠的质量分数,并判断包装袋上碳酸氢钠含量的标注是否准确。(计算结果百分号前保留一位小数)
4.4
专题六 计算应用题
解:设该小苏打样品中碳酸氢钠的质量为 x。
则该小苏打样品中碳酸氢钠的质量分数为 ,93.3%<99%
答:该小苏打样品中碳酸氢钠的质量分数为 99%,包装袋上碳酸氢钠含量的标注不准确。
专题六 计算应用题
3. 某氯化钠溶液中含有少量氯化钡(BaCl2),学习小组为测定其中氯化钡的质量分数,在50.0 g 该溶液中加入 50.0 g 硫酸钠溶液恰好完全反应,经测定生成沉淀的质量为 4.66 g。请回答下列问题。
(1)反应后溶液的质量为 ______ g。
(2)原氯化钠溶液中氯化钡的质量分数。
95.34
专题六 计算应用题
解:设参加反应的氯化钡的质量为 x。
原氯化钠溶液中氯化钡的质量分数为
答:原氯化钠溶液中氯化钡的质量分数为 8.32%。
专题六 计算应用题
■类型二 实物流程图类
1. 化学兴趣小组为测定一瓶久置过氧化氢溶液的溶质质量分数,进行了如图实验:请分析并计算:
(1)制得氧气的质量是 _______ g。
(2)计算该过氧化氢溶液的溶质质量分数。
2.4
专题六 计算应用题
解:设参加反应的 H2O2 的质量为 x。
该过氧化氢溶液的溶质质量分数为
答:该过氧化氢溶液的溶质质量分数为 5%。
专题六 计算应用题
2.[2024·绥化节选]某毕业班同学去制纯碱化工厂实习,对该厂生产的纯碱产生兴趣,于是取 10.7 g 纯碱样品(含有少量的氯化钠)进行如下探究,完成以下问题。
(1)生成 CO2 的质量为 ________。
(2)该样品中碳酸钠的质量分数是多少?(计算结果百分号前保留一位小数)
4.4 g
专题六 计算应用题
专题六 计算应用题
解::设参加反应的 Na2CO3 的质量为 x。
样品中碳酸钠的质量分数为
答:该样品中碳酸钠的质量分数是99.1%。
3. 某补钙剂的有效成分是碳酸钙,其他成分不含钙且不与稀盐酸反应。 学习小组的同学进行如图所示实验。
(1)产生气体的质量为 _______ g。
(2)计算补钙剂中碳酸钙的质量分数。
1.1
专题六 计算应用题
专题六 计算应用题
解:设 5 g 补钙剂中碳酸钙的质量为 x。
补钙剂中碳酸钙的质量分数为
答:补钙剂中碳酸钙的质量分数为50%。
4.[2024·保定莲池区一模]金属涂层光纤是在光纤的表面涂布 Cu-Al 合金层的光纤。 为测定 Cu-Al 合金样品中铝的质量分数,小明取一定质量的样品放入烧杯中,分 2 次加入质量分数相同的稀硫酸,实验过程如图所示。请计算:
(1)生成氢气的总质量为 _______ g。
(2)Cu-Al 合金样品中铝的质量分数。
0.6
专题六 计算应用题
专题六 计算应用题
解:设 Cu-Al 合金样品中铝的质量为 x。
Cu-Al 合金样品中铝的质量分数为
答:Cu-Al 合金样品中铝的质量分数为 54%
■类型三 表格数据分析类
1.[2024·兰州]兴趣小组同学得知鸡蛋壳的主要成分是碳酸钙,就用它来测定某瓶标签破损的稀盐酸中溶质的质量分数。 称取 5.5 g干燥的鸡蛋壳(杂质不参加反应)于烧杯中,再将 75 g 该稀盐酸分 3 次加入,充分反应后得到实验数据如下:
请计算:
(1)鸡蛋壳中碳酸钙的质量为 _______ g。
5
专题六 计算应用题
解:由题中表格数据分析可知,25 g 稀盐酸能与 2.5 g 碳酸钙恰好完全反应。
设 25 g 稀盐酸中溶质的质量为 x。
该稀盐酸中溶质的质量分数是
答:该稀盐酸中溶质的质量分数是7.3%。
(2)该稀盐酸中溶质的质量分数是多少?
专题六 计算应用题
2. 实验室有一瓶含杂质的高锰酸钾。 某校课外兴趣小组用该试剂加热制取氧气(杂质不参加反应)。 反应过程中固体质量随时间变化的数据见表:
请计算:
(1)反应过程中共制得气体的质量 _____。
(2)该试剂中所含高锰酸钾的质量分数。
6.4 g
专题六 计算应用题
解:设参加反应的高锰酸钾的质量为x。
该药品中所含高锰酸钾的质量分数为
答:该药品中所含高锰酸钾的质量分数为 80%。
专题六 计算应用题
3.[2024·潍坊改编]“金粉”(Cu-Zn 合金)是一种金属颜料,可用于文物修复。 某化学兴趣小组通过实验测定“金粉”中铜的含量:称取25 g“金粉”样品放入锥形瓶中,将 100 g 稀硫酸分 5 次加入,记录每次反应后锥形瓶内物质的总质量。 实验过程和数据如表。
回答下列问题。
专题六 计算应用题
解:根据质量守恒定律,生成氢气的总质量为 25 g+100 g-124.8 g=0.2 g。
设参加反应锌的质量为 x。
故样品中铜的质量分数为
答:样品中铜的质量分数为 74%。
(1)a 的数值为 _____。
(2)计算样品中铜的质量分数。
专题六 计算应用题
104.8
1. 工业上,煅烧石灰石可制生石灰和二氧化碳。某化学兴趣小组在实验室煅烧 25 g 石灰石样品(样品中杂质不反应),在煅烧过程中,剩余固体的质量随时间的变化如图所示。 求:
(1)石灰石完全分解产生的二氧化碳的质量
是 _______ g。
(2)计算 25 g 石灰石样品中碳酸钙的质
量分数。
8.8
专题六 计算应用题
■类型四 坐标曲线类
专题六 计算应用题
解:设 25 g 样品中碳酸钙的质量为 x。
样品中碳酸钙的质量分数为
答:样品中碳酸钙的质量分数为80%。
2.[2024·自贡]实验室现有一瓶失去标签的氢氧化钠溶液,某化学课外活动小组为测定该溶液溶质的质量分数。 取该氢氧化钠溶液20 g,向其中滴加质量分数为 7.3%的稀盐酸,同时测得其 pH 变化与加入稀盐酸的质量关系如图所示。
(1)图中 a 点时所得溶液中溶质为 ________
(填化学式)。
(2)试计算该氢氧化钠溶液溶质的质量分数。
NaCl
专题六 计算应用题
专题六 计算应用题
解:设该氢氧化钠溶液溶质的质量为 x。
该氢氧化钠溶液溶质的质量分数为
答:该氢氧化钠溶液溶质的质量分数为 4%。
3. 学校环保小组检测发现实验室的某酸性废液中含有 CuSO4。 该小组取 100 g 废液,为了测定废液中 CuSO4 的质量分数,逐滴加入KOH 溶 液 至 过 量 。测得生成沉淀(无其他沉淀)的质量与所加 KOH 溶液的质量关系如图所示:
(1)反应结束后生成沉淀质量是 _______ g。
(2)计算废液中 CuSO4 的质量分数。
9.8
专题六 计算应用题
专题六 计算应用题
解:设参加反应的 CuSO4 的质量为 x。
废液中 CuSO4 的质量分数为
答:废液中 CuSO4的质量分数为16%。
4. 将一定质量分数的稀盐酸加入放有一块已生锈铁片的烧杯中,充分反应后,测得生成H2 的质量与稀盐酸的质量关系如图所示(假设铁片除有 Fe2O3 外不含其他杂质)。请回答下列问题。
(1)生成氢气的质量为 _______ g。
(2)计算所用的稀盐酸的溶质质量分数。
0.4
专题六 计算应用题
专题六 计算应用题
解:设与铁反应消耗稀盐酸的溶质质量为 x。
所用稀盐酸的溶质质量分数为
答:所用的稀盐酸的溶质质量分数为 14.6%。
1. 小明为了测定某硫酸溶液中溶质的质量分数,如图甲,向 60 g 硫酸溶液中缓缓注入质量分数为 10%的氢氧化钠溶液,测得溶液的pH 与氢氧化钠溶液的质量对应关系如图乙。 请回答下列问题。
专题六 计算应用题
■类型五 组合类
(1)图乙中 a 点溶液含有的溶质是 ____________________。
(2)请计算硫酸溶液中溶质的质量分数。(计算结果百分号前保留一位小数)
专题六 计算应用题
解:设参加反应的硫酸的质量为 x。
硫酸溶液中溶质的质量分数为
答:硫酸溶液中溶质的质量分数为 4.1%。
氢氧化钠、硫酸钠
2. 航天员王亚平在天和核心舱开展科普实验:将泡腾片塞入一个蓝色水球里,泡腾片逐渐溶解并不断冒泡,水球变成“气泡球”。某兴趣小组为了测定某泡腾片中 NaHCO3 的含量(该泡腾片成分如图所示),先将装有水的烧杯放在电子天平上,再将 10.00 g 该泡腾片投入水中并搅拌,当质量不再变化时,为确保 NaHCO3 完全反应,他又向烧杯中分次加入 10%的稀硫酸,每次加 2.00 g,总质量变化如表所示:
专题六 计算应用题
专题六 计算应用题
【提示】泡腾片中的柠檬酸(用 H3R 表示)溶于水后,与 NaHCO3 反应生成的盐为 Na3R。
(1)泡腾片中的 NaHCO3 在表中 ____(填序号)时已反应完全。
(2)计算这种泡腾片中 NaHCO3 的质量分数。
专题六 计算应用题
③
专题六 计算应用题
解:生成二氧化碳的质量为40.00 g-39.56 g=0.44 g。
设 10.00 g 该泡腾片中NaHCO3 的质量为 x。
则这种泡腾片中 NaHCO3 的质量分数为
答:这种泡腾片中 NaHCO3 的质量分数为 8.4%。
同课章节目录
