2.3.2气体摩尔体积(共33张ppt)化学人教版(2019)必修第一册
文档属性
| 名称 | 2.3.2气体摩尔体积(共33张ppt)化学人教版(2019)必修第一册 |

|
|
| 格式 | pptx | ||
| 文件大小 | 638.2KB | ||
| 资源类型 | 教案 | ||
| 版本资源 | 人教版(2019) | ||
| 科目 | 化学 | ||
| 更新时间 | 2024-12-25 00:00:00 | ||
图片预览







文档简介
(共33张PPT)
第三节 物质的量
第2课时 气体摩尔体积
1.了解气体摩尔体积的含义和应用,体会定量研究对化学科学的重要作用。
2.能运用物质的量、摩尔质量、气体摩尔体积之间的相互关系进行简单计算(重点、难点)
3.理解阿伏加德罗定律及其简单推论(难点)
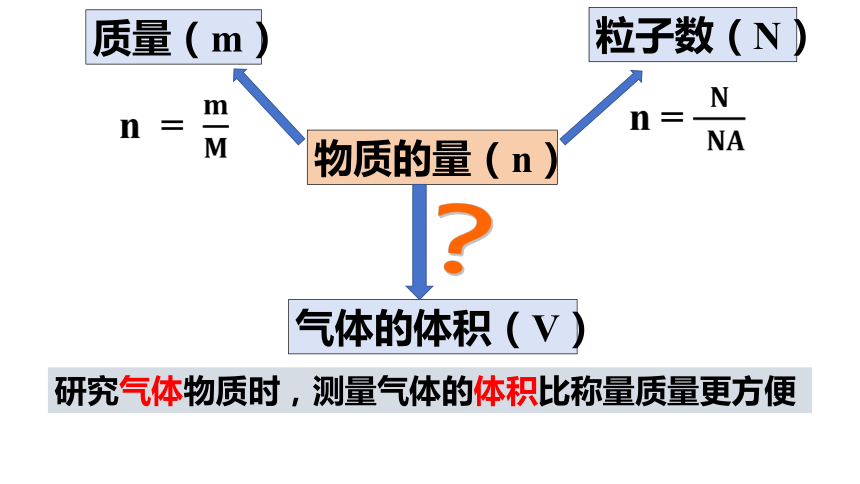
物质的量(n)
质量(m)
粒子数(N)
气体的体积(V)
n =
n =
?
研究气体物质时,测量气体的体积比称量质量更方便
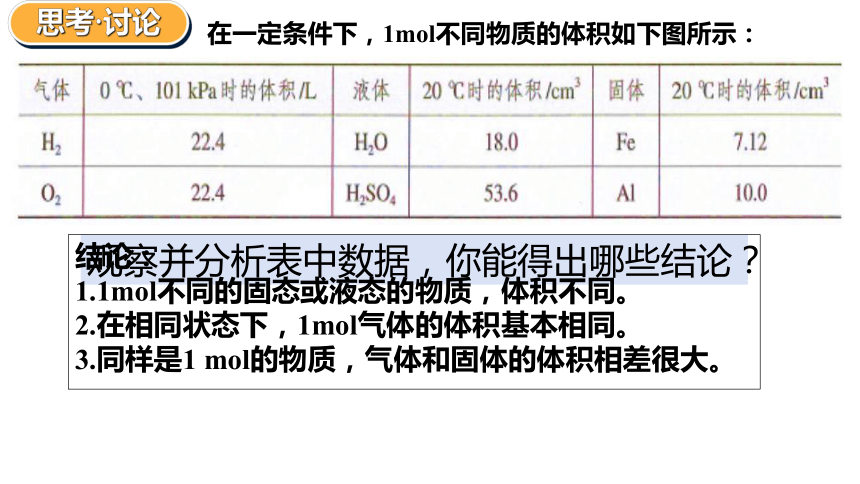
在一定条件下,1mol不同物质的体积如下图所示:
思考·讨论
观察并分析表中数据,你能得出哪些结论?
结论:
1.1mol不同的固态或液态的物质,体积不同。
2.在相同状态下,1mol气体的体积基本相同。
3.同样是1 mol的物质,气体和固体的体积相差很大。
思考·交流
1、影响物质体积大小的因素有哪些?
2、为什么在相同的外界条件下:
1mol固、液态物质所具有的的体积不同,
而1mol气态物质所具有的体积却基本相同?
1个乒乓球所占的体积和1个篮球所占的体积哪个大?
影响物质体积大小的因素:①粒子本身的大小
10个乒乓球所占的体积和1个乒乓球所占的体积哪个大?
影响物质体积大小的因素:②粒子数目
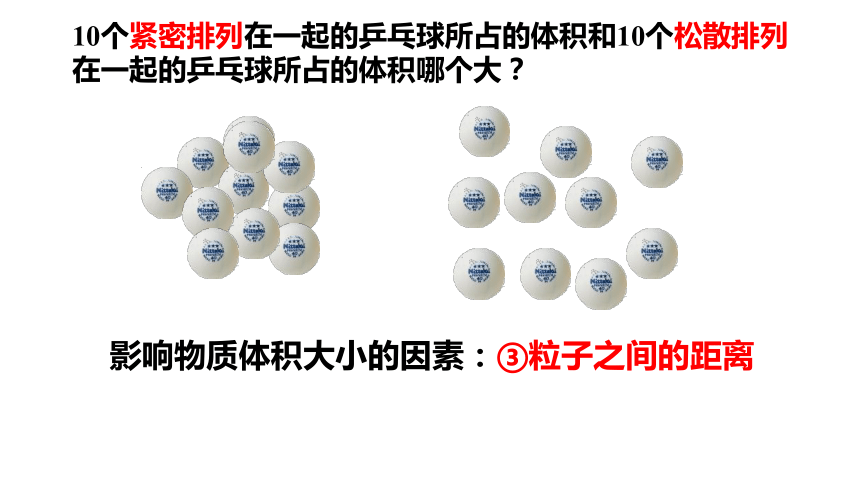
10个紧密排列在一起的乒乓球所占的体积和10个松散排列在一起的乒乓球所占的体积哪个大?
影响物质体积大小的因素:③粒子之间的距离
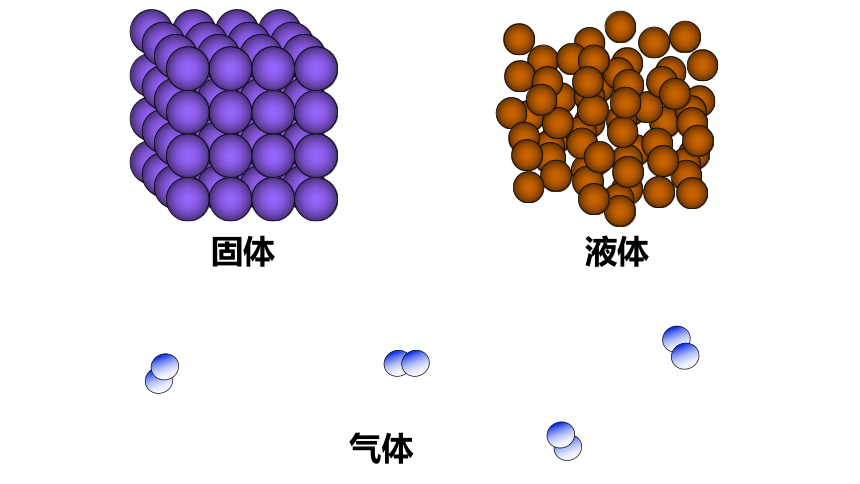
固体
液体
气体
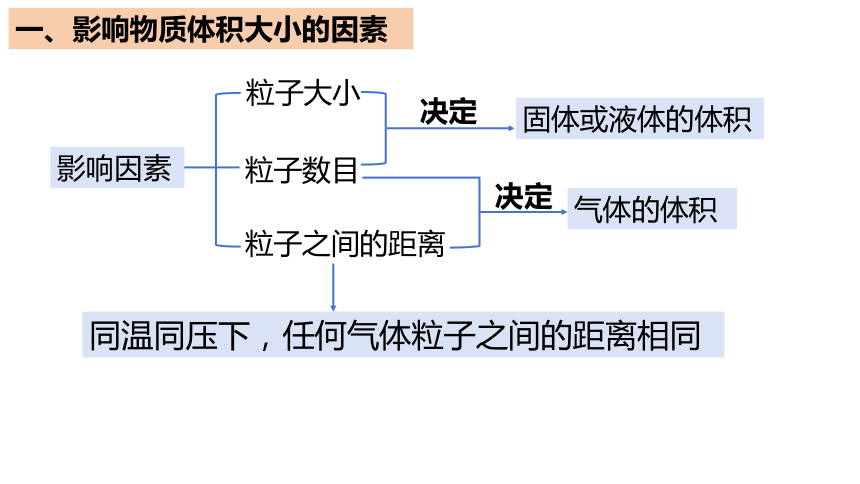
一、影响物质体积大小的因素
影响因素
粒子大小
粒子数目
粒子之间的距离
固体或液体的体积
气体的体积
决定
决定
同温同压下,任何气体粒子之间的距离相同
相同
粒子大小
不相同
粒子间的距离
在同温同压下,下列与气体体积大小有关的因素是( )
A 气体的种类 B 气体的分子数
C 分子本身的大小 D分子间的平均距离
B
两种气体体积相同,所含分子数一定相同吗?
思考·交流
粒子数目
粒子之间的距离
气体的体积
决定
温度、压强
决定
变大
增大
变小
减小
减小
相等
温度
压强
相同的体积
相同数目
二、阿伏加德罗定律
1、含义:同温同压下,相同体积的任何气体都含有相同数目的粒子。
“三同”
定
“一同”
同温
同压
同体积
同分子数
2、适用范围:只适用于气体,可以是单一气体,也可以是混合气体。
D
B
3、同温同压下,相同体积的氢气和甲烷的
原子个数之比为( )
A 2:5 B 1:1 C 1:5 D 1:8
A
3、阿伏加德罗定律的推论
依据: PV=nRT(理想气体状态方程,其中R为常数)
1、同温同压下,相同体积的H2和CO2气体,具有相同的 ( )
A.分子数 B.原子数
C.质量 D.摩尔质量
A
2、在相同的温度和压强下,下列气体密度最小的( )
A CO2 B H2 C O2 D Cl2
B
3、同温同压下,等质量的SO2和CO2相比较,下列叙述正确的是( )
A 体积比1:1 B 体积比11:16
C 密度比16:11 D 密度比11:16
BC
4、在同温同压下,相同质量的下列气体,占有的体积由大到小的顺序是 .
①Cl2 ②N2 ③H2 ④CO2 ⑤O2
③>②>⑤>④>①
5、同温同压下,将1体积的CO2和2体积的CO进行比较,则CO2与CO的:
(1)分子数之比为 ;
(2)原子数之比为 ;
(3)质量之比为 ___________;
(4)物质的量之比为——————;
(5)密度之比为 ___________;
(6)摩尔质量之比为——————;
1:2
3:4
11:14
1:2
11:7
11:7
三、气体摩尔体积(Vm)
1、定义:单位物质的量(1mol)的气体所占的体积。
2、单位:L / mol( L · mol-1 )或 m3/mol
3、公式: Vm=
V
n
4、影响 Vm 的因素:温度和压强
5、标准状况下(0 ℃ 1.01 kPa),1mol任何气体所占的体积都约为22.4 L。即标况下,气体的摩尔体积 Vm≈ 22.4 L/mol。
思考·交流
气体在非标准状况下的气体摩尔体积一定不为22.4 L/mol吗?
不一定.升高温度,体积增大,增大压强,体积减小,所以在适当的压强和温度下,气体的摩尔体积也可能为22.4 L/mol.
1. 标准状况下,1mol任何物质的体积都约是22.4L。
2. 1mol气体的体积约为22.4L。
(缺标况)
3. 标准状况下,1molO2和N2混合气体的体积约为22.4L。
4. 22.4L气体所含分子数一定大于11.2L气体所含的分子数。
5. 标准状况下,气体的摩尔体积都是22.4L。
6. 只有在标准状况下,气体的摩尔体积才可能约为22.4L/mol。
判断正误
×
×
√
×
×
×
课堂小结
气体的体积
物质的量
质量
分子数
摩尔质量
(1)
(2)
(4)
(3)
(1)标况下,0.5molH2占有的体积是 L
(2)标况下,2molO2占有的体积是 L
(3)标况下,4.48L CO2的物质的量是 mol
(4)标况下,33.6L H2的物质的量是 mol
(5)标况下,16gO2 的体积为 L
(6)标况下,11.2LN2 中含有N2分子的个数是__________个
练一练
11.2
44.8
0.2
1.5
11.2
3.01×1023
(7)标况下,0.5mol N2和1mol O2 的混合气体的体积为______L
33.6
2、标准状况下, 112 mL 某气体的质量为 0 . 14 g , 则其摩尔质量为 ,相对分子质量为 。
解:
n =
V
Vm
=
0 . 112 L
22 . 4 L · mol -1
n = m / M
M =
0 . 14 g
0 . 005 mol
=
A
D
B
D
1:1
1:1
5:3
4:11
4:11
H2
H2
H2O
H2O
第三节 物质的量
第2课时 气体摩尔体积
1.了解气体摩尔体积的含义和应用,体会定量研究对化学科学的重要作用。
2.能运用物质的量、摩尔质量、气体摩尔体积之间的相互关系进行简单计算(重点、难点)
3.理解阿伏加德罗定律及其简单推论(难点)
物质的量(n)
质量(m)
粒子数(N)
气体的体积(V)
n =
n =
?
研究气体物质时,测量气体的体积比称量质量更方便
在一定条件下,1mol不同物质的体积如下图所示:
思考·讨论
观察并分析表中数据,你能得出哪些结论?
结论:
1.1mol不同的固态或液态的物质,体积不同。
2.在相同状态下,1mol气体的体积基本相同。
3.同样是1 mol的物质,气体和固体的体积相差很大。
思考·交流
1、影响物质体积大小的因素有哪些?
2、为什么在相同的外界条件下:
1mol固、液态物质所具有的的体积不同,
而1mol气态物质所具有的体积却基本相同?
1个乒乓球所占的体积和1个篮球所占的体积哪个大?
影响物质体积大小的因素:①粒子本身的大小
10个乒乓球所占的体积和1个乒乓球所占的体积哪个大?
影响物质体积大小的因素:②粒子数目
10个紧密排列在一起的乒乓球所占的体积和10个松散排列在一起的乒乓球所占的体积哪个大?
影响物质体积大小的因素:③粒子之间的距离
固体
液体
气体
一、影响物质体积大小的因素
影响因素
粒子大小
粒子数目
粒子之间的距离
固体或液体的体积
气体的体积
决定
决定
同温同压下,任何气体粒子之间的距离相同
相同
粒子大小
不相同
粒子间的距离
在同温同压下,下列与气体体积大小有关的因素是( )
A 气体的种类 B 气体的分子数
C 分子本身的大小 D分子间的平均距离
B
两种气体体积相同,所含分子数一定相同吗?
思考·交流
粒子数目
粒子之间的距离
气体的体积
决定
温度、压强
决定
变大
增大
变小
减小
减小
相等
温度
压强
相同的体积
相同数目
二、阿伏加德罗定律
1、含义:同温同压下,相同体积的任何气体都含有相同数目的粒子。
“三同”
定
“一同”
同温
同压
同体积
同分子数
2、适用范围:只适用于气体,可以是单一气体,也可以是混合气体。
D
B
3、同温同压下,相同体积的氢气和甲烷的
原子个数之比为( )
A 2:5 B 1:1 C 1:5 D 1:8
A
3、阿伏加德罗定律的推论
依据: PV=nRT(理想气体状态方程,其中R为常数)
1、同温同压下,相同体积的H2和CO2气体,具有相同的 ( )
A.分子数 B.原子数
C.质量 D.摩尔质量
A
2、在相同的温度和压强下,下列气体密度最小的( )
A CO2 B H2 C O2 D Cl2
B
3、同温同压下,等质量的SO2和CO2相比较,下列叙述正确的是( )
A 体积比1:1 B 体积比11:16
C 密度比16:11 D 密度比11:16
BC
4、在同温同压下,相同质量的下列气体,占有的体积由大到小的顺序是 .
①Cl2 ②N2 ③H2 ④CO2 ⑤O2
③>②>⑤>④>①
5、同温同压下,将1体积的CO2和2体积的CO进行比较,则CO2与CO的:
(1)分子数之比为 ;
(2)原子数之比为 ;
(3)质量之比为 ___________;
(4)物质的量之比为——————;
(5)密度之比为 ___________;
(6)摩尔质量之比为——————;
1:2
3:4
11:14
1:2
11:7
11:7
三、气体摩尔体积(Vm)
1、定义:单位物质的量(1mol)的气体所占的体积。
2、单位:L / mol( L · mol-1 )或 m3/mol
3、公式: Vm=
V
n
4、影响 Vm 的因素:温度和压强
5、标准状况下(0 ℃ 1.01 kPa),1mol任何气体所占的体积都约为22.4 L。即标况下,气体的摩尔体积 Vm≈ 22.4 L/mol。
思考·交流
气体在非标准状况下的气体摩尔体积一定不为22.4 L/mol吗?
不一定.升高温度,体积增大,增大压强,体积减小,所以在适当的压强和温度下,气体的摩尔体积也可能为22.4 L/mol.
1. 标准状况下,1mol任何物质的体积都约是22.4L。
2. 1mol气体的体积约为22.4L。
(缺标况)
3. 标准状况下,1molO2和N2混合气体的体积约为22.4L。
4. 22.4L气体所含分子数一定大于11.2L气体所含的分子数。
5. 标准状况下,气体的摩尔体积都是22.4L。
6. 只有在标准状况下,气体的摩尔体积才可能约为22.4L/mol。
判断正误
×
×
√
×
×
×
课堂小结
气体的体积
物质的量
质量
分子数
摩尔质量
(1)
(2)
(4)
(3)
(1)标况下,0.5molH2占有的体积是 L
(2)标况下,2molO2占有的体积是 L
(3)标况下,4.48L CO2的物质的量是 mol
(4)标况下,33.6L H2的物质的量是 mol
(5)标况下,16gO2 的体积为 L
(6)标况下,11.2LN2 中含有N2分子的个数是__________个
练一练
11.2
44.8
0.2
1.5
11.2
3.01×1023
(7)标况下,0.5mol N2和1mol O2 的混合气体的体积为______L
33.6
2、标准状况下, 112 mL 某气体的质量为 0 . 14 g , 则其摩尔质量为 ,相对分子质量为 。
解:
n =
V
Vm
=
0 . 112 L
22 . 4 L · mol -1
n = m / M
M =
0 . 14 g
0 . 005 mol
=
A
D
B
D
1:1
1:1
5:3
4:11
4:11
H2
H2
H2O
H2O
