2025年九年级中考化学专题复习 构成物质的微观粒子 课件(共26张PPT)
文档属性
| 名称 | 2025年九年级中考化学专题复习 构成物质的微观粒子 课件(共26张PPT) |  | |
| 格式 | pptx | ||
| 文件大小 | 587.3KB | ||
| 资源类型 | 教案 | ||
| 版本资源 | 通用版 | ||
| 科目 | 化学 | ||
| 更新时间 | 2024-12-25 21:00:38 | ||
图片预览







文档简介
(共26张PPT)
构成物质的微观粒子
实验 分子运动现象的实验
1. 品红分子在水中运动的实验
如图实验,实验中的变量为 ________________________,观察到的实验现象为 ________________________________________________,该实验得出的结论是 ___________________________________________________________。
第 10 讲 构成物质的微观粒子
热水中的品红比冷水中的品红扩散得快
水的温度
温度越高,分子运动速率越快
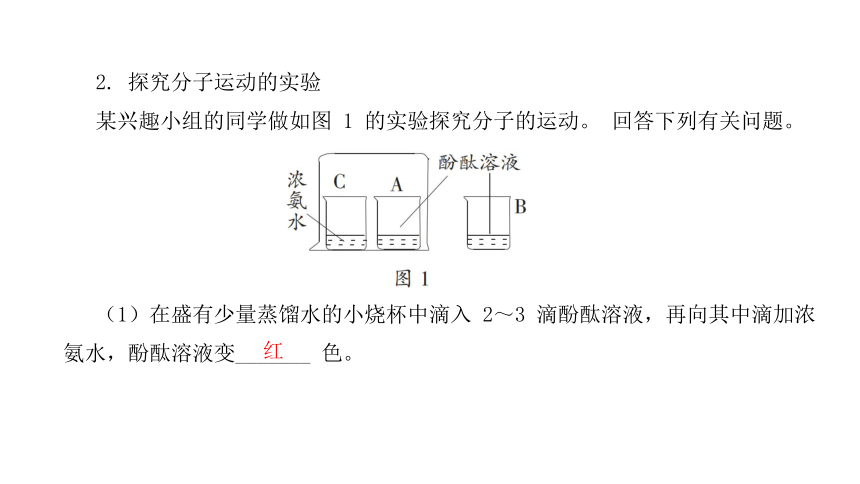
2. 探究分子运动的实验
某兴趣小组的同学做如图 1 的实验探究分子的运动。 回答下列有关问题。
(1)在盛有少量蒸馏水的小烧杯中滴入 2~3 滴酚酞溶液,再向其中滴加浓氨水,酚酞溶液变_______ 色。
第 10 讲 构成物质的微观粒子
红
(2)在盛有少量蒸馏水的小烧杯 A、B 中滴入2~3 滴酚酞溶液,再向 C 烧杯其中滴加约5 mL 浓氨水。 如图 1 所示,几分钟后观察到的现象是 _______________________________________________________;产生这一现象的原因是 _______________________________________________________。
(3)该实验证明了 _______________________________________________(写一条)。
第 10 讲 构成物质的微观粒子
烧杯 A 中的酚酞溶液变红色,烧杯 B 中的酚酞溶液不变色
氨分子在不断运动,运动到 A 中形成氨水,使酚酞溶液变红
(3)分子是不断运动的(或浓氨水具有挥发性)
(4)[创新装置]用滤纸折叠成两朵大小相同的纸花,在纸花上都均匀喷洒酚酞溶液,用细线将纸花固定在两个相同的塑料瓶内,按照图 4 的操作方式分别用注射器向图 2 和图 3的塑料瓶中同时注入 5 滴浓氨水,然后将针孔处密封,再将两个塑料瓶分别同时放入等体积的冷水和 40 ℃的热水中。
创新考法
第 10 讲 构成物质的微观粒子
①两瓶中观察到的相同现象是 ________________________。
②与实验图 1 相比,改进后的图 2、3 所示实验的主要优点是 _____________________________________________________(写一条)。
第 10 讲 构成物质的微观粒子
小纸花由下而上依次变红
减少对环境的污染(或节约试剂)
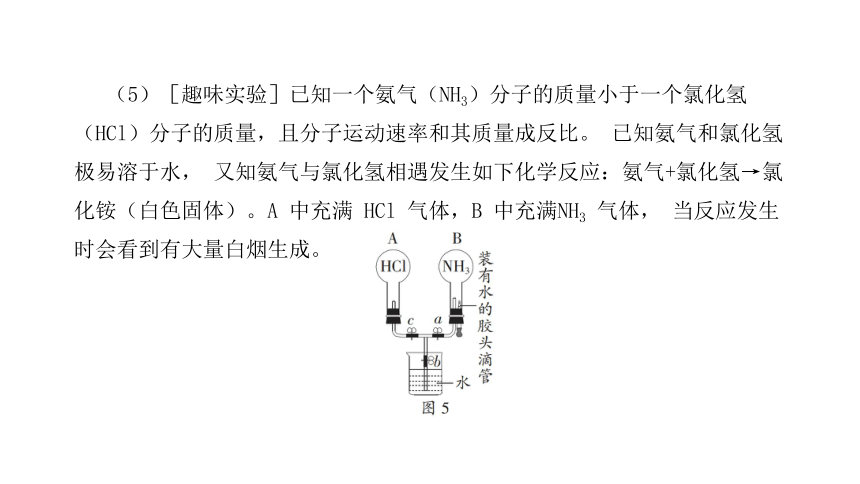
(5)[趣味实验]已知一个氨气(NH3)分子的质量小于一个氯化氢(HCl)分子的质量,且分子运动速率和其质量成反比。 已知氨气和氯化氢极易溶于水, 又知氨气与氯化氢相遇发生如下化学反应:氨气+氯化氢→氯化铵(白色固体)。A 中充满 HCl 气体,B 中充满NH3 气体, 当反应发生时会看到有大量白烟生成。
第 10 讲 构成物质的微观粒子
实验装置如图 5 所示。 若要在该装置中产生白烟现象,进行的操作是 ______________________________________;白烟首先产生在 _____(选填“A”或“B”)瓶,原因是 _____________________________________________________________________________________________________________________________。
第 10 讲 构成物质的微观粒子
关闭弹簧夹 b,同时打开弹簧夹a 和 c
A
分子是在不断运动的,氨气分子的质量小于氯化氢分子的质量,则氨气分子运动速率较快,氨气分子首先到达 A 瓶中,在此二者发生反应
■题型一 用微粒的观点解释现象
第 10 讲 构成物质的微观粒子
思路点拨
题型解法
1. 由分子构成的物质,在发生三态变化时,分子间的间隔大小发生变化,分子本身的体积、种类、质量、数目均不变。
2. 物质不管是固态、液态还是气态,都在不断地运动,分子运动的速率与温度有关,温度越高分子运动越快。
第 10 讲 构成物质的微观粒子
例 1 [2024·河北 10 题]2024 年 6 月 2 日,“嫦娥六号”在月球背面成功着陆,当环境温度过高时,其自备的降温装置能通过冰的升华达到降温目的。 冰升华的过程中,水分子的 ( )
A. 间隔增大 B. 质量增大 C. 种类改变 D. 数目改变
A
衍生一 多情境组合
下列对于宏观现象的微观解释中错误的是 ( )
A. 皮球在阳光下胀大———分子间的间隔增大
B. 氧气助燃,氢气可燃———分子种类不同,物质化学性质不同
C. 矿石能被粉碎———分子可以再分
D. 用扫描隧道显微镜才能观测到苯分子———分子的体积很小
C
第 10 讲 构成物质的微观粒子
衍生二 实验探究
空气受热实验如图。 从微观角度分析,正确的是( )
A. 分子体积变大 B. 分子个数增多
C. 分子运动加快 D. 分子种类改变
C
第 10 讲 构成物质的微观粒子
■题型二 考查微观粒子结构示意图
题型解法
1. 原子由原子核与核外电子构成,原子核一般由质子和中子构成,原子中质子数=核外电子数,原子的相对原子质量约等于质子数与中子数的和。
2. 具有多个电子的原子,其核外电子分层排布:第一层最多 排 2 个电子,第二层最多排 8 个电子,第三层最多排18个电子,最外层不能超过8,排满第一层再排第二层,依此类推。
3. 原子的核外电子层数与元素在元素周期表中所处的周期数相等。
4. 核内质子数=核外电子数为原子,核内质子数>核外电子数为阳离子,核内质子数<核外电子数为阴离子。
第 10 讲 构成物质的微观粒子
例 2 高精度地磁监测系统可实现“震前”预报,该仪器的材料中含有金属钴,钴原子的结构示意图如图所示,下列有关说法正确的是( )
A. x 的数值为 8
B. 钴原子核外有 4 个电子层
C. 钴在化学反应中容易得到电子
D. 钴原子的中子数为 27
B
第 10 讲 构成物质的微观粒子
C
类题一 如图是四种微粒结构示意图,下列有关各微粒的说法,正确的是 ( )
A. ③④不属于同种元素
B. ④对应的元素位于第 2 周期
C. ①④都达到了相对稳定结构
D. 以上四种微观粒子中不含阳离子
C
第 10 讲 构成物质的微观粒子
类题二 对下列微观粒子示意图的理解正确的是 ( )
A.与 示意图对应的微观粒子符号为 O2-
B. 表示阳离子结构示意图
C. 表示钠原子结构示意图,该微观粒子在化学反应中易失去最外层的电子
D. 和 两种微观粒子核外电子数相同,属于同种元素的微观粒子
A
第 10 讲 构成物质的微观粒子
■考点 构成物质的粒子(必考)
分子
定义:保持物质①__________的最小粒子
化学性质
第 10 讲 构成物质的微观粒子
基本性质及其应用
分子的体积和质量都很②_____。
分子总是在不断③ ________ 着。且温度越高,分子运动的速率越④______。
分子之间有⑤__________,分子间的间隔与物质的状态有关,一般气体物质分子间的间隔最大。
分子运动现象的探究(详见本讲中基础实验过关 )
小
运动
快
间隔
由于气体分子间的间隔>液体分子间的间隔,所以气体比液体更容易被压缩。
满分备考
第 10 讲 构成物质的微观粒子
1. 1 滴水中有 1.67×1021 个水分子,说明 ___________
____________。
2. 湿衣服在阳光下干得快,说明 _________________________________。
3. 6 000 L 氧气在加压后可压缩在 40 L 钢瓶中,说明 __________________。
小实例辨析
分子很小
温度越高,分子运动速率越快
分子之间有间隔
定义:⑥_________ 中的最小粒子
化学变化
第 10 讲 构成物质的微观粒子
构成
⑦_________:每个质子带1个单位正电荷
⑧_________:不带带电
核外电子:每个电子带一个单位负电荷,电子分层排布,⑨________________ 决定元素的化学性质
⑩________ =核内质子数=核外电子
原子核
原子结构示意图: 图示粒子为 ______,核外有 ___ 个电子层,核外共有 ____个电子,核内质子数为 ____,最外层电子数为 ____,核电荷数为 ______,在化学反应中易 ________(选填“得到”或“失去”)电子。
质子
中子
最外层电子数
核电荷数
钠原子
3
11
11
1
11
失去
原子
原子的结构
最外层电子数 元素的种类 原子得失电子的情况
n<4(氢、氦、硼除外) 金属元素 易失去电子
4n=8(氦为 2) 稀有气体元素 不易得失电子(相对稳定结构)
第 10 讲 构成物质的微观粒子
最外层电子数(n)的应用
近似计算式:相对原子质量≈ __________+ _________
单位:相对原子质量单位为“ ______”,一般省略不写
相对原子质量
该原子的实际质量
一种碳-12原子质量的
表达式:某原子的相对原子质量=
中子数
质子数
1
离子
概念:带电的 ______(或原子团)叫做离子
原子
第 10 讲 构成物质的微观粒子
分类
阳离子:带 _________ 的离子,如 Na+、Mg2+等
阴离子:带 _________ 的离子,如 Cl-、O2-等
写法:在元素符号的 _________ 写上所带的电荷数和电性符号。先写
_______,后写 __________,当数字为1时,通常省略不写
意义:如 Na+表示 ______________________________
27
正电荷
负电荷
右上角
25
26
24
23
22
21
数字
正负符号
一个钠离子带一个单位正电荷
判断一种粒子是原子还是阳离子、阴离子,关键要看质子数和核外电子数的关系:若该粒子的质子数等于核外电子数,则为 原子;若该粒子的质子数大于核外电子数,则为阳离子;若该粒子的质子数小于核外电子数,则为阴离子。
满分备考
第 10 讲 构成物质的微观粒子
第 10 讲 构成物质的微观粒子
粒子种类 分子 原子 离子
区别 化学变化中 可以再分 不可再分 原子团在有些变化中可以再分
电性 不显电性 不显电性 阳离子带正电;阴离子带负电
相同点 a. 都是构成物质的微粒;b. 都在不断运动着;c. 微粒间都有一定的间隔;d. 都有一定的质量;e. 微粒都很小
联系
分子、原子与离子的区别与联系
易错归纳
判断下列说法是否正确,正确的打“√”,错误的打“×”并改正或举出反例。
1. 分子和原子可以构成物质,则物质都是由分子和原子构成的。( )
_________________________________________________________________
2. 分子在 0 ℃时停止运动。 ( )
____________________________________________________________________
3. 分子可以再分,原子不可以再分。 ( )
___________________________________________________________________
______________
×
离子也可以构成物质,如氯化钠是由钠离子和氯离子构成的。
×
分子在不断地运动,0 ℃时也在不断运动。
×
在化学变化中分子可以再分,原子不可以再分。 抛开化学变化这个前提,原子可以再分。
第 10 讲 构成物质的微观粒子
4. 原子不能保持物质的化学性质。 ( )
_________________________________________________________________
5. 质子数相同的两种微观粒子,其核外电子数一定相等。 ( )
_________________________________________________________________
______________________________________________
6. 物质的状态变化、热胀冷缩都是由分子的大小发生改变引起的。( )
__________________________________________________________________
×
由原子构成的物质,原子保持物质的化学性质,如铜。
×
物质的状态变化、热胀冷缩是分子间的间隔发生改变,分子的大小不变。
×
第 10 讲 构成物质的微观粒子
质子数相同的两种微观粒子,其核外电子数不一定相等,如钠原子与钠离子,质子数相同,但核外电子数不同。
7. 相对原子质量就是原子的实际质量。 ( )
_________________________________________________________________
_____________________________
8. 中子数等于质子数。 ( )
_______________________________________________________________
×
中子数不一定等于质子数。
×
第 10 讲 构成物质的微观粒子
相对原子质量等于该原子的实际质量与一种碳-12 原子质量的1/12 的比值,不是原子的实际质量。
构成物质的微观粒子
实验 分子运动现象的实验
1. 品红分子在水中运动的实验
如图实验,实验中的变量为 ________________________,观察到的实验现象为 ________________________________________________,该实验得出的结论是 ___________________________________________________________。
第 10 讲 构成物质的微观粒子
热水中的品红比冷水中的品红扩散得快
水的温度
温度越高,分子运动速率越快
2. 探究分子运动的实验
某兴趣小组的同学做如图 1 的实验探究分子的运动。 回答下列有关问题。
(1)在盛有少量蒸馏水的小烧杯中滴入 2~3 滴酚酞溶液,再向其中滴加浓氨水,酚酞溶液变_______ 色。
第 10 讲 构成物质的微观粒子
红
(2)在盛有少量蒸馏水的小烧杯 A、B 中滴入2~3 滴酚酞溶液,再向 C 烧杯其中滴加约5 mL 浓氨水。 如图 1 所示,几分钟后观察到的现象是 _______________________________________________________;产生这一现象的原因是 _______________________________________________________。
(3)该实验证明了 _______________________________________________(写一条)。
第 10 讲 构成物质的微观粒子
烧杯 A 中的酚酞溶液变红色,烧杯 B 中的酚酞溶液不变色
氨分子在不断运动,运动到 A 中形成氨水,使酚酞溶液变红
(3)分子是不断运动的(或浓氨水具有挥发性)
(4)[创新装置]用滤纸折叠成两朵大小相同的纸花,在纸花上都均匀喷洒酚酞溶液,用细线将纸花固定在两个相同的塑料瓶内,按照图 4 的操作方式分别用注射器向图 2 和图 3的塑料瓶中同时注入 5 滴浓氨水,然后将针孔处密封,再将两个塑料瓶分别同时放入等体积的冷水和 40 ℃的热水中。
创新考法
第 10 讲 构成物质的微观粒子
①两瓶中观察到的相同现象是 ________________________。
②与实验图 1 相比,改进后的图 2、3 所示实验的主要优点是 _____________________________________________________(写一条)。
第 10 讲 构成物质的微观粒子
小纸花由下而上依次变红
减少对环境的污染(或节约试剂)
(5)[趣味实验]已知一个氨气(NH3)分子的质量小于一个氯化氢(HCl)分子的质量,且分子运动速率和其质量成反比。 已知氨气和氯化氢极易溶于水, 又知氨气与氯化氢相遇发生如下化学反应:氨气+氯化氢→氯化铵(白色固体)。A 中充满 HCl 气体,B 中充满NH3 气体, 当反应发生时会看到有大量白烟生成。
第 10 讲 构成物质的微观粒子
实验装置如图 5 所示。 若要在该装置中产生白烟现象,进行的操作是 ______________________________________;白烟首先产生在 _____(选填“A”或“B”)瓶,原因是 _____________________________________________________________________________________________________________________________。
第 10 讲 构成物质的微观粒子
关闭弹簧夹 b,同时打开弹簧夹a 和 c
A
分子是在不断运动的,氨气分子的质量小于氯化氢分子的质量,则氨气分子运动速率较快,氨气分子首先到达 A 瓶中,在此二者发生反应
■题型一 用微粒的观点解释现象
第 10 讲 构成物质的微观粒子
思路点拨
题型解法
1. 由分子构成的物质,在发生三态变化时,分子间的间隔大小发生变化,分子本身的体积、种类、质量、数目均不变。
2. 物质不管是固态、液态还是气态,都在不断地运动,分子运动的速率与温度有关,温度越高分子运动越快。
第 10 讲 构成物质的微观粒子
例 1 [2024·河北 10 题]2024 年 6 月 2 日,“嫦娥六号”在月球背面成功着陆,当环境温度过高时,其自备的降温装置能通过冰的升华达到降温目的。 冰升华的过程中,水分子的 ( )
A. 间隔增大 B. 质量增大 C. 种类改变 D. 数目改变
A
衍生一 多情境组合
下列对于宏观现象的微观解释中错误的是 ( )
A. 皮球在阳光下胀大———分子间的间隔增大
B. 氧气助燃,氢气可燃———分子种类不同,物质化学性质不同
C. 矿石能被粉碎———分子可以再分
D. 用扫描隧道显微镜才能观测到苯分子———分子的体积很小
C
第 10 讲 构成物质的微观粒子
衍生二 实验探究
空气受热实验如图。 从微观角度分析,正确的是( )
A. 分子体积变大 B. 分子个数增多
C. 分子运动加快 D. 分子种类改变
C
第 10 讲 构成物质的微观粒子
■题型二 考查微观粒子结构示意图
题型解法
1. 原子由原子核与核外电子构成,原子核一般由质子和中子构成,原子中质子数=核外电子数,原子的相对原子质量约等于质子数与中子数的和。
2. 具有多个电子的原子,其核外电子分层排布:第一层最多 排 2 个电子,第二层最多排 8 个电子,第三层最多排18个电子,最外层不能超过8,排满第一层再排第二层,依此类推。
3. 原子的核外电子层数与元素在元素周期表中所处的周期数相等。
4. 核内质子数=核外电子数为原子,核内质子数>核外电子数为阳离子,核内质子数<核外电子数为阴离子。
第 10 讲 构成物质的微观粒子
例 2 高精度地磁监测系统可实现“震前”预报,该仪器的材料中含有金属钴,钴原子的结构示意图如图所示,下列有关说法正确的是( )
A. x 的数值为 8
B. 钴原子核外有 4 个电子层
C. 钴在化学反应中容易得到电子
D. 钴原子的中子数为 27
B
第 10 讲 构成物质的微观粒子
C
类题一 如图是四种微粒结构示意图,下列有关各微粒的说法,正确的是 ( )
A. ③④不属于同种元素
B. ④对应的元素位于第 2 周期
C. ①④都达到了相对稳定结构
D. 以上四种微观粒子中不含阳离子
C
第 10 讲 构成物质的微观粒子
类题二 对下列微观粒子示意图的理解正确的是 ( )
A.与 示意图对应的微观粒子符号为 O2-
B. 表示阳离子结构示意图
C. 表示钠原子结构示意图,该微观粒子在化学反应中易失去最外层的电子
D. 和 两种微观粒子核外电子数相同,属于同种元素的微观粒子
A
第 10 讲 构成物质的微观粒子
■考点 构成物质的粒子(必考)
分子
定义:保持物质①__________的最小粒子
化学性质
第 10 讲 构成物质的微观粒子
基本性质及其应用
分子的体积和质量都很②_____。
分子总是在不断③ ________ 着。且温度越高,分子运动的速率越④______。
分子之间有⑤__________,分子间的间隔与物质的状态有关,一般气体物质分子间的间隔最大。
分子运动现象的探究(详见本讲中基础实验过关 )
小
运动
快
间隔
由于气体分子间的间隔>液体分子间的间隔,所以气体比液体更容易被压缩。
满分备考
第 10 讲 构成物质的微观粒子
1. 1 滴水中有 1.67×1021 个水分子,说明 ___________
____________。
2. 湿衣服在阳光下干得快,说明 _________________________________。
3. 6 000 L 氧气在加压后可压缩在 40 L 钢瓶中,说明 __________________。
小实例辨析
分子很小
温度越高,分子运动速率越快
分子之间有间隔
定义:⑥_________ 中的最小粒子
化学变化
第 10 讲 构成物质的微观粒子
构成
⑦_________:每个质子带1个单位正电荷
⑧_________:不带带电
核外电子:每个电子带一个单位负电荷,电子分层排布,⑨________________ 决定元素的化学性质
⑩________ =核内质子数=核外电子
原子核
原子结构示意图: 图示粒子为 ______,核外有 ___ 个电子层,核外共有 ____个电子,核内质子数为 ____,最外层电子数为 ____,核电荷数为 ______,在化学反应中易 ________(选填“得到”或“失去”)电子。
质子
中子
最外层电子数
核电荷数
钠原子
3
11
11
1
11
失去
原子
原子的结构
最外层电子数 元素的种类 原子得失电子的情况
n<4(氢、氦、硼除外) 金属元素 易失去电子
4
第 10 讲 构成物质的微观粒子
最外层电子数(n)的应用
近似计算式:相对原子质量≈ __________+ _________
单位:相对原子质量单位为“ ______”,一般省略不写
相对原子质量
该原子的实际质量
一种碳-12原子质量的
表达式:某原子的相对原子质量=
中子数
质子数
1
离子
概念:带电的 ______(或原子团)叫做离子
原子
第 10 讲 构成物质的微观粒子
分类
阳离子:带 _________ 的离子,如 Na+、Mg2+等
阴离子:带 _________ 的离子,如 Cl-、O2-等
写法:在元素符号的 _________ 写上所带的电荷数和电性符号。先写
_______,后写 __________,当数字为1时,通常省略不写
意义:如 Na+表示 ______________________________
27
正电荷
负电荷
右上角
25
26
24
23
22
21
数字
正负符号
一个钠离子带一个单位正电荷
判断一种粒子是原子还是阳离子、阴离子,关键要看质子数和核外电子数的关系:若该粒子的质子数等于核外电子数,则为 原子;若该粒子的质子数大于核外电子数,则为阳离子;若该粒子的质子数小于核外电子数,则为阴离子。
满分备考
第 10 讲 构成物质的微观粒子
第 10 讲 构成物质的微观粒子
粒子种类 分子 原子 离子
区别 化学变化中 可以再分 不可再分 原子团在有些变化中可以再分
电性 不显电性 不显电性 阳离子带正电;阴离子带负电
相同点 a. 都是构成物质的微粒;b. 都在不断运动着;c. 微粒间都有一定的间隔;d. 都有一定的质量;e. 微粒都很小
联系
分子、原子与离子的区别与联系
易错归纳
判断下列说法是否正确,正确的打“√”,错误的打“×”并改正或举出反例。
1. 分子和原子可以构成物质,则物质都是由分子和原子构成的。( )
_________________________________________________________________
2. 分子在 0 ℃时停止运动。 ( )
____________________________________________________________________
3. 分子可以再分,原子不可以再分。 ( )
___________________________________________________________________
______________
×
离子也可以构成物质,如氯化钠是由钠离子和氯离子构成的。
×
分子在不断地运动,0 ℃时也在不断运动。
×
在化学变化中分子可以再分,原子不可以再分。 抛开化学变化这个前提,原子可以再分。
第 10 讲 构成物质的微观粒子
4. 原子不能保持物质的化学性质。 ( )
_________________________________________________________________
5. 质子数相同的两种微观粒子,其核外电子数一定相等。 ( )
_________________________________________________________________
______________________________________________
6. 物质的状态变化、热胀冷缩都是由分子的大小发生改变引起的。( )
__________________________________________________________________
×
由原子构成的物质,原子保持物质的化学性质,如铜。
×
物质的状态变化、热胀冷缩是分子间的间隔发生改变,分子的大小不变。
×
第 10 讲 构成物质的微观粒子
质子数相同的两种微观粒子,其核外电子数不一定相等,如钠原子与钠离子,质子数相同,但核外电子数不同。
7. 相对原子质量就是原子的实际质量。 ( )
_________________________________________________________________
_____________________________
8. 中子数等于质子数。 ( )
_______________________________________________________________
×
中子数不一定等于质子数。
×
第 10 讲 构成物质的微观粒子
相对原子质量等于该原子的实际质量与一种碳-12 原子质量的1/12 的比值,不是原子的实际质量。
同课章节目录
