2025年九年级中考化学专题复习 质量守恒定律 课件(共29张PPT)
文档属性
| 名称 | 2025年九年级中考化学专题复习 质量守恒定律 课件(共29张PPT) |  | |
| 格式 | pptx | ||
| 文件大小 | 634.0KB | ||
| 资源类型 | 教案 | ||
| 版本资源 | 通用版 | ||
| 科目 | 化学 | ||
| 更新时间 | 2024-12-25 21:15:09 | ||
图片预览







文档简介
(共29张PPT)
质量守恒定律
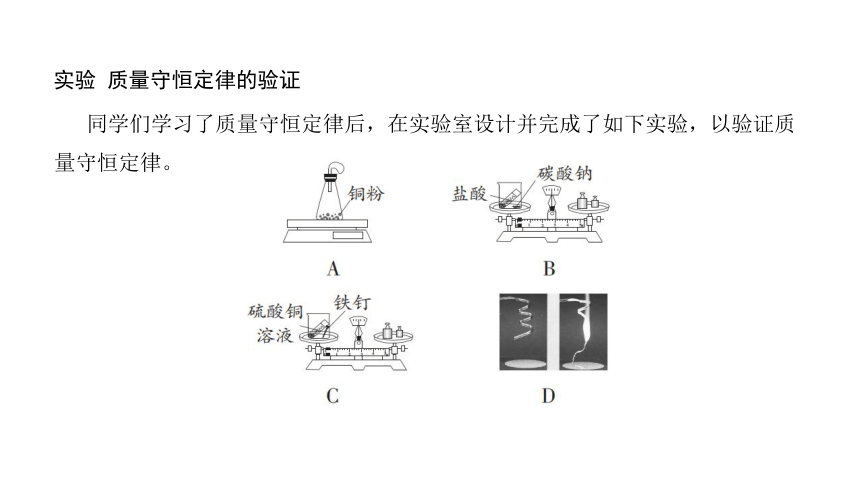
实验 质量守恒定律的验证
同学们学习了质量守恒定律后,在实验室设计并完成了如下实验,以验证质量守恒定律。
第 13 讲 质量守恒定律
第 13 讲 质量守恒定律
(1)图 A 先用电子天平秤量总质量,再将锥形瓶置于陶土网上用酒精灯加
热,反应的化学方程式为 _______________________。 实验现象为 ___________________,气球 ________________,冷却后再次称量,电
子天平两次示数相等。
(2)该实验的注意事项是 ______________________________________________。
(3)乙同学用图 B 所示装置研究质量守恒定律。 写出反应的化学方程式:________________________________, 一段时间后发现天平的指针偏右。 造成天平的指针向右偏转的原因是____________________________________________
____________________________________________________________。
2Cu+O2 2CuO
△
固体由红色变为黑色
先变大后变小
装置气密性要良好(或冷却后再洗涤仪器等合理即可)
生成的二氧化碳气体逸散到空气中,造成左侧质量减小
Na2CO3+2HCl 2NaCl+H2O+CO2↑
(4)丙同学用图 C 实验验证了质量守恒定律。C 实验能在敞口容器中进行的原因是 ____________________________,写出反应的化学方程式:_________________________________。
(5)丁同学用图 D 中镁带在空气中燃烧的实验来探究质量守恒定律。 镁条燃烧时,发出________________,放出热量,生成 ________固体。 实验时发现一定质量的镁完全燃烧后留下的固体质量比反应前镁带的质量轻,联系实验现象,可能的原因是 _________________________________。
(6)以上四个实验,_________(填字母,下同)能验证质量守恒定律,________ 不能直接验证质量守恒定律。
第 13 讲 质量守恒定律
耀眼的白光
白色
燃烧生成的固体没有被全部收集
AC
BD
反应过程中没有气体参与和生成
Fe+CuSO4 FeSO4+Cu
(7)[意外现象分析]图 B 实验,小明改用如图甲装置,当反应结束时,气球已经完全鼓起,小明发现天平的指针已经向右偏了。 小明又重新称量,记录了数据。 他感到困惑:其他操作均正常,实验现象与数据为何与预测结果不符? 你认为出现该实验现象的合理解释最应该是下列中的 ______(填选项字母)。
A. 该反应前后原子的种类、数目变少
B. 该反应生成物的总质量小于反应物的总质量
C. 空气的浮力作用干扰了实验结果
D. 生成气体的反应不遵守质量守恒定律
创新考法
第 13 讲 质量守恒定律
C
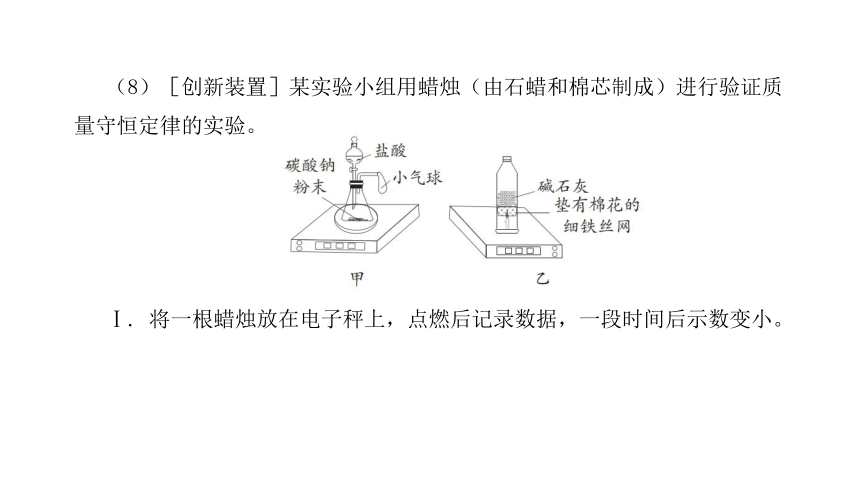
(8)[创新装置]某实验小组用蜡烛(由石蜡和棉芯制成)进行验证质量守恒定律的实验。
Ⅰ. 将一根蜡烛放在电子秤上,点燃后记录数据,一段时间后示数变小。
第 13 讲 质量守恒定律
Ⅱ. 如图乙,将另一根蜡烛点燃后,立即在火焰上方罩一个塑料瓶(底部已剪掉,内部填充有足量的碱石灰,可吸收二氧化碳和水),记录数据,发现示数不断增大。两次实验的结果均不符合质量守恒定律反应前后物质总质量不变的规律,请解释原因:
①______________________________________________________________;
②____________________________________________________________________________________________________________________________。
第 13 讲 质量守恒定律
①实验Ⅰ中蜡烛燃烧生成的水蒸气和二氧化碳逸散到空气中
②实验Ⅱ中蜡烛燃烧生成的水蒸气和二氧化碳气体被碱石灰吸收,氧
气不断参与反应
■题型一 质量守恒定律的验证
思路点拨
第 13 讲 质量守恒定律
题型解法
1. 明确质量守恒定律只适用于化学变化。
2. 在验证时,对于有气体参加或生成的反应,要在密闭容器中进行,若在敞口容器中进行,造成反应前后天平不平衡,不能说这个反应不遵循质量守恒定律(所有的化学变化都遵循质量守恒定律),而应改进实验装置或更换药品试剂,重新进行实验。
第 13 讲 质量守恒定律
例 1 [2024·唐山路南区二模改编]根据如图所示实验回答问题。
(1)如图是测定空气中氧气的含量并验证质量守恒定律的实验,在加入白磷前应先 _______________________________,该实验用注射器的优点是 ______________________________________________。
(2)从微观角度解释质量守恒的原因:____________________________________________。
第 13 讲 质量守恒定律
检查装置的气密性
测空气中氧气含量时便于读数(合理即可)
化学反应前后原子种类、数目、质量都不变
拓题一 (3)该实验反应的化学方程式为 _________________________,若最后测得的空气中氧气的质量分数偏大,可能的原因是 ___________________________________。若称量点燃白磷前后整个装置(包括装置内试剂)的质量,但发现两次读数并不相等,那么是不是说明该反应不遵循质量守恒定律? _______________________________________________________________________。
第 13 讲 质量守恒定律
4P+5O2 2P2O5
点燃
弹簧夹未夹紧(合理即可)
不是,反应前后质量不相等,可能是装置漏气,一切化学变化都遵循质量守恒定律
拓题二 (4)白磷的用量对验证质量守恒定律和测定空气中氧气的含量是否有影响,谈谈你的看法:
____________________________________________________________________
____________________________________________________________________
____________________________________________________________________
____________________________________________________________________。
第 13 讲 质量守恒定律
白磷的量不足对空气中氧气含量的测定实验有影响,因为白磷量不足,不能充分将空气中的氧气消耗完,使测定的结果偏小,但是对质量守恒定律的验证没有影响,因为是在密闭容器中,反应前后总质量不变,白磷的量不足,不会影响天平的平衡
■题型二 未知化学式的推断
思路点拨
题型解法
根据质量守恒定律实质:反应前后,原子种类、数目均不变,观察给出的反应的化学方程式,分别判断等号两边除未知物质外其他元素所含原子的种类和数目,则等号两边相差的原子的种类和数目即为 X(或 nX)中所含的原子的种类和数目,进而推断出 X 的化学式。
第 13 讲 质量守恒定律
例 2 [2021·河北 5 题]利用催化剂将废气中的二氧化碳转化为燃料 X,是实现“碳中和”的路径之一。 该反应的化学方程式为 CO2+3H2 X+H2O,X 的化学式为 ( )
A. CO B. CH4 C. CH3OH D. C2H5OH
C
第 13 讲 质量守恒定律
催化剂
衍生 化学式及化学计量数同时考查
发射通讯卫星的火箭助推器中发生下列化学反应:2N2Hx+N2O4 yN2+4H2O,其中 x、y 的数值是 ( )
A. 3、4 B. 4、4
C. 4、3 D. 3、3
C
第 13 讲 质量守恒定律
点燃
■题型三 微观反应示意图的应用
思路点拨
题型解法
解答微观反应示意图类试题时,首先明确每个“小球”代表的原子种类及对应原子个数,去除不参加反应的微观粒子,写出反应物和生成物的化学式,配平,标注条件,写出反应的化学方程式,再据此回答有关问题。
第 13 讲 质量守恒定律
第 13 讲 质量守恒定律
例 3 [2023·河北 5 题]《天工开物》中记载了用黏土烧制砖的过程,如图所示为该过程中某反应的示意图(其中 “ ”“ ”和“ ”分别代表不同元素的原子)。则微粒 X 中 ( )
A. 只含有 B. 一定含有 和
C. 一定含有 和 D. 一定含有 、 和
B
类题 2024 年 2 月 4 日,我国化学家利用碳化钼负载金催化剂实现了直接用水作为氢源的乙炔加氢制乙烯的新反应过程。 其反应微观示意图如图所示,下列有关说法错误的是 ( )
A. 乙烯的化学式为 C2H4
B. 参加反应的乙炔和水的分子个数比为 1∶1
C. 碳化钼负载金催化剂在反应前后性质不变
D. 该反应前后各种原子的数目不变
C
第 13 讲 质量守恒定律
■题型四 密闭容器中化学反应的数据分析
思路点拨
第 13 讲 质量守恒定律
题型解法
1. 解答密闭容器中化学反应的数据分析类试题时,首先根据反应前后各物质的质量总和不变,计算出未知物的质量,然后利用反应物质量会减小,生成物质量会增加,判断出反应物和生成物,最后再进行反应类型和物质种类的判断以及计算反应的质量比等。
2. 催化剂的特点:“一变,两不变”。 某物质在化学反应前后质量没有改变,则该物质可能为该反应的催化剂也可能没有参加反应。
第 13 讲 质量守恒定律
例 4[2024·河北 6 题]当前,氨气(NH3)的能源化应用逐渐成为研究热点。 工业上常用氮气和氢气合成氨气,一定条件下,在密闭容器中加入反应物和催化剂进行该反应,反应前后各物质的质量如图所示,图中有两处被墨迹遮盖。 下列说法正确的是 ( )
A. 反应后催化剂的质量为 8 g
B. 参加反应的氢气质量为 6 g
C. 氨气分子的微观示意图为
D. 参加反应的氮气和生成的氨气分子个数比为 4∶1
B
第 13 讲 质量守恒定律
衍生一 表格数据
在一密闭容器中加入 a、b、c、d 四种物质, 测得反应前后各物质的质量如下表。 下列说法正确的是 ( )
A. x 等于 100
B. b 可能是单质
B. c 一定是催化剂
D. 参加反应的 a 与 d 的质量比为 3∶8
A
第 13 讲 质量守恒定律
衍生二 扇形统计图
密闭容器内有甲、乙、丙、丁四种物质,在一定条件下充分反应,测得反应前后各物质的质量分数如图所示。 下列说法正确的是 ( )
A. 物质甲是生成物
B. 反应后乙物质的质量分数是 17%
C. 该化学反应中乙、丙两物质的质量比是 17∶5
D. 物质丁一定是该反应的催化剂
C
第 13 讲 质量守恒定律
■考点 质量守恒定律(必考)
质量守恒定律
内容:参加化学反应的各物质的①__________,等于反应后生成的各物质的②_________
适用范围:所有的化学变化,不适用于物理变化
实质:分子分裂为原子,原子的重新组合
第 13 讲 质量守恒定律
质量总和
质量总和
化学反应过程中的“变”与“不变”
宏观———元素的③______、质量不变;反应前后物质的 ④______ 不变
微观———原子的种类、⑤______、质量不变
六个一定不变
种类
总质量
第 13 讲 质量守恒定律
宏观———物质⑥______ 一定改变
微观———分子种类一定改变
两个一定改变
宏观———物质组成元素的化合价可能改变
微观———分子总数可能改变
两个可能改变
数目
种类
质量守恒定律的应用
a. 推断物质的组成:依据化学反应前后元素种类不变
b. 确定物质的化学式:依据化学反应前后原子的种类和数目不变
c. 推断反应中的化学计量数:依据化学反应前后原子的数目不变
d. 解释反应前后物质的质量变化及计算某一物质的质量:依据化学反应中反应物和生成物的总质量不变
第 13 讲 质量守恒定律
质量守恒定律的验证(详见本讲中基础实验过关)
1. 质量守恒定律只强调质量守恒,不包括分子个数、体
积等。
2. 质量守恒指参加化学反应的各物质的质量总和与生成的各物质的质量总和相等,不包括未参加反应的物质的质量,也不包括杂质的质量。
满分备考
第 13 讲 质量守恒定律
下列现象中,能否用质量守恒定律解释(选填“能”或“不能)。
①蔗糖溶于水,总质量不变 _______ ②10 mL 水与 10 mL 酒精混合后体积小于 20 mL_______
③打开盛酒精的试剂瓶瓶盖,酒精质量逐渐变小 _______
小实例辨析
不能
不能
不能
易错归纳
判断下列说法是否正确,正确的打“√”,错误的打“×”并改正或举出反例。
1. 10 g 水加热变成 10 g 水蒸气,这一变化遵循质量守恒定律。( )
_________________________________________________________________
2. 蜡烛燃烧,质量减少,不遵循质量守恒定律。 ( )
____________________________________________________________________
___________________________________
×
水变为水蒸气是物理变化,不适用于质量守恒定律。
×
蜡烛燃烧生成二氧化碳气体和水,二氧化碳气体逸散到空气中了,所以质量减少,但仍遵循质量守恒定律。
第 13 讲 质量守恒定律
3. 3 g 碳和 10 g 氧气充分反应一定能生成 13 g 二氧化碳。 ( )
___________________________________________________________________
___________________________________________________________________
_________________________________________________
4. 化学反应前后,原子的种类、数目、质量不变,分子的数目一定变。( )
_________________________________________________________________
5. 某化合物在氧气中完全燃烧,生成二氧化硫和水,则该化合物中一定含硫、氢、氧三种元素。 ( )
_________________________________________________________________
_________________________________________________________________
×
水由水分子构成,一个水分子由3 g 碳和 10 g 氧气并不是恰好反 应,不能简单的加和,根据化学方程式计算可知实际参加反应的氧气只有 8 g, 故 3 g 碳和 10 g 氧气充分反应生成 11 g 二氧化碳。
×
第 13 讲 质量守恒定律
化学反应前后,分子的数目可能变,也可能不变。
×
根据质量守恒定律,生成物中的硫、氢元素一定来自该化合物,氧元素可能来自于氧气,也可能来自该化合物,故不能确定该物质中是否含氧元素。
质量守恒定律
实验 质量守恒定律的验证
同学们学习了质量守恒定律后,在实验室设计并完成了如下实验,以验证质量守恒定律。
第 13 讲 质量守恒定律
第 13 讲 质量守恒定律
(1)图 A 先用电子天平秤量总质量,再将锥形瓶置于陶土网上用酒精灯加
热,反应的化学方程式为 _______________________。 实验现象为 ___________________,气球 ________________,冷却后再次称量,电
子天平两次示数相等。
(2)该实验的注意事项是 ______________________________________________。
(3)乙同学用图 B 所示装置研究质量守恒定律。 写出反应的化学方程式:________________________________, 一段时间后发现天平的指针偏右。 造成天平的指针向右偏转的原因是____________________________________________
____________________________________________________________。
2Cu+O2 2CuO
△
固体由红色变为黑色
先变大后变小
装置气密性要良好(或冷却后再洗涤仪器等合理即可)
生成的二氧化碳气体逸散到空气中,造成左侧质量减小
Na2CO3+2HCl 2NaCl+H2O+CO2↑
(4)丙同学用图 C 实验验证了质量守恒定律。C 实验能在敞口容器中进行的原因是 ____________________________,写出反应的化学方程式:_________________________________。
(5)丁同学用图 D 中镁带在空气中燃烧的实验来探究质量守恒定律。 镁条燃烧时,发出________________,放出热量,生成 ________固体。 实验时发现一定质量的镁完全燃烧后留下的固体质量比反应前镁带的质量轻,联系实验现象,可能的原因是 _________________________________。
(6)以上四个实验,_________(填字母,下同)能验证质量守恒定律,________ 不能直接验证质量守恒定律。
第 13 讲 质量守恒定律
耀眼的白光
白色
燃烧生成的固体没有被全部收集
AC
BD
反应过程中没有气体参与和生成
Fe+CuSO4 FeSO4+Cu
(7)[意外现象分析]图 B 实验,小明改用如图甲装置,当反应结束时,气球已经完全鼓起,小明发现天平的指针已经向右偏了。 小明又重新称量,记录了数据。 他感到困惑:其他操作均正常,实验现象与数据为何与预测结果不符? 你认为出现该实验现象的合理解释最应该是下列中的 ______(填选项字母)。
A. 该反应前后原子的种类、数目变少
B. 该反应生成物的总质量小于反应物的总质量
C. 空气的浮力作用干扰了实验结果
D. 生成气体的反应不遵守质量守恒定律
创新考法
第 13 讲 质量守恒定律
C
(8)[创新装置]某实验小组用蜡烛(由石蜡和棉芯制成)进行验证质量守恒定律的实验。
Ⅰ. 将一根蜡烛放在电子秤上,点燃后记录数据,一段时间后示数变小。
第 13 讲 质量守恒定律
Ⅱ. 如图乙,将另一根蜡烛点燃后,立即在火焰上方罩一个塑料瓶(底部已剪掉,内部填充有足量的碱石灰,可吸收二氧化碳和水),记录数据,发现示数不断增大。两次实验的结果均不符合质量守恒定律反应前后物质总质量不变的规律,请解释原因:
①______________________________________________________________;
②____________________________________________________________________________________________________________________________。
第 13 讲 质量守恒定律
①实验Ⅰ中蜡烛燃烧生成的水蒸气和二氧化碳逸散到空气中
②实验Ⅱ中蜡烛燃烧生成的水蒸气和二氧化碳气体被碱石灰吸收,氧
气不断参与反应
■题型一 质量守恒定律的验证
思路点拨
第 13 讲 质量守恒定律
题型解法
1. 明确质量守恒定律只适用于化学变化。
2. 在验证时,对于有气体参加或生成的反应,要在密闭容器中进行,若在敞口容器中进行,造成反应前后天平不平衡,不能说这个反应不遵循质量守恒定律(所有的化学变化都遵循质量守恒定律),而应改进实验装置或更换药品试剂,重新进行实验。
第 13 讲 质量守恒定律
例 1 [2024·唐山路南区二模改编]根据如图所示实验回答问题。
(1)如图是测定空气中氧气的含量并验证质量守恒定律的实验,在加入白磷前应先 _______________________________,该实验用注射器的优点是 ______________________________________________。
(2)从微观角度解释质量守恒的原因:____________________________________________。
第 13 讲 质量守恒定律
检查装置的气密性
测空气中氧气含量时便于读数(合理即可)
化学反应前后原子种类、数目、质量都不变
拓题一 (3)该实验反应的化学方程式为 _________________________,若最后测得的空气中氧气的质量分数偏大,可能的原因是 ___________________________________。若称量点燃白磷前后整个装置(包括装置内试剂)的质量,但发现两次读数并不相等,那么是不是说明该反应不遵循质量守恒定律? _______________________________________________________________________。
第 13 讲 质量守恒定律
4P+5O2 2P2O5
点燃
弹簧夹未夹紧(合理即可)
不是,反应前后质量不相等,可能是装置漏气,一切化学变化都遵循质量守恒定律
拓题二 (4)白磷的用量对验证质量守恒定律和测定空气中氧气的含量是否有影响,谈谈你的看法:
____________________________________________________________________
____________________________________________________________________
____________________________________________________________________
____________________________________________________________________。
第 13 讲 质量守恒定律
白磷的量不足对空气中氧气含量的测定实验有影响,因为白磷量不足,不能充分将空气中的氧气消耗完,使测定的结果偏小,但是对质量守恒定律的验证没有影响,因为是在密闭容器中,反应前后总质量不变,白磷的量不足,不会影响天平的平衡
■题型二 未知化学式的推断
思路点拨
题型解法
根据质量守恒定律实质:反应前后,原子种类、数目均不变,观察给出的反应的化学方程式,分别判断等号两边除未知物质外其他元素所含原子的种类和数目,则等号两边相差的原子的种类和数目即为 X(或 nX)中所含的原子的种类和数目,进而推断出 X 的化学式。
第 13 讲 质量守恒定律
例 2 [2021·河北 5 题]利用催化剂将废气中的二氧化碳转化为燃料 X,是实现“碳中和”的路径之一。 该反应的化学方程式为 CO2+3H2 X+H2O,X 的化学式为 ( )
A. CO B. CH4 C. CH3OH D. C2H5OH
C
第 13 讲 质量守恒定律
催化剂
衍生 化学式及化学计量数同时考查
发射通讯卫星的火箭助推器中发生下列化学反应:2N2Hx+N2O4 yN2+4H2O,其中 x、y 的数值是 ( )
A. 3、4 B. 4、4
C. 4、3 D. 3、3
C
第 13 讲 质量守恒定律
点燃
■题型三 微观反应示意图的应用
思路点拨
题型解法
解答微观反应示意图类试题时,首先明确每个“小球”代表的原子种类及对应原子个数,去除不参加反应的微观粒子,写出反应物和生成物的化学式,配平,标注条件,写出反应的化学方程式,再据此回答有关问题。
第 13 讲 质量守恒定律
第 13 讲 质量守恒定律
例 3 [2023·河北 5 题]《天工开物》中记载了用黏土烧制砖的过程,如图所示为该过程中某反应的示意图(其中 “ ”“ ”和“ ”分别代表不同元素的原子)。则微粒 X 中 ( )
A. 只含有 B. 一定含有 和
C. 一定含有 和 D. 一定含有 、 和
B
类题 2024 年 2 月 4 日,我国化学家利用碳化钼负载金催化剂实现了直接用水作为氢源的乙炔加氢制乙烯的新反应过程。 其反应微观示意图如图所示,下列有关说法错误的是 ( )
A. 乙烯的化学式为 C2H4
B. 参加反应的乙炔和水的分子个数比为 1∶1
C. 碳化钼负载金催化剂在反应前后性质不变
D. 该反应前后各种原子的数目不变
C
第 13 讲 质量守恒定律
■题型四 密闭容器中化学反应的数据分析
思路点拨
第 13 讲 质量守恒定律
题型解法
1. 解答密闭容器中化学反应的数据分析类试题时,首先根据反应前后各物质的质量总和不变,计算出未知物的质量,然后利用反应物质量会减小,生成物质量会增加,判断出反应物和生成物,最后再进行反应类型和物质种类的判断以及计算反应的质量比等。
2. 催化剂的特点:“一变,两不变”。 某物质在化学反应前后质量没有改变,则该物质可能为该反应的催化剂也可能没有参加反应。
第 13 讲 质量守恒定律
例 4[2024·河北 6 题]当前,氨气(NH3)的能源化应用逐渐成为研究热点。 工业上常用氮气和氢气合成氨气,一定条件下,在密闭容器中加入反应物和催化剂进行该反应,反应前后各物质的质量如图所示,图中有两处被墨迹遮盖。 下列说法正确的是 ( )
A. 反应后催化剂的质量为 8 g
B. 参加反应的氢气质量为 6 g
C. 氨气分子的微观示意图为
D. 参加反应的氮气和生成的氨气分子个数比为 4∶1
B
第 13 讲 质量守恒定律
衍生一 表格数据
在一密闭容器中加入 a、b、c、d 四种物质, 测得反应前后各物质的质量如下表。 下列说法正确的是 ( )
A. x 等于 100
B. b 可能是单质
B. c 一定是催化剂
D. 参加反应的 a 与 d 的质量比为 3∶8
A
第 13 讲 质量守恒定律
衍生二 扇形统计图
密闭容器内有甲、乙、丙、丁四种物质,在一定条件下充分反应,测得反应前后各物质的质量分数如图所示。 下列说法正确的是 ( )
A. 物质甲是生成物
B. 反应后乙物质的质量分数是 17%
C. 该化学反应中乙、丙两物质的质量比是 17∶5
D. 物质丁一定是该反应的催化剂
C
第 13 讲 质量守恒定律
■考点 质量守恒定律(必考)
质量守恒定律
内容:参加化学反应的各物质的①__________,等于反应后生成的各物质的②_________
适用范围:所有的化学变化,不适用于物理变化
实质:分子分裂为原子,原子的重新组合
第 13 讲 质量守恒定律
质量总和
质量总和
化学反应过程中的“变”与“不变”
宏观———元素的③______、质量不变;反应前后物质的 ④______ 不变
微观———原子的种类、⑤______、质量不变
六个一定不变
种类
总质量
第 13 讲 质量守恒定律
宏观———物质⑥______ 一定改变
微观———分子种类一定改变
两个一定改变
宏观———物质组成元素的化合价可能改变
微观———分子总数可能改变
两个可能改变
数目
种类
质量守恒定律的应用
a. 推断物质的组成:依据化学反应前后元素种类不变
b. 确定物质的化学式:依据化学反应前后原子的种类和数目不变
c. 推断反应中的化学计量数:依据化学反应前后原子的数目不变
d. 解释反应前后物质的质量变化及计算某一物质的质量:依据化学反应中反应物和生成物的总质量不变
第 13 讲 质量守恒定律
质量守恒定律的验证(详见本讲中基础实验过关)
1. 质量守恒定律只强调质量守恒,不包括分子个数、体
积等。
2. 质量守恒指参加化学反应的各物质的质量总和与生成的各物质的质量总和相等,不包括未参加反应的物质的质量,也不包括杂质的质量。
满分备考
第 13 讲 质量守恒定律
下列现象中,能否用质量守恒定律解释(选填“能”或“不能)。
①蔗糖溶于水,总质量不变 _______ ②10 mL 水与 10 mL 酒精混合后体积小于 20 mL_______
③打开盛酒精的试剂瓶瓶盖,酒精质量逐渐变小 _______
小实例辨析
不能
不能
不能
易错归纳
判断下列说法是否正确,正确的打“√”,错误的打“×”并改正或举出反例。
1. 10 g 水加热变成 10 g 水蒸气,这一变化遵循质量守恒定律。( )
_________________________________________________________________
2. 蜡烛燃烧,质量减少,不遵循质量守恒定律。 ( )
____________________________________________________________________
___________________________________
×
水变为水蒸气是物理变化,不适用于质量守恒定律。
×
蜡烛燃烧生成二氧化碳气体和水,二氧化碳气体逸散到空气中了,所以质量减少,但仍遵循质量守恒定律。
第 13 讲 质量守恒定律
3. 3 g 碳和 10 g 氧气充分反应一定能生成 13 g 二氧化碳。 ( )
___________________________________________________________________
___________________________________________________________________
_________________________________________________
4. 化学反应前后,原子的种类、数目、质量不变,分子的数目一定变。( )
_________________________________________________________________
5. 某化合物在氧气中完全燃烧,生成二氧化硫和水,则该化合物中一定含硫、氢、氧三种元素。 ( )
_________________________________________________________________
_________________________________________________________________
×
水由水分子构成,一个水分子由3 g 碳和 10 g 氧气并不是恰好反 应,不能简单的加和,根据化学方程式计算可知实际参加反应的氧气只有 8 g, 故 3 g 碳和 10 g 氧气充分反应生成 11 g 二氧化碳。
×
第 13 讲 质量守恒定律
化学反应前后,分子的数目可能变,也可能不变。
×
根据质量守恒定律,生成物中的硫、氢元素一定来自该化合物,氧元素可能来自于氧气,也可能来自该化合物,故不能确定该物质中是否含氧元素。
同课章节目录
