人教版九年级化学下册课件:9.2 溶解度(共22张PPT)
文档属性
| 名称 | 人教版九年级化学下册课件:9.2 溶解度(共22张PPT) |

|
|
| 格式 | zip | ||
| 文件大小 | 188.5KB | ||
| 资源类型 | 教案 | ||
| 版本资源 | 人教版(新课程标准) | ||
| 科目 | 化学 | ||
| 更新时间 | 2016-04-11 00:00:00 | ||
图片预览






文档简介
课件22张PPT。课题2 溶解度1.将少量下列物质分别加入到足量水中,充分搅拌后,属于溶液的是( )
A.花生油 B.面粉 C.冰块 D.硝酸钾 课前练习: 2.下列关于溶液的说法,正确的是( )
A.溶质一定是固体,溶剂也一定是液体
B.无色的液体一定是溶液
C.溶液一定是均一、稳定的混合物
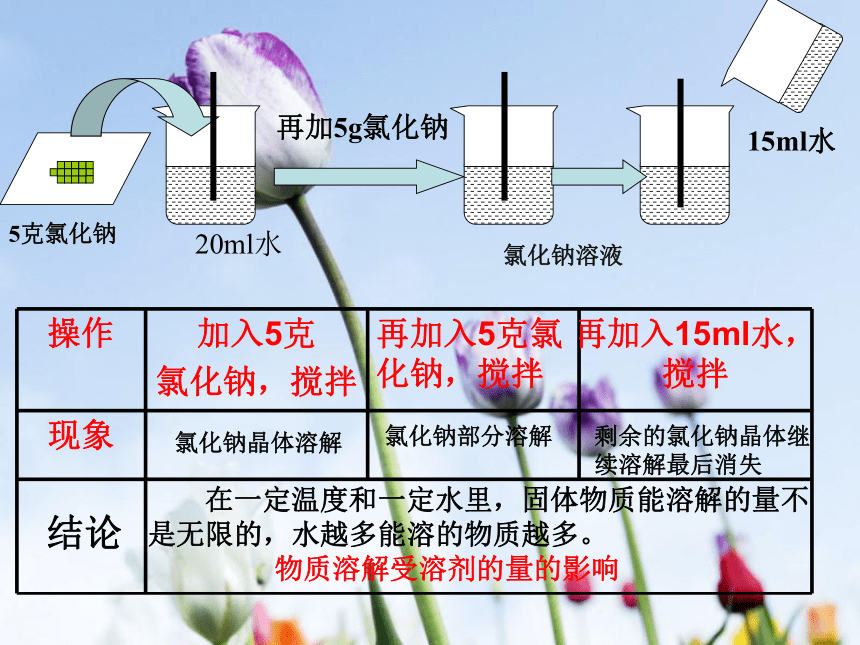
D.大量酒精和少量水形成的是水的酒精溶液DC 我们知道,蔗糖或食盐很容易溶解在水中形成溶液。但是,它们能不能无限制地溶解在一定量的水中呢?5克氯化钠20ml水15ml水再加5g氯化钠氯化钠溶液氯化钠晶体溶解氯化钠部分溶解剩余的氯化钠晶体继续溶解最后消失 在一定温度和一定水里,固体物质能溶解的量不
是无限的,水越多能溶的物质越多。
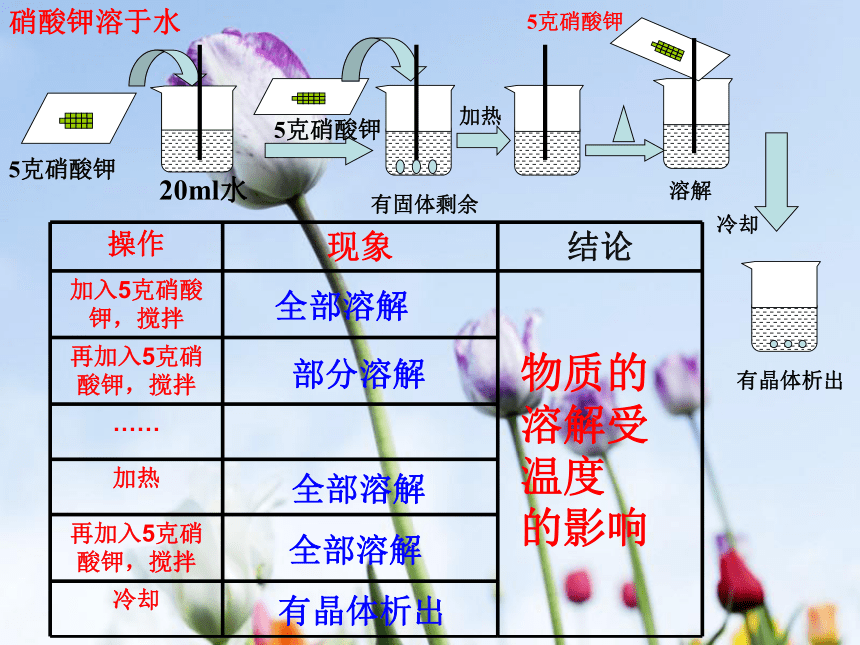
物质溶解受溶剂的量的影响结论 实验9-5说明物质的溶解受溶剂的量的影响。那么物质的溶解与温度有没有关系呢?20ml水5克硝酸钾5克硝酸钾有固体剩余5克硝酸钾冷却硝酸钾溶于水全部溶解部分溶解全部溶解全部溶解有晶体析出物质的溶解受温度
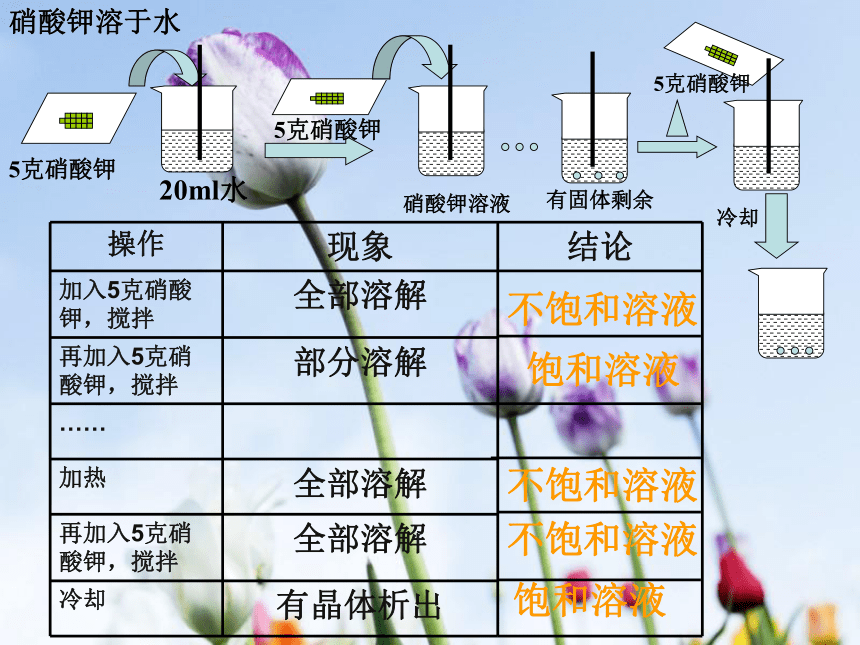
的影响加热溶解有晶体析出物质可以无限制的溶解在水中。但是,如果在“一定的温度”和“一定的溶剂”,则物质的溶解是有限的。5克氯化钠20ml水15ml水待溶解后氯化钠溶液氯化钠晶体溶解氯化钠晶体部分溶解剩余的氯化钠晶体继续溶解最后消失不饱和溶液饱和溶液不饱和溶液结论20ml水5克硝酸钾5克硝酸钾硝酸钾溶液有固体剩余5克硝酸钾冷却硝酸钾溶于水饱和溶液不饱和溶液不饱和溶液不饱和溶液饱和溶液饱和溶液与不饱和溶液在一定温度下,向一定量溶剂里加入某种溶质,当溶质不能继续溶解时所得到的溶液叫做某种溶质饱和溶液1、什么叫饱和溶液、不饱和溶液在一定温度下,向一定量溶剂里加入某种溶质,当溶质还能继续溶解时所得到的溶液叫做某种溶质不饱和溶液如何判断一种溶液是否饱和呢?(1).只要看在一定温度下,有没有不能继续溶解的剩余溶质存在。如有,那么这种溶液就是饱和溶液。
(2).加入此种溶质,如果溶质的量没有减少,则说明这种溶液就是饱和溶液。否则,就是不饱和溶液。想一想,做一做
1、为什么必须说明是“这种溶质”的饱和溶液?(即为什么必须指明溶质是什么?)硝酸钾饱和溶液说明:1.硝酸钾的饱和溶液中还能继续溶解高锰酸钾想一想,做一做
2、我们在说某溶液是饱和溶液,还是不饱和溶液时,为什么总要强调“一定温度下,一定量的溶剂里,”这两个条件?硝酸钾饱和溶液说明:1.硝酸钾的饱和溶液中还能继续溶解高锰酸钾氯化钠晶体溶解氯化钠晶体部分溶解剩余的氯化钠晶体继续溶解最后消失增加溶质的量,能使不饱和溶液变成饱和溶液想一想,做一做
2、我们在说某溶液是饱和溶液,还是不饱和溶液时,为什么总要强调“一定温度下,一定量的溶剂里,”这两个条件?增加溶剂的量,能使饱和溶液变成不饱和溶液20ml水5克硝酸钾5克硝酸钾硝酸钾溶液有固体剩余5克硝酸钾冷却硝酸钾溶于水溶解 部分溶解溶解溶解有晶体析出升高温度能使饱和溶液变成不饱和溶液。降低温度能使不饱和溶液变成饱和溶液。2、饱和溶液与不饱和溶液的转化饱和
溶液 不饱和
溶液1.增加溶剂2.升高温度1.增加溶质3.蒸发溶剂2.降低温度1.把烧杯中80℃时硝酸钾饱和盛液冷却至室温,下列说法
错误的是( )
A.烧杯中溶剂的质量不变 B.烧杯中溶液的质量减少
C.烧杯中硝酸钾的质量不变D. 烧坏中溶液的质量不变试试身手2、某物质的溶解度随温度升高而增大。现有一瓶常温时该物质的饱和溶液,要使它变成不饱和溶液而又保持其溶剂的质量不变,可采用的方法是 。怎样使溶质从溶液中结晶析出海盐晶体明矾晶体开开眼界 二: 结晶2. 晶体的定义:3. 结晶的方法: 降温结晶(冷却热饱和溶液)蒸发结晶1. 结晶的定义:溶质从溶液中析出的过程叫结晶。具有一定规则的几何外形的物质结晶溶解固体溶质溶液溶质 (1)0.1克NaCl溶于10克水,可以再溶解 (2)1克NaCl溶于10克水,可以再溶解 (4)0.1克CaCl2溶于10克水,不能再溶解 饱和溶液、不饱和溶液与浓溶液、稀溶液之间的关系:不饱和溶液、稀溶液不饱和溶液、浓溶液饱和溶液、稀溶液 (3)10克NaCl溶于10克水,底部有固体物质,不能再溶解了饱和溶液、浓溶液①相同溶质:相同温度:饱和溶液一定比不饱和溶液浓。
②不同的溶质:浓溶液不一定是饱和溶液,稀溶液不一定是不饱和溶液。
A.花生油 B.面粉 C.冰块 D.硝酸钾 课前练习: 2.下列关于溶液的说法,正确的是( )
A.溶质一定是固体,溶剂也一定是液体
B.无色的液体一定是溶液
C.溶液一定是均一、稳定的混合物
D.大量酒精和少量水形成的是水的酒精溶液DC 我们知道,蔗糖或食盐很容易溶解在水中形成溶液。但是,它们能不能无限制地溶解在一定量的水中呢?5克氯化钠20ml水15ml水再加5g氯化钠氯化钠溶液氯化钠晶体溶解氯化钠部分溶解剩余的氯化钠晶体继续溶解最后消失 在一定温度和一定水里,固体物质能溶解的量不
是无限的,水越多能溶的物质越多。
物质溶解受溶剂的量的影响结论 实验9-5说明物质的溶解受溶剂的量的影响。那么物质的溶解与温度有没有关系呢?20ml水5克硝酸钾5克硝酸钾有固体剩余5克硝酸钾冷却硝酸钾溶于水全部溶解部分溶解全部溶解全部溶解有晶体析出物质的溶解受温度
的影响加热溶解有晶体析出物质可以无限制的溶解在水中。但是,如果在“一定的温度”和“一定的溶剂”,则物质的溶解是有限的。5克氯化钠20ml水15ml水待溶解后氯化钠溶液氯化钠晶体溶解氯化钠晶体部分溶解剩余的氯化钠晶体继续溶解最后消失不饱和溶液饱和溶液不饱和溶液结论20ml水5克硝酸钾5克硝酸钾硝酸钾溶液有固体剩余5克硝酸钾冷却硝酸钾溶于水饱和溶液不饱和溶液不饱和溶液不饱和溶液饱和溶液饱和溶液与不饱和溶液在一定温度下,向一定量溶剂里加入某种溶质,当溶质不能继续溶解时所得到的溶液叫做某种溶质饱和溶液1、什么叫饱和溶液、不饱和溶液在一定温度下,向一定量溶剂里加入某种溶质,当溶质还能继续溶解时所得到的溶液叫做某种溶质不饱和溶液如何判断一种溶液是否饱和呢?(1).只要看在一定温度下,有没有不能继续溶解的剩余溶质存在。如有,那么这种溶液就是饱和溶液。
(2).加入此种溶质,如果溶质的量没有减少,则说明这种溶液就是饱和溶液。否则,就是不饱和溶液。想一想,做一做
1、为什么必须说明是“这种溶质”的饱和溶液?(即为什么必须指明溶质是什么?)硝酸钾饱和溶液说明:1.硝酸钾的饱和溶液中还能继续溶解高锰酸钾想一想,做一做
2、我们在说某溶液是饱和溶液,还是不饱和溶液时,为什么总要强调“一定温度下,一定量的溶剂里,”这两个条件?硝酸钾饱和溶液说明:1.硝酸钾的饱和溶液中还能继续溶解高锰酸钾氯化钠晶体溶解氯化钠晶体部分溶解剩余的氯化钠晶体继续溶解最后消失增加溶质的量,能使不饱和溶液变成饱和溶液想一想,做一做
2、我们在说某溶液是饱和溶液,还是不饱和溶液时,为什么总要强调“一定温度下,一定量的溶剂里,”这两个条件?增加溶剂的量,能使饱和溶液变成不饱和溶液20ml水5克硝酸钾5克硝酸钾硝酸钾溶液有固体剩余5克硝酸钾冷却硝酸钾溶于水溶解 部分溶解溶解溶解有晶体析出升高温度能使饱和溶液变成不饱和溶液。降低温度能使不饱和溶液变成饱和溶液。2、饱和溶液与不饱和溶液的转化饱和
溶液 不饱和
溶液1.增加溶剂2.升高温度1.增加溶质3.蒸发溶剂2.降低温度1.把烧杯中80℃时硝酸钾饱和盛液冷却至室温,下列说法
错误的是( )
A.烧杯中溶剂的质量不变 B.烧杯中溶液的质量减少
C.烧杯中硝酸钾的质量不变D. 烧坏中溶液的质量不变试试身手2、某物质的溶解度随温度升高而增大。现有一瓶常温时该物质的饱和溶液,要使它变成不饱和溶液而又保持其溶剂的质量不变,可采用的方法是 。怎样使溶质从溶液中结晶析出海盐晶体明矾晶体开开眼界 二: 结晶2. 晶体的定义:3. 结晶的方法: 降温结晶(冷却热饱和溶液)蒸发结晶1. 结晶的定义:溶质从溶液中析出的过程叫结晶。具有一定规则的几何外形的物质结晶溶解固体溶质溶液溶质 (1)0.1克NaCl溶于10克水,可以再溶解 (2)1克NaCl溶于10克水,可以再溶解 (4)0.1克CaCl2溶于10克水,不能再溶解 饱和溶液、不饱和溶液与浓溶液、稀溶液之间的关系:不饱和溶液、稀溶液不饱和溶液、浓溶液饱和溶液、稀溶液 (3)10克NaCl溶于10克水,底部有固体物质,不能再溶解了饱和溶液、浓溶液①相同溶质:相同温度:饱和溶液一定比不饱和溶液浓。
②不同的溶质:浓溶液不一定是饱和溶液,稀溶液不一定是不饱和溶液。
同课章节目录
