3.1.1铁的单质和氧化物 学案 (含答案) 2024-2025学年高一上学期化学人教版(2019)必修一
文档属性
| 名称 | 3.1.1铁的单质和氧化物 学案 (含答案) 2024-2025学年高一上学期化学人教版(2019)必修一 |

|
|
| 格式 | docx | ||
| 文件大小 | 186.4KB | ||
| 资源类型 | 教案 | ||
| 版本资源 | 人教版(2019) | ||
| 科目 | 化学 | ||
| 更新时间 | 2024-12-26 00:00:00 | ||
图片预览

文档简介
“学为中心”探究式学习高效课堂导学案
年级: 高一 班别: 姓名: 制作人: 化学备课组 科目: 化学
第一节 铁及其化合物
第1课时 铁的单质
Ⅰ.学习目标
了解单质铁的性质及用途。掌握铁、氧化亚铁、氧化铁、四氧化三铁性质及转化。
通过实验探究掌握铁单质与水蒸气的反应条件,
Ⅱ.导学与检测
【任务一】认识铁的单质及其性质
【阅读展示】阅读教材68到69页,完成下列填空。
1.铁的存在和冶炼
(1)存在
铁在自然界中可以以 形态(陨铁)存在,但主要是以 价和 价化合物的形态存在于矿石中。铁元素在地壳中的含量居第四位,仅次于 、 和 。
(2)冶炼
工业炼铁的原理是用还原法把铁从铁矿石中提炼出来,化学方程式(以Fe2O3为例):
。
2.铁的物理性质
铁有 性、 性、 性,但其导电性不如铜和铝,其熔、沸点较 。
【对点训练】
1.纯净铁的物理性质有( )
①光亮的银白色 ②黑色 ③在潮湿的空气中易被腐蚀 ④有延展性 ⑤能导电导热 ⑥硬而脆
⑦能被磁铁吸,引易被磁化
A.①③④⑤⑦ B.①④⑤⑦ C.①③⑤⑦ D.全部
【思考讨论】回顾已学知识,写出下列有关反应的化学方程式或离子方程式。比较不同反应,铁的化合价的变化有何异同,为什么会有这样的异同?
3.铁的化学性质
(1)与某些非金属单质、非氧化性酸和盐溶液反应
①Fe与非金属单质反应(氯气、氧气、硫、稀硫酸、硫酸铜)
类别 物质 化学方程式
①非金属 Cl2
O2
S
②非氧化性酸 H2SO4
③盐溶液 CuSO4
【总结】Fe3+ Fe Fe2+
【对点训练】
1、判断正误
(1)FeS、FeCl2、FeCl3均可以通过单质化合得到( )
(2)根据铁与Cl2、S反应的条件可以判断Cl2、S的氧化性强弱( )
(3) Fe在足量Cl2中燃烧生成FeCl3,在少量Cl2中燃烧生成FeCl2 ( )
(4)铁与硫混合共热生成Fe2S3。( )
【任务二】铁与水蒸气反应
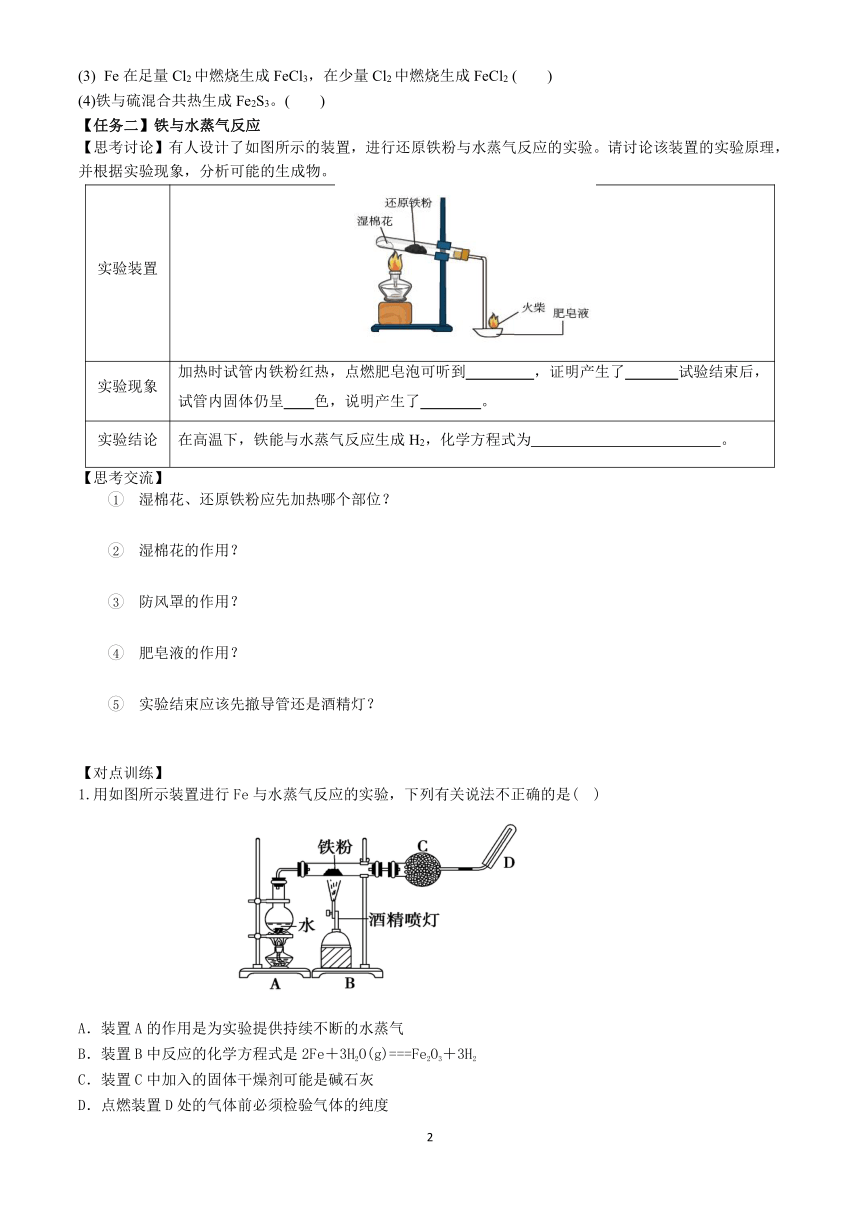
【思考讨论】有人设计了如图所示的装置,进行还原铁粉与水蒸气反应的实验。请讨论该装置的实验原理,并根据实验现象,分析可能的生成物。
实验装置
实验现象 加热时试管内铁粉红热,点燃肥皂泡可听到 ,证明产生了 试验结束后, 试管内固体仍呈 色,说明产生了 。
实验结论 在高温下,铁能与水蒸气反应生成H2,化学方程式为 。
【思考交流】
湿棉花、还原铁粉应先加热哪个部位?
湿棉花的作用?
防风罩的作用?
肥皂液的作用?
实验结束应该先撤导管还是酒精灯?
【对点训练】
1.用如图所示装置进行Fe与水蒸气反应的实验,下列有关说法不正确的是( )
A.装置A的作用是为实验提供持续不断的水蒸气
B.装置B中反应的化学方程式是2Fe+3H2O(g)===Fe2O3+3H2
C.装置C中加入的固体干燥剂可能是碱石灰
D.点燃装置D处的气体前必须检验气体的纯度
2.某化学兴趣小组利用如图装置进行“铁与水反应”的实验,下列说法错误的是( )
A.a、b两个装置中应先点燃a处的酒精(喷)灯
B.b中反应的化学方程式为
C.d的作用是除去未反应的水蒸气,干燥H2
D.e中的现象是红色粉末变黑
【课堂建构】
【巩固练习】
1.在常温下,Fe与水并不起反应,但在高温下,Fe与水蒸气可发生反应。应用下列装置,在硬质玻璃管中放入还原铁粉和石棉绒的混合物,加热,并通入水蒸气,就可以完成高温下“Fe与水蒸气的反应实验”。
请回答该实验中的问题。
(1)写出该反应的反应方程式:________________________________________,还原剂是_____________,氧化剂是____________。
(2)圆底烧瓶中盛装的水,该装置受热后的主要作用是__________________,碎瓷片的作是________。
(3)酒精灯和酒精喷灯点燃的顺序是________________________________________。
(4)干燥管中盛装是的物质是___________________,作用是___________________。
2.某工厂的工业废水中含有大量的FeSO4、较多的Cu2+和少量的Na+。为了减少污染并变废为宝,工厂计划从该废水回收硫酸亚铁和金属铜。请根据流程图(所加试剂均过量),回答下列问题:
(1)物质X的化学式为: ,操作2的名称:___。
(2)已知Y为稀硫酸,写出C中成分的化学式:__ ,
在A中加入Y的化学方程式为:___ 。
(3)工业废水中加入X所发生的离子方程式为: ;该反应是否为氧化还原反应___ (填“是”或“否”),如果是氧化还原反应,发生还原反应的离子是: 。
(4)流程中的操作3是:蒸发浓缩、 、过滤、洗涤、烘干。
【答案】
1、(1) 单质 、 +2 、 +3 氧 、 硅 和 铝 (2) 3CO+Fe2O32Fe+3CO2 。
2、延展性、导热性、导电性、高
【对点训练】1、B
①3Fe+2O2Fe3O4 2Fe+3Cl22FeCl3;:Fe+SFeS。
Fe+2H+===Fe2++H2↑。Fe+Cu2+===Fe2++Cu。
【对点训练】1.××××2、① ④⑤⑦⑧ ②③
爆鸣声、氢气、黑色、Fe3O4\__3Fe+4H2O(g)Fe3O4+4H2__
【思考交流】
先加热湿棉花/提供水蒸汽/提高温度,加热效果更好/收集氢气先撤导管,再移酒精灯
【对点训练】1、B 2、D
【任务二】
化学式 FeO Fe2O3 Fe3O4
俗名 - 铁红 磁性氧化铁
颜色状态 黑色粉末 红棕色粉末 黑色晶体(有磁性)
溶解性 难溶于水
铁元素的化合价 +2 +3 +2,+3
稳定性 不稳定 稳定 稳定
类别 碱性氧化物 碱性氧化物 特殊氧化物
与H+反应的 离子方程式 FeO+2H+===Fe2++H2O Fe2O3+6H+=== 2Fe3++3H2O Fe3O4+8H+=== Fe2++2Fe3++4H2O
【巩固练习】1.【答案】3Fe+4H2O(g)Fe3O4+4H2 Fe H2O 为实验提供水蒸气 防爆沸 先点燃酒精灯,产生水蒸气后,再点燃酒精喷灯;防止先点燃酒精喷灯所导致的Fe与O2的反应 碱石灰干燥剂 除去反应产生的H2中的水蒸气
2、【答案】Fe 过滤 Cu Fe+H2SO4=FeSO4+H2↑ Cu2++Fe=Fe2++Cu 是 Cu2+ 冷却结晶
年级: 高一 班别: 姓名: 制作人: 化学备课组 科目: 化学
第一节 铁及其化合物
第1课时 铁的单质
Ⅰ.学习目标
了解单质铁的性质及用途。掌握铁、氧化亚铁、氧化铁、四氧化三铁性质及转化。
通过实验探究掌握铁单质与水蒸气的反应条件,
Ⅱ.导学与检测
【任务一】认识铁的单质及其性质
【阅读展示】阅读教材68到69页,完成下列填空。
1.铁的存在和冶炼
(1)存在
铁在自然界中可以以 形态(陨铁)存在,但主要是以 价和 价化合物的形态存在于矿石中。铁元素在地壳中的含量居第四位,仅次于 、 和 。
(2)冶炼
工业炼铁的原理是用还原法把铁从铁矿石中提炼出来,化学方程式(以Fe2O3为例):
。
2.铁的物理性质
铁有 性、 性、 性,但其导电性不如铜和铝,其熔、沸点较 。
【对点训练】
1.纯净铁的物理性质有( )
①光亮的银白色 ②黑色 ③在潮湿的空气中易被腐蚀 ④有延展性 ⑤能导电导热 ⑥硬而脆
⑦能被磁铁吸,引易被磁化
A.①③④⑤⑦ B.①④⑤⑦ C.①③⑤⑦ D.全部
【思考讨论】回顾已学知识,写出下列有关反应的化学方程式或离子方程式。比较不同反应,铁的化合价的变化有何异同,为什么会有这样的异同?
3.铁的化学性质
(1)与某些非金属单质、非氧化性酸和盐溶液反应
①Fe与非金属单质反应(氯气、氧气、硫、稀硫酸、硫酸铜)
类别 物质 化学方程式
①非金属 Cl2
O2
S
②非氧化性酸 H2SO4
③盐溶液 CuSO4
【总结】Fe3+ Fe Fe2+
【对点训练】
1、判断正误
(1)FeS、FeCl2、FeCl3均可以通过单质化合得到( )
(2)根据铁与Cl2、S反应的条件可以判断Cl2、S的氧化性强弱( )
(3) Fe在足量Cl2中燃烧生成FeCl3,在少量Cl2中燃烧生成FeCl2 ( )
(4)铁与硫混合共热生成Fe2S3。( )
【任务二】铁与水蒸气反应
【思考讨论】有人设计了如图所示的装置,进行还原铁粉与水蒸气反应的实验。请讨论该装置的实验原理,并根据实验现象,分析可能的生成物。
实验装置
实验现象 加热时试管内铁粉红热,点燃肥皂泡可听到 ,证明产生了 试验结束后, 试管内固体仍呈 色,说明产生了 。
实验结论 在高温下,铁能与水蒸气反应生成H2,化学方程式为 。
【思考交流】
湿棉花、还原铁粉应先加热哪个部位?
湿棉花的作用?
防风罩的作用?
肥皂液的作用?
实验结束应该先撤导管还是酒精灯?
【对点训练】
1.用如图所示装置进行Fe与水蒸气反应的实验,下列有关说法不正确的是( )
A.装置A的作用是为实验提供持续不断的水蒸气
B.装置B中反应的化学方程式是2Fe+3H2O(g)===Fe2O3+3H2
C.装置C中加入的固体干燥剂可能是碱石灰
D.点燃装置D处的气体前必须检验气体的纯度
2.某化学兴趣小组利用如图装置进行“铁与水反应”的实验,下列说法错误的是( )
A.a、b两个装置中应先点燃a处的酒精(喷)灯
B.b中反应的化学方程式为
C.d的作用是除去未反应的水蒸气,干燥H2
D.e中的现象是红色粉末变黑
【课堂建构】
【巩固练习】
1.在常温下,Fe与水并不起反应,但在高温下,Fe与水蒸气可发生反应。应用下列装置,在硬质玻璃管中放入还原铁粉和石棉绒的混合物,加热,并通入水蒸气,就可以完成高温下“Fe与水蒸气的反应实验”。
请回答该实验中的问题。
(1)写出该反应的反应方程式:________________________________________,还原剂是_____________,氧化剂是____________。
(2)圆底烧瓶中盛装的水,该装置受热后的主要作用是__________________,碎瓷片的作是________。
(3)酒精灯和酒精喷灯点燃的顺序是________________________________________。
(4)干燥管中盛装是的物质是___________________,作用是___________________。
2.某工厂的工业废水中含有大量的FeSO4、较多的Cu2+和少量的Na+。为了减少污染并变废为宝,工厂计划从该废水回收硫酸亚铁和金属铜。请根据流程图(所加试剂均过量),回答下列问题:
(1)物质X的化学式为: ,操作2的名称:___。
(2)已知Y为稀硫酸,写出C中成分的化学式:__ ,
在A中加入Y的化学方程式为:___ 。
(3)工业废水中加入X所发生的离子方程式为: ;该反应是否为氧化还原反应___ (填“是”或“否”),如果是氧化还原反应,发生还原反应的离子是: 。
(4)流程中的操作3是:蒸发浓缩、 、过滤、洗涤、烘干。
【答案】
1、(1) 单质 、 +2 、 +3 氧 、 硅 和 铝 (2) 3CO+Fe2O32Fe+3CO2 。
2、延展性、导热性、导电性、高
【对点训练】1、B
①3Fe+2O2Fe3O4 2Fe+3Cl22FeCl3;:Fe+SFeS。
Fe+2H+===Fe2++H2↑。Fe+Cu2+===Fe2++Cu。
【对点训练】1.××××2、① ④⑤⑦⑧ ②③
爆鸣声、氢气、黑色、Fe3O4\__3Fe+4H2O(g)Fe3O4+4H2__
【思考交流】
先加热湿棉花/提供水蒸汽/提高温度,加热效果更好/收集氢气先撤导管,再移酒精灯
【对点训练】1、B 2、D
【任务二】
化学式 FeO Fe2O3 Fe3O4
俗名 - 铁红 磁性氧化铁
颜色状态 黑色粉末 红棕色粉末 黑色晶体(有磁性)
溶解性 难溶于水
铁元素的化合价 +2 +3 +2,+3
稳定性 不稳定 稳定 稳定
类别 碱性氧化物 碱性氧化物 特殊氧化物
与H+反应的 离子方程式 FeO+2H+===Fe2++H2O Fe2O3+6H+=== 2Fe3++3H2O Fe3O4+8H+=== Fe2++2Fe3++4H2O
【巩固练习】1.【答案】3Fe+4H2O(g)Fe3O4+4H2 Fe H2O 为实验提供水蒸气 防爆沸 先点燃酒精灯,产生水蒸气后,再点燃酒精喷灯;防止先点燃酒精喷灯所导致的Fe与O2的反应 碱石灰干燥剂 除去反应产生的H2中的水蒸气
2、【答案】Fe 过滤 Cu Fe+H2SO4=FeSO4+H2↑ Cu2++Fe=Fe2++Cu 是 Cu2+ 冷却结晶
