7.1 第2课时 酸的化学性质 课件(共23张PPT) 2024-2025学年化学鲁教版九年级下册
文档属性
| 名称 | 7.1 第2课时 酸的化学性质 课件(共23张PPT) 2024-2025学年化学鲁教版九年级下册 |

|
|
| 格式 | pptx | ||
| 文件大小 | 654.3KB | ||
| 资源类型 | 教案 | ||
| 版本资源 | 鲁教版 | ||
| 科目 | 化学 | ||
| 更新时间 | 2024-12-28 00:00:00 | ||
图片预览






文档简介
(共23张PPT)
第七单元 认识酸和碱
第一节 酸及其性质
第2课时 酸的化学性质
小明家的一个铁制工具生锈了,小明的爸爸把生锈的工具放在一种溶液里面,两个小时后,小明的爸爸把工具拿出来,工具就光洁如新了。小明问爸爸为什么工具上的锈没有了?小明的爸爸告诉小明,这是利用了稀盐酸的化学性质。你知道稀盐酸具有什么化学性质吗?
这节课我们就用实验来探究酸的化学性质。
新知导学:
活动探究7-1 盐酸能与哪些物质发生化学反应
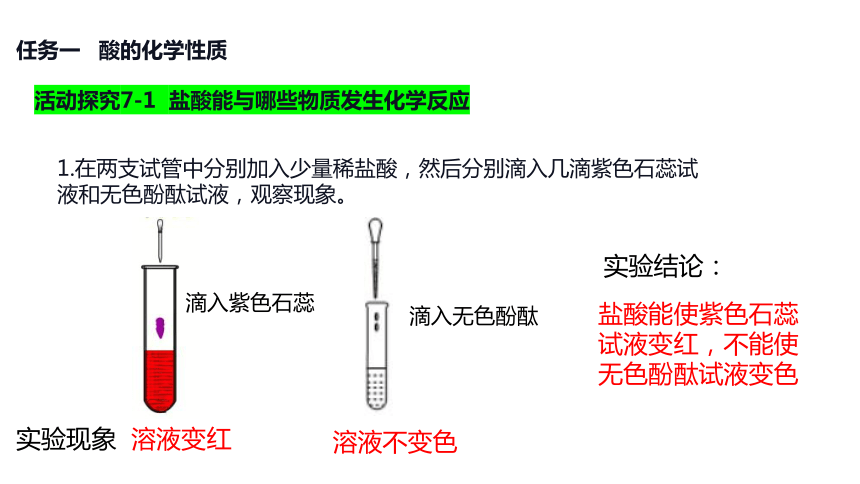
1.在两支试管中分别加入少量稀盐酸,然后分别滴入几滴紫色石蕊试液和无色酚酞试液,观察现象。
实验现象
滴入无色酚酞
溶液变红
溶液不变色
滴入紫色石蕊
实验结论:
盐酸能使紫色石蕊试液变红,不能使无色酚酞试液变色
任务一 酸的化学性质
活动探究7-1 盐酸能与哪些物质发生化学反应
任务一 酸的化学性质
2.向盛有生锈铁钉的试管中加入少量稀盐酸,观察现象。
物质 生锈铁钉
实验现象
化学方程式
Fe2O3+6HCl=2FeCl3+3H2O
铁锈溶解,溶液变黄
铁元素显+3价,形成的是铁盐,溶液呈黄色
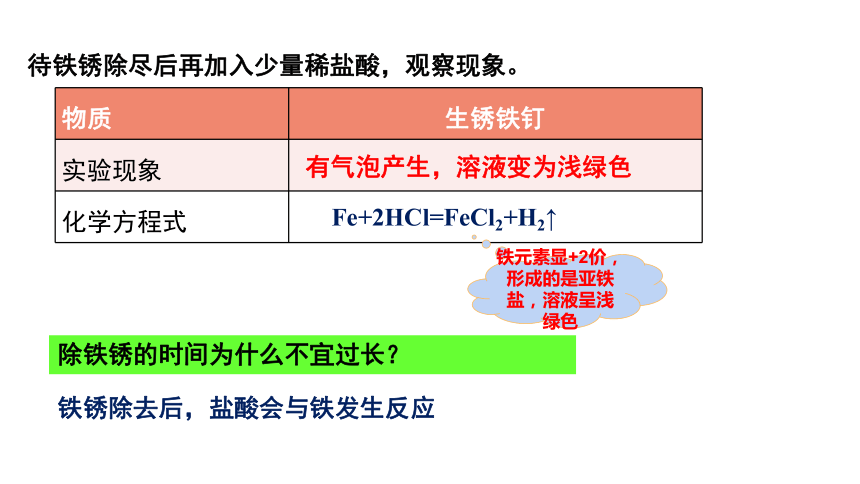
待铁锈除尽后再加入少量稀盐酸,观察现象。
物质 生锈铁钉
实验现象
化学方程式
Fe+2HCl=FeCl2+H2↑
除铁锈的时间为什么不宜过长?
有气泡产生,溶液变为浅绿色
铁锈除去后,盐酸会与铁发生反应
铁元素显+2价,形成的是亚铁盐,溶液呈浅绿色
1.在两支试管中分别加入少量稀硫酸,然后分别滴入几滴紫色石蕊试液和无色酚酞试液,观察现象。
实验现象
滴入无色酚酞
溶液变红
溶液不变色
滴入紫色石蕊
实验结论:
硫酸能使紫色石蕊试液变红,不能使无色酚酞试液变色
活动探究7-2 硫酸与盐酸性质的比较
2.向盛有生锈铁钉的试管中加入少量稀硫酸,观察现象。
物质 生锈铁钉
实验现象
化学方程式
Fe2O3+3H2SO4=Fe2(SO4)3+3H2O
铁锈溶解,溶液变黄
活动探究7-2 硫酸与盐酸性质的比较
待铁锈除尽后再加入少量稀硫酸,观察现象。
物质 生锈铁钉
实验现象
化学方程式
Fe+H2SO4=FeSO4+H2↑
有气泡产生,溶液变为浅绿色
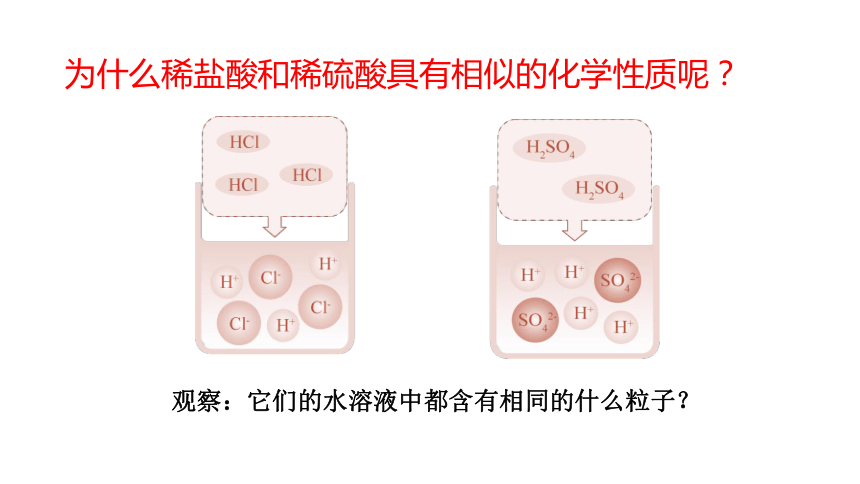
为什么稀盐酸和稀硫酸具有相似的化学性质呢?
观察:它们的水溶液中都含有相同的什么粒子?
讨论:为什么酸具有相似的化学性质呢?
因为它们在溶于水时,都解离出了共同的阳离子—氢离子,正是由于氢离子的存在,导致它们具有相似的化学性质,称作酸的通性。
盐酸 HCl=H++Cl-
硫酸 H2SO4=2H++SO42-
硝酸 HNO3=H++NO3-
(1)能使紫色石蕊试液变成红色。
(2)能与某些金属氧化物反应,生成水。
(3)能与某些金属反应,生成氢气。
归纳总结:酸的通性
物质 加入稀硫酸 加入稀盐酸
实验现象
反应的化学方程式
BaCl2+H2SO4=BaSO4↓+2HCl
产生白色沉淀
活动探究:向盛有氯化钡溶液的两支试管中分别加入少量稀硫酸和稀盐酸,观察现象。
无现象
不反应
BaSO4是一种既不溶于水,又不溶于酸的沉淀。
由于不同的酸溶于水时解离出的酸根离子不同,其性质也存在差异。
思考:上述探究中稀盐酸不能与氯化钡溶液反应,而稀硫酸能与氯化钡溶液反应,为什么?
.
如何鉴别稀盐酸和稀硫酸?
1、紫色石蕊试液
2、无色酚酞试液
3、金属镁
4、氧化铁
5、氯化钡溶液
在上面的化学反应中,我们得到了下面一些物质,观察它们有什么共同点:
BaCl2、FeCl3、BaSO4、CaCO3
任务二 盐
HCl=H+ + Cl-
H2SO4=2H+ + SO42-
HNO3=H+ + NO3-
H2CO3=2H+ + CO32-
酸根阴离子
像BaCl2、FeCl3、BaSO4、CaCO3等由金属阳离子和酸根阴离子构成的化合物称为盐。
像NH4Cl﹑ (NH4)2SO4等由铵根离子(NH4+)和酸根阴离子构成的化合物 也是盐。
物质
纯净物
混合物
化合物
单质
氧
化
物
酸
盐
金属氧化物
非金属氧化物
金属
非金属
物质的分类
硫酸:70%以上用于生产化肥,其余用于农药、炸药、染料及冶炼金属、石油化工和金属除锈等
盐酸:制药、作除锈剂等
任务三 常见酸的用途
酸的通性
酸能使紫色石蕊试液变红
2.盐的定义
由金属阳离子和酸根阴离子构成的化合物,化学上把这类化合物称为盐。
1.酸的通性
酸+某些金属→盐+氢气
酸+某些金属氧化物→盐+水
3.常见酸的用途
课堂小结
1.酸具有酸的通性的原因是( )
B
A.酸都有酸根阴离子 B.酸都能解离出H+
C.酸中都含有氢元素 D.酸中都含有氧元素
课堂练习
2.盐酸和稀硫酸常用作金属表面的除锈剂,是利用了它们化学性质中的( )
A.能与金属反应 B.能与金属氧化物反应
C.能使指示剂变色 D.能溶于水
B
课堂练习
3.将生锈的铁钉放在盐酸中,最先看到的现象是铁锈逐渐溶解,溶液由无色变成黄色,反应的化学方程式为 ,当时间稍长时,又看到有气泡产生,其反应的方程式为 。
Fe2O3+6HCl=2FeCl3+3H2O
Fe+2HCl=FeCl2+H2↑
课堂练习
4.学习了酸的化学性质后,小科同学以稀硫酸为主题,绘制了“多彩酸世界”思维导图。请据图回答:
(1)若用紫色石蕊试液实现①,会得到 色溶液。
(2)若要实现④,可选用 (填化学式)和稀硫酸反应。
(3)写出⑤有白色沉淀生成的反应方程
式: 。
红
Fe2O3
BaCl2 + H2SO4 = BaSO4↓+ 2HCl
课堂练习
谢 谢 观 看
第七单元 认识酸和碱
第一节 酸及其性质
第2课时 酸的化学性质
小明家的一个铁制工具生锈了,小明的爸爸把生锈的工具放在一种溶液里面,两个小时后,小明的爸爸把工具拿出来,工具就光洁如新了。小明问爸爸为什么工具上的锈没有了?小明的爸爸告诉小明,这是利用了稀盐酸的化学性质。你知道稀盐酸具有什么化学性质吗?
这节课我们就用实验来探究酸的化学性质。
新知导学:
活动探究7-1 盐酸能与哪些物质发生化学反应
1.在两支试管中分别加入少量稀盐酸,然后分别滴入几滴紫色石蕊试液和无色酚酞试液,观察现象。
实验现象
滴入无色酚酞
溶液变红
溶液不变色
滴入紫色石蕊
实验结论:
盐酸能使紫色石蕊试液变红,不能使无色酚酞试液变色
任务一 酸的化学性质
活动探究7-1 盐酸能与哪些物质发生化学反应
任务一 酸的化学性质
2.向盛有生锈铁钉的试管中加入少量稀盐酸,观察现象。
物质 生锈铁钉
实验现象
化学方程式
Fe2O3+6HCl=2FeCl3+3H2O
铁锈溶解,溶液变黄
铁元素显+3价,形成的是铁盐,溶液呈黄色
待铁锈除尽后再加入少量稀盐酸,观察现象。
物质 生锈铁钉
实验现象
化学方程式
Fe+2HCl=FeCl2+H2↑
除铁锈的时间为什么不宜过长?
有气泡产生,溶液变为浅绿色
铁锈除去后,盐酸会与铁发生反应
铁元素显+2价,形成的是亚铁盐,溶液呈浅绿色
1.在两支试管中分别加入少量稀硫酸,然后分别滴入几滴紫色石蕊试液和无色酚酞试液,观察现象。
实验现象
滴入无色酚酞
溶液变红
溶液不变色
滴入紫色石蕊
实验结论:
硫酸能使紫色石蕊试液变红,不能使无色酚酞试液变色
活动探究7-2 硫酸与盐酸性质的比较
2.向盛有生锈铁钉的试管中加入少量稀硫酸,观察现象。
物质 生锈铁钉
实验现象
化学方程式
Fe2O3+3H2SO4=Fe2(SO4)3+3H2O
铁锈溶解,溶液变黄
活动探究7-2 硫酸与盐酸性质的比较
待铁锈除尽后再加入少量稀硫酸,观察现象。
物质 生锈铁钉
实验现象
化学方程式
Fe+H2SO4=FeSO4+H2↑
有气泡产生,溶液变为浅绿色
为什么稀盐酸和稀硫酸具有相似的化学性质呢?
观察:它们的水溶液中都含有相同的什么粒子?
讨论:为什么酸具有相似的化学性质呢?
因为它们在溶于水时,都解离出了共同的阳离子—氢离子,正是由于氢离子的存在,导致它们具有相似的化学性质,称作酸的通性。
盐酸 HCl=H++Cl-
硫酸 H2SO4=2H++SO42-
硝酸 HNO3=H++NO3-
(1)能使紫色石蕊试液变成红色。
(2)能与某些金属氧化物反应,生成水。
(3)能与某些金属反应,生成氢气。
归纳总结:酸的通性
物质 加入稀硫酸 加入稀盐酸
实验现象
反应的化学方程式
BaCl2+H2SO4=BaSO4↓+2HCl
产生白色沉淀
活动探究:向盛有氯化钡溶液的两支试管中分别加入少量稀硫酸和稀盐酸,观察现象。
无现象
不反应
BaSO4是一种既不溶于水,又不溶于酸的沉淀。
由于不同的酸溶于水时解离出的酸根离子不同,其性质也存在差异。
思考:上述探究中稀盐酸不能与氯化钡溶液反应,而稀硫酸能与氯化钡溶液反应,为什么?
.
如何鉴别稀盐酸和稀硫酸?
1、紫色石蕊试液
2、无色酚酞试液
3、金属镁
4、氧化铁
5、氯化钡溶液
在上面的化学反应中,我们得到了下面一些物质,观察它们有什么共同点:
BaCl2、FeCl3、BaSO4、CaCO3
任务二 盐
HCl=H+ + Cl-
H2SO4=2H+ + SO42-
HNO3=H+ + NO3-
H2CO3=2H+ + CO32-
酸根阴离子
像BaCl2、FeCl3、BaSO4、CaCO3等由金属阳离子和酸根阴离子构成的化合物称为盐。
像NH4Cl﹑ (NH4)2SO4等由铵根离子(NH4+)和酸根阴离子构成的化合物 也是盐。
物质
纯净物
混合物
化合物
单质
氧
化
物
酸
盐
金属氧化物
非金属氧化物
金属
非金属
物质的分类
硫酸:70%以上用于生产化肥,其余用于农药、炸药、染料及冶炼金属、石油化工和金属除锈等
盐酸:制药、作除锈剂等
任务三 常见酸的用途
酸的通性
酸能使紫色石蕊试液变红
2.盐的定义
由金属阳离子和酸根阴离子构成的化合物,化学上把这类化合物称为盐。
1.酸的通性
酸+某些金属→盐+氢气
酸+某些金属氧化物→盐+水
3.常见酸的用途
课堂小结
1.酸具有酸的通性的原因是( )
B
A.酸都有酸根阴离子 B.酸都能解离出H+
C.酸中都含有氢元素 D.酸中都含有氧元素
课堂练习
2.盐酸和稀硫酸常用作金属表面的除锈剂,是利用了它们化学性质中的( )
A.能与金属反应 B.能与金属氧化物反应
C.能使指示剂变色 D.能溶于水
B
课堂练习
3.将生锈的铁钉放在盐酸中,最先看到的现象是铁锈逐渐溶解,溶液由无色变成黄色,反应的化学方程式为 ,当时间稍长时,又看到有气泡产生,其反应的方程式为 。
Fe2O3+6HCl=2FeCl3+3H2O
Fe+2HCl=FeCl2+H2↑
课堂练习
4.学习了酸的化学性质后,小科同学以稀硫酸为主题,绘制了“多彩酸世界”思维导图。请据图回答:
(1)若用紫色石蕊试液实现①,会得到 色溶液。
(2)若要实现④,可选用 (填化学式)和稀硫酸反应。
(3)写出⑤有白色沉淀生成的反应方程
式: 。
红
Fe2O3
BaCl2 + H2SO4 = BaSO4↓+ 2HCl
课堂练习
谢 谢 观 看
同课章节目录
