第八单元 第二节 第2课时 海水“晒盐”的原理 课件 (共24张PPT) 2024-2025学年化学鲁教版九年级下册
文档属性
| 名称 | 第八单元 第二节 第2课时 海水“晒盐”的原理 课件 (共24张PPT) 2024-2025学年化学鲁教版九年级下册 |

|
|
| 格式 | pptx | ||
| 文件大小 | 1.4MB | ||
| 资源类型 | 教案 | ||
| 版本资源 | 鲁教版 | ||
| 科目 | 化学 | ||
| 更新时间 | 2024-12-29 00:00:00 | ||
图片预览








文档简介
(共24张PPT)
第八单元 海洋化学资源的利用
第二节 海水“晒盐”
第2课时 海水“晒盐”的原理
海水
蒸发池
结晶池
粗盐
母液
海水晒盐的主要流程
不饱和溶液
饱和溶液
蒸发溶剂(水)
食盐在水中的溶解是有限度的
新知导学:
许多物质在水中的溶解是有限度的
一定温度下,某固体物质在100g溶剂(通常为水)里达到饱和状态时所能溶解的溶质的质量,称为该物质的溶解度
一定温度
100g溶剂(水)
达到饱和状态
溶质的质量
溶解度四要素
任务一 溶解度
20 ℃时,100 g水中最多溶解31.6 g硝酸钾。
20 ℃时,100 g水中溶解31.6 g硝酸钾就达到饱和状态了。
20℃时,硝酸钾的溶解度为31.6g的含义是什么
思考
20℃时,氯化钠的溶解度是36g。向50g 20 ℃的水中加入20g氯化钠,所得溶液为 溶液。该溶液中溶质、溶剂、溶液的质量比为 。
此时溶液的质量分数是______。
饱和
18:50:68
26.5%
饱和溶液的溶质质量分数=
溶解度
100g+溶解度
×100%
拓展
物质溶解度与溶解能力的对应关系
.
.
.
10g
1g
0.01g
易溶
可溶
微溶
难溶
物质的溶解能力是根据20℃时的溶解度来区分的,记准分界的三个数:10g、1g和0.01g。
多识一点:气体的溶解度
鱼能在水中生存,打开汽水瓶盖时常会冒出大量气泡,这都证实了气体能溶解在水里。气体的溶解度与压强和温度有关:在一定温度下,压强越大气体的溶解度越大,压强越小气体的溶解度越小;在一定压强下,温度越高气体的溶解度越小,温度越低气体的溶解度越大。
思考:有科学家提出,在高压下将二氧化碳气体封存在海洋深处,以解决大气中二氧化碳含量增大的问题。你认为这种方案可行吗 这对海洋生态会产生什么影响
不可行,这样会造成海洋酸化。
任务二 溶解度曲线
温度
溶解度
观察思考8-2 认识溶解度曲线
下图是根据几种常见物质在不同温度下的溶解度绘制出来的曲线——溶解度曲线。
氢氧化钙的溶解度曲线
A
B
C
曲线上的点B:
表示物质在某温度下的溶解度,溶液恰好饱和。
曲线上面的点A:
饱和溶液,且有未溶解的溶质。
曲线下面的点C:
不饱和溶液
从溶解度曲线上获取的信息
温度
溶解度
从溶解度曲线上获取的信息
线:某物质溶解度受温度影响的变化情况
交点:曲线的交点表示这两种物质在该温度下的溶解度相同,饱和溶液的溶质质量分数也相同。
(1)“上升型”:多数固体物质的溶解度随着温度的升高而增大,如硝酸钾KNO3;
(2)“平缓型”:少数固体物质的溶解度受温度变化的影响小,如氯化钠NaCl;
(3)“下降型”:极少数固体物质的溶解度随着温度的升高而减小,如氢氧化钙Ca(OH)2。
固体物质溶解度随温度变化的规律
氢氧化钙
从溶解度曲线上还能获取的信息
四.溶解度的表示方法---溶解度曲线
(5)确定结晶的方法。
(1)查询某物质在某温度下的溶解度;
(2)比较不同物质在同一温度时的溶解度大小;
(3)判断各种物质溶解度受温度影响的变化趋势;
(4)判断溶液是否饱和;
多识一点
降温结晶
观察硝酸钾的溶解度曲线,可以看出硝酸钾的溶解度受温度的影响较大。
对于这样的物质,可采取冷却热饱和溶液的方法,使溶质从溶液中结晶析出,这种方法称为降温结晶。
0
20
80
31.6
169
溶解度
/g
温度/℃
80 ℃时,100 g水中最多溶解169 g硝酸钾
由80 ℃冷却到20 ℃
20 ℃时,100 g水中只能溶解31.6 g硝酸钾,析出硝酸钾晶体的质量为:169 g-31.6 g=137.4 g
思考
观察氯化钠的溶解度曲线,判断
氯化钠的溶解度受温度变化的影
响是大还是小?为什么要用蒸发
结晶的方法从海水中得到盐,而
不用降温结晶的方法?
氯化钠溶解度随温度升高变化不明显,故用蒸发结晶。
降温结晶(冷却热饱和溶液):
提纯溶解度随温度升高显著增大的物质。
除杂:KNO3 (NaCl)
方法:
步骤:
降温结晶
①溶解
②蒸发浓缩
③降温结晶
④过滤
从溶解度曲线分析结晶法除杂
蒸发结晶法(蒸发溶剂法):
提纯溶解度随温度升高而变化不明显的物质。
除杂: NaCl (KNO3)
方法:
蒸发结晶
步骤:
①溶解
③过滤
②蒸发结晶
从溶解度曲线分析结晶法除杂
总结:提纯谁,就让谁结晶,陡用降温,平用蒸发。
溶解度
概念
溶质质量
饱和状态
一定温度
100g水
表示
溶解度曲线
结晶
溶解性
定量表示
蒸发结晶
降温结晶
盘点收获
课堂小结
1.下列说法中正确的是( )
A.20℃时,100g水里最多能溶解36g氯化钠,所以20℃时氯化钠的溶解度为36g
B.20℃时,硝酸钾的溶解度为31.6
C.20℃时,在100g水中加入35g氯化钠完全溶解,则20℃时,氯化钠的溶解度为35g
D.20℃时,100g氯化钠的饱和溶液中有26.5g氯化钠,则 20℃
时,氯化钠的溶解度为26.5g
E.硝酸钾的溶解度为31.6g
A
课堂练习
课堂练习
2. 增大二氧化碳在水中的溶解度的方法( )
A. 升温增压
B. 升温减压
C. 降温增压
D. 降温减压
C
课堂练习
3.下表是KNO3部分溶解度数据,回答问题
(1)40℃时,将70gKNO3固体加入100g水中,充分搅拌,形成的溶液质量为
g。
(2)0℃时,使KNO3的饱和溶液要变成不饱和溶液方法是 (写一种)。
163.9
加入水
4.如图是A、B、C三种固体的溶解度曲线,回答下列问题。
(1)点P表示 。
(2)t2 ℃时,A、B、C的溶解度由大到小的顺序为 。
(3)要使接近饱和的C的溶液变为饱和,需要 温度。
(4)t2 ℃时,A物质的饱和溶液150 g降温到t1 ℃析出A g。
(5)t2 ℃时,将等质量A、B、C三种物质的饱和溶液降温到t1 ℃,析出晶体的质量由大到小的顺序是 。
(6)当A中含有少量B时,提纯A,可采用 的方法;当B中含有少量A时,提纯B,可采用 的方法。
t1℃时,A、C的溶解度相同
A>B>C
升高
30
A>B>C
降温结晶
蒸发结晶
课堂练习
谢 谢 观 看
第八单元 海洋化学资源的利用
第二节 海水“晒盐”
第2课时 海水“晒盐”的原理
海水
蒸发池
结晶池
粗盐
母液
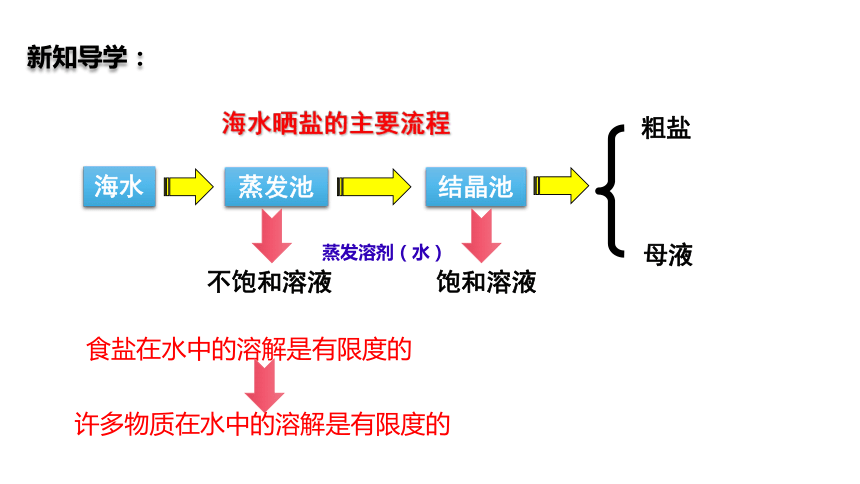
海水晒盐的主要流程
不饱和溶液
饱和溶液
蒸发溶剂(水)
食盐在水中的溶解是有限度的
新知导学:
许多物质在水中的溶解是有限度的
一定温度下,某固体物质在100g溶剂(通常为水)里达到饱和状态时所能溶解的溶质的质量,称为该物质的溶解度
一定温度
100g溶剂(水)
达到饱和状态
溶质的质量
溶解度四要素
任务一 溶解度
20 ℃时,100 g水中最多溶解31.6 g硝酸钾。
20 ℃时,100 g水中溶解31.6 g硝酸钾就达到饱和状态了。
20℃时,硝酸钾的溶解度为31.6g的含义是什么
思考
20℃时,氯化钠的溶解度是36g。向50g 20 ℃的水中加入20g氯化钠,所得溶液为 溶液。该溶液中溶质、溶剂、溶液的质量比为 。
此时溶液的质量分数是______。
饱和
18:50:68
26.5%
饱和溶液的溶质质量分数=
溶解度
100g+溶解度
×100%
拓展
物质溶解度与溶解能力的对应关系
.
.
.
10g
1g
0.01g
易溶
可溶
微溶
难溶
物质的溶解能力是根据20℃时的溶解度来区分的,记准分界的三个数:10g、1g和0.01g。
多识一点:气体的溶解度
鱼能在水中生存,打开汽水瓶盖时常会冒出大量气泡,这都证实了气体能溶解在水里。气体的溶解度与压强和温度有关:在一定温度下,压强越大气体的溶解度越大,压强越小气体的溶解度越小;在一定压强下,温度越高气体的溶解度越小,温度越低气体的溶解度越大。
思考:有科学家提出,在高压下将二氧化碳气体封存在海洋深处,以解决大气中二氧化碳含量增大的问题。你认为这种方案可行吗 这对海洋生态会产生什么影响
不可行,这样会造成海洋酸化。
任务二 溶解度曲线
温度
溶解度
观察思考8-2 认识溶解度曲线
下图是根据几种常见物质在不同温度下的溶解度绘制出来的曲线——溶解度曲线。
氢氧化钙的溶解度曲线
A
B
C
曲线上的点B:
表示物质在某温度下的溶解度,溶液恰好饱和。
曲线上面的点A:
饱和溶液,且有未溶解的溶质。
曲线下面的点C:
不饱和溶液
从溶解度曲线上获取的信息
温度
溶解度
从溶解度曲线上获取的信息
线:某物质溶解度受温度影响的变化情况
交点:曲线的交点表示这两种物质在该温度下的溶解度相同,饱和溶液的溶质质量分数也相同。
(1)“上升型”:多数固体物质的溶解度随着温度的升高而增大,如硝酸钾KNO3;
(2)“平缓型”:少数固体物质的溶解度受温度变化的影响小,如氯化钠NaCl;
(3)“下降型”:极少数固体物质的溶解度随着温度的升高而减小,如氢氧化钙Ca(OH)2。
固体物质溶解度随温度变化的规律
氢氧化钙
从溶解度曲线上还能获取的信息
四.溶解度的表示方法---溶解度曲线
(5)确定结晶的方法。
(1)查询某物质在某温度下的溶解度;
(2)比较不同物质在同一温度时的溶解度大小;
(3)判断各种物质溶解度受温度影响的变化趋势;
(4)判断溶液是否饱和;
多识一点
降温结晶
观察硝酸钾的溶解度曲线,可以看出硝酸钾的溶解度受温度的影响较大。
对于这样的物质,可采取冷却热饱和溶液的方法,使溶质从溶液中结晶析出,这种方法称为降温结晶。
0
20
80
31.6
169
溶解度
/g
温度/℃
80 ℃时,100 g水中最多溶解169 g硝酸钾
由80 ℃冷却到20 ℃
20 ℃时,100 g水中只能溶解31.6 g硝酸钾,析出硝酸钾晶体的质量为:169 g-31.6 g=137.4 g
思考
观察氯化钠的溶解度曲线,判断
氯化钠的溶解度受温度变化的影
响是大还是小?为什么要用蒸发
结晶的方法从海水中得到盐,而
不用降温结晶的方法?
氯化钠溶解度随温度升高变化不明显,故用蒸发结晶。
降温结晶(冷却热饱和溶液):
提纯溶解度随温度升高显著增大的物质。
除杂:KNO3 (NaCl)
方法:
步骤:
降温结晶
①溶解
②蒸发浓缩
③降温结晶
④过滤
从溶解度曲线分析结晶法除杂
蒸发结晶法(蒸发溶剂法):
提纯溶解度随温度升高而变化不明显的物质。
除杂: NaCl (KNO3)
方法:
蒸发结晶
步骤:
①溶解
③过滤
②蒸发结晶
从溶解度曲线分析结晶法除杂
总结:提纯谁,就让谁结晶,陡用降温,平用蒸发。
溶解度
概念
溶质质量
饱和状态
一定温度
100g水
表示
溶解度曲线
结晶
溶解性
定量表示
蒸发结晶
降温结晶
盘点收获
课堂小结
1.下列说法中正确的是( )
A.20℃时,100g水里最多能溶解36g氯化钠,所以20℃时氯化钠的溶解度为36g
B.20℃时,硝酸钾的溶解度为31.6
C.20℃时,在100g水中加入35g氯化钠完全溶解,则20℃时,氯化钠的溶解度为35g
D.20℃时,100g氯化钠的饱和溶液中有26.5g氯化钠,则 20℃
时,氯化钠的溶解度为26.5g
E.硝酸钾的溶解度为31.6g
A
课堂练习
课堂练习
2. 增大二氧化碳在水中的溶解度的方法( )
A. 升温增压
B. 升温减压
C. 降温增压
D. 降温减压
C
课堂练习
3.下表是KNO3部分溶解度数据,回答问题
(1)40℃时,将70gKNO3固体加入100g水中,充分搅拌,形成的溶液质量为
g。
(2)0℃时,使KNO3的饱和溶液要变成不饱和溶液方法是 (写一种)。
163.9
加入水
4.如图是A、B、C三种固体的溶解度曲线,回答下列问题。
(1)点P表示 。
(2)t2 ℃时,A、B、C的溶解度由大到小的顺序为 。
(3)要使接近饱和的C的溶液变为饱和,需要 温度。
(4)t2 ℃时,A物质的饱和溶液150 g降温到t1 ℃析出A g。
(5)t2 ℃时,将等质量A、B、C三种物质的饱和溶液降温到t1 ℃,析出晶体的质量由大到小的顺序是 。
(6)当A中含有少量B时,提纯A,可采用 的方法;当B中含有少量A时,提纯B,可采用 的方法。
t1℃时,A、C的溶解度相同
A>B>C
升高
30
A>B>C
降温结晶
蒸发结晶
课堂练习
谢 谢 观 看
同课章节目录
