2.2 第3课时 相对原子质量、离子 课件(共24张PPT内嵌视频) 2024-2025学年化学科粤版九年级上册
文档属性
| 名称 | 2.2 第3课时 相对原子质量、离子 课件(共24张PPT内嵌视频) 2024-2025学年化学科粤版九年级上册 |

|
|
| 格式 | pptx | ||
| 文件大小 | 13.7MB | ||
| 资源类型 | 教案 | ||
| 版本资源 | 科粤版 | ||
| 科目 | 化学 | ||
| 更新时间 | 2024-12-28 00:00:00 | ||
图片预览







文档简介
(共24张PPT)
第二单元 空气、物质的构成与组成
2.2 构成物质的微观粒子
第3课时 相对原子质量、离子
新知导入:
原子的体积很小
原子直径约为发丝直径的万分之一
原子的质量约为羽毛质量的10-23
.
原子
乒乓球
、质量也很小
主问题一:原子的质量有多大?
一个氢原子的质量
0.000000000000000000000000001674 kg
=1.674×10-27 kg
H
=1.993×10-26 kg
=2.657×10-26 kg
一个碳原子的质量
0.00000000000000000000000002657 kg
C
O
0.00000000000000000000000001993 kg
一个氧原子的质量
主问题一:原子的质量有多大?
相对原子质量(Ar)
三层楼高
一箭之地
两袋烟的功夫
两层楼高
相对
高度
相对
长度
相对
时间
相对就是要找个标准与其进行比较,相对原子质量的标准又是什么呢?
主问题一:原子的质量有多大?
1803年
1959年
1927年
发现氧含有三种原子
道尔顿提出,以氢原子质量为1作为原子量的标准。
改用氧原子质量的1/16为标准。
后来
经过计算,改用16O的1/16作为标准。
1959年,国际提出以12C的1/12作为最终标准。
发展史:
沿用至今
相对原子质量(Ar)
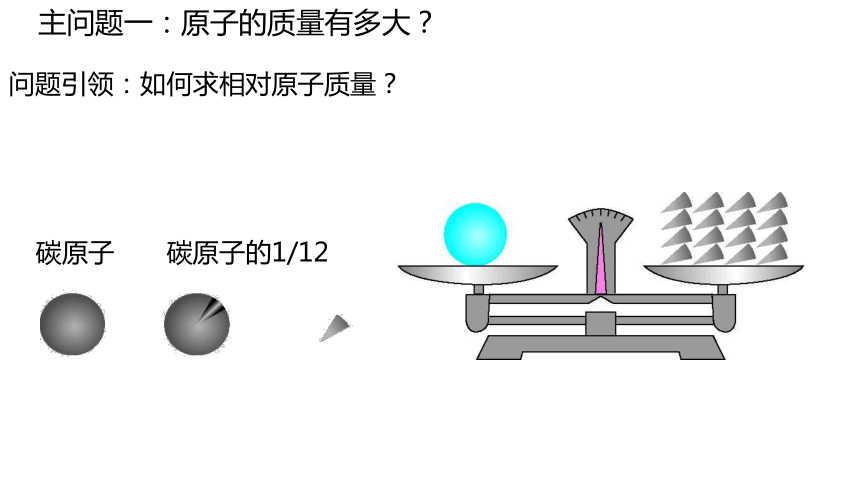
主问题一:原子的质量有多大?
问题引领:如何求相对原子质量?
碳原子
碳原子的1/12
主问题一:原子的质量有多大?
相对原子质量
以一种碳原子(碳12)质量的1/12作为标准,把其他原子的质量跟这个标准相比较所得到的比值,称为这种原子的相对原子质量(Ar)
相对原子质量的数学计算式
相对原子质量 =
(Ar)
一个该原子的质量
一种碳12原子的质量×1/12
主问题一:原子的质量有多大?
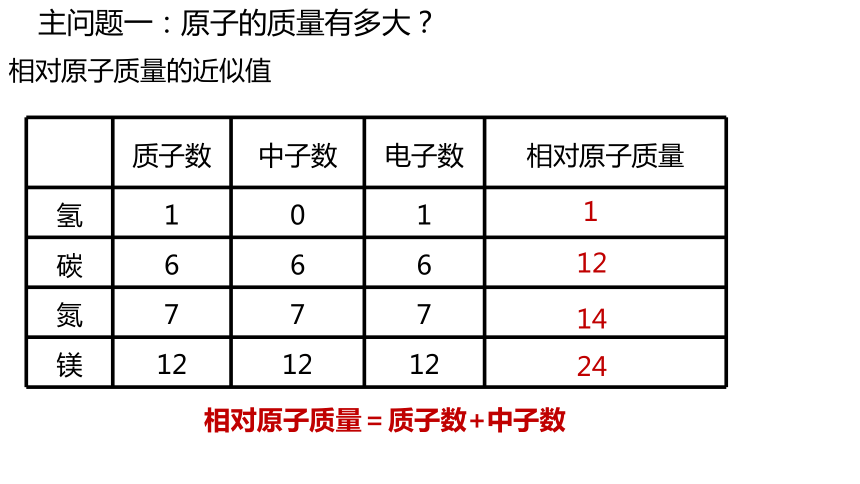
相对原子质量的近似值
质子数 中子数 电子数 相对原子质量
氢 1 0 1
碳 6 6 6
氮 7 7 7
镁 12 12 12
1
12
14
24
相对原子质量=质子数+中子数
主问题一:原子的质量有多大?
相对原子质量与原子质量的区别
相对原子质量是一个 “比值”,单位为“1” ,通常省略不写。
而原子质量指的是原子的实际质量,一般以“克(g)”或“千克(kg)”为单位。
中国科学院院士张青莲教授为相对原子质量的测定作出了卓越贡献。他于1983年当选为国际原子量委员会衔称委员。他主持测定了铟、铱、锑、铕、铈、铒、锗、锌、钐、镝等的相对原子质量的新值,被国际原子量委员会采用为国际新标准。
张青莲(1908~2006)
科学成就
主问题二 :离子是如何形成的?如何表示离子?
主问题二 :离子是如何形成的?如何表示离子?
氯化钠(NaCl)的形成过程
Cl
-
Na
+
Na
+
Cl
-
阳离子
阴离子
化合物
1个e-
+11
2
8
1
+17
2
8
7
Na
Cl
+17
2
8
8
+11
2
8
主问题二 :离子是如何形成的?如何表示离子?
总结归纳
离子:带电的原子(或原子团)
得电子带负电荷,形成阴离子,如S2-、Cl-
失电子带正电荷,形成阳离子,如Na+、Al3+
阳离子( + )
失电子
原子
阴离子( - )
得电子
离子也是构成物质的一种微观粒子。
主问题二 :离子是如何形成的?如何表示离子?
离子如何表示:
在元素符号的右上角标出离子所带的电荷数,数值在前,正、负号在后。
当离子带1个单位的正电荷或1个单位的负电荷时,“1” 省略不写。
如:Na+ Mg2+ Cl- O2-
主问题二 :离子是如何形成的?如何表示离子?
离子符号的意义:
Mg2+
表示1个镁离子带2个单位的正电荷
表示1个X离子带X个单位的正(或负)电荷
主问题二 :离子是如何形成的?如何表示离子?
离子符号的意义(说出其中2的含义)
2Mg2+
表示2个镁离子
表示1个镁离子带2个单位的正电荷
说出下面符号的意义
表示1个钙离子带2个单位的正电荷
表示2个钙离子
Ca2+
2
主问题二 :离子是如何形成的?如何表示离子?
粒子结构特征
原 子: 核电荷数 质子数 核外电子数
阳离子: 核电荷数 质子数 核外电子数
阴离子: 核电荷数 质子数 核外电子数
=
=
=
=
>
<
主问题二 :原子和离子的关系
原子和离子的区别与联系
原子 阳离子 阴离子
结构 质子数=核外电子数 质子数>核外电子数 质子数<核外电子数
电性 不显电性 带正电荷 带负电荷
是否达到 稳定结构 大多数原子最外层 没有达到稳定结构 最外层达到 稳定结构 最外层达到
稳定结构
联系 阳离子 原子 阴离子 失电子
得电子
课堂小结
课堂小结
课堂练习
课堂练习
1.如图所示的原子中,在化学反应中易得到电子的是 ( )
2.下列关于相对原子质量的说法,不正确的是 ( )
A.相对原子质量是一个比值
B.相对原子质量代表各类原子实际质量的相对大小
C.相对原子质量就是原子的实际质量
D.相对原子质量也有单位
D
C
课堂练习
3.制造北斗三号卫星使用了钛合金材料,钛原子的质子数为22,相对原子质量为48,则钛原子的核外电子数为 ( )
A.22 B.48 C.70 D.26
4.如图为四种原子的结构示意图,其中化学性质相似的一组是 ( )
A.①和② B.①和③ C.②和③ D.③和④
A
B
课堂练习
5.“Ca2+”右上角的数字表示的意义是 ( )
A.钙原子最外层有2个电子
B.钙原子有2个电子层
C.1个钙离子带2个单位的正电荷
D.2个钙离子
C
课堂练习
6.A、B、C三种粒子的结构示意图如图所示。
(1)当A、B为原子时,x= ;y= 。
(2)C表示的粒子符号是 。
8
1
Cl-
谢 谢 观 看
第二单元 空气、物质的构成与组成
2.2 构成物质的微观粒子
第3课时 相对原子质量、离子
新知导入:
原子的体积很小
原子直径约为发丝直径的万分之一
原子的质量约为羽毛质量的10-23
.
原子
乒乓球
、质量也很小
主问题一:原子的质量有多大?
一个氢原子的质量
0.000000000000000000000000001674 kg
=1.674×10-27 kg
H
=1.993×10-26 kg
=2.657×10-26 kg
一个碳原子的质量
0.00000000000000000000000002657 kg
C
O
0.00000000000000000000000001993 kg
一个氧原子的质量
主问题一:原子的质量有多大?
相对原子质量(Ar)
三层楼高
一箭之地
两袋烟的功夫
两层楼高
相对
高度
相对
长度
相对
时间
相对就是要找个标准与其进行比较,相对原子质量的标准又是什么呢?
主问题一:原子的质量有多大?
1803年
1959年
1927年
发现氧含有三种原子
道尔顿提出,以氢原子质量为1作为原子量的标准。
改用氧原子质量的1/16为标准。
后来
经过计算,改用16O的1/16作为标准。
1959年,国际提出以12C的1/12作为最终标准。
发展史:
沿用至今
相对原子质量(Ar)
主问题一:原子的质量有多大?
问题引领:如何求相对原子质量?
碳原子
碳原子的1/12
主问题一:原子的质量有多大?
相对原子质量
以一种碳原子(碳12)质量的1/12作为标准,把其他原子的质量跟这个标准相比较所得到的比值,称为这种原子的相对原子质量(Ar)
相对原子质量的数学计算式
相对原子质量 =
(Ar)
一个该原子的质量
一种碳12原子的质量×1/12
主问题一:原子的质量有多大?
相对原子质量的近似值
质子数 中子数 电子数 相对原子质量
氢 1 0 1
碳 6 6 6
氮 7 7 7
镁 12 12 12
1
12
14
24
相对原子质量=质子数+中子数
主问题一:原子的质量有多大?
相对原子质量与原子质量的区别
相对原子质量是一个 “比值”,单位为“1” ,通常省略不写。
而原子质量指的是原子的实际质量,一般以“克(g)”或“千克(kg)”为单位。
中国科学院院士张青莲教授为相对原子质量的测定作出了卓越贡献。他于1983年当选为国际原子量委员会衔称委员。他主持测定了铟、铱、锑、铕、铈、铒、锗、锌、钐、镝等的相对原子质量的新值,被国际原子量委员会采用为国际新标准。
张青莲(1908~2006)
科学成就
主问题二 :离子是如何形成的?如何表示离子?
主问题二 :离子是如何形成的?如何表示离子?
氯化钠(NaCl)的形成过程
Cl
-
Na
+
Na
+
Cl
-
阳离子
阴离子
化合物
1个e-
+11
2
8
1
+17
2
8
7
Na
Cl
+17
2
8
8
+11
2
8
主问题二 :离子是如何形成的?如何表示离子?
总结归纳
离子:带电的原子(或原子团)
得电子带负电荷,形成阴离子,如S2-、Cl-
失电子带正电荷,形成阳离子,如Na+、Al3+
阳离子( + )
失电子
原子
阴离子( - )
得电子
离子也是构成物质的一种微观粒子。
主问题二 :离子是如何形成的?如何表示离子?
离子如何表示:
在元素符号的右上角标出离子所带的电荷数,数值在前,正、负号在后。
当离子带1个单位的正电荷或1个单位的负电荷时,“1” 省略不写。
如:Na+ Mg2+ Cl- O2-
主问题二 :离子是如何形成的?如何表示离子?
离子符号的意义:
Mg2+
表示1个镁离子带2个单位的正电荷
表示1个X离子带X个单位的正(或负)电荷
主问题二 :离子是如何形成的?如何表示离子?
离子符号的意义(说出其中2的含义)
2Mg2+
表示2个镁离子
表示1个镁离子带2个单位的正电荷
说出下面符号的意义
表示1个钙离子带2个单位的正电荷
表示2个钙离子
Ca2+
2
主问题二 :离子是如何形成的?如何表示离子?
粒子结构特征
原 子: 核电荷数 质子数 核外电子数
阳离子: 核电荷数 质子数 核外电子数
阴离子: 核电荷数 质子数 核外电子数
=
=
=
=
>
<
主问题二 :原子和离子的关系
原子和离子的区别与联系
原子 阳离子 阴离子
结构 质子数=核外电子数 质子数>核外电子数 质子数<核外电子数
电性 不显电性 带正电荷 带负电荷
是否达到 稳定结构 大多数原子最外层 没有达到稳定结构 最外层达到 稳定结构 最外层达到
稳定结构
联系 阳离子 原子 阴离子 失电子
得电子
课堂小结
课堂小结
课堂练习
课堂练习
1.如图所示的原子中,在化学反应中易得到电子的是 ( )
2.下列关于相对原子质量的说法,不正确的是 ( )
A.相对原子质量是一个比值
B.相对原子质量代表各类原子实际质量的相对大小
C.相对原子质量就是原子的实际质量
D.相对原子质量也有单位
D
C
课堂练习
3.制造北斗三号卫星使用了钛合金材料,钛原子的质子数为22,相对原子质量为48,则钛原子的核外电子数为 ( )
A.22 B.48 C.70 D.26
4.如图为四种原子的结构示意图,其中化学性质相似的一组是 ( )
A.①和② B.①和③ C.②和③ D.③和④
A
B
课堂练习
5.“Ca2+”右上角的数字表示的意义是 ( )
A.钙原子最外层有2个电子
B.钙原子有2个电子层
C.1个钙离子带2个单位的正电荷
D.2个钙离子
C
课堂练习
6.A、B、C三种粒子的结构示意图如图所示。
(1)当A、B为原子时,x= ;y= 。
(2)C表示的粒子符号是 。
8
1
Cl-
谢 谢 观 看
同课章节目录
