2.2 课时1 分子结构测定 多样分子空间结构 课件(共25张PPT) 2024-2025学年高二化学人教版(2019)选择性必修2
文档属性
| 名称 | 2.2 课时1 分子结构测定 多样分子空间结构 课件(共25张PPT) 2024-2025学年高二化学人教版(2019)选择性必修2 |

|
|
| 格式 | pptx | ||
| 文件大小 | 6.8MB | ||
| 资源类型 | 教案 | ||
| 版本资源 | 人教版(2019) | ||
| 科目 | 化学 | ||
| 更新时间 | 2024-12-29 00:00:00 | ||
图片预览





文档简介
(共25张PPT)
分子结构的测定与多样性
多样的分子空间结构
第二章 分子结构与性质
1.了解分子结构的测定方法。
2.通过对典型分子空间结构的学习,认识微观结构对分子空间结构的影响,了解共价分子结构的多样性和复杂性。
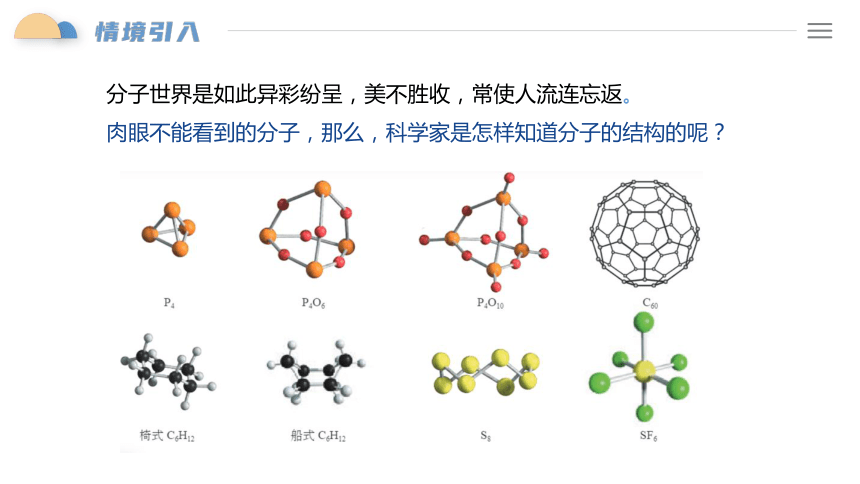
分子世界是如此异彩纷呈,美不胜收,常使人流连忘返。
肉眼不能看到的分子,那么,科学家是怎样知道分子的结构的呢?
一、分子结构的测定
早年科学家主要靠对物质的化学性质进行系统总结得出规律后进行推测,现代科学家应用了许多测定分子结构的现代仪器和方法,如红外光谱、晶体X射线衍射以及质谱仪等
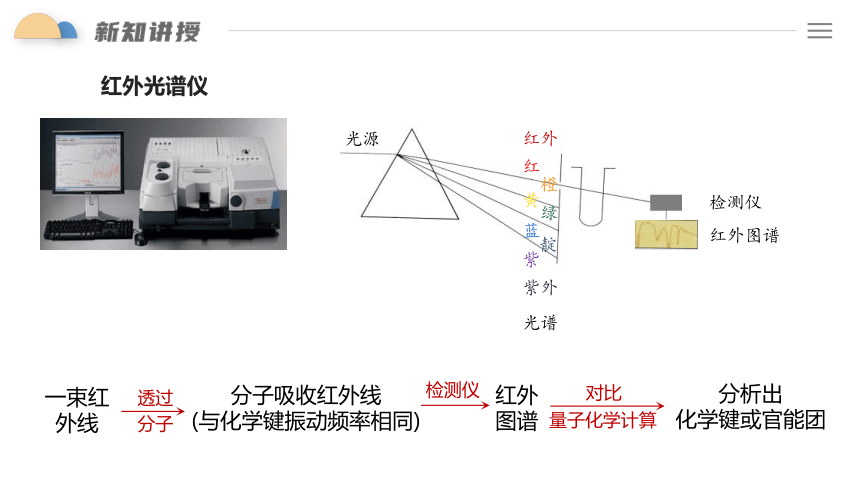
红外光谱仪
X射线衍射仪
质谱仪
测定化学键或官能团
测定键长、键角等
测定相对分子质量
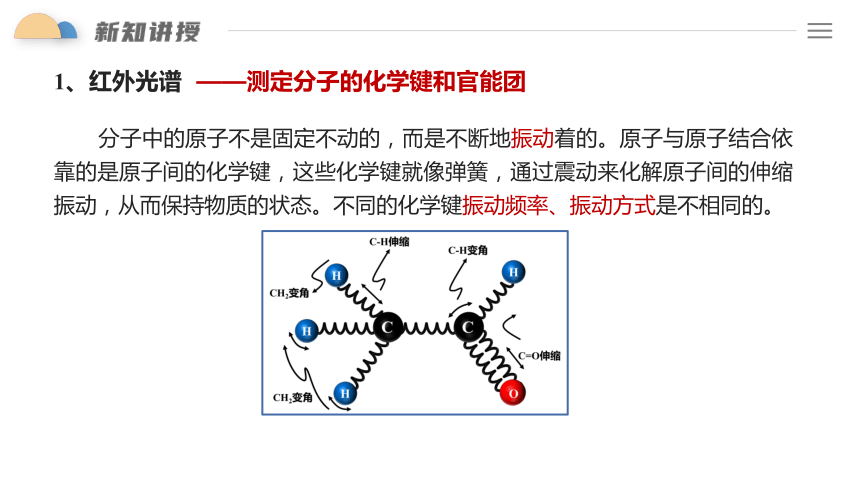
1、红外光谱
——测定分子的化学键和官能团
分子中的原子不是固定不动的,而是不断地振动着的。原子与原子结合依靠的是原子间的化学键,这些化学键就像弹簧,通过震动来化解原子间的伸缩振动,从而保持物质的状态。不同的化学键振动频率、振动方式是不相同的。
紫外
光谱
检测仪
红外图谱
光源
红
红外
紫
靛
蓝
橙
黄
绿
红外光谱仪
分子吸收红外线
(与化学键振动频率相同)
分析出
化学键或官能团
对比
量子化学计算
一束红外线
透过分子
红外图谱
检测仪
分子式为C2H6O
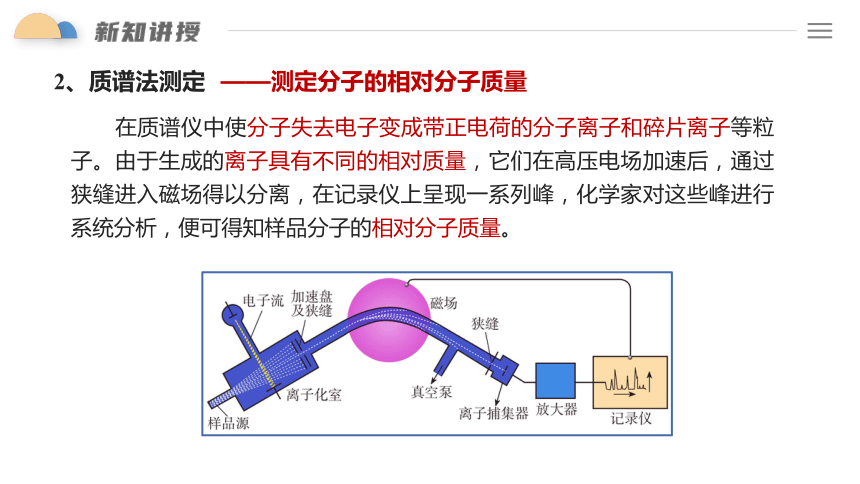
2、质谱法测定
——测定分子的相对分子质量
在质谱仪中使分子失去电子变成带正电荷的分子离子和碎片离子等粒子。由于生成的离子具有不同的相对质量,它们在高压电场加速后,通过狭缝进入磁场得以分离,在记录仪上呈现一系列峰,化学家对这些峰进行系统分析,便可得知样品分子的相对分子质量。
质谱仪
质谱仪原理示意图
分析
图谱
分子离子和
碎片离子
分子
失去电子
高压电
场加速
通过狭缝进
入磁场分离
记录仪
质谱图
得出分子的相
对分子质量
相对分子质量=最大质荷比
质谱仪图
质谱:纵坐标表示相对丰度,横坐标表示粒子的相对质量与其电荷数之比(m/z),简称荷质比,化学家通过分析得知,被测物的相对分子质量是92,该物质是甲苯。
2.如图有机物A质谱图,则A的相对分子质量是
A.29 B.43 C.57 D.72
D
1.下列关于红外光谱法测定分子结构的说法中,不正确的是( )
A.红外线透过分子时,分子会吸收特定频率的红外线
B.分子中原子是固定不动的
C.红外光谱法可初步判断有机物分子中基团的种类
D.所用仪器为红外光谱仪
B
思考与讨论
1、利用几何知识分析一下,空间分布的两个点是否一定在同一直线?
迁移:两个原子构成的分子,将这2个原子看成两个点
O2
HCl
2、空间分布的三个点是否一定在同一直线上?
CO2
H2O
二、多样的分子空间结构
在多原子构成的分子中,由于原子间排列的空间顺序不一样,于是分子就有了原子的几何学关系和形状,这就是分子的空间结构。
单原子分子(稀有气体分子)、双原子分子不存在空间结构
三原子分子
化学式
电子式
分子的空间结构模型
结构式
键角
CO2
H2O
直线形
V形
180
105
180
105
四原子分子
化学式
电子式
分子的空间结构模型
结构式
CH2O
NH3
平面三角形
三角锥形
键角
约120
107
120
107
四原子分子其他立体构型(直线形、正四面体形)
C2H2 180°
P4 60°正四面体形
BF3
平面正三角形 120°
H2O2 H-O-O-H
H2O2分子不是直线形,两个H原子犹如在半展开的书的两页上,两个氧原子则在书的夹缝上。
五原子分子
化学式
电子式
分子的空间结构模型
结构式
CH4
CCl4
正四面体形
正四面体形
键角
109°28′
109°28′
其他多原子分子的空间结构
P4
P4O6
P4O10
C60
椅式C6H12
船式C6H12
S8
SF6
分子空间结构与其稳定性有关
又如,椅式C6H12 比 船式 C6H12稳定。
108°
例如,S8像顶皇冠,如果把其中一个向上的硫原子倒转向下,尽管也可以存在,却不如皇冠式稳定。
分子的空间结构与键角关系的一般规律
分子类型 键角 空间结构 实例
AB2 180 直线形 CO2、BeCl2、CS2
<180 V形 H2O、H2S
AB3 120 平面三角形 BF3、BCl3、CH2O
<120 三角锥形 NH3、PH3
AB4 109 28′ 正四面体形 CH4、CCl4
C60
C70
C240
(1)四原子分子一定都是平面三角形或三角锥形( )
(2)正四面体形的键角均为109°28′( )
(3)SiCl4、SiH4、NH、CH3Cl均为正四面体结构( )
(4)SF6分子的空间结构为正八面体形( )
(5)椅式C6H12比船式C6H12稳定( )
1.判断正误。
C
2.可以准确判断有机物分子中含有哪些官能团的分析方法是( )
A.核磁共振氢谱 B.质谱
C.红外光谱 D.紫外光谱
×
×
×
√
√
3.下列分子的空间结构模型正确的是( )
A.CO2的空间结构模型:
B.H2O的空间结构模型:
C.NH3的空间结构模型:
D.CH4的空间结构模型:
D
4.下列分子的空间结构与分子中共价键键角对应正确的是 ( )
A.V形:105° B.平面正三角形:120°
C.三角锥形:109°28 D.正四面体形:109°28
5.下列物质分子的空间结构与CH4相同的是( )
A. H2O B. P4 C. NH3 D. CO2
B
B
6. (1)硫化氢(H2S)分子中,两个H—S的夹角接近90°,说明H2S分子的空间结构为________。
(2)二硫化碳(CS2)分子中,两个C==S的夹角是180°,说明CS2分子的空间结构为________。
(3)能说明CH4分子不是平面四边形,而是正四面体结构的是__________(填字母)。
a.两个键之间的夹角为109°28′
b.C—H为极性共价键
c.4个C—H的键能、键长都相等
d.二氯甲烷(CH2Cl2)只有一种(不存在同分异构体)
V形
直线形
ad
分子结构的测定与多样性
多样的分子空间结构
第二章 分子结构与性质
1.了解分子结构的测定方法。
2.通过对典型分子空间结构的学习,认识微观结构对分子空间结构的影响,了解共价分子结构的多样性和复杂性。
分子世界是如此异彩纷呈,美不胜收,常使人流连忘返。
肉眼不能看到的分子,那么,科学家是怎样知道分子的结构的呢?
一、分子结构的测定
早年科学家主要靠对物质的化学性质进行系统总结得出规律后进行推测,现代科学家应用了许多测定分子结构的现代仪器和方法,如红外光谱、晶体X射线衍射以及质谱仪等
红外光谱仪
X射线衍射仪
质谱仪
测定化学键或官能团
测定键长、键角等
测定相对分子质量
1、红外光谱
——测定分子的化学键和官能团
分子中的原子不是固定不动的,而是不断地振动着的。原子与原子结合依靠的是原子间的化学键,这些化学键就像弹簧,通过震动来化解原子间的伸缩振动,从而保持物质的状态。不同的化学键振动频率、振动方式是不相同的。
紫外
光谱
检测仪
红外图谱
光源
红
红外
紫
靛
蓝
橙
黄
绿
红外光谱仪
分子吸收红外线
(与化学键振动频率相同)
分析出
化学键或官能团
对比
量子化学计算
一束红外线
透过分子
红外图谱
检测仪
分子式为C2H6O
2、质谱法测定
——测定分子的相对分子质量
在质谱仪中使分子失去电子变成带正电荷的分子离子和碎片离子等粒子。由于生成的离子具有不同的相对质量,它们在高压电场加速后,通过狭缝进入磁场得以分离,在记录仪上呈现一系列峰,化学家对这些峰进行系统分析,便可得知样品分子的相对分子质量。
质谱仪
质谱仪原理示意图
分析
图谱
分子离子和
碎片离子
分子
失去电子
高压电
场加速
通过狭缝进
入磁场分离
记录仪
质谱图
得出分子的相
对分子质量
相对分子质量=最大质荷比
质谱仪图
质谱:纵坐标表示相对丰度,横坐标表示粒子的相对质量与其电荷数之比(m/z),简称荷质比,化学家通过分析得知,被测物的相对分子质量是92,该物质是甲苯。
2.如图有机物A质谱图,则A的相对分子质量是
A.29 B.43 C.57 D.72
D
1.下列关于红外光谱法测定分子结构的说法中,不正确的是( )
A.红外线透过分子时,分子会吸收特定频率的红外线
B.分子中原子是固定不动的
C.红外光谱法可初步判断有机物分子中基团的种类
D.所用仪器为红外光谱仪
B
思考与讨论
1、利用几何知识分析一下,空间分布的两个点是否一定在同一直线?
迁移:两个原子构成的分子,将这2个原子看成两个点
O2
HCl
2、空间分布的三个点是否一定在同一直线上?
CO2
H2O
二、多样的分子空间结构
在多原子构成的分子中,由于原子间排列的空间顺序不一样,于是分子就有了原子的几何学关系和形状,这就是分子的空间结构。
单原子分子(稀有气体分子)、双原子分子不存在空间结构
三原子分子
化学式
电子式
分子的空间结构模型
结构式
键角
CO2
H2O
直线形
V形
180
105
180
105
四原子分子
化学式
电子式
分子的空间结构模型
结构式
CH2O
NH3
平面三角形
三角锥形
键角
约120
107
120
107
四原子分子其他立体构型(直线形、正四面体形)
C2H2 180°
P4 60°正四面体形
BF3
平面正三角形 120°
H2O2 H-O-O-H
H2O2分子不是直线形,两个H原子犹如在半展开的书的两页上,两个氧原子则在书的夹缝上。
五原子分子
化学式
电子式
分子的空间结构模型
结构式
CH4
CCl4
正四面体形
正四面体形
键角
109°28′
109°28′
其他多原子分子的空间结构
P4
P4O6
P4O10
C60
椅式C6H12
船式C6H12
S8
SF6
分子空间结构与其稳定性有关
又如,椅式C6H12 比 船式 C6H12稳定。
108°
例如,S8像顶皇冠,如果把其中一个向上的硫原子倒转向下,尽管也可以存在,却不如皇冠式稳定。
分子的空间结构与键角关系的一般规律
分子类型 键角 空间结构 实例
AB2 180 直线形 CO2、BeCl2、CS2
<180 V形 H2O、H2S
AB3 120 平面三角形 BF3、BCl3、CH2O
<120 三角锥形 NH3、PH3
AB4 109 28′ 正四面体形 CH4、CCl4
C60
C70
C240
(1)四原子分子一定都是平面三角形或三角锥形( )
(2)正四面体形的键角均为109°28′( )
(3)SiCl4、SiH4、NH、CH3Cl均为正四面体结构( )
(4)SF6分子的空间结构为正八面体形( )
(5)椅式C6H12比船式C6H12稳定( )
1.判断正误。
C
2.可以准确判断有机物分子中含有哪些官能团的分析方法是( )
A.核磁共振氢谱 B.质谱
C.红外光谱 D.紫外光谱
×
×
×
√
√
3.下列分子的空间结构模型正确的是( )
A.CO2的空间结构模型:
B.H2O的空间结构模型:
C.NH3的空间结构模型:
D.CH4的空间结构模型:
D
4.下列分子的空间结构与分子中共价键键角对应正确的是 ( )
A.V形:105° B.平面正三角形:120°
C.三角锥形:109°28 D.正四面体形:109°28
5.下列物质分子的空间结构与CH4相同的是( )
A. H2O B. P4 C. NH3 D. CO2
B
B
6. (1)硫化氢(H2S)分子中,两个H—S的夹角接近90°,说明H2S分子的空间结构为________。
(2)二硫化碳(CS2)分子中,两个C==S的夹角是180°,说明CS2分子的空间结构为________。
(3)能说明CH4分子不是平面四边形,而是正四面体结构的是__________(填字母)。
a.两个键之间的夹角为109°28′
b.C—H为极性共价键
c.4个C—H的键能、键长都相等
d.二氯甲烷(CH2Cl2)只有一种(不存在同分异构体)
V形
直线形
ad
