甘肃省武威第二十中2024-2025学年第一学期九年级化学新人教版期末模拟练习(含答案)
文档属性
| 名称 | 甘肃省武威第二十中2024-2025学年第一学期九年级化学新人教版期末模拟练习(含答案) | 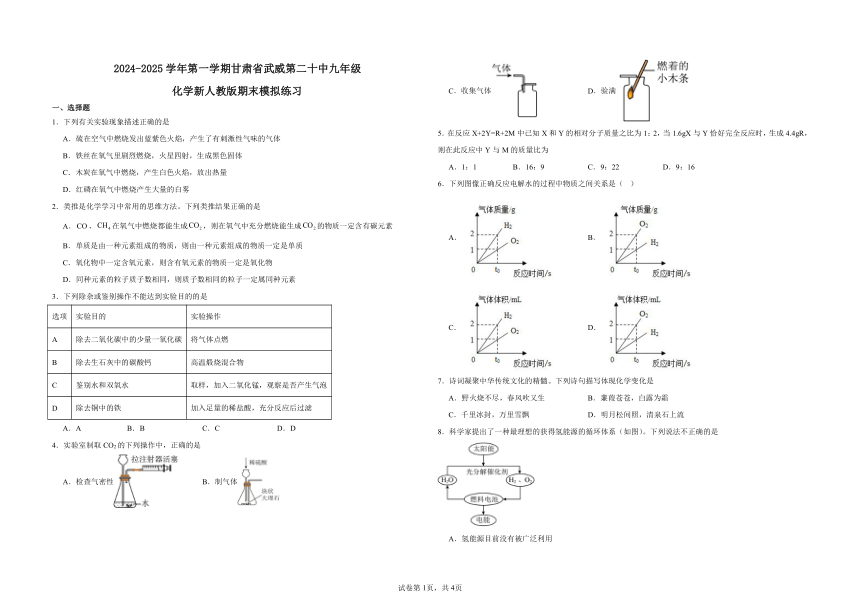 | |
| 格式 | docx | ||
| 文件大小 | 767.8KB | ||
| 资源类型 | 教案 | ||
| 版本资源 | 人教版 | ||
| 科目 | 化学 | ||
| 更新时间 | 2025-01-03 07:51:31 | ||
图片预览

文档简介
2024-2025学年第一学期甘肃省武威第二十中九年级
化学新人教版期末模拟练习
一、选择题
1.下列有关实验现象描述正确的是
A.硫在空气中燃烧发出蓝紫色火焰,产生了有刺激性气味的气体
B.铁丝在氧气里剧烈燃烧,火星四射,生成黑色固体
C.木炭在氧气中燃烧,产生白色火焰,放出热量
D.红磷在氧气中燃烧产生大量的白雾
2.类推是化学学习中常用的思维方法。下列类推结果正确的是
A.、在氧气中燃烧都能生成,则在氧气中充分燃烧能生成的物质一定含有碳元素
B.单质是由一种元素组成的物质,则由一种元素组成的物质一定是单质
C.氧化物中一定含氧元素,则含有氧元素的物质一定是氧化物
D.同种元素的粒子质子数相同,则质子数相同的粒子一定属同种元素
3.下列除杂或鉴别操作不能达到实验目的的是
选项 实验目的 实验操作
A 除去二氧化碳中的少量一氧化碳 将气体点燃
B 除去生石灰中的碳酸钙 高温煅烧混合物
C 鉴别水和双氧水 取样,加入二氧化锰,观察是否产生气泡
D 除去铜中的铁 加入足量的稀盐酸,充分反应后过滤
A.A B.B C.C D.D
4.实验室制取CO2的下列操作中,正确的是
A.检查气密性 B.制气体
C.收集气体 D.验满
5.在反应X+2Y=R+2M中已知X和Y的相对分子质量之比为1:2,当1.6gX与Y恰好完全反应时,生成4.4gR,则在此反应中Y与M的质量比为
A.1:1 B.16:9 C.9:22 D.9:16
6.下列图像正确反应电解水的过程中物质之间关系是( )
A. B.
C. D.
7.诗词凝聚中华传统文化的精髓。下列诗句描写体现化学变化是
A.野火烧不尽,春风吹又生 B.蒹葭苍苍,白露为霜
C.千里冰封,万里雪飘 D.明月松间照,清泉石上流
8.科学家提出了一种最理想的获得氢能源的循环体系(如图)。下列说法不正确的是
A.氢能源目前没有被广泛利用
B.光分解催化剂在化学反应前后质量和性质会改变
C.该氢能源循环体系能实现将太阳能转化为电能
D.分解的水的质量等于生成的氧气和氢气的质量和
9.我国古代将炉甘石、赤铜和木炭粉混合加热到约800℃,可制得外观似金子的合金,其中发生的一个反应的化学方程式为,下列说法正确的是
A.X的化学式为CO
B.中铜元素与氧元素的质量比为
C.中Cu的化合价为+2
D.该反应体现了木炭的还原性
10.同学们前往实验室参观,实验员正将甲、乙、丙、丁四种物质在密闭容器中混合,使其在一定条件下反应一段时间,测得反应前后各物质质量如表,则下列说法中不正确的是
甲 乙 丙 丁
反应前质量/g 40 3 2 3
反应后质量/g x 3 16 14
A.乙可能是催化剂 B.x的值为25
C.该反应是分解反应 D.生成的丙、丁质量之比为14:11
11.某反应的微观示意图如下(一种小球代表一种元素的原子),下列说法正确的是
A.该反应中共有四种原子
B.反应中各元素的化合价都不变
C.该反应的本质是分子分为原子,原子重新组合为新的分子
D.该反应属于化合反应
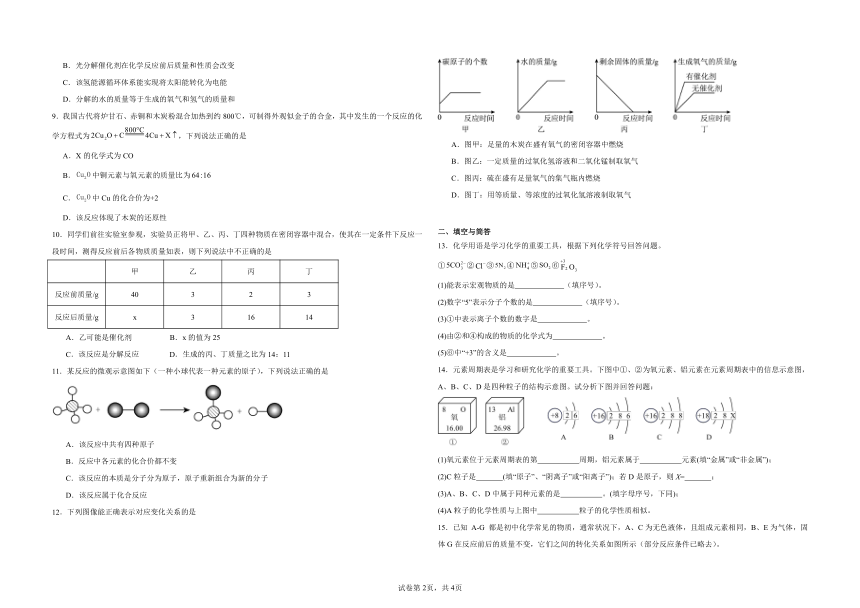
12.下列图像能正确表示对应变化关系的是
A.图甲:足量的木炭在盛有氧气的密闭容器中燃烧
B.图乙:一定质量的过氧化氢溶液和二氧化锰制取氧气
C.图丙:硫在盛有足量氧气的集气瓶内燃烧
D.图丁:用等质量、等浓度的过氧化氢溶液制取氧气
二、填空与简答
13.化学用语是学习化学的重要工具,根据下列化学符号回答问题。
①②③④⑤⑥
(1)能表示宏观物质的是 (填序号)。
(2)数字“5”表示分子个数的是 (填序号)。
(3)①中表示离子个数的数字是 。
(4)由②和④构成的物质的化学式为 。
(5)⑥中“+3”的含义是 。
14.元素周期表是学习和研究化学的重要工具。下图中①、②为氧元素、铝元素在元素周期表中的信息示意图,A、B、C、D是四种粒子的结构示意图。试分析下图并回答问题:
(1)氧元素位于元素周期表的第 周期,铝元素属于 元素(填“金属”或“非金属”);
(2)C粒子是 (填“原子”、“阴离子”或“阳离子”);若D是原子,则X= ;
(3)A、B、C、D中属于同种元素的是 。(填字母序号,下同);
(4)A粒子的化学性质与上图中 粒子的化学性质相似。
15.已知 A-G 都是初中化学常见的物质,通常状况下,A、C为无色液体,且组成元素相同,B、E为气体,固体G在反应前后的质量不变,它们之间的转化关系如图所示(部分反应条件已略去)。
(1)G 在化学反应中起 作用。
(2)写出③的化学方程式 。
(3)若D为黑色固体,反应②的化学方程式为 ;若燃烧产物F为黑色固体,反应②的化学方程式 。
16.如图是自来水厂净水过程示意图,据图回答下列问题。
(1)在沉淀池之前常加入适量 作混凝剂,以除去水中的悬浮杂质。
(2)通过沉淀池、过滤池除去的是水中的 (填“可溶性”或“不溶性”)杂质。
(3)吸附池中常用 吸附色素和异味。
(4)投药消毒过程中发生了 (填“化学”或“物理”)变化。
17.中华传统文化、中国前沿科技中蕴含着丰富的化学知识。
(1)毛笔笔杆常用竹管制作。竹管的主要成分为纤维素,化学式为(C6H10O5)n,纤维素由 种元素组成。
(2)《丹经》记载用硝石、硫黄、炭化的皂角经“伏火法”制成火药,其爆炸发生反应的化学方程式是2KNO3+3C+SK2S+3X↑+N2↑,则X为 。
(3)“长征五号”大推力运载火箭助力我国天宫空间站建设。该火箭助推器使用煤油(含C11H24、C12H26、C13H28等分子)作燃料,液氧作助燃剂。工业上利用石油中各成分的沸点不同,生产制备煤油,该生产过程发生的是 (填“物理变化”或“化学变化”)。
(4)“天舟号”货运飞船换装了以LiFePO4做正极材料的新型锂电池,用到的LiFePO4 (填“属于”或“不属于”)氧化物。
(5)空间站建设中,钛和钛合金以其优良的性能而得到普遍应用。钛是用铝粉与二氧化钛(TiO2)在高温条件下发生反应制得的,同时生成氧化铝,写出该反应的化学方程式 。
三、实验题
18.二氧化碳是空气的重要组成部分。下面是同学们在实验室制取二氧化碳并验证其性质的实验活动。
【制取二氧化碳】如图是实验室制取气体常用装置,请完成实验步骤、内容与分析。
(1)仪器a的名称是 。
(2)在实验室可选用装置 (填字母)组合制取并收集二氧化碳,连接仪器后,需 。
(3)加入试剂。先往试管内加入 ,然后加入其他试剂,立即用带有导管的橡胶塞塞住管口。观察到试管内发生的现象为 ,反应的化学方程式为 。
固定装置。连接好反应装置,将试管竖直固定在铁架台上。
(4)收集二氧化碳。用向上排空气法收集二氧化碳,将燃着的木条放在集气瓶 (填“口”或“内”),火焰熄灭,说明已收集满。收集满二氧化碳的集气瓶盖好玻璃片,正放在实验台上备用。
【验证二氧化碳性质】
(5)
示意图 活动内容、步骤与分析
①向盛有澄清石灰水的试管中通入二氧化碳,观察到
②将二氧化碳倒入放有燃着蜡烛的烧杯中,观察到
【实验拓展】
(6)实验室里一瓶石灰水中含有氢氧化钙,要使该石灰水中的氢氧化钙全部转化为碳酸钙沉淀,至少需要二氧化碳的质量是 g。
19.化学是以实验为基础的科学,同学们用如下实验装置进行气体制取和性质的探究,请回答下列问题。
任务一:制取气体
(1)利用如图1所示装置制取气体,完成下列表格。
制取气体 反应原理(化学方程式) 常用发生和收集装置(填序号)
O2
CO2
【分析讨论】
(2)用图1中B装置制取气体需要满足的条件是 。
(3)装置C与B相比较其优点是 。
【拓展探究】探究二氧化锰、氧化铜对过氧化氢分解的催化效果,设计了如下对比实验:
用如图2所示的装置进行了两次实验,在试管中分别加入等质量的氧化铜和二氧化锰,分别将注射器内盛有的3mL5%的双氧水注入试管中,利用注射器收集氧气,收集到氧气的体积和时间关系如图3所示。
(4)图2实验中观察到U形管内红墨水液面左低右高,说明此化学反应 (填“吸热”或“放热”)。
(5)分析图3可知二氧化锰催化效果比氧化铜好,此外还能得出的结论是 (写一点即可)。
任务二:探究性质
如图是探究氧气和二氧化碳性质的相关实验。
(6)为保证实验1现象明显,请写出一条有效措施 。图中集气瓶底部留有少量水的作用是 。
(7)实验2中先后观察到的现象是 ,其中体现二氧化碳化学性质的反应是 (用化学方程式表示),该反应的基本类型是 。
四、计算题
20.某生产化肥硝酸铵的企业,做了一个大型户外广告,如图所示。根据相关信息回答并计算:
主要成分:硝酸铵 含氮量居全球化肥之首:40% 净含量:袋
(1)硝酸铵中氮、氧、氢三种元素的质量比为 。
(2)硝酸铵中氮元素的质量分数为 。
(3)通过计算判断该广告属于 (填“虚假”或“真实”)广告。
(4)每袋该化肥中实际氮元素的质量不会超过 。
21.为测定某种贝壳中碳酸钙的含量,取25g贝壳,逐渐加入稀盐酸,充分反应后,测得剩余固体质量与加入稀盐酸的质量关系如图所示(已知杂质不参与反应,也不溶于水)请计算:
(1)这种贝壳中碳酸钙的质量分数是__________
(2)25g贝壳与稀盐酸恰好完全反应时,生成二氧化碳的质量为多少?(写出计算步骤)
(3)本实验是否可以用稀硫酸代替稀盐酸完成实验,并说明理由_____。
试卷第1页,共3页
试卷第1页,共3页
参考答案:
题号 1 2 3 4 5 6 7 8 9 10
答案 B A A A B C A B D B
题号 11 12
答案 C C
13.(1)⑤
(2)③
(3)5
(4)
(5)氧化铁中铁元素的化合价为+3
14.(1) 二 金属
(2) 阴离子 8
(3)B、C
(4)B
15.(1)催化
(2)
(3)
16.(1)明矾
(2)不溶性
(3)活性炭
(4)化学
17.(1)3/三
(2)CO2
(3)物理变化
(4)不属于
(5)
18.(1)铁架台
(2) BC 检查装置气密性
(3) 大理石(或石灰石) 有大量气泡产生
(4)口
(5) 澄清石灰水变浑浊 燃着蜡烛熄灭
(6)1.76
19.(1) 2KMnO4K2MnO4+MnO2+O2↑(或2H2O22H2O+O2↑) A和D(或A和E或B和D或B和E) CaCO3+2HCl=CaCl2+H2O+CO2↑ B和E(或C和E)
(2)反应物是固体与液体反应,是在常温下进行的
(3)可以控制反应的发生与停止
(4)放热
(5)催化剂不能改变生成氧气的量
(6) 铁丝表面要除锈(合理即可) 防止高温生成物溅落炸裂瓶底
(7) 紫色石蕊溶液变红,加热后红色消失,又恢复成紫色 H2O+CO2=H2CO3 化合反应
20.(1)7:12:1
(2)35%
(3)虚假
(4)17.5
21.(1)由图可以看出固体减少了20g,即碳酸钙的质量为20g,所以贝壳中碳酸钙的质量分数为;
(2)设恰好反应时,产生二氧化碳的质量为x
x=8.8g
(3)本实验不可以用稀硫酸代替稀盐酸完成实验,因为碳酸钙和稀硫酸反应生成微溶的硫酸钙,硫酸钙覆盖在碳酸钙的表面阻碍碳酸钙与稀硫酸的接触,导致不能继续反应,使反应慢慢停止。
答案第1页,共2页
答案第1页,共2页
化学新人教版期末模拟练习
一、选择题
1.下列有关实验现象描述正确的是
A.硫在空气中燃烧发出蓝紫色火焰,产生了有刺激性气味的气体
B.铁丝在氧气里剧烈燃烧,火星四射,生成黑色固体
C.木炭在氧气中燃烧,产生白色火焰,放出热量
D.红磷在氧气中燃烧产生大量的白雾
2.类推是化学学习中常用的思维方法。下列类推结果正确的是
A.、在氧气中燃烧都能生成,则在氧气中充分燃烧能生成的物质一定含有碳元素
B.单质是由一种元素组成的物质,则由一种元素组成的物质一定是单质
C.氧化物中一定含氧元素,则含有氧元素的物质一定是氧化物
D.同种元素的粒子质子数相同,则质子数相同的粒子一定属同种元素
3.下列除杂或鉴别操作不能达到实验目的的是
选项 实验目的 实验操作
A 除去二氧化碳中的少量一氧化碳 将气体点燃
B 除去生石灰中的碳酸钙 高温煅烧混合物
C 鉴别水和双氧水 取样,加入二氧化锰,观察是否产生气泡
D 除去铜中的铁 加入足量的稀盐酸,充分反应后过滤
A.A B.B C.C D.D
4.实验室制取CO2的下列操作中,正确的是
A.检查气密性 B.制气体
C.收集气体 D.验满
5.在反应X+2Y=R+2M中已知X和Y的相对分子质量之比为1:2,当1.6gX与Y恰好完全反应时,生成4.4gR,则在此反应中Y与M的质量比为
A.1:1 B.16:9 C.9:22 D.9:16
6.下列图像正确反应电解水的过程中物质之间关系是( )
A. B.
C. D.
7.诗词凝聚中华传统文化的精髓。下列诗句描写体现化学变化是
A.野火烧不尽,春风吹又生 B.蒹葭苍苍,白露为霜
C.千里冰封,万里雪飘 D.明月松间照,清泉石上流
8.科学家提出了一种最理想的获得氢能源的循环体系(如图)。下列说法不正确的是
A.氢能源目前没有被广泛利用
B.光分解催化剂在化学反应前后质量和性质会改变
C.该氢能源循环体系能实现将太阳能转化为电能
D.分解的水的质量等于生成的氧气和氢气的质量和
9.我国古代将炉甘石、赤铜和木炭粉混合加热到约800℃,可制得外观似金子的合金,其中发生的一个反应的化学方程式为,下列说法正确的是
A.X的化学式为CO
B.中铜元素与氧元素的质量比为
C.中Cu的化合价为+2
D.该反应体现了木炭的还原性
10.同学们前往实验室参观,实验员正将甲、乙、丙、丁四种物质在密闭容器中混合,使其在一定条件下反应一段时间,测得反应前后各物质质量如表,则下列说法中不正确的是
甲 乙 丙 丁
反应前质量/g 40 3 2 3
反应后质量/g x 3 16 14
A.乙可能是催化剂 B.x的值为25
C.该反应是分解反应 D.生成的丙、丁质量之比为14:11
11.某反应的微观示意图如下(一种小球代表一种元素的原子),下列说法正确的是
A.该反应中共有四种原子
B.反应中各元素的化合价都不变
C.该反应的本质是分子分为原子,原子重新组合为新的分子
D.该反应属于化合反应
12.下列图像能正确表示对应变化关系的是
A.图甲:足量的木炭在盛有氧气的密闭容器中燃烧
B.图乙:一定质量的过氧化氢溶液和二氧化锰制取氧气
C.图丙:硫在盛有足量氧气的集气瓶内燃烧
D.图丁:用等质量、等浓度的过氧化氢溶液制取氧气
二、填空与简答
13.化学用语是学习化学的重要工具,根据下列化学符号回答问题。
①②③④⑤⑥
(1)能表示宏观物质的是 (填序号)。
(2)数字“5”表示分子个数的是 (填序号)。
(3)①中表示离子个数的数字是 。
(4)由②和④构成的物质的化学式为 。
(5)⑥中“+3”的含义是 。
14.元素周期表是学习和研究化学的重要工具。下图中①、②为氧元素、铝元素在元素周期表中的信息示意图,A、B、C、D是四种粒子的结构示意图。试分析下图并回答问题:
(1)氧元素位于元素周期表的第 周期,铝元素属于 元素(填“金属”或“非金属”);
(2)C粒子是 (填“原子”、“阴离子”或“阳离子”);若D是原子,则X= ;
(3)A、B、C、D中属于同种元素的是 。(填字母序号,下同);
(4)A粒子的化学性质与上图中 粒子的化学性质相似。
15.已知 A-G 都是初中化学常见的物质,通常状况下,A、C为无色液体,且组成元素相同,B、E为气体,固体G在反应前后的质量不变,它们之间的转化关系如图所示(部分反应条件已略去)。
(1)G 在化学反应中起 作用。
(2)写出③的化学方程式 。
(3)若D为黑色固体,反应②的化学方程式为 ;若燃烧产物F为黑色固体,反应②的化学方程式 。
16.如图是自来水厂净水过程示意图,据图回答下列问题。
(1)在沉淀池之前常加入适量 作混凝剂,以除去水中的悬浮杂质。
(2)通过沉淀池、过滤池除去的是水中的 (填“可溶性”或“不溶性”)杂质。
(3)吸附池中常用 吸附色素和异味。
(4)投药消毒过程中发生了 (填“化学”或“物理”)变化。
17.中华传统文化、中国前沿科技中蕴含着丰富的化学知识。
(1)毛笔笔杆常用竹管制作。竹管的主要成分为纤维素,化学式为(C6H10O5)n,纤维素由 种元素组成。
(2)《丹经》记载用硝石、硫黄、炭化的皂角经“伏火法”制成火药,其爆炸发生反应的化学方程式是2KNO3+3C+SK2S+3X↑+N2↑,则X为 。
(3)“长征五号”大推力运载火箭助力我国天宫空间站建设。该火箭助推器使用煤油(含C11H24、C12H26、C13H28等分子)作燃料,液氧作助燃剂。工业上利用石油中各成分的沸点不同,生产制备煤油,该生产过程发生的是 (填“物理变化”或“化学变化”)。
(4)“天舟号”货运飞船换装了以LiFePO4做正极材料的新型锂电池,用到的LiFePO4 (填“属于”或“不属于”)氧化物。
(5)空间站建设中,钛和钛合金以其优良的性能而得到普遍应用。钛是用铝粉与二氧化钛(TiO2)在高温条件下发生反应制得的,同时生成氧化铝,写出该反应的化学方程式 。
三、实验题
18.二氧化碳是空气的重要组成部分。下面是同学们在实验室制取二氧化碳并验证其性质的实验活动。
【制取二氧化碳】如图是实验室制取气体常用装置,请完成实验步骤、内容与分析。
(1)仪器a的名称是 。
(2)在实验室可选用装置 (填字母)组合制取并收集二氧化碳,连接仪器后,需 。
(3)加入试剂。先往试管内加入 ,然后加入其他试剂,立即用带有导管的橡胶塞塞住管口。观察到试管内发生的现象为 ,反应的化学方程式为 。
固定装置。连接好反应装置,将试管竖直固定在铁架台上。
(4)收集二氧化碳。用向上排空气法收集二氧化碳,将燃着的木条放在集气瓶 (填“口”或“内”),火焰熄灭,说明已收集满。收集满二氧化碳的集气瓶盖好玻璃片,正放在实验台上备用。
【验证二氧化碳性质】
(5)
示意图 活动内容、步骤与分析
①向盛有澄清石灰水的试管中通入二氧化碳,观察到
②将二氧化碳倒入放有燃着蜡烛的烧杯中,观察到
【实验拓展】
(6)实验室里一瓶石灰水中含有氢氧化钙,要使该石灰水中的氢氧化钙全部转化为碳酸钙沉淀,至少需要二氧化碳的质量是 g。
19.化学是以实验为基础的科学,同学们用如下实验装置进行气体制取和性质的探究,请回答下列问题。
任务一:制取气体
(1)利用如图1所示装置制取气体,完成下列表格。
制取气体 反应原理(化学方程式) 常用发生和收集装置(填序号)
O2
CO2
【分析讨论】
(2)用图1中B装置制取气体需要满足的条件是 。
(3)装置C与B相比较其优点是 。
【拓展探究】探究二氧化锰、氧化铜对过氧化氢分解的催化效果,设计了如下对比实验:
用如图2所示的装置进行了两次实验,在试管中分别加入等质量的氧化铜和二氧化锰,分别将注射器内盛有的3mL5%的双氧水注入试管中,利用注射器收集氧气,收集到氧气的体积和时间关系如图3所示。
(4)图2实验中观察到U形管内红墨水液面左低右高,说明此化学反应 (填“吸热”或“放热”)。
(5)分析图3可知二氧化锰催化效果比氧化铜好,此外还能得出的结论是 (写一点即可)。
任务二:探究性质
如图是探究氧气和二氧化碳性质的相关实验。
(6)为保证实验1现象明显,请写出一条有效措施 。图中集气瓶底部留有少量水的作用是 。
(7)实验2中先后观察到的现象是 ,其中体现二氧化碳化学性质的反应是 (用化学方程式表示),该反应的基本类型是 。
四、计算题
20.某生产化肥硝酸铵的企业,做了一个大型户外广告,如图所示。根据相关信息回答并计算:
主要成分:硝酸铵 含氮量居全球化肥之首:40% 净含量:袋
(1)硝酸铵中氮、氧、氢三种元素的质量比为 。
(2)硝酸铵中氮元素的质量分数为 。
(3)通过计算判断该广告属于 (填“虚假”或“真实”)广告。
(4)每袋该化肥中实际氮元素的质量不会超过 。
21.为测定某种贝壳中碳酸钙的含量,取25g贝壳,逐渐加入稀盐酸,充分反应后,测得剩余固体质量与加入稀盐酸的质量关系如图所示(已知杂质不参与反应,也不溶于水)请计算:
(1)这种贝壳中碳酸钙的质量分数是__________
(2)25g贝壳与稀盐酸恰好完全反应时,生成二氧化碳的质量为多少?(写出计算步骤)
(3)本实验是否可以用稀硫酸代替稀盐酸完成实验,并说明理由_____。
试卷第1页,共3页
试卷第1页,共3页
参考答案:
题号 1 2 3 4 5 6 7 8 9 10
答案 B A A A B C A B D B
题号 11 12
答案 C C
13.(1)⑤
(2)③
(3)5
(4)
(5)氧化铁中铁元素的化合价为+3
14.(1) 二 金属
(2) 阴离子 8
(3)B、C
(4)B
15.(1)催化
(2)
(3)
16.(1)明矾
(2)不溶性
(3)活性炭
(4)化学
17.(1)3/三
(2)CO2
(3)物理变化
(4)不属于
(5)
18.(1)铁架台
(2) BC 检查装置气密性
(3) 大理石(或石灰石) 有大量气泡产生
(4)口
(5) 澄清石灰水变浑浊 燃着蜡烛熄灭
(6)1.76
19.(1) 2KMnO4K2MnO4+MnO2+O2↑(或2H2O22H2O+O2↑) A和D(或A和E或B和D或B和E) CaCO3+2HCl=CaCl2+H2O+CO2↑ B和E(或C和E)
(2)反应物是固体与液体反应,是在常温下进行的
(3)可以控制反应的发生与停止
(4)放热
(5)催化剂不能改变生成氧气的量
(6) 铁丝表面要除锈(合理即可) 防止高温生成物溅落炸裂瓶底
(7) 紫色石蕊溶液变红,加热后红色消失,又恢复成紫色 H2O+CO2=H2CO3 化合反应
20.(1)7:12:1
(2)35%
(3)虚假
(4)17.5
21.(1)由图可以看出固体减少了20g,即碳酸钙的质量为20g,所以贝壳中碳酸钙的质量分数为;
(2)设恰好反应时,产生二氧化碳的质量为x
x=8.8g
(3)本实验不可以用稀硫酸代替稀盐酸完成实验,因为碳酸钙和稀硫酸反应生成微溶的硫酸钙,硫酸钙覆盖在碳酸钙的表面阻碍碳酸钙与稀硫酸的接触,导致不能继续反应,使反应慢慢停止。
答案第1页,共2页
答案第1页,共2页
同课章节目录
