4.2 课时2 电解原理在工业上的应用——电解食盐水的应用及分析(22页)课件 2024-2025学年高二化学人教版(2019)选择性必修1
文档属性
| 名称 | 4.2 课时2 电解原理在工业上的应用——电解食盐水的应用及分析(22页)课件 2024-2025学年高二化学人教版(2019)选择性必修1 |

|
|
| 格式 | pptx | ||
| 文件大小 | 98.0MB | ||
| 资源类型 | 教案 | ||
| 版本资源 | 人教版(2019) | ||
| 科目 | 化学 | ||
| 更新时间 | 2025-01-04 00:00:00 | ||
图片预览








文档简介
(共22张PPT)
电解原理在工业上的应用
——电解食盐水的应用及分析
第四章 化学反应与电能
1.通过对氯碱工业原理的分析,掌握电解饱和食盐水的原理,认识电能与化学能之间的能量转化。
2.建立电解应用问题的分析思维模型和电解相关计算的思维模型,加深对电解原理的理解和应用。
【史料1】1774年瑞典化学家舍勒将软锰矿与浓盐酸混合加热,第一次制得 Cl2。
MnO2+4HCl(浓) MnCl2+Cl2↑+2H2O
△
卡尔·威尔海姆·舍勒
缺点:能耗大、污染大、产量低、成本高
阴极
阳极
e-
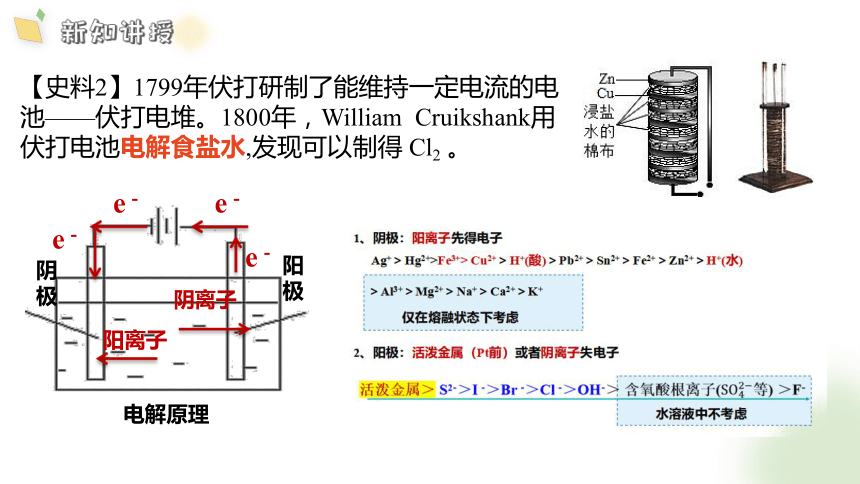
【史料2】1799年伏打研制了能维持一定电流的电池——伏打电堆。1800年,William Cruikshank用伏打电池电解食盐水,发现可以制得 Cl2 。
e-
e-
e-
阴离子
阳离子
电解原理
实验电解饱和食盐水
任务一:认识电解食盐水
请根据电解原理,书写惰性电极(石墨)电解食盐水的电极反应式和总反应方程式。
阴极:_____________________
阳极:_____________________
总离子反应:____________________________
2H2O+2e-===H2↑+2OH-
2Cl-+2H2O === Cl2↑+H2↑+2OH-
电解
2Cl--2e-===Cl2↑
问题1:两极区电解质溶液pH如何变化?
如何验证pH变化?
活动1:书写电解食盐水电极式
任务一:认识电解食盐水
氯碱工业
(3)溶液中存在的离子
Na+、 H+、 Cl-、 OH-
(4)比较放电顺序
阳极: Cl- > OH-
阴极: H+ > Na+
阳极 2Cl--2e-=Cl2↑
阴极 2H2O+2e-=H2↑+2OH-
(1)确定电解池的阴阳极
(2)电极材料
惰性,溶液中的离子放电
(5)写出电极反应
电解总反应方程式: 2NaCl+2H2O==Cl2↑+H2↑+2NaOH
电解
惰性电极电解饱和食盐水
思考: 若在两极附近均滴加酚酞试液,会有什么现象
阴极试液变红!阳极无明显变化!
如何验证pH变化?
紫甘蓝
pH试纸
pH计
酚酞
石蕊
甲基橙
酸碱指示剂
任务一:认识电解食盐水
活动2:实验验证两极区溶液pH变化
任务一:认识电解食盐水
预测实验现象 预测依据
两电极上:
阴极区溶液:
阳极区溶液:
气球
NaCl
溶液
阳极
阴极
紫甘蓝
活动2:实验验证两极区溶液pH变化
任务一:认识电解食盐水
气球
NaCl
溶液
阳极
阴极
预测实验现象 预测依据
Cl2+2H2O HCl+HClO
2Cl-+2H2O === Cl2↑+H2↑+2OH-
电解
阴极区生成NaOH
两电极均产生气泡,且阴极较快
阴极区溶液由紫色逐渐变为蓝色,再变为绿色
阳极区溶液由紫色逐渐变为红色
再变为无色
思考讨论
阴极
阳极
饱和NaCl溶液
生成H2、NaOH
生成Cl2
根据以上实验分析,你觉得电解饱和食盐水可用于制备什么生活用品?
电解食盐水的简易装置可以得到纯净的工业原料Cl2和NaOH吗?
漂白液:NaClO、NaCl
Cl2+2NaOH =NaCl+NaClO+H2O
1、产品Cl2和NaOH溶液会反应吗,那么Cl2能和NaOH溶液接触吗?
Cl2+2NaOH =NaCl+NaClO+H2O
2、产品Cl2和H2能混合吗?
遇火或强光会爆炸
解决方法:
生产设备:阳离子交换膜电解槽
不能
若工业上采用下图的装置制备NaOH、H2 、Cl2,存在何种不足之处?如何解决这个问题?
使用离子交换膜
H+
Na+
Cl-
OH-
活动3:完善氯碱工业装置
任务一:认识电解食盐水
+
-
阳 极
阴 极
请根据以上分析,在下图方框中填入所选交换膜、电解原料、电解产品,完善氯碱工业装置图。
+
-
Cl2
H2
Na+
淡盐水
NaOH溶液
饱和NaCl溶液
阳离子交换膜
阳 极
阴 极
饱和NaCl溶液
稀NaOH溶液
浓NaOH溶液
【思考】使用阳离子交换膜后,电路中每通过1mole-,阴极区溶液质量如何变化?
含氯漂白剂
有机合成、造纸
玻璃、肥皂
纺织、印染
有机合成
氯化物合成
农药
金属冶炼
有机合成
HCl
盐酸
H2
NaOH
湿氯气
湿氢气
液碱
Cl2
电解饱和食盐水
任务二:电解食盐水的应用——湿法冶铁
活动4:分析湿法冶铁的装置图,写出该装置的电极反应。
一种基于氯碱工艺的新型电解池,可用于湿法冶铁的研究。
该装置是否需要使用交换膜?
何种交换膜?
Na+
任务二:电解食盐水的应用——湿法冶铁
活动4:分析湿法冶铁的装置图,写出该装置的电极反应。
一种基于氯碱工艺的新型电解池,可用于湿法冶铁的研究。
问:电解过程中,理论上每消耗1molFe2O3,阳极室溶液质量如何变化?
减少351g
阴极:Fe2O3 + 6e- + 3H2O = Fe + 6OH-
阳极:2Cl- - 2e-=Cl2↑
Na+
Cl2
阴极
阳极
根据以上的分析过程,总结分析电解原理的思维模型。
分析离子,判断离子移向,比较放电顺序
判断电极
离子放电
写反应式
隔膜选取
定量计算
根据电源电极、电子得失、离子移向、或电解目的等判断电解池的阴、阳极
利用守恒写出电极反应式、总反应式
关注生产目标
守恒关系:失电子数=得电子数=转移离子电荷数
电极区溶液变化:考虑粒子的生成、消耗、转移
1、在新冠肺炎疫情期间,“84”消毒液是环境消毒液之一。某学生想制作一种家用环保型消毒液发生器,用石墨作电极电解饱和氯化钠溶液,通电时,为使Cl2被完全吸收制得有较强杀菌能力的消毒液,设计了如图所示的装置。c、d都为碳电极。
完成下列填空:
(1)a为电源的 极,c为电解池的 极(填“正”“负”或“阴”“阳”)。
(2)d电极上发生的电极反应式:_________________________,电解产生消毒液的总化学方程式为 。
负
阳
2H2O+2e-=H2↑+2OH-
NaCl+H2O===NaClO+H2↑
电解
2、三室式电渗析法处理含NH4NO3废水的原理如图所示,在直流电源的作用下,两膜中间的 可通过离子交换膜,而两端隔室中离子被阻挡不能进入中间隔室。工作一段时间后,在两极区均得到副产品NH4NO3。下列叙述正确的是( )
A.a极为电源负极,b极为电源正极
B.c膜是阴离子交换膜,d膜是阳离子交换膜
C.阴极电极反应式为
D.当电路中通过2 mol电子的电量时,阳极区溶液质量减少8g
A
阴极
阳极
饱和NaCl溶液
生成H2、NaOH
生成Cl2
3、请设计一款通过电解食盐水制漂白液的生产装置,装置要求:简易环保、且产量较高。画出装置示意图。
+
-
4、下图所示装置中,a、b都是惰性电极,通电一段时间后,b电极附近溶液呈红色。下列说法正确的是( )
A、X是负极,Y是正极
B、Pt是阴极,Cu是阳极
C、CuSO4溶液的pH逐渐减小
D、CuSO4溶液的pH不变
C
电解原理在工业上的应用
——电解食盐水的应用及分析
第四章 化学反应与电能
1.通过对氯碱工业原理的分析,掌握电解饱和食盐水的原理,认识电能与化学能之间的能量转化。
2.建立电解应用问题的分析思维模型和电解相关计算的思维模型,加深对电解原理的理解和应用。
【史料1】1774年瑞典化学家舍勒将软锰矿与浓盐酸混合加热,第一次制得 Cl2。
MnO2+4HCl(浓) MnCl2+Cl2↑+2H2O
△
卡尔·威尔海姆·舍勒
缺点:能耗大、污染大、产量低、成本高
阴极
阳极
e-
【史料2】1799年伏打研制了能维持一定电流的电池——伏打电堆。1800年,William Cruikshank用伏打电池电解食盐水,发现可以制得 Cl2 。
e-
e-
e-
阴离子
阳离子
电解原理
实验电解饱和食盐水
任务一:认识电解食盐水
请根据电解原理,书写惰性电极(石墨)电解食盐水的电极反应式和总反应方程式。
阴极:_____________________
阳极:_____________________
总离子反应:____________________________
2H2O+2e-===H2↑+2OH-
2Cl-+2H2O === Cl2↑+H2↑+2OH-
电解
2Cl--2e-===Cl2↑
问题1:两极区电解质溶液pH如何变化?
如何验证pH变化?
活动1:书写电解食盐水电极式
任务一:认识电解食盐水
氯碱工业
(3)溶液中存在的离子
Na+、 H+、 Cl-、 OH-
(4)比较放电顺序
阳极: Cl- > OH-
阴极: H+ > Na+
阳极 2Cl--2e-=Cl2↑
阴极 2H2O+2e-=H2↑+2OH-
(1)确定电解池的阴阳极
(2)电极材料
惰性,溶液中的离子放电
(5)写出电极反应
电解总反应方程式: 2NaCl+2H2O==Cl2↑+H2↑+2NaOH
电解
惰性电极电解饱和食盐水
思考: 若在两极附近均滴加酚酞试液,会有什么现象
阴极试液变红!阳极无明显变化!
如何验证pH变化?
紫甘蓝
pH试纸
pH计
酚酞
石蕊
甲基橙
酸碱指示剂
任务一:认识电解食盐水
活动2:实验验证两极区溶液pH变化
任务一:认识电解食盐水
预测实验现象 预测依据
两电极上:
阴极区溶液:
阳极区溶液:
气球
NaCl
溶液
阳极
阴极
紫甘蓝
活动2:实验验证两极区溶液pH变化
任务一:认识电解食盐水
气球
NaCl
溶液
阳极
阴极
预测实验现象 预测依据
Cl2+2H2O HCl+HClO
2Cl-+2H2O === Cl2↑+H2↑+2OH-
电解
阴极区生成NaOH
两电极均产生气泡,且阴极较快
阴极区溶液由紫色逐渐变为蓝色,再变为绿色
阳极区溶液由紫色逐渐变为红色
再变为无色
思考讨论
阴极
阳极
饱和NaCl溶液
生成H2、NaOH
生成Cl2
根据以上实验分析,你觉得电解饱和食盐水可用于制备什么生活用品?
电解食盐水的简易装置可以得到纯净的工业原料Cl2和NaOH吗?
漂白液:NaClO、NaCl
Cl2+2NaOH =NaCl+NaClO+H2O
1、产品Cl2和NaOH溶液会反应吗,那么Cl2能和NaOH溶液接触吗?
Cl2+2NaOH =NaCl+NaClO+H2O
2、产品Cl2和H2能混合吗?
遇火或强光会爆炸
解决方法:
生产设备:阳离子交换膜电解槽
不能
若工业上采用下图的装置制备NaOH、H2 、Cl2,存在何种不足之处?如何解决这个问题?
使用离子交换膜
H+
Na+
Cl-
OH-
活动3:完善氯碱工业装置
任务一:认识电解食盐水
+
-
阳 极
阴 极
请根据以上分析,在下图方框中填入所选交换膜、电解原料、电解产品,完善氯碱工业装置图。
+
-
Cl2
H2
Na+
淡盐水
NaOH溶液
饱和NaCl溶液
阳离子交换膜
阳 极
阴 极
饱和NaCl溶液
稀NaOH溶液
浓NaOH溶液
【思考】使用阳离子交换膜后,电路中每通过1mole-,阴极区溶液质量如何变化?
含氯漂白剂
有机合成、造纸
玻璃、肥皂
纺织、印染
有机合成
氯化物合成
农药
金属冶炼
有机合成
HCl
盐酸
H2
NaOH
湿氯气
湿氢气
液碱
Cl2
电解饱和食盐水
任务二:电解食盐水的应用——湿法冶铁
活动4:分析湿法冶铁的装置图,写出该装置的电极反应。
一种基于氯碱工艺的新型电解池,可用于湿法冶铁的研究。
该装置是否需要使用交换膜?
何种交换膜?
Na+
任务二:电解食盐水的应用——湿法冶铁
活动4:分析湿法冶铁的装置图,写出该装置的电极反应。
一种基于氯碱工艺的新型电解池,可用于湿法冶铁的研究。
问:电解过程中,理论上每消耗1molFe2O3,阳极室溶液质量如何变化?
减少351g
阴极:Fe2O3 + 6e- + 3H2O = Fe + 6OH-
阳极:2Cl- - 2e-=Cl2↑
Na+
Cl2
阴极
阳极
根据以上的分析过程,总结分析电解原理的思维模型。
分析离子,判断离子移向,比较放电顺序
判断电极
离子放电
写反应式
隔膜选取
定量计算
根据电源电极、电子得失、离子移向、或电解目的等判断电解池的阴、阳极
利用守恒写出电极反应式、总反应式
关注生产目标
守恒关系:失电子数=得电子数=转移离子电荷数
电极区溶液变化:考虑粒子的生成、消耗、转移
1、在新冠肺炎疫情期间,“84”消毒液是环境消毒液之一。某学生想制作一种家用环保型消毒液发生器,用石墨作电极电解饱和氯化钠溶液,通电时,为使Cl2被完全吸收制得有较强杀菌能力的消毒液,设计了如图所示的装置。c、d都为碳电极。
完成下列填空:
(1)a为电源的 极,c为电解池的 极(填“正”“负”或“阴”“阳”)。
(2)d电极上发生的电极反应式:_________________________,电解产生消毒液的总化学方程式为 。
负
阳
2H2O+2e-=H2↑+2OH-
NaCl+H2O===NaClO+H2↑
电解
2、三室式电渗析法处理含NH4NO3废水的原理如图所示,在直流电源的作用下,两膜中间的 可通过离子交换膜,而两端隔室中离子被阻挡不能进入中间隔室。工作一段时间后,在两极区均得到副产品NH4NO3。下列叙述正确的是( )
A.a极为电源负极,b极为电源正极
B.c膜是阴离子交换膜,d膜是阳离子交换膜
C.阴极电极反应式为
D.当电路中通过2 mol电子的电量时,阳极区溶液质量减少8g
A
阴极
阳极
饱和NaCl溶液
生成H2、NaOH
生成Cl2
3、请设计一款通过电解食盐水制漂白液的生产装置,装置要求:简易环保、且产量较高。画出装置示意图。
+
-
4、下图所示装置中,a、b都是惰性电极,通电一段时间后,b电极附近溶液呈红色。下列说法正确的是( )
A、X是负极,Y是正极
B、Pt是阴极,Cu是阳极
C、CuSO4溶液的pH逐渐减小
D、CuSO4溶液的pH不变
C
