专题8 有机化合物的获得与应用 阶段重点突破练(四)(原卷版+解析版)2024-2025学年高一化学必修2(苏教版2019)
文档属性
| 名称 | 专题8 有机化合物的获得与应用 阶段重点突破练(四)(原卷版+解析版)2024-2025学年高一化学必修2(苏教版2019) |

|
|
| 格式 | docx | ||
| 文件大小 | 643.1KB | ||
| 资源类型 | 教案 | ||
| 版本资源 | 苏教版(2019) | ||
| 科目 | 化学 | ||
| 更新时间 | 2025-01-05 00:00:00 | ||
图片预览




文档简介
专题8 有机化合物的获得与应用 阶段重点突破练(四)
一、常见烃的成键特点与结构
1.下列说法正确的是( )
A.甲烷为平面正方形结构,其结构式为
B.甲烷的电子式为
C.CH2Cl2为正四面体结构
D.CCl4为平面正方形结构
2.下列有关说法不正确的是( )
A.由乙烯分子的组成和结构推测含一个碳碳双键的单烯烃通式为CnH2n(n≥2)
B.分子式为C3H6的烃分子一定含有碳碳双键
C.从乙烯与溴发生加成反应生成1,2-二溴乙烷可知乙烯分子的碳碳双键中有一个键不稳定,易发生断裂
D.乙烯在空气中燃烧的现象与甲烷不同的原因是乙烯的含碳量高
3.(2023·上海华师大二附中期末)由丁烯与氯气加成得到的分子式为C4H8Cl2的有机物,其结构简式不可能为( )
A.CH3CH(CH2Cl)2
B.CH3—CHCl—CHCl—CH3
C.CH2ClCHCl—CH2—CH3
D.
4.已知某种气态化石燃料中含有碳和氢两种元素。为了测定这种燃料中碳和氢两种元素的质量分数,可将气态燃料放入足量的氧气中燃烧,并使产生的气体全部通入如图所示的装置,得到如表所列的实验数据(U形管中干燥剂只吸收水蒸气且假设产生的气体完全被吸收)。
实验前 实验后
干燥剂和U形管的总质量 101.1 g 102.9 g
石灰水和广口瓶的总质量 312.0 g 314.2 g
根据实验数据求:
(1)实验完毕后,生成物中水的质量为________g。假设广口瓶里生成一种正盐,其质量为________g。
(2)生成的水中氢元素的质量为________g。
(3)生成的CO2中碳元素的质量为________g。
(4)气态化石燃料中碳元素与氢元素的质量比为________,该烃的分子式为________。
二、化石燃料的综合利用
5.下列有关煤的叙述正确的是( )
A.煤是由有机物和无机物组成的复杂的混合物,主要含碳、氢元素
B.煤在空气中加强热可得焦炭、煤焦油、粗氨水和焦炉气
C.推广使用煤液化和气化技术,可减少二氧化碳等温室气体的排放
D.煤的气化的主要反应是C(s)+2H2O(g)CO2(g)+2H2(g)
6.实验室可用苯(沸点为80.1 ℃)与浓硝酸、浓硫酸组成的混酸反应制取硝基苯(难溶于水,不与酸或碱溶液反应,密度比水大,无色液体),装置如图所示,下列说法不正确的是( )
A.配制混酸时,将浓硫酸慢慢加入浓硝酸中并不断搅拌
B.水浴加热时,一般用沸水浴
C.反应的化学方程式为+HO—NO2+H2O
D.反应后纯化硝基苯,需经冷却、水洗、碱液洗、水洗、干燥及蒸馏
7.我国在CO2催化加氢制取汽油方面取得突破性进展,CO2转化过程示意图如图:
下列说法不正确的是( )
A.反应①的产物中含有水
B.反应②中只有碳碳键形成
C.汽油主要是C5~C12的烃类混合物
D.a的结构简式为,和C(CH3)4互为同分异构体
8.煤是一种重要能源,工业上常把煤进行气化和液化处理,变为清洁能源。由水蒸气和炽热的无烟煤作用可得水煤气,水煤气是混合气体,主要由两种无色无味气体组成,是重要的工业原料。
(1)在工业生产水煤气时,燃料层的温度会下降,这说明___________________。
(2)提出猜想:水煤气的成分可能是①________(填化学式,下同)和氢气,②________和氢气;提出以上猜想的依据是_______________________________________________。
设计实验:请从下列装置中选择一种,设计简单的实验证明猜想。
(3)你选择的装置是________(填字母)。
(4)实验结论:如果__________________________,那么猜想______________(填序号)合理。
三、同系物与同分异构体的判断及应用
9.有A、B两种烃,碳元素的质量分数相同,下列关于A和B的叙述正确的是( )
A.A和B一定互为同分异构体
B.A和B不可能互为同系物
C.燃烧等质量的A和B,消耗氧气的量一定相等
D.A和B各1 mol完全燃烧后生成的二氧化碳的质量一定相等
10.有以下结构的三种烃分子,下列有关说法错误的是( )
A.1 mol甲分子内含有10 mol共价键
B.由乙分子构成的物质不能使溴的四氯化碳溶液褪色
C.丙分子的二氯取代产物只有3种
D.三种分子内成键方式相同,而且最简式相同,故互为同系物
11.C5H12有3种不同的结构,甲:CH3(CH2)3CH3,乙:CH3CH(CH3)CH2CH3,丙:C(CH3)4,下列相关叙述正确的是( )
A.甲、乙、丙互为同系物,均可与氯气、溴蒸气发生取代反应
B.C5H12表示一种纯净物
C.甲、乙、丙中,丙的沸点最低
D.乙有3种不同沸点的一氯取代物
12.(2021·河北,8)苯并降冰片烯是一种重要的药物合成中间体,结构简式如图。关于该化合物,下列说法正确的是( )
A.是苯的同系物
B.分子中最多8个碳原子共平面
C.一氯代物有6种(不考虑立体异构)
D.分子中含有4个碳碳双键
四、常见烃的性质及应用
13.下列反应中前者属于取代反应,后者属于加成反应的是( )
A.甲烷与氯气混合后光照反应;乙烯使酸性高锰酸钾溶液褪色
B.乙烯与溴的四氯化碳溶液反应;苯与氢气在一定条件下反应生成环己烷
C.在苯中滴入溴水,溴水褪色;甲烷与氯气混合后光照反应
D.苯滴入浓硝酸和浓硫酸的混合液中,有油状物生成;乙烯与水生成乙醇的反应
14.(2022·福建高一检测)下列有关常见烃性质的描述正确的是( )
A.光照下,1 mol CH4最多能与4 mol Cl2发生取代反应,产物中物质的量最多的是CCl4
B.苯与液溴在一定条件下能发生取代反应
C.甲烷与乙烯的混合物可通过溴的四氯化碳溶液分离
D.乙烯和苯分子中均含独立的碳碳双键,都能与H2发生加成反应
15.(1)乙烯能使酸性高锰酸钾溶液和溴的四氯化碳溶液褪色,其中,与高锰酸钾发生的反应是________(填反应类型,下同)反应;与溴发生的反应是_______反应。
(2)一种能使溴水褪色的气态烃,标准状况下5.6 L该气态烃的质量为10.5 g,10.5 g该烃完全燃烧时生成16.8 L二氧化碳(标准状况)和13.5 g水。则该烃的分子式为________________。
16.分析下列烃分子,完成填空。
①CH3—CH2—CH2—CH2—CH3 ② ③ ④ ⑤ ⑥
(1)属于烷烃的有________(填序号,下同);互为同系物的有________、________。
(2)任写一种①的同分异构体的结构简式:_________________________________。
(3)④生成一氯乙烷的化学方程式:______________________________________________。
(4)③在一定条件下与液溴反应的化学方程式:____________________________________。
(5)②与水反应的化学方程式:__________________________________________________。
(6)④的二氯代物有________种。
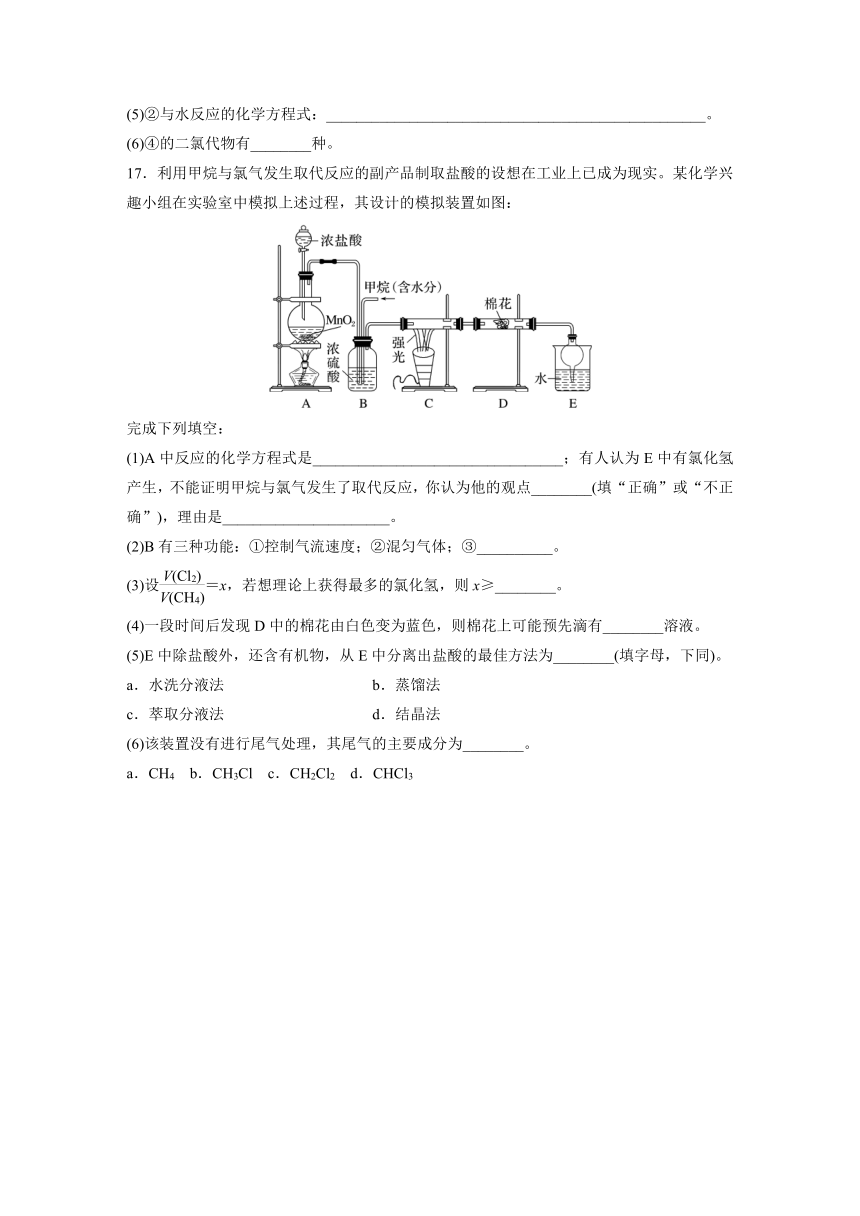
17.利用甲烷与氯气发生取代反应的副产品制取盐酸的设想在工业上已成为现实。某化学兴趣小组在实验室中模拟上述过程,其设计的模拟装置如图:
完成下列填空:
(1)A中反应的化学方程式是_________________________________;有人认为E中有氯化氢产生,不能证明甲烷与氯气发生了取代反应,你认为他的观点________(填“正确”或“不正确”),理由是______________________。
(2)B有三种功能:①控制气流速度;②混匀气体;③__________。
(3)设=x,若想理论上获得最多的氯化氢,则x≥________。
(4)一段时间后发现D中的棉花由白色变为蓝色,则棉花上可能预先滴有________溶液。
(5)E中除盐酸外,还含有机物,从E中分离出盐酸的最佳方法为________(填字母,下同)。
a.水洗分液法 b.蒸馏法
c.萃取分液法 d.结晶法
(6)该装置没有进行尾气处理,其尾气的主要成分为________。
a.CH4 b.CH3Cl c.CH2Cl2 d.CHCl3
阶段重点突破练(四)
一、常见烃的成键特点与结构
1.下列说法正确的是( )
A.甲烷为平面正方形结构,其结构式为
B.甲烷的电子式为
C.CH2Cl2为正四面体结构
D.CCl4为平面正方形结构
答案 B
解析 甲烷是正四面体结构,而不是平面结构,其结构式为,故A错误;甲烷分子中,每个H原子与C原子间形成1对共用电子,电子式为,故B正确;CH2Cl2中C—Cl键键长与C—H键键长不相同,CH2Cl2为四面体结构,但不是正四面体结构,故C错误;甲烷是正四面体结构,四个H全部被Cl取代后得到CCl4,则CCl4是正四面体结构,故D错误。
2.下列有关说法不正确的是( )
A.由乙烯分子的组成和结构推测含一个碳碳双键的单烯烃通式为CnH2n(n≥2)
B.分子式为C3H6的烃分子一定含有碳碳双键
C.从乙烯与溴发生加成反应生成1,2-二溴乙烷可知乙烯分子的碳碳双键中有一个键不稳定,易发生断裂
D.乙烯在空气中燃烧的现象与甲烷不同的原因是乙烯的含碳量高
答案 B
解析 乙烯分子式为C2H4,其他单烯烃与其相差n个CH2,因此可知,单烯烃通式为CnH2n(n≥2),A正确;分子式为C3H6的烃分子可以是环烃,B错误;乙烯分子的碳碳双键中有一个键不稳定,易发生断裂,因此易发生加成等化学反应,C正确;乙烯在空气中燃烧有黑烟,因为乙烯中碳含量高于甲烷,碳不完全燃烧产生黑烟,D正确。
3.(2023·上海华师大二附中期末)由丁烯与氯气加成得到的分子式为C4H8Cl2的有机物,其结构简式不可能为( )
A.CH3CH(CH2Cl)2
B.CH3—CHCl—CHCl—CH3
C.CH2ClCHCl—CH2—CH3
D.
答案 A
解析 丁烯的分子式为C4H8,可能的结构简式为CH3—CH2—CH==CH2、CH3—CH==CH—CH3、,它们与Cl2发生加成反应产物可能的结构有CH3—CH2—CHCl—CH2Cl、CH3—CHCl—CHCl—CH3、,而不可能得到物质CH3CH—(CH2Cl)2,故选A。
4.已知某种气态化石燃料中含有碳和氢两种元素。为了测定这种燃料中碳和氢两种元素的质量分数,可将气态燃料放入足量的氧气中燃烧,并使产生的气体全部通入如图所示的装置,得到如表所列的实验数据(U形管中干燥剂只吸收水蒸气且假设产生的气体完全被吸收)。
实验前 实验后
干燥剂和U形管的总质量 101.1 g 102.9 g
石灰水和广口瓶的总质量 312.0 g 314.2 g
根据实验数据求:
(1)实验完毕后,生成物中水的质量为________g。假设广口瓶里生成一种正盐,其质量为________g。
(2)生成的水中氢元素的质量为________g。
(3)生成的CO2中碳元素的质量为________g。
(4)气态化石燃料中碳元素与氢元素的质量比为________,该烃的分子式为________。
答案 (1)1.8 5 (2)0.2 (3)0.6 (4)3∶1 CH4
解析 (1)生成水的质量为102.9 g-101.1 g=1.8 g,生成正盐(即CaCO3)的质量为×100 g·mol-1=5 g。
(2)生成的水中氢元素的质量为×2 g·mol-1=0.2 g。
(3)生成的CO2中碳元素的质量为×12 g·mol-1=0.6 g。
(4)碳元素与氢元素的质量比为0.6 g∶0.2 g=3∶1,由此可求出碳和氢的原子个数之比为∶=1∶4,根据碳原子的成键特点可知,该烃为CH4。
二、化石燃料的综合利用
5.下列有关煤的叙述正确的是( )
A.煤是由有机物和无机物组成的复杂的混合物,主要含碳、氢元素
B.煤在空气中加强热可得焦炭、煤焦油、粗氨水和焦炉气
C.推广使用煤液化和气化技术,可减少二氧化碳等温室气体的排放
D.煤的气化的主要反应是C(s)+2H2O(g)CO2(g)+2H2(g)
答案 A
解析 煤干馏需隔绝空气加强热,B错误;煤的液化和气化,不能减少二氧化碳等温室气体的排放,C错误;煤的气化主要是煤与水蒸气发生置换反应生成水煤气:C(s)+H2O(g)CO(g)+H2(g),D错误。
6.实验室可用苯(沸点为80.1 ℃)与浓硝酸、浓硫酸组成的混酸反应制取硝基苯(难溶于水,不与酸或碱溶液反应,密度比水大,无色液体),装置如图所示,下列说法不正确的是( )
A.配制混酸时,将浓硫酸慢慢加入浓硝酸中并不断搅拌
B.水浴加热时,一般用沸水浴
C.反应的化学方程式为+HO—NO2+H2O
D.反应后纯化硝基苯,需经冷却、水洗、碱液洗、水洗、干燥及蒸馏
答案 B
解析 反应温度为50~60 ℃,水浴加热。
7.我国在CO2催化加氢制取汽油方面取得突破性进展,CO2转化过程示意图如图:
下列说法不正确的是( )
A.反应①的产物中含有水
B.反应②中只有碳碳键形成
C.汽油主要是C5~C12的烃类混合物
D.a的结构简式为,和C(CH3)4互为同分异构体
答案 B
解析 从质量守恒的角度判断,二氧化碳和氢气反应的化学方程式为CO2+H2===CO+H2O,则产物中含有水,故A说法正确;反应②生成烃类物质,含有C—C键、C—H键,故B说法错误;汽油所含烃类物质常温下为液态,易挥发,主要是C5~C12的烃类混合物,故C说法正确;图中a中含5个C,结构简式为,和C(CH3)4分子式相同,结构不同,二者互为同分异构体,D说法正确。
8.煤是一种重要能源,工业上常把煤进行气化和液化处理,变为清洁能源。由水蒸气和炽热的无烟煤作用可得水煤气,水煤气是混合气体,主要由两种无色无味气体组成,是重要的工业原料。
(1)在工业生产水煤气时,燃料层的温度会下降,这说明___________________。
(2)提出猜想:水煤气的成分可能是①________(填化学式,下同)和氢气,②________和氢气;提出以上猜想的依据是_______________________________________________。
设计实验:请从下列装置中选择一种,设计简单的实验证明猜想。
(3)你选择的装置是________(填字母)。
(4)实验结论:如果__________________________,那么猜想______________(填序号)合理。
答案 (1)碳和水蒸气的反应为吸热反应 (2)CO CO2 化学反应前后元素C、H、O种类不变 (3)B (4)澄清石灰水变浑浊 ②(或澄清石灰水不变浑浊 ①)
解析 (1)生产水煤气时,燃料层的温度下降,说明碳和水蒸气的反应为吸热反应。(2)根据质量守恒可推出水煤气可能有两种组成,①CO和H2,②CO2和H2。(3)CO2可以通过澄清石灰水检验。(4)如果澄清石灰水不变浑浊,则猜想①正确;如果澄清石灰水变浑浊,则猜想②正确。
三、同系物与同分异构体的判断及应用
9.有A、B两种烃,碳元素的质量分数相同,下列关于A和B的叙述正确的是( )
A.A和B一定互为同分异构体
B.A和B不可能互为同系物
C.燃烧等质量的A和B,消耗氧气的量一定相等
D.A和B各1 mol完全燃烧后生成的二氧化碳的质量一定相等
答案 C
解析 因烃中只有碳、氢两种元素,碳元素的质量分数相同,所以氢元素的质量分数也相同,最简式相同,因此燃烧相同质量的两种物质,消耗氧气的量一定相等,C正确;最简式相同的烃,可能互为同分异构体,如丙烯与环丙烷,也可能不是,如乙炔和苯,A错误;最简式相同的烃,可能互为同系物,如乙烯与丙烯,B错误;若互为同分异构体,则A和B各1 mol完全燃烧后生成的二氧化碳的质量一定相等;若互为同系物,则A和B各1 mol完全燃烧后生成的二氧化碳的质量一定不相等,D错误。
10.有以下结构的三种烃分子,下列有关说法错误的是( )
A.1 mol甲分子内含有10 mol共价键
B.由乙分子构成的物质不能使溴的四氯化碳溶液褪色
C.丙分子的二氯取代产物只有3种
D.三种分子内成键方式相同,而且最简式相同,故互为同系物
答案 D
解析 1 mol甲分子中含有6 mol碳碳单键和4 mol碳氢键,A正确;乙分子中不存在不饱和的“”或“—C≡C—”,不能使溴的四氯化碳溶液褪色,B正确;丙分子有位于棱边、面对角线、体对角线3种位置关系的二氯代物,C正确;甲、乙、丙三种分子的分子式分别为C4H4、C6H6和C8H8,最简式相同,但分子组成上不是相差若干个CH2原子团,故不互为同系物,D错误。
11.C5H12有3种不同的结构,甲:CH3(CH2)3CH3,乙:CH3CH(CH3)CH2CH3,丙:C(CH3)4,下列相关叙述正确的是( )
A.甲、乙、丙互为同系物,均可与氯气、溴蒸气发生取代反应
B.C5H12表示一种纯净物
C.甲、乙、丙中,丙的沸点最低
D.乙有3种不同沸点的一氯取代物
答案 C
解析 甲、乙、丙的分子式相同,结构不同,互为同分异构体,A错误;C5H12有3种同分异构体,所以不能表示纯净物,B错误;烷烃的同分异构体中,支链越多,沸点越低,丙分子中支链最多,所以沸点最低,C正确;乙分子中有4种位置的氢原子,即,故一氯代物有4种,D错误。
12.(2021·河北,8)苯并降冰片烯是一种重要的药物合成中间体,结构简式如图。关于该化合物,下列说法正确的是( )
A.是苯的同系物
B.分子中最多8个碳原子共平面
C.一氯代物有6种(不考虑立体异构)
D.分子中含有4个碳碳双键
答案 B
解析 由结构简式可知,苯并降冰片烯分子中苯环上的6个碳原子和连在苯环上的2个碳原子共平面,最多共有8个碳原子共平面,故B正确;由结构简式可知,苯并降冰片烯分子的结构上下对称,分子中含有5种类型的氢原子,则其一氯代物有5种,故C错误;苯环不是单双键交替的结构,由结构简式可知,苯并降冰片烯分子中只含有1个碳碳双键,故D错误。
四、常见烃的性质及应用
13.下列反应中前者属于取代反应,后者属于加成反应的是( )
A.甲烷与氯气混合后光照反应;乙烯使酸性高锰酸钾溶液褪色
B.乙烯与溴的四氯化碳溶液反应;苯与氢气在一定条件下反应生成环己烷
C.在苯中滴入溴水,溴水褪色;甲烷与氯气混合后光照反应
D.苯滴入浓硝酸和浓硫酸的混合液中,有油状物生成;乙烯与水生成乙醇的反应
答案 D
14.(2022·福建高一检测)下列有关常见烃性质的描述正确的是( )
A.光照下,1 mol CH4最多能与4 mol Cl2发生取代反应,产物中物质的量最多的是CCl4
B.苯与液溴在一定条件下能发生取代反应
C.甲烷与乙烯的混合物可通过溴的四氯化碳溶液分离
D.乙烯和苯分子中均含独立的碳碳双键,都能与H2发生加成反应
答案 B
解析 甲烷和氯气发生取代反应生成多种氯代烃,同时生成氯化氢,产物中物质的量最多的是氯化氢,A错误;苯与液溴在一定条件下可发生取代反应,生成溴苯,B正确;乙烯与溴的四氯化碳溶液发生加成反应,被除去,且甲烷易溶于四氯化碳,不能实现分离,C错误;苯不含碳碳双键,但可与氢气发生加成反应,D错误。
15.(1)乙烯能使酸性高锰酸钾溶液和溴的四氯化碳溶液褪色,其中,与高锰酸钾发生的反应是________(填反应类型,下同)反应;与溴发生的反应是_______反应。
(2)一种能使溴水褪色的气态烃,标准状况下5.6 L该气态烃的质量为10.5 g,10.5 g该烃完全燃烧时生成16.8 L二氧化碳(标准状况)和13.5 g水。则该烃的分子式为________________。
答案 (1)氧化 加成 (2)C3H6
解析 (1)乙烯分子中的碳碳双键易断裂,因此易被酸性高锰酸钾氧化,能与溴发生加成反应。
(2)设该气态烃的分子式为CxHy,
n(烃)==0.25 mol,
n(H2O)==0.75 mol,
n(CO2)==0.75 mol,
CxHy+(x+)O2xCO2 + H2O
1 mol x mol mol
0.25 mol 0.75 mol 0.75 mol
则x=3,y=6,该气态烃的分子式为C3H6。
16.分析下列烃分子,完成填空。
①CH3—CH2—CH2—CH2—CH3 ② ③ ④ ⑤ ⑥
(1)属于烷烃的有________(填序号,下同);互为同系物的有________、________。
(2)任写一种①的同分异构体的结构简式:_________________________________。
(3)④生成一氯乙烷的化学方程式:______________________________________________。
(4)③在一定条件下与液溴反应的化学方程式:____________________________________。
(5)②与水反应的化学方程式:__________________________________________________。
(6)④的二氯代物有________种。
答案 (1)①④⑥ ①④⑥ ③⑤
(2)CH3CH(CH3)CH2CH3[或C(CH3)4]
(3)CH3CH3+Cl2CH3CH2Cl+HCl
(4)+Br2+HBr
(5)CH2==CH2+H2OCH3CH2OH
(6)2
解析 (1)六种物质的分子式分别为①C5H12,②C2H4,③C6H6,④C2H6,⑤C7H8,⑥CH4;烷烃的通式为CnH2n+2(n≥1),所以属于烷烃的有①④⑥;同系物指的是结构相似,分子组成相差若干个“CH2”原子团的有机物,因此互为同系物的有①④⑥和③⑤。
(2)①为C5H12,其结构除了CH3—CH2—CH2—CH2—CH3外,还有CH3CH(CH3)CH2CH3和C(CH3)4。
(3)乙烷和氯气在光照条件下发生取代反应生成氯乙烷,反应的化学方程式:CH3CH3+Cl2CH3CH2Cl+HCl。
(4)苯和液溴在溴化铁作催化剂条件下发生取代反应生成溴苯和溴化氢,反应的化学方程式:+Br2+HBr。
(5)乙烯和水发生加成反应生成乙醇,反应的化学方程式:CH2==CH2+H2OCH3CH2OH。
(6)两个氯原子连在同一个碳上,结构有1种,分别连在两个碳上,结构有1种,共计有2种。
17.利用甲烷与氯气发生取代反应的副产品制取盐酸的设想在工业上已成为现实。某化学兴趣小组在实验室中模拟上述过程,其设计的模拟装置如图:
完成下列填空:
(1)A中反应的化学方程式是_________________________________;有人认为E中有氯化氢产生,不能证明甲烷与氯气发生了取代反应,你认为他的观点________(填“正确”或“不正确”),理由是______________________。
(2)B有三种功能:①控制气流速度;②混匀气体;③__________。
(3)设=x,若想理论上获得最多的氯化氢,则x≥________。
(4)一段时间后发现D中的棉花由白色变为蓝色,则棉花上可能预先滴有________溶液。
(5)E中除盐酸外,还含有机物,从E中分离出盐酸的最佳方法为________(填字母,下同)。
a.水洗分液法 b.蒸馏法
c.萃取分液法 d.结晶法
(6)该装置没有进行尾气处理,其尾气的主要成分为________。
a.CH4 b.CH3Cl c.CH2Cl2 d.CHCl3
答案 (1)MnO2+4HCl(浓)MnCl2+Cl2↑+2H2O 正确 制备的Cl2中混有HCl,若氯气与甲烷发生置换反应,也有氯化氢生成 (2)干燥氯气、氯化氢和甲烷 (3)4 (4)淀粉-KI (5)a (6)ab
解析 (1)A中二氧化锰与浓盐酸共热生成二氯化锰、氯气和水,反应的化学方程式为MnO2+4HCl(浓)MnCl2+Cl2↑+2H2O。(2)B为浓硫酸,可以干燥气体。(3)1 mol甲烷最多与4 mol氯气发生反应生成4 mol HCl,所以要获得更多氯化氢,氯气≥甲烷的4倍。(4)氯气能将碘化钾氧化为碘单质,淀粉遇到碘单质会变蓝色,故棉花上可能预先滴有淀粉-KI溶液。
(5)生成的有机物为氯代甲烷,难溶于水,可用分液的方法分离。(6)二氯甲烷、三氯甲烷和四氯化碳均为液体,则尾气的主要成分为未反应的甲烷和一氯甲烷气体。
一、常见烃的成键特点与结构
1.下列说法正确的是( )
A.甲烷为平面正方形结构,其结构式为
B.甲烷的电子式为
C.CH2Cl2为正四面体结构
D.CCl4为平面正方形结构
2.下列有关说法不正确的是( )
A.由乙烯分子的组成和结构推测含一个碳碳双键的单烯烃通式为CnH2n(n≥2)
B.分子式为C3H6的烃分子一定含有碳碳双键
C.从乙烯与溴发生加成反应生成1,2-二溴乙烷可知乙烯分子的碳碳双键中有一个键不稳定,易发生断裂
D.乙烯在空气中燃烧的现象与甲烷不同的原因是乙烯的含碳量高
3.(2023·上海华师大二附中期末)由丁烯与氯气加成得到的分子式为C4H8Cl2的有机物,其结构简式不可能为( )
A.CH3CH(CH2Cl)2
B.CH3—CHCl—CHCl—CH3
C.CH2ClCHCl—CH2—CH3
D.
4.已知某种气态化石燃料中含有碳和氢两种元素。为了测定这种燃料中碳和氢两种元素的质量分数,可将气态燃料放入足量的氧气中燃烧,并使产生的气体全部通入如图所示的装置,得到如表所列的实验数据(U形管中干燥剂只吸收水蒸气且假设产生的气体完全被吸收)。
实验前 实验后
干燥剂和U形管的总质量 101.1 g 102.9 g
石灰水和广口瓶的总质量 312.0 g 314.2 g
根据实验数据求:
(1)实验完毕后,生成物中水的质量为________g。假设广口瓶里生成一种正盐,其质量为________g。
(2)生成的水中氢元素的质量为________g。
(3)生成的CO2中碳元素的质量为________g。
(4)气态化石燃料中碳元素与氢元素的质量比为________,该烃的分子式为________。
二、化石燃料的综合利用
5.下列有关煤的叙述正确的是( )
A.煤是由有机物和无机物组成的复杂的混合物,主要含碳、氢元素
B.煤在空气中加强热可得焦炭、煤焦油、粗氨水和焦炉气
C.推广使用煤液化和气化技术,可减少二氧化碳等温室气体的排放
D.煤的气化的主要反应是C(s)+2H2O(g)CO2(g)+2H2(g)
6.实验室可用苯(沸点为80.1 ℃)与浓硝酸、浓硫酸组成的混酸反应制取硝基苯(难溶于水,不与酸或碱溶液反应,密度比水大,无色液体),装置如图所示,下列说法不正确的是( )
A.配制混酸时,将浓硫酸慢慢加入浓硝酸中并不断搅拌
B.水浴加热时,一般用沸水浴
C.反应的化学方程式为+HO—NO2+H2O
D.反应后纯化硝基苯,需经冷却、水洗、碱液洗、水洗、干燥及蒸馏
7.我国在CO2催化加氢制取汽油方面取得突破性进展,CO2转化过程示意图如图:
下列说法不正确的是( )
A.反应①的产物中含有水
B.反应②中只有碳碳键形成
C.汽油主要是C5~C12的烃类混合物
D.a的结构简式为,和C(CH3)4互为同分异构体
8.煤是一种重要能源,工业上常把煤进行气化和液化处理,变为清洁能源。由水蒸气和炽热的无烟煤作用可得水煤气,水煤气是混合气体,主要由两种无色无味气体组成,是重要的工业原料。
(1)在工业生产水煤气时,燃料层的温度会下降,这说明___________________。
(2)提出猜想:水煤气的成分可能是①________(填化学式,下同)和氢气,②________和氢气;提出以上猜想的依据是_______________________________________________。
设计实验:请从下列装置中选择一种,设计简单的实验证明猜想。
(3)你选择的装置是________(填字母)。
(4)实验结论:如果__________________________,那么猜想______________(填序号)合理。
三、同系物与同分异构体的判断及应用
9.有A、B两种烃,碳元素的质量分数相同,下列关于A和B的叙述正确的是( )
A.A和B一定互为同分异构体
B.A和B不可能互为同系物
C.燃烧等质量的A和B,消耗氧气的量一定相等
D.A和B各1 mol完全燃烧后生成的二氧化碳的质量一定相等
10.有以下结构的三种烃分子,下列有关说法错误的是( )
A.1 mol甲分子内含有10 mol共价键
B.由乙分子构成的物质不能使溴的四氯化碳溶液褪色
C.丙分子的二氯取代产物只有3种
D.三种分子内成键方式相同,而且最简式相同,故互为同系物
11.C5H12有3种不同的结构,甲:CH3(CH2)3CH3,乙:CH3CH(CH3)CH2CH3,丙:C(CH3)4,下列相关叙述正确的是( )
A.甲、乙、丙互为同系物,均可与氯气、溴蒸气发生取代反应
B.C5H12表示一种纯净物
C.甲、乙、丙中,丙的沸点最低
D.乙有3种不同沸点的一氯取代物
12.(2021·河北,8)苯并降冰片烯是一种重要的药物合成中间体,结构简式如图。关于该化合物,下列说法正确的是( )
A.是苯的同系物
B.分子中最多8个碳原子共平面
C.一氯代物有6种(不考虑立体异构)
D.分子中含有4个碳碳双键
四、常见烃的性质及应用
13.下列反应中前者属于取代反应,后者属于加成反应的是( )
A.甲烷与氯气混合后光照反应;乙烯使酸性高锰酸钾溶液褪色
B.乙烯与溴的四氯化碳溶液反应;苯与氢气在一定条件下反应生成环己烷
C.在苯中滴入溴水,溴水褪色;甲烷与氯气混合后光照反应
D.苯滴入浓硝酸和浓硫酸的混合液中,有油状物生成;乙烯与水生成乙醇的反应
14.(2022·福建高一检测)下列有关常见烃性质的描述正确的是( )
A.光照下,1 mol CH4最多能与4 mol Cl2发生取代反应,产物中物质的量最多的是CCl4
B.苯与液溴在一定条件下能发生取代反应
C.甲烷与乙烯的混合物可通过溴的四氯化碳溶液分离
D.乙烯和苯分子中均含独立的碳碳双键,都能与H2发生加成反应
15.(1)乙烯能使酸性高锰酸钾溶液和溴的四氯化碳溶液褪色,其中,与高锰酸钾发生的反应是________(填反应类型,下同)反应;与溴发生的反应是_______反应。
(2)一种能使溴水褪色的气态烃,标准状况下5.6 L该气态烃的质量为10.5 g,10.5 g该烃完全燃烧时生成16.8 L二氧化碳(标准状况)和13.5 g水。则该烃的分子式为________________。
16.分析下列烃分子,完成填空。
①CH3—CH2—CH2—CH2—CH3 ② ③ ④ ⑤ ⑥
(1)属于烷烃的有________(填序号,下同);互为同系物的有________、________。
(2)任写一种①的同分异构体的结构简式:_________________________________。
(3)④生成一氯乙烷的化学方程式:______________________________________________。
(4)③在一定条件下与液溴反应的化学方程式:____________________________________。
(5)②与水反应的化学方程式:__________________________________________________。
(6)④的二氯代物有________种。
17.利用甲烷与氯气发生取代反应的副产品制取盐酸的设想在工业上已成为现实。某化学兴趣小组在实验室中模拟上述过程,其设计的模拟装置如图:
完成下列填空:
(1)A中反应的化学方程式是_________________________________;有人认为E中有氯化氢产生,不能证明甲烷与氯气发生了取代反应,你认为他的观点________(填“正确”或“不正确”),理由是______________________。
(2)B有三种功能:①控制气流速度;②混匀气体;③__________。
(3)设=x,若想理论上获得最多的氯化氢,则x≥________。
(4)一段时间后发现D中的棉花由白色变为蓝色,则棉花上可能预先滴有________溶液。
(5)E中除盐酸外,还含有机物,从E中分离出盐酸的最佳方法为________(填字母,下同)。
a.水洗分液法 b.蒸馏法
c.萃取分液法 d.结晶法
(6)该装置没有进行尾气处理,其尾气的主要成分为________。
a.CH4 b.CH3Cl c.CH2Cl2 d.CHCl3
阶段重点突破练(四)
一、常见烃的成键特点与结构
1.下列说法正确的是( )
A.甲烷为平面正方形结构,其结构式为
B.甲烷的电子式为
C.CH2Cl2为正四面体结构
D.CCl4为平面正方形结构
答案 B
解析 甲烷是正四面体结构,而不是平面结构,其结构式为,故A错误;甲烷分子中,每个H原子与C原子间形成1对共用电子,电子式为,故B正确;CH2Cl2中C—Cl键键长与C—H键键长不相同,CH2Cl2为四面体结构,但不是正四面体结构,故C错误;甲烷是正四面体结构,四个H全部被Cl取代后得到CCl4,则CCl4是正四面体结构,故D错误。
2.下列有关说法不正确的是( )
A.由乙烯分子的组成和结构推测含一个碳碳双键的单烯烃通式为CnH2n(n≥2)
B.分子式为C3H6的烃分子一定含有碳碳双键
C.从乙烯与溴发生加成反应生成1,2-二溴乙烷可知乙烯分子的碳碳双键中有一个键不稳定,易发生断裂
D.乙烯在空气中燃烧的现象与甲烷不同的原因是乙烯的含碳量高
答案 B
解析 乙烯分子式为C2H4,其他单烯烃与其相差n个CH2,因此可知,单烯烃通式为CnH2n(n≥2),A正确;分子式为C3H6的烃分子可以是环烃,B错误;乙烯分子的碳碳双键中有一个键不稳定,易发生断裂,因此易发生加成等化学反应,C正确;乙烯在空气中燃烧有黑烟,因为乙烯中碳含量高于甲烷,碳不完全燃烧产生黑烟,D正确。
3.(2023·上海华师大二附中期末)由丁烯与氯气加成得到的分子式为C4H8Cl2的有机物,其结构简式不可能为( )
A.CH3CH(CH2Cl)2
B.CH3—CHCl—CHCl—CH3
C.CH2ClCHCl—CH2—CH3
D.
答案 A
解析 丁烯的分子式为C4H8,可能的结构简式为CH3—CH2—CH==CH2、CH3—CH==CH—CH3、,它们与Cl2发生加成反应产物可能的结构有CH3—CH2—CHCl—CH2Cl、CH3—CHCl—CHCl—CH3、,而不可能得到物质CH3CH—(CH2Cl)2,故选A。
4.已知某种气态化石燃料中含有碳和氢两种元素。为了测定这种燃料中碳和氢两种元素的质量分数,可将气态燃料放入足量的氧气中燃烧,并使产生的气体全部通入如图所示的装置,得到如表所列的实验数据(U形管中干燥剂只吸收水蒸气且假设产生的气体完全被吸收)。
实验前 实验后
干燥剂和U形管的总质量 101.1 g 102.9 g
石灰水和广口瓶的总质量 312.0 g 314.2 g
根据实验数据求:
(1)实验完毕后,生成物中水的质量为________g。假设广口瓶里生成一种正盐,其质量为________g。
(2)生成的水中氢元素的质量为________g。
(3)生成的CO2中碳元素的质量为________g。
(4)气态化石燃料中碳元素与氢元素的质量比为________,该烃的分子式为________。
答案 (1)1.8 5 (2)0.2 (3)0.6 (4)3∶1 CH4
解析 (1)生成水的质量为102.9 g-101.1 g=1.8 g,生成正盐(即CaCO3)的质量为×100 g·mol-1=5 g。
(2)生成的水中氢元素的质量为×2 g·mol-1=0.2 g。
(3)生成的CO2中碳元素的质量为×12 g·mol-1=0.6 g。
(4)碳元素与氢元素的质量比为0.6 g∶0.2 g=3∶1,由此可求出碳和氢的原子个数之比为∶=1∶4,根据碳原子的成键特点可知,该烃为CH4。
二、化石燃料的综合利用
5.下列有关煤的叙述正确的是( )
A.煤是由有机物和无机物组成的复杂的混合物,主要含碳、氢元素
B.煤在空气中加强热可得焦炭、煤焦油、粗氨水和焦炉气
C.推广使用煤液化和气化技术,可减少二氧化碳等温室气体的排放
D.煤的气化的主要反应是C(s)+2H2O(g)CO2(g)+2H2(g)
答案 A
解析 煤干馏需隔绝空气加强热,B错误;煤的液化和气化,不能减少二氧化碳等温室气体的排放,C错误;煤的气化主要是煤与水蒸气发生置换反应生成水煤气:C(s)+H2O(g)CO(g)+H2(g),D错误。
6.实验室可用苯(沸点为80.1 ℃)与浓硝酸、浓硫酸组成的混酸反应制取硝基苯(难溶于水,不与酸或碱溶液反应,密度比水大,无色液体),装置如图所示,下列说法不正确的是( )
A.配制混酸时,将浓硫酸慢慢加入浓硝酸中并不断搅拌
B.水浴加热时,一般用沸水浴
C.反应的化学方程式为+HO—NO2+H2O
D.反应后纯化硝基苯,需经冷却、水洗、碱液洗、水洗、干燥及蒸馏
答案 B
解析 反应温度为50~60 ℃,水浴加热。
7.我国在CO2催化加氢制取汽油方面取得突破性进展,CO2转化过程示意图如图:
下列说法不正确的是( )
A.反应①的产物中含有水
B.反应②中只有碳碳键形成
C.汽油主要是C5~C12的烃类混合物
D.a的结构简式为,和C(CH3)4互为同分异构体
答案 B
解析 从质量守恒的角度判断,二氧化碳和氢气反应的化学方程式为CO2+H2===CO+H2O,则产物中含有水,故A说法正确;反应②生成烃类物质,含有C—C键、C—H键,故B说法错误;汽油所含烃类物质常温下为液态,易挥发,主要是C5~C12的烃类混合物,故C说法正确;图中a中含5个C,结构简式为,和C(CH3)4分子式相同,结构不同,二者互为同分异构体,D说法正确。
8.煤是一种重要能源,工业上常把煤进行气化和液化处理,变为清洁能源。由水蒸气和炽热的无烟煤作用可得水煤气,水煤气是混合气体,主要由两种无色无味气体组成,是重要的工业原料。
(1)在工业生产水煤气时,燃料层的温度会下降,这说明___________________。
(2)提出猜想:水煤气的成分可能是①________(填化学式,下同)和氢气,②________和氢气;提出以上猜想的依据是_______________________________________________。
设计实验:请从下列装置中选择一种,设计简单的实验证明猜想。
(3)你选择的装置是________(填字母)。
(4)实验结论:如果__________________________,那么猜想______________(填序号)合理。
答案 (1)碳和水蒸气的反应为吸热反应 (2)CO CO2 化学反应前后元素C、H、O种类不变 (3)B (4)澄清石灰水变浑浊 ②(或澄清石灰水不变浑浊 ①)
解析 (1)生产水煤气时,燃料层的温度下降,说明碳和水蒸气的反应为吸热反应。(2)根据质量守恒可推出水煤气可能有两种组成,①CO和H2,②CO2和H2。(3)CO2可以通过澄清石灰水检验。(4)如果澄清石灰水不变浑浊,则猜想①正确;如果澄清石灰水变浑浊,则猜想②正确。
三、同系物与同分异构体的判断及应用
9.有A、B两种烃,碳元素的质量分数相同,下列关于A和B的叙述正确的是( )
A.A和B一定互为同分异构体
B.A和B不可能互为同系物
C.燃烧等质量的A和B,消耗氧气的量一定相等
D.A和B各1 mol完全燃烧后生成的二氧化碳的质量一定相等
答案 C
解析 因烃中只有碳、氢两种元素,碳元素的质量分数相同,所以氢元素的质量分数也相同,最简式相同,因此燃烧相同质量的两种物质,消耗氧气的量一定相等,C正确;最简式相同的烃,可能互为同分异构体,如丙烯与环丙烷,也可能不是,如乙炔和苯,A错误;最简式相同的烃,可能互为同系物,如乙烯与丙烯,B错误;若互为同分异构体,则A和B各1 mol完全燃烧后生成的二氧化碳的质量一定相等;若互为同系物,则A和B各1 mol完全燃烧后生成的二氧化碳的质量一定不相等,D错误。
10.有以下结构的三种烃分子,下列有关说法错误的是( )
A.1 mol甲分子内含有10 mol共价键
B.由乙分子构成的物质不能使溴的四氯化碳溶液褪色
C.丙分子的二氯取代产物只有3种
D.三种分子内成键方式相同,而且最简式相同,故互为同系物
答案 D
解析 1 mol甲分子中含有6 mol碳碳单键和4 mol碳氢键,A正确;乙分子中不存在不饱和的“”或“—C≡C—”,不能使溴的四氯化碳溶液褪色,B正确;丙分子有位于棱边、面对角线、体对角线3种位置关系的二氯代物,C正确;甲、乙、丙三种分子的分子式分别为C4H4、C6H6和C8H8,最简式相同,但分子组成上不是相差若干个CH2原子团,故不互为同系物,D错误。
11.C5H12有3种不同的结构,甲:CH3(CH2)3CH3,乙:CH3CH(CH3)CH2CH3,丙:C(CH3)4,下列相关叙述正确的是( )
A.甲、乙、丙互为同系物,均可与氯气、溴蒸气发生取代反应
B.C5H12表示一种纯净物
C.甲、乙、丙中,丙的沸点最低
D.乙有3种不同沸点的一氯取代物
答案 C
解析 甲、乙、丙的分子式相同,结构不同,互为同分异构体,A错误;C5H12有3种同分异构体,所以不能表示纯净物,B错误;烷烃的同分异构体中,支链越多,沸点越低,丙分子中支链最多,所以沸点最低,C正确;乙分子中有4种位置的氢原子,即,故一氯代物有4种,D错误。
12.(2021·河北,8)苯并降冰片烯是一种重要的药物合成中间体,结构简式如图。关于该化合物,下列说法正确的是( )
A.是苯的同系物
B.分子中最多8个碳原子共平面
C.一氯代物有6种(不考虑立体异构)
D.分子中含有4个碳碳双键
答案 B
解析 由结构简式可知,苯并降冰片烯分子中苯环上的6个碳原子和连在苯环上的2个碳原子共平面,最多共有8个碳原子共平面,故B正确;由结构简式可知,苯并降冰片烯分子的结构上下对称,分子中含有5种类型的氢原子,则其一氯代物有5种,故C错误;苯环不是单双键交替的结构,由结构简式可知,苯并降冰片烯分子中只含有1个碳碳双键,故D错误。
四、常见烃的性质及应用
13.下列反应中前者属于取代反应,后者属于加成反应的是( )
A.甲烷与氯气混合后光照反应;乙烯使酸性高锰酸钾溶液褪色
B.乙烯与溴的四氯化碳溶液反应;苯与氢气在一定条件下反应生成环己烷
C.在苯中滴入溴水,溴水褪色;甲烷与氯气混合后光照反应
D.苯滴入浓硝酸和浓硫酸的混合液中,有油状物生成;乙烯与水生成乙醇的反应
答案 D
14.(2022·福建高一检测)下列有关常见烃性质的描述正确的是( )
A.光照下,1 mol CH4最多能与4 mol Cl2发生取代反应,产物中物质的量最多的是CCl4
B.苯与液溴在一定条件下能发生取代反应
C.甲烷与乙烯的混合物可通过溴的四氯化碳溶液分离
D.乙烯和苯分子中均含独立的碳碳双键,都能与H2发生加成反应
答案 B
解析 甲烷和氯气发生取代反应生成多种氯代烃,同时生成氯化氢,产物中物质的量最多的是氯化氢,A错误;苯与液溴在一定条件下可发生取代反应,生成溴苯,B正确;乙烯与溴的四氯化碳溶液发生加成反应,被除去,且甲烷易溶于四氯化碳,不能实现分离,C错误;苯不含碳碳双键,但可与氢气发生加成反应,D错误。
15.(1)乙烯能使酸性高锰酸钾溶液和溴的四氯化碳溶液褪色,其中,与高锰酸钾发生的反应是________(填反应类型,下同)反应;与溴发生的反应是_______反应。
(2)一种能使溴水褪色的气态烃,标准状况下5.6 L该气态烃的质量为10.5 g,10.5 g该烃完全燃烧时生成16.8 L二氧化碳(标准状况)和13.5 g水。则该烃的分子式为________________。
答案 (1)氧化 加成 (2)C3H6
解析 (1)乙烯分子中的碳碳双键易断裂,因此易被酸性高锰酸钾氧化,能与溴发生加成反应。
(2)设该气态烃的分子式为CxHy,
n(烃)==0.25 mol,
n(H2O)==0.75 mol,
n(CO2)==0.75 mol,
CxHy+(x+)O2xCO2 + H2O
1 mol x mol mol
0.25 mol 0.75 mol 0.75 mol
则x=3,y=6,该气态烃的分子式为C3H6。
16.分析下列烃分子,完成填空。
①CH3—CH2—CH2—CH2—CH3 ② ③ ④ ⑤ ⑥
(1)属于烷烃的有________(填序号,下同);互为同系物的有________、________。
(2)任写一种①的同分异构体的结构简式:_________________________________。
(3)④生成一氯乙烷的化学方程式:______________________________________________。
(4)③在一定条件下与液溴反应的化学方程式:____________________________________。
(5)②与水反应的化学方程式:__________________________________________________。
(6)④的二氯代物有________种。
答案 (1)①④⑥ ①④⑥ ③⑤
(2)CH3CH(CH3)CH2CH3[或C(CH3)4]
(3)CH3CH3+Cl2CH3CH2Cl+HCl
(4)+Br2+HBr
(5)CH2==CH2+H2OCH3CH2OH
(6)2
解析 (1)六种物质的分子式分别为①C5H12,②C2H4,③C6H6,④C2H6,⑤C7H8,⑥CH4;烷烃的通式为CnH2n+2(n≥1),所以属于烷烃的有①④⑥;同系物指的是结构相似,分子组成相差若干个“CH2”原子团的有机物,因此互为同系物的有①④⑥和③⑤。
(2)①为C5H12,其结构除了CH3—CH2—CH2—CH2—CH3外,还有CH3CH(CH3)CH2CH3和C(CH3)4。
(3)乙烷和氯气在光照条件下发生取代反应生成氯乙烷,反应的化学方程式:CH3CH3+Cl2CH3CH2Cl+HCl。
(4)苯和液溴在溴化铁作催化剂条件下发生取代反应生成溴苯和溴化氢,反应的化学方程式:+Br2+HBr。
(5)乙烯和水发生加成反应生成乙醇,反应的化学方程式:CH2==CH2+H2OCH3CH2OH。
(6)两个氯原子连在同一个碳上,结构有1种,分别连在两个碳上,结构有1种,共计有2种。
17.利用甲烷与氯气发生取代反应的副产品制取盐酸的设想在工业上已成为现实。某化学兴趣小组在实验室中模拟上述过程,其设计的模拟装置如图:
完成下列填空:
(1)A中反应的化学方程式是_________________________________;有人认为E中有氯化氢产生,不能证明甲烷与氯气发生了取代反应,你认为他的观点________(填“正确”或“不正确”),理由是______________________。
(2)B有三种功能:①控制气流速度;②混匀气体;③__________。
(3)设=x,若想理论上获得最多的氯化氢,则x≥________。
(4)一段时间后发现D中的棉花由白色变为蓝色,则棉花上可能预先滴有________溶液。
(5)E中除盐酸外,还含有机物,从E中分离出盐酸的最佳方法为________(填字母,下同)。
a.水洗分液法 b.蒸馏法
c.萃取分液法 d.结晶法
(6)该装置没有进行尾气处理,其尾气的主要成分为________。
a.CH4 b.CH3Cl c.CH2Cl2 d.CHCl3
答案 (1)MnO2+4HCl(浓)MnCl2+Cl2↑+2H2O 正确 制备的Cl2中混有HCl,若氯气与甲烷发生置换反应,也有氯化氢生成 (2)干燥氯气、氯化氢和甲烷 (3)4 (4)淀粉-KI (5)a (6)ab
解析 (1)A中二氧化锰与浓盐酸共热生成二氯化锰、氯气和水,反应的化学方程式为MnO2+4HCl(浓)MnCl2+Cl2↑+2H2O。(2)B为浓硫酸,可以干燥气体。(3)1 mol甲烷最多与4 mol氯气发生反应生成4 mol HCl,所以要获得更多氯化氢,氯气≥甲烷的4倍。(4)氯气能将碘化钾氧化为碘单质,淀粉遇到碘单质会变蓝色,故棉花上可能预先滴有淀粉-KI溶液。
(5)生成的有机物为氯代甲烷,难溶于水,可用分液的方法分离。(6)二氯甲烷、三氯甲烷和四氯化碳均为液体,则尾气的主要成分为未反应的甲烷和一氯甲烷气体。
