江苏省苏州市2024-2025学年九年级化学上学期期末检测模拟卷(含答案)
文档属性
| 名称 | 江苏省苏州市2024-2025学年九年级化学上学期期末检测模拟卷(含答案) |

|
|
| 格式 | docx | ||
| 文件大小 | 1.1MB | ||
| 资源类型 | 教案 | ||
| 版本资源 | 沪教版 | ||
| 科目 | 化学 | ||
| 更新时间 | 2025-01-05 00:00:00 | ||
图片预览




文档简介
2024-2025学年上学期期末检测模拟卷(江苏 苏州)
九年级化学
注意事项:
1.考试时间:100分钟,试卷满分:100分。答卷前,考生务必用黑色签字笔将准考证号、姓名、考场号和座位号填写在答题卡上。用2B 铅笔在“考场号”和“座位号”栏相应位置填涂考场号和座位号。将条形码粘贴在答题卡“条形码粘贴处”。
2.作答选择题时,选出每小题答案后,用 2B 铅笔把答题卡上对应题目选项的答案信息点涂黑;如需改动,用橡皮擦干净后,再选涂其他答案,答案不能答在试卷上。
3.非选择题必须用黑色签字笔作答,答案必须写在答题卡各题目指定区域内相应位置上;如需改动,先划掉原来的答案,然后再写上新的答案;不准使用铅笔和涂改液。不按以上要求作答的答案无效。
4.考试结束后,将本试卷和答题卡一并交回。
一、单项选择题(包括20题,每题2分,共40分。每题只有一个选项最符合题意。)
1.《天工开物》中记载了古法造纸工艺。下列造纸步骤中一定发生化学变化的是()
A.斩竹漂塘 B.煮徨足火
C.荡料入帘 D.覆帘压纸
2.“碳中和”是指二氧化碳或温室气体的产生和消耗能够抵消,达到相对“零排放”,以下做法不利于实现“碳中和”的是()
A.植树造林,增大植被面积 B.加大煤和石油的使用,节约成本
C.节能减排,低碳绿色出行 D.研发新工艺,有效捕集二氧化碳
3.下列物质属于氧化物的是()
A. B.
C. D.
4.下列物质由分子构成的是()
A.二氧化碳 B.铁
C.高锰酸钾 D.氯化钠
阅读下列材料,回答第下列问题:
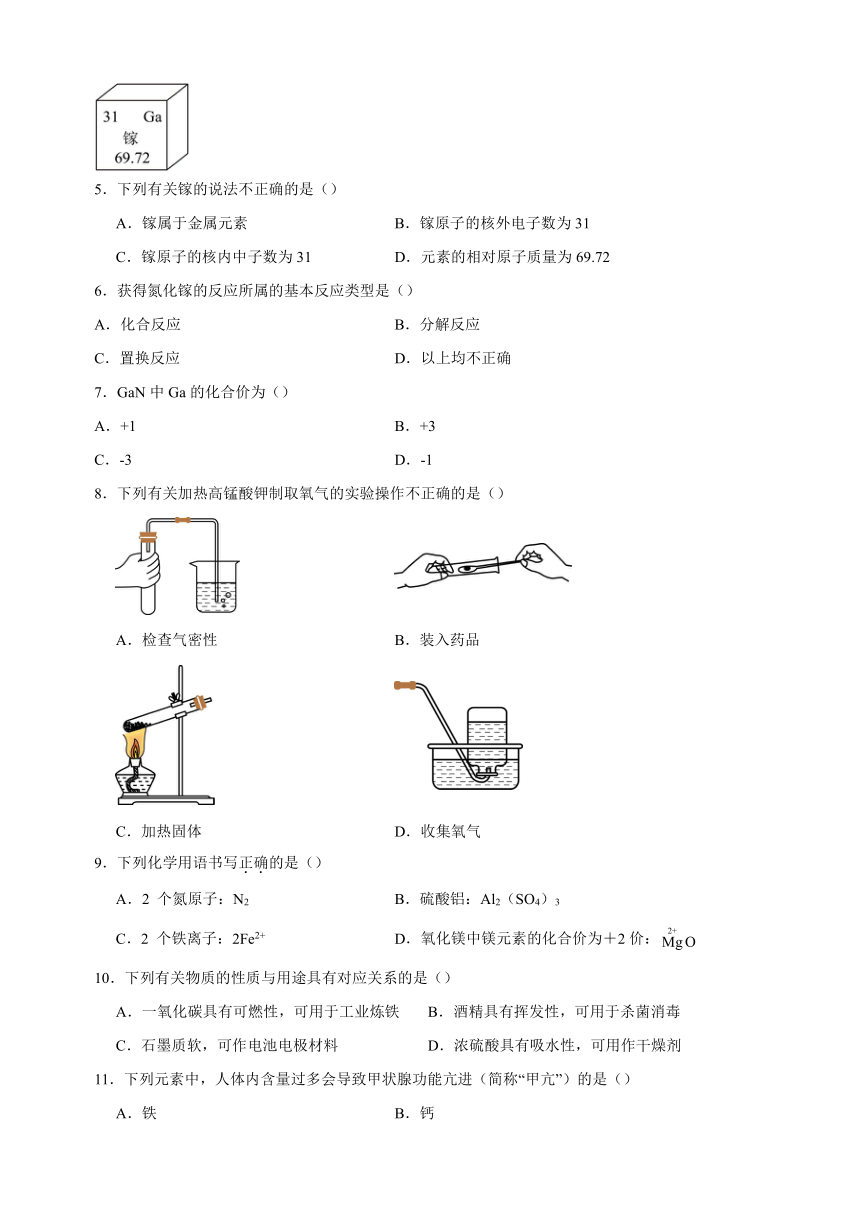
镓元素在元素周期表中的信息如图所示,其形成的化合物氮化镓(GaN)是一种新型半导体材料,可通过以下反应获得:,反应中氮元素的化合价不变。
5.下列有关镓的说法不正确的是()
A.镓属于金属元素 B.镓原子的核外电子数为31
C.镓原子的核内中子数为31 D.元素的相对原子质量为69.72
6.获得氮化镓的反应所属的基本反应类型是()
A.化合反应 B.分解反应
C.置换反应 D.以上均不正确
7.GaN中Ga的化合价为()
A.+1 B.+3
C.-3 D.-1
8.下列有关加热高锰酸钾制取氧气的实验操作不正确的是()
A.检查气密性 B.装入药品
C.加热固体 D.收集氧气
9.下列化学用语书写正确的是()
A.2 个氮原子:N2 B.硫酸铝:Al2(SO4)3
C.2 个铁离子:2Fe2+ D.氧化镁中镁元素的化合价为+2价:
10.下列有关物质的性质与用途具有对应关系的是()
A.一氧化碳具有可燃性,可用于工业炼铁 B.酒精具有挥发性,可用于杀菌消毒
C.石墨质软,可作电池电极材料 D.浓硫酸具有吸水性,可用作干燥剂
11.下列元素中,人体内含量过多会导致甲状腺功能亢进(简称“甲亢”)的是()
A.铁 B.钙
C.锌 D.碘
12.某净水装置使用膜处理技术,其原理如图所示。下列说法正确的是()
A.微滤膜能滤去大分子和蛋白质,而超滤膜不能
B.超滤膜的孔隙直径小于微滤膜
C.经膜处理净化后得到的水样是纯净物
D.实验室通过过滤也可滤去悬浮颗粒和细菌
13.下列有关空气的说法正确的是()
A.氧气是无色无味、易溶于水的气体
B.空气中的二氧化碳含量过高不会对环境造成影响
C.空气污染指数值越高,空气质量越好
D.机动车尾气中的氮氧化物会对空气造成污染
14.“雨过天晴云破处”是对汝窑瓷器的一种赞美。陶瓷以黏土等天然硅酸盐为主要原料烧成的制品,在烧制过程中会发生4FeS+7O22Fe2O3+4X等反应。下列叙述错误的是()
A.陶瓷是混合物 B.该反应方程式中FeS与X物质的质量比为4:7
C.X是SO2 D.该反应中有三种元素化合价发生改变
15.磷酸奥司他韦胶囊是治疗流感的特效药,奥司他韦的化学式可表示为C16H28N2O4。下列说法正确的是()
A.从物质分类上看:C16H28N2O4属于混合物
B.从宏观组成上看:C16H28N2O4由碳、氢、氮、氧四种元素组成
C.从微观结构上看:C16H28N2O4中有1个氮分子
D.从质量占比上看:C16H28N2O4中碳元素和氢元素的质量比为16:28
16.下列关于金属材料的认识,不正确的是()
A.武德合金比成分金属熔点低可做保险丝 B.黄铜(铜与锌的合金)的硬度大于纯铜
C.合金是由两种或多种金属熔合而成 D.生活中应用最广泛的金属是铁
17.如图是a、b、c的溶解度曲线,下列说法正确的是()
A.t1℃时,a、c的饱和溶液中溶质的质量相等
B.t2℃时,把50g a放入50g水中,得到50%的a溶液
C.a中混有少量的b,可通过蒸发结晶的方式进行提纯
D.t2℃时a、b、c的三种物质的饱和溶液降温到t1℃,所得溶液的溶质质量分数大小关系是b>a>c
18.下列区分两种不同物质的方法不合理的是()
A.纯铜和黄铜:相互刻划后比较硬度
B.硬水和软水:加肥皂水后振荡
C.碳粉和氧化铜粉末:观察固体的颜色
D.和:加水溶解后测温度
19.下列实验的原理与操作,不能达到相应实验目的的是()
A.验证石蜡中含有碳元素 B.验证二氧化碳能与水反应
C.验证分子在不断地运动 D.验证质量守恒定律
20.科学工作者研发了一种SUNCAT系统,借助该系统利用如图所示的原理可持续合成氨。下列说法正确的是()
A.该系统中只有Li、O的化合价发生了改变
B.涉及的反应类型只有化合反应和分解反应
C.理论上,每合成68gNH3,就需要消耗56gN2
D.理论上,每消耗28gN2,需额外补充42gLi
非选择题(共60分)
21.(8分)苏州的许多传统与现代工艺都与化学息息相关。
(1)传统工艺
①文物贴金。金箔不易变色,说明黄金化学性质_____(填“稳定”或“活泼”)。
②传统粉墙。用石灰浆(氢氧化钙的悬浊液)抹墙后,墙壁表面变白且坚硬。在上述过程中,氢氧化钙发生反应的化学方程式为_____。
③钻石切割。钻石和石墨均由碳原子构成,硬度差异很大的原因是_____。
(2)矿物颜料
①朱砂可制成鲜红色颜料,主要成分为硫化汞(、的化合价分别为+2和-2)。硫化汞的化学式为_____。
②赤铁矿(主要成分)可用于制作红棕色颜料,其中铁元素化合价为_____。
③孔雀石[主要成分为]可用于制作青色颜料,对酸敏感。补充完整下列化学方程式:_____。
(3)创新科技
①新能源客车。电池充电时的能量转化方式:电能转化为_____。
②多晶硅制备。气体被加热分解为硅和氢气,反应的化学方程式为_____。
22.(6分)高铁已成为中国铁路高质量发展的靓丽名片。结合图所示信息回答问题。
(1)电网通过石墨电剧给动车供电,体现了石墨具有良好的_____性。
(2)动车车身表面防锈采用的方法是_____。
(3)制造铁轨的锰钢是一种铁合金,与纯铁相比,其硬度更_____(填“大”或“小”)。
(4)晶体硅是高铁信息传输系统中电子芯片的关键电刷车身材料。工业上制取硅的反应为:SiO2+2CSi+2X↑,则生成物X的化学式为_____。
(5)乘客喝完矿泉水后的塑料瓶应放入_____(填“可回收”或“不可回收”)垃圾箱中。
23.(12分)食盐是生产生活中常见的物质,自然界中氯化钠储量很大,海水中氯化钠的含量在2%~3%。
(1)构成氯化钠的阳离子是_____(填微粒符号)。
(2)据记载,炎帝时期人们就掌握了熬煮海水获得食盐的技术。这种技术与实验室的_____(填操作名称)原理相同。
(3)科学家从海水中取样,根据样品中氯化钠和海水的质量比,进而计算出海水中大致的含盐量,理由是溶液具有_____性。
(4)配制100g2%的食盐水并模拟熬煮海水实验。
①配制该溶液的正确操作顺序是:_____(填序号)。
②量取上述实验所需蒸馏水时,选用的仪器是_____(填字母)。
a.100mL烧杯 b.100mL量筒 c.50mL烧杯 b.50mL量筒
③为加快氯化钠的溶解速率,可采用的措施有_____。
④模拟熬煮海水时,需用玻璃棒搅拌的目的是_____。
(5)现有60℃时100g20%的氯化钠溶液,恒温蒸发_____g(结果保留整数)水后开始有晶体析出,并在下图中画出析出氯化钠的质量与蒸发水的质量关系_____。
已知:60℃时,氯化钠的溶解度约为37g。
24.(10分)阅读下列材料,回答相关问题。
石墨烯是21世纪最具前景的新型纳米材料,它是从石墨中剥离出来的单层碳原子晶体,其微观结构如图1所示。工业上可采用甲烷气体(CH4)在高温和催化剂的作用下分解制取石墨烯并产生氢气。
石墨烯:晶体管的传输速度远远超过目前的硅晶体管,因此有希望应用于全新超级计算机的研发。纺织面料掺入石墨烯后,在低温情况下,石墨烯可将来自远红外线的热量传送给人体,改善人体微循环系统,促进新陈代谢。另外石墨烯还能影响菌体的正常代谢,从而使茵体无法吸收养分直至死亡。不同面料中掺入石墨烯后的抗菌效果如图2所示。
(1)石墨烯属于(填物质类别)。
(2)石墨烯有希望应用于全新超级计算机的研发,说明石墨烯具有性。
(3)在一定条件下,石墨烯在氧气中完全燃烧的产物是(填化学式)。
(4)纺织面料中掺入石墨烯后具有的优点有(任写一条)。
(5)下列有关说法正确的有(填字母)。
a.抑菌率越高,表明抗菌性能越弱
b.面料的抑菌率与面料种类、菌体种类均有关
c.石墨烯纺织面料的抗菌性能比普通面料强
(6)工业上制取石墨烯的化学方程式为。
25.(12分)某同学用稀盐酸和大理石制取少量气体,并进行相关实验研究。
(1)配制溶质质量分数为的稀盐酸
需要溶质质量分数为的盐酸(密度为)的体积为。蒸馏水(密度为)的体积为。
(2)用稀盐酸和大理石制取
①写出上述反应的化学方程式:。
②图中仪器的名称为。
③制取的发生装置可选用图-1中的(填字母)。若用装置收集,则气体应从导管(填“a”或“b”)端通入。
(3)的性质实验
①将通入装置,观察到的现象是。
②将通入装置,观察到脱脂棉剧烈燃烧。脱脂棉燃烧的原因除与反应生成外,还可能是。
③如图-2所示,在容积为的三颈烧瓶中集满,将注射器中的蒸馏水全部压入烧瓶,并立即夹紧止水夹。开始注水后,烧瓶内气体压强和温度随时间的变化情况如图-3所示。曲线段气体压强逐渐减小,且最终压强略高于起始压强的原因是。
26.(12分)实验室用氧化铁粉末模拟炼铁,装置如图所示。
(1)B装置的两个作用是、。(已知:氢氧化钠、碳酸钠易溶于水,
(2)某同学用酒精灯和酒精喷灯两种不同的热源进行加热,对模拟炼铁进一步探究,装置如图所示。
完全反应后,两组生成物均为黑色粉末(纯净物),分别用两组生成物进行如下实验:
步骤 实验操作 甲组 乙组
1 称量黑色粉末的质量 m1 m2
2 取黑色粉末,用磁铁吸引 能被吸引 能被吸引
3 取黑色粉末,加入稀盐酸 固体全部溶解,有大量气泡 固体不溶解,无气泡产生
4 取黑色粉末,加入足量硫酸铜溶液 有红色物质析出 无红色物质析出
查阅资料:a.常温下Fe3O4不与稀盐酸或硫酸铜溶液反应。
b.CO与Fe2O3反应时的产物受温度的影响如图所示:
根据实验分析:
①甲组产物是,乙组用的热源是。
②某同学猜想乙组的生成物为Fe3O4。若该同学称量黑色粉末m2=g,则可证实他的猜想。
(3)某钢铁厂采用赤铁矿(主要成分为Fe2O3)炼铁,日产含铁7×104t的生铁,至少需要含Fe2O380%的赤铁矿的质量是多少?(写出计算过程)。
参考答案
1.B
2.B
3.B
4.A
5.C6.C7.B
8.C
9.B
10.D
11.D
12.B
13.D
14.B
15.B
16.C
17.D
18.C
19.D
20.C
21.(1) 稳定 Ca(OH)2+CO2=CaCO3↓+H2O 碳原子排列方式不同
(2) HgS +3 H2O
(3) 化学能
22.(1)导电(2)喷漆(刷漆、涂漆)(3)大(4)CO(5)可回收
23.(1)(2)蒸发(3)均一
(4) ACDB b 搅拌、加热、或将氯化钠研磨成细小颗粒等(答案合理即可)使液体受热均匀,防止因局部温度过高造成液滴飞
(5)
24.(1)单质(2)导电(性)(3)CO2
(4)在低温情况下,石墨烯可将来自远红外线的热量传送给人体,改善人体微循环系统,促进新陈代谢。(抗菌)(5)bc(6)CH4C+2H2
25.(1) 25 70
(2) CaCO3+2HCl=CaCl2+CO2↑+H2O 酒精灯 B b
(3) 紫色石蕊溶液变红过氧化钠和二氧化碳反应生成氧气的反应放热,使温度升至着火点以上二氧化碳与水反应生成碳酸,所以导致瓶内气压降低,但生成的碳酸不稳定,会分解生成少量二氧化碳,所以最终压强略高于起始压强
26.(1) 吸收CO2收集CO(2) Fe/铁酒精灯 4.64
(3)解:设至少需要含Fe2O380%的赤铁矿的质量是x
x=1.25×105t
答:至少需要含Fe2O380%的赤铁矿的质量是1.25×105t。
九年级化学
注意事项:
1.考试时间:100分钟,试卷满分:100分。答卷前,考生务必用黑色签字笔将准考证号、姓名、考场号和座位号填写在答题卡上。用2B 铅笔在“考场号”和“座位号”栏相应位置填涂考场号和座位号。将条形码粘贴在答题卡“条形码粘贴处”。
2.作答选择题时,选出每小题答案后,用 2B 铅笔把答题卡上对应题目选项的答案信息点涂黑;如需改动,用橡皮擦干净后,再选涂其他答案,答案不能答在试卷上。
3.非选择题必须用黑色签字笔作答,答案必须写在答题卡各题目指定区域内相应位置上;如需改动,先划掉原来的答案,然后再写上新的答案;不准使用铅笔和涂改液。不按以上要求作答的答案无效。
4.考试结束后,将本试卷和答题卡一并交回。
一、单项选择题(包括20题,每题2分,共40分。每题只有一个选项最符合题意。)
1.《天工开物》中记载了古法造纸工艺。下列造纸步骤中一定发生化学变化的是()
A.斩竹漂塘 B.煮徨足火
C.荡料入帘 D.覆帘压纸
2.“碳中和”是指二氧化碳或温室气体的产生和消耗能够抵消,达到相对“零排放”,以下做法不利于实现“碳中和”的是()
A.植树造林,增大植被面积 B.加大煤和石油的使用,节约成本
C.节能减排,低碳绿色出行 D.研发新工艺,有效捕集二氧化碳
3.下列物质属于氧化物的是()
A. B.
C. D.
4.下列物质由分子构成的是()
A.二氧化碳 B.铁
C.高锰酸钾 D.氯化钠
阅读下列材料,回答第下列问题:
镓元素在元素周期表中的信息如图所示,其形成的化合物氮化镓(GaN)是一种新型半导体材料,可通过以下反应获得:,反应中氮元素的化合价不变。
5.下列有关镓的说法不正确的是()
A.镓属于金属元素 B.镓原子的核外电子数为31
C.镓原子的核内中子数为31 D.元素的相对原子质量为69.72
6.获得氮化镓的反应所属的基本反应类型是()
A.化合反应 B.分解反应
C.置换反应 D.以上均不正确
7.GaN中Ga的化合价为()
A.+1 B.+3
C.-3 D.-1
8.下列有关加热高锰酸钾制取氧气的实验操作不正确的是()
A.检查气密性 B.装入药品
C.加热固体 D.收集氧气
9.下列化学用语书写正确的是()
A.2 个氮原子:N2 B.硫酸铝:Al2(SO4)3
C.2 个铁离子:2Fe2+ D.氧化镁中镁元素的化合价为+2价:
10.下列有关物质的性质与用途具有对应关系的是()
A.一氧化碳具有可燃性,可用于工业炼铁 B.酒精具有挥发性,可用于杀菌消毒
C.石墨质软,可作电池电极材料 D.浓硫酸具有吸水性,可用作干燥剂
11.下列元素中,人体内含量过多会导致甲状腺功能亢进(简称“甲亢”)的是()
A.铁 B.钙
C.锌 D.碘
12.某净水装置使用膜处理技术,其原理如图所示。下列说法正确的是()
A.微滤膜能滤去大分子和蛋白质,而超滤膜不能
B.超滤膜的孔隙直径小于微滤膜
C.经膜处理净化后得到的水样是纯净物
D.实验室通过过滤也可滤去悬浮颗粒和细菌
13.下列有关空气的说法正确的是()
A.氧气是无色无味、易溶于水的气体
B.空气中的二氧化碳含量过高不会对环境造成影响
C.空气污染指数值越高,空气质量越好
D.机动车尾气中的氮氧化物会对空气造成污染
14.“雨过天晴云破处”是对汝窑瓷器的一种赞美。陶瓷以黏土等天然硅酸盐为主要原料烧成的制品,在烧制过程中会发生4FeS+7O22Fe2O3+4X等反应。下列叙述错误的是()
A.陶瓷是混合物 B.该反应方程式中FeS与X物质的质量比为4:7
C.X是SO2 D.该反应中有三种元素化合价发生改变
15.磷酸奥司他韦胶囊是治疗流感的特效药,奥司他韦的化学式可表示为C16H28N2O4。下列说法正确的是()
A.从物质分类上看:C16H28N2O4属于混合物
B.从宏观组成上看:C16H28N2O4由碳、氢、氮、氧四种元素组成
C.从微观结构上看:C16H28N2O4中有1个氮分子
D.从质量占比上看:C16H28N2O4中碳元素和氢元素的质量比为16:28
16.下列关于金属材料的认识,不正确的是()
A.武德合金比成分金属熔点低可做保险丝 B.黄铜(铜与锌的合金)的硬度大于纯铜
C.合金是由两种或多种金属熔合而成 D.生活中应用最广泛的金属是铁
17.如图是a、b、c的溶解度曲线,下列说法正确的是()
A.t1℃时,a、c的饱和溶液中溶质的质量相等
B.t2℃时,把50g a放入50g水中,得到50%的a溶液
C.a中混有少量的b,可通过蒸发结晶的方式进行提纯
D.t2℃时a、b、c的三种物质的饱和溶液降温到t1℃,所得溶液的溶质质量分数大小关系是b>a>c
18.下列区分两种不同物质的方法不合理的是()
A.纯铜和黄铜:相互刻划后比较硬度
B.硬水和软水:加肥皂水后振荡
C.碳粉和氧化铜粉末:观察固体的颜色
D.和:加水溶解后测温度
19.下列实验的原理与操作,不能达到相应实验目的的是()
A.验证石蜡中含有碳元素 B.验证二氧化碳能与水反应
C.验证分子在不断地运动 D.验证质量守恒定律
20.科学工作者研发了一种SUNCAT系统,借助该系统利用如图所示的原理可持续合成氨。下列说法正确的是()
A.该系统中只有Li、O的化合价发生了改变
B.涉及的反应类型只有化合反应和分解反应
C.理论上,每合成68gNH3,就需要消耗56gN2
D.理论上,每消耗28gN2,需额外补充42gLi
非选择题(共60分)
21.(8分)苏州的许多传统与现代工艺都与化学息息相关。
(1)传统工艺
①文物贴金。金箔不易变色,说明黄金化学性质_____(填“稳定”或“活泼”)。
②传统粉墙。用石灰浆(氢氧化钙的悬浊液)抹墙后,墙壁表面变白且坚硬。在上述过程中,氢氧化钙发生反应的化学方程式为_____。
③钻石切割。钻石和石墨均由碳原子构成,硬度差异很大的原因是_____。
(2)矿物颜料
①朱砂可制成鲜红色颜料,主要成分为硫化汞(、的化合价分别为+2和-2)。硫化汞的化学式为_____。
②赤铁矿(主要成分)可用于制作红棕色颜料,其中铁元素化合价为_____。
③孔雀石[主要成分为]可用于制作青色颜料,对酸敏感。补充完整下列化学方程式:_____。
(3)创新科技
①新能源客车。电池充电时的能量转化方式:电能转化为_____。
②多晶硅制备。气体被加热分解为硅和氢气,反应的化学方程式为_____。
22.(6分)高铁已成为中国铁路高质量发展的靓丽名片。结合图所示信息回答问题。
(1)电网通过石墨电剧给动车供电,体现了石墨具有良好的_____性。
(2)动车车身表面防锈采用的方法是_____。
(3)制造铁轨的锰钢是一种铁合金,与纯铁相比,其硬度更_____(填“大”或“小”)。
(4)晶体硅是高铁信息传输系统中电子芯片的关键电刷车身材料。工业上制取硅的反应为:SiO2+2CSi+2X↑,则生成物X的化学式为_____。
(5)乘客喝完矿泉水后的塑料瓶应放入_____(填“可回收”或“不可回收”)垃圾箱中。
23.(12分)食盐是生产生活中常见的物质,自然界中氯化钠储量很大,海水中氯化钠的含量在2%~3%。
(1)构成氯化钠的阳离子是_____(填微粒符号)。
(2)据记载,炎帝时期人们就掌握了熬煮海水获得食盐的技术。这种技术与实验室的_____(填操作名称)原理相同。
(3)科学家从海水中取样,根据样品中氯化钠和海水的质量比,进而计算出海水中大致的含盐量,理由是溶液具有_____性。
(4)配制100g2%的食盐水并模拟熬煮海水实验。
①配制该溶液的正确操作顺序是:_____(填序号)。
②量取上述实验所需蒸馏水时,选用的仪器是_____(填字母)。
a.100mL烧杯 b.100mL量筒 c.50mL烧杯 b.50mL量筒
③为加快氯化钠的溶解速率,可采用的措施有_____。
④模拟熬煮海水时,需用玻璃棒搅拌的目的是_____。
(5)现有60℃时100g20%的氯化钠溶液,恒温蒸发_____g(结果保留整数)水后开始有晶体析出,并在下图中画出析出氯化钠的质量与蒸发水的质量关系_____。
已知:60℃时,氯化钠的溶解度约为37g。
24.(10分)阅读下列材料,回答相关问题。
石墨烯是21世纪最具前景的新型纳米材料,它是从石墨中剥离出来的单层碳原子晶体,其微观结构如图1所示。工业上可采用甲烷气体(CH4)在高温和催化剂的作用下分解制取石墨烯并产生氢气。
石墨烯:晶体管的传输速度远远超过目前的硅晶体管,因此有希望应用于全新超级计算机的研发。纺织面料掺入石墨烯后,在低温情况下,石墨烯可将来自远红外线的热量传送给人体,改善人体微循环系统,促进新陈代谢。另外石墨烯还能影响菌体的正常代谢,从而使茵体无法吸收养分直至死亡。不同面料中掺入石墨烯后的抗菌效果如图2所示。
(1)石墨烯属于(填物质类别)。
(2)石墨烯有希望应用于全新超级计算机的研发,说明石墨烯具有性。
(3)在一定条件下,石墨烯在氧气中完全燃烧的产物是(填化学式)。
(4)纺织面料中掺入石墨烯后具有的优点有(任写一条)。
(5)下列有关说法正确的有(填字母)。
a.抑菌率越高,表明抗菌性能越弱
b.面料的抑菌率与面料种类、菌体种类均有关
c.石墨烯纺织面料的抗菌性能比普通面料强
(6)工业上制取石墨烯的化学方程式为。
25.(12分)某同学用稀盐酸和大理石制取少量气体,并进行相关实验研究。
(1)配制溶质质量分数为的稀盐酸
需要溶质质量分数为的盐酸(密度为)的体积为。蒸馏水(密度为)的体积为。
(2)用稀盐酸和大理石制取
①写出上述反应的化学方程式:。
②图中仪器的名称为。
③制取的发生装置可选用图-1中的(填字母)。若用装置收集,则气体应从导管(填“a”或“b”)端通入。
(3)的性质实验
①将通入装置,观察到的现象是。
②将通入装置,观察到脱脂棉剧烈燃烧。脱脂棉燃烧的原因除与反应生成外,还可能是。
③如图-2所示,在容积为的三颈烧瓶中集满,将注射器中的蒸馏水全部压入烧瓶,并立即夹紧止水夹。开始注水后,烧瓶内气体压强和温度随时间的变化情况如图-3所示。曲线段气体压强逐渐减小,且最终压强略高于起始压强的原因是。
26.(12分)实验室用氧化铁粉末模拟炼铁,装置如图所示。
(1)B装置的两个作用是、。(已知:氢氧化钠、碳酸钠易溶于水,
(2)某同学用酒精灯和酒精喷灯两种不同的热源进行加热,对模拟炼铁进一步探究,装置如图所示。
完全反应后,两组生成物均为黑色粉末(纯净物),分别用两组生成物进行如下实验:
步骤 实验操作 甲组 乙组
1 称量黑色粉末的质量 m1 m2
2 取黑色粉末,用磁铁吸引 能被吸引 能被吸引
3 取黑色粉末,加入稀盐酸 固体全部溶解,有大量气泡 固体不溶解,无气泡产生
4 取黑色粉末,加入足量硫酸铜溶液 有红色物质析出 无红色物质析出
查阅资料:a.常温下Fe3O4不与稀盐酸或硫酸铜溶液反应。
b.CO与Fe2O3反应时的产物受温度的影响如图所示:
根据实验分析:
①甲组产物是,乙组用的热源是。
②某同学猜想乙组的生成物为Fe3O4。若该同学称量黑色粉末m2=g,则可证实他的猜想。
(3)某钢铁厂采用赤铁矿(主要成分为Fe2O3)炼铁,日产含铁7×104t的生铁,至少需要含Fe2O380%的赤铁矿的质量是多少?(写出计算过程)。
参考答案
1.B
2.B
3.B
4.A
5.C6.C7.B
8.C
9.B
10.D
11.D
12.B
13.D
14.B
15.B
16.C
17.D
18.C
19.D
20.C
21.(1) 稳定 Ca(OH)2+CO2=CaCO3↓+H2O 碳原子排列方式不同
(2) HgS +3 H2O
(3) 化学能
22.(1)导电(2)喷漆(刷漆、涂漆)(3)大(4)CO(5)可回收
23.(1)(2)蒸发(3)均一
(4) ACDB b 搅拌、加热、或将氯化钠研磨成细小颗粒等(答案合理即可)使液体受热均匀,防止因局部温度过高造成液滴飞
(5)
24.(1)单质(2)导电(性)(3)CO2
(4)在低温情况下,石墨烯可将来自远红外线的热量传送给人体,改善人体微循环系统,促进新陈代谢。(抗菌)(5)bc(6)CH4C+2H2
25.(1) 25 70
(2) CaCO3+2HCl=CaCl2+CO2↑+H2O 酒精灯 B b
(3) 紫色石蕊溶液变红过氧化钠和二氧化碳反应生成氧气的反应放热,使温度升至着火点以上二氧化碳与水反应生成碳酸,所以导致瓶内气压降低,但生成的碳酸不稳定,会分解生成少量二氧化碳,所以最终压强略高于起始压强
26.(1) 吸收CO2收集CO(2) Fe/铁酒精灯 4.64
(3)解:设至少需要含Fe2O380%的赤铁矿的质量是x
x=1.25×105t
答:至少需要含Fe2O380%的赤铁矿的质量是1.25×105t。
同课章节目录
