浙江省临海市杜桥中学高中化学选修四课件:专题一 第二单元 化学电源(共13张PPT)
文档属性
| 名称 | 浙江省临海市杜桥中学高中化学选修四课件:专题一 第二单元 化学电源(共13张PPT) |

|
|
| 格式 | zip | ||
| 文件大小 | 225.1KB | ||
| 资源类型 | 教案 | ||
| 版本资源 | 苏教版 | ||
| 科目 | 化学 | ||
| 更新时间 | 2016-04-17 00:00:00 | ||
图片预览




文档简介
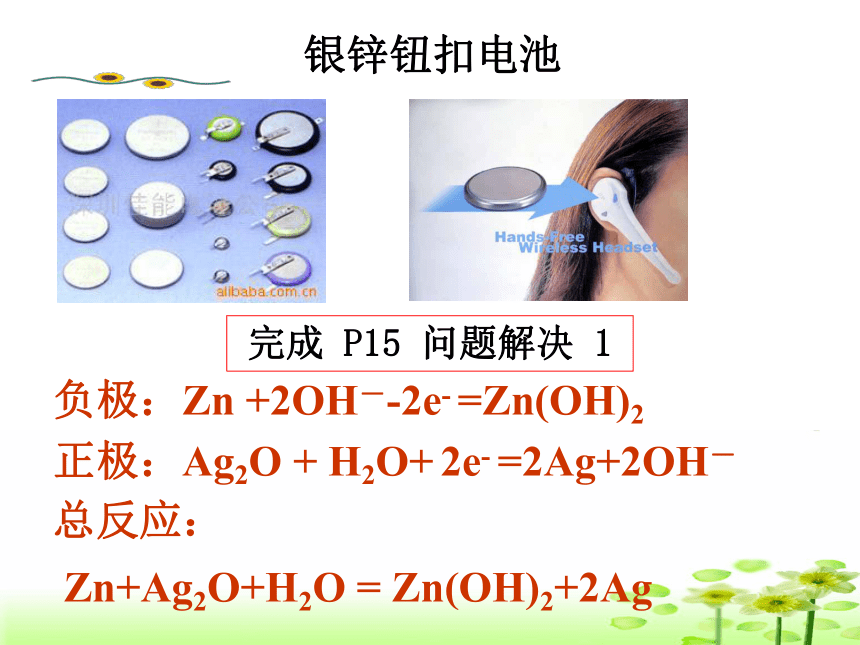
课件13张PPT。专题1 化学反应与能量变化 第二单元 化学能与电能的转化化学电源化学电池银锌钮扣电池正极:Ag2O + H2O+ 2e- =2Ag+2OH-负极:Zn +2OH--2e- =Zn(OH)2总反应:
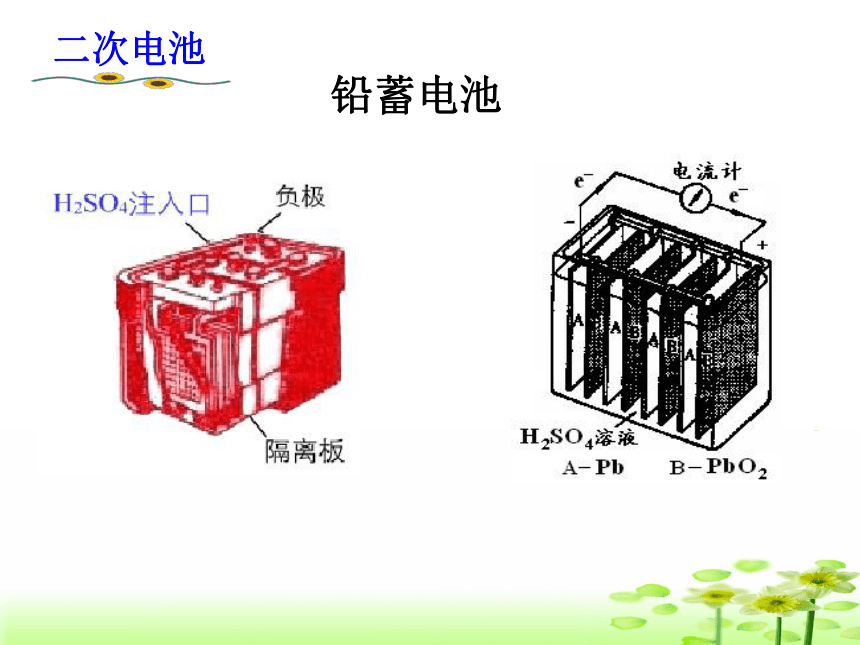
Zn+Ag2O+H2O = Zn(OH)2+2Ag完成 P15 问题解决 1碱性锌-锰干电池负极:正极:碱性电池 一次电池完成 P15 问题解决 2二次电池铅蓄电池放电过程总反应:Pb+PbO2+2H2SO4=2PbSO4+2H2O Pb + SO42- -2e- =PbSO4 正极:PbO2 + 4H++SO42-+2e- =PbSO4 +2H2O 氧化反应 还原反应负极:①放电过程铅蓄电池充电的反应则是上述反应的逆过程铅蓄电池②充电过程PbSO4 +2e- =Pb + SO42- 还原反应阴极:阳极:PbSO4 +2H2O -2e- = PbO2 + 4H++ SO42- 氧化反应接电源负极接电源正极充电过程总反应:2PbSO4+2H2O=Pb+PbO2+2H2SO4铅蓄电池的充放电过程:Pb+PbO2+2H2SO4 2PbSO4+2H2O燃料电池燃料电池是利用燃料和氧化剂之间的氧化还原反应,将化学能直接转换成电能的化学电源。(氢气、甲烷、甲醇等燃料电池……) 氢氧燃料电池 负极: 2H2-4e-+4OH-==4H2O
正极: O2+2H2O+4e-==4OH-
总反应: 2H2+O2==2H2O若把氢氧化钾换成硫酸电极反应式又该如何呢?碱性电解质(KOH)想一想电极反应
负极:
正极:
总反应:2H2 + O2=2H2O2H2 - 4e- = 4H+O2 + 4H+ + 4e- = 2H2O酸性氢氧燃料电池氢气是燃料电池最简单的燃料,虽然使用方便,却受到价格和来源的限制。常用的燃料往往是某些碳氢化合物,如:甲烷、汽油等。请写出将图中氢气换成甲烷时所构成的甲烷燃料电池中a极的电极反应式:
,
此时电池内总的反应式:
。
CH4+10OH- - 8e-=CO32- +7H2OCH4+2O2+2KOH=K2CO3+3H2O知识拓展小结原电池电极反应式的书写注意事项:
(1)负氧正还。
(2)要注意溶液的酸碱性,适当的在电极方程式两边添加H+、OH—、H2O,以遵循电荷守恒和质量守恒。
(3)要注意电极反应产物是否与电解质溶液发生反应。(2004年江苏高考)碱性电池具有容量大、放电电流大的特点,因而得到广泛应用。锌-锰碱性电池以氢氧化钾溶液为电解液,电流总反应式为:
Zn?s?+2MnO2?s?+H2O?l?=Zn?OH?2?s?+Mn2O3?s?
下列说法错误的是 ( )
A? 电池工作时,锌失去电子
B? 电池正极电极反应式为:
2MnO2?s?+H2O?l?+2e?=Mn2O3?s?+2OH??aq?
C? 电池工作时,电子由正极通过外电路流向负极
D? 外电路中每通过0?2 mol电子,锌的质量理论上减少6?5 g C练习1: 练习2:市场上经常见到的标记为Li-ion的电池称为“锂离子电池”。它的负极材料是金属锂和碳的复合材料(碳作为金属锂的载体),电解质为一种能传导Li+的高分子材料。这种锂离子电池的电池反应为:
Li+2Li0.35NiO2 2Li0.85NiO2????
放电充电下列说法不正确的是 ( )
A.放电时,负极的电极反应式:Li-e?=Li+
B.充电时,Li0.85NiO2既发生氧化反应又发生还原反应
C.该电池不能用水溶液作为电解质
D.放电过程中Li+向负极移动
Zn+Ag2O+H2O = Zn(OH)2+2Ag完成 P15 问题解决 1碱性锌-锰干电池负极:正极:碱性电池 一次电池完成 P15 问题解决 2二次电池铅蓄电池放电过程总反应:Pb+PbO2+2H2SO4=2PbSO4+2H2O Pb + SO42- -2e- =PbSO4 正极:PbO2 + 4H++SO42-+2e- =PbSO4 +2H2O 氧化反应 还原反应负极:①放电过程铅蓄电池充电的反应则是上述反应的逆过程铅蓄电池②充电过程PbSO4 +2e- =Pb + SO42- 还原反应阴极:阳极:PbSO4 +2H2O -2e- = PbO2 + 4H++ SO42- 氧化反应接电源负极接电源正极充电过程总反应:2PbSO4+2H2O=Pb+PbO2+2H2SO4铅蓄电池的充放电过程:Pb+PbO2+2H2SO4 2PbSO4+2H2O燃料电池燃料电池是利用燃料和氧化剂之间的氧化还原反应,将化学能直接转换成电能的化学电源。(氢气、甲烷、甲醇等燃料电池……) 氢氧燃料电池 负极: 2H2-4e-+4OH-==4H2O
正极: O2+2H2O+4e-==4OH-
总反应: 2H2+O2==2H2O若把氢氧化钾换成硫酸电极反应式又该如何呢?碱性电解质(KOH)想一想电极反应
负极:
正极:
总反应:2H2 + O2=2H2O2H2 - 4e- = 4H+O2 + 4H+ + 4e- = 2H2O酸性氢氧燃料电池氢气是燃料电池最简单的燃料,虽然使用方便,却受到价格和来源的限制。常用的燃料往往是某些碳氢化合物,如:甲烷、汽油等。请写出将图中氢气换成甲烷时所构成的甲烷燃料电池中a极的电极反应式:
,
此时电池内总的反应式:
。
CH4+10OH- - 8e-=CO32- +7H2OCH4+2O2+2KOH=K2CO3+3H2O知识拓展小结原电池电极反应式的书写注意事项:
(1)负氧正还。
(2)要注意溶液的酸碱性,适当的在电极方程式两边添加H+、OH—、H2O,以遵循电荷守恒和质量守恒。
(3)要注意电极反应产物是否与电解质溶液发生反应。(2004年江苏高考)碱性电池具有容量大、放电电流大的特点,因而得到广泛应用。锌-锰碱性电池以氢氧化钾溶液为电解液,电流总反应式为:
Zn?s?+2MnO2?s?+H2O?l?=Zn?OH?2?s?+Mn2O3?s?
下列说法错误的是 ( )
A? 电池工作时,锌失去电子
B? 电池正极电极反应式为:
2MnO2?s?+H2O?l?+2e?=Mn2O3?s?+2OH??aq?
C? 电池工作时,电子由正极通过外电路流向负极
D? 外电路中每通过0?2 mol电子,锌的质量理论上减少6?5 g C练习1: 练习2:市场上经常见到的标记为Li-ion的电池称为“锂离子电池”。它的负极材料是金属锂和碳的复合材料(碳作为金属锂的载体),电解质为一种能传导Li+的高分子材料。这种锂离子电池的电池反应为:
Li+2Li0.35NiO2 2Li0.85NiO2????
放电充电下列说法不正确的是 ( )
A.放电时,负极的电极反应式:Li-e?=Li+
B.充电时,Li0.85NiO2既发生氧化反应又发生还原反应
C.该电池不能用水溶液作为电解质
D.放电过程中Li+向负极移动
