第二节《铝 金属材料》课件 (共35张PPT)
文档属性
| 名称 | 第二节《铝 金属材料》课件 (共35张PPT) |

|
|
| 格式 | zip | ||
| 文件大小 | 1.7MB | ||
| 资源类型 | 教案 | ||
| 版本资源 | 鲁科版 | ||
| 科目 | 化学 | ||
| 更新时间 | 2016-04-17 00:00:00 | ||
图片预览










文档简介
课件35张PPT。第二节 铝 金属材料
第 1 课时高中化学必修1:第四章第二节《铝 金属材料》课件联想·质疑金属单质的基本性质 我们已经学习过钠、镁、铁等金属单质的知识,
这些金属在性质上具有相似之处。 1、铝作为一种金属,它具有哪些性质?
2、铝是一种重要的金属材料,这可能与它 具有哪些性质有关?讨论1、铝的物理性质和相应用途易加工成各种形状,包装、装饰工艺,铝箔、铝丝、银粉涂料铝锅、铝壶等加热器具铝芯电线、电缆导热性能好导电性能较好(仅次于银、
铜和金)一、铝与铝合金金属 Al还原性例如:2Al + 3Cl2 == 2AlCl3
2Al+6H+=2Al3++3H2↑
2Al +3Cu2+=3Cu+2Al3+
2Al+3CuO==3Cu+Al2O3点燃思考探究:铝锅为什么可以用来煮饭?
不易被腐蚀?2、铝的化学性质用途:制燃烧弹、信号弹、火箭推进剂等铝在氧气中燃烧 实验 一、铝在氧气中燃烧剧烈燃烧,放出大量的热和耀眼的白光。常温下铝的表面被氧化,生
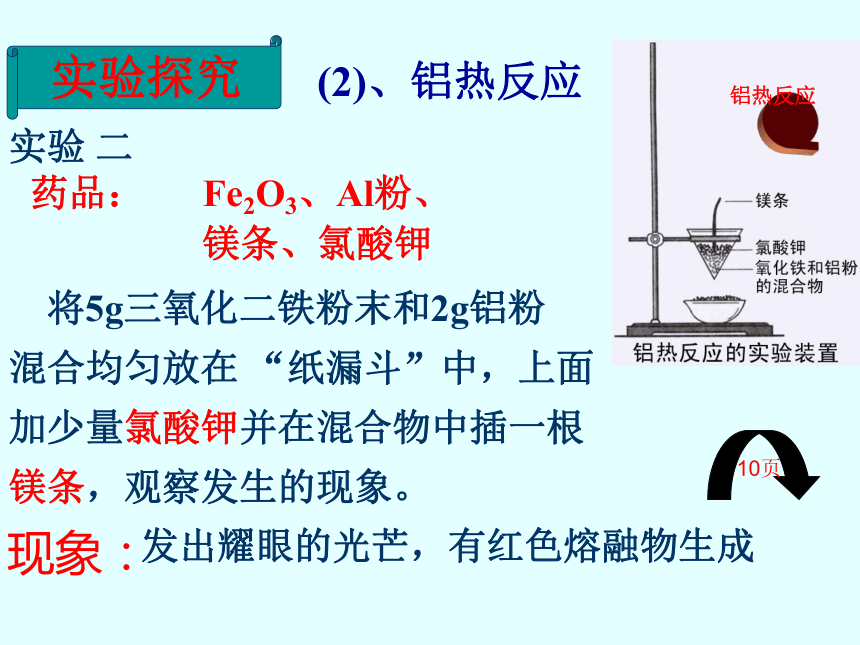
成一层致密氧化物薄膜。(1)、铝与非金属的反应因此铝具有抗腐蚀性。再如:2Al + 3S == Al2S3—铝表现出强的还原性点燃4Al+3O2==2Al2O3点燃实验探究实验 二现象:发出耀眼的光芒,有红色熔融物生成 将5g三氧化二铁粉末和2g铝粉
混合均匀放在 “纸漏斗”中,上面
加少量氯酸钾并在混合物中插一根
镁条,观察发生的现象。药品: Fe2O3、Al粉、
镁条、氯酸钾(2)、铝热反应铝热反应10页思考:问题探究1、引发此反应的操作是什么?
2、镁条、氯酸钾在这个反应中起
什么作用?
3、该反应的条件是什么?
4、此反应是放热反应还是吸热反应?
5、此反应属于什么反应类型?
6、铝和氧化镁是否反应?
7、铝热反应的用途?9页铝热反应的原理? Al在高温下表现出强还原性,把某些
金属从它的氧化物中置换出来。2Al + Fe2O3 == 2Fe + Al2O3铝热剂高温铝热反应用途
①冶炼难熔的金属 ②焊接钢轨
反应方程式:该反应叫铝热反应
写出Al与V2O5 、Cr2O3反应的化学方式。学以致用:铝是活泼金属,能与盐酸、稀硫酸等反应例如:3、铝与酸溶液反应4、铝与碱溶液反应2Al+2NaOH+6H2O==2 Na[ Al(OH)4 ] +3H2↑四羟基合铝酸钠o铝与氢氧化钠溶液反应注:铝在冷的浓硫酸、浓硝酸中发生钝化(5)与盐溶液反应 根据金属活动性顺序的应用,铝能把排在它后面的金属从它们的盐溶液中置换出来,如:2Al+3CuSO4 =3Cu+Al2(SO4)32Al+3Cu2+=3Cu+2Al3+【学用结合】:写出下列离子反应的离子方程式:
①铝丝与稀硫酸反应:
②铝片与氢氧化钠溶液反应:
2Al+6H+=2Al3++3H2↑2Al+2OHˉ+6H2O=2 [Al(OH)4] ˉ+ 3H2↑问题探究1、为什么铝制餐具不宜蒸煮或长期存放有酸性或碱性的食物? 2、Al与氨水反应能生成H2吗?Al能与酸或碱起反应不能! Al与强碱反应才能生成H2 ! 某课外活动小组做如下实验:往一铝制易拉罐内充满CO2,然后往罐内注入足量的NaOH溶液,立即用胶布严封罐口,过一段时间后,发现罐内凹而瘪,再过一段时间后,瘪了的罐壁重新鼓起,试解释:1、罐壁内凹而瘪的原因是 ,化学方程式为 .
罐壁再鼓起的原因是 ,
化学方程式为 . 2、如果用金属薄铁制易拉罐做上述实验,
出现的结果是 . 随堂练习CO2+2NaOH==Na2CO3+H2O2Al+6H2O+2NaOH==2 Na[Al(OH)4 ] +3H2↑CO2溶于与NaOH溶液,压强减小铝与与NaOH溶液反应生成H2,压强增大罐变瘪后不会再鼓起知识小结第2节铝 金属材料第2课时产生白色
胶状沉淀白色胶状
沉淀溶解白色胶状
沉淀溶解氢氧化铝溶于盐酸氢氧化铝溶于
氢氧化钠溶液可溶性铝盐遇碱
生成Al(OH)3沉淀。 3、氢氧化铝的性质氢氧化铝的性质实验结论:Al(OH) 3——即溶于盐酸又溶于氢氧化钠
溶液属于两性氢氧化物 既能与强酸反应,
又能与强碱反应的氢氧化物。
例:Al(OH) 3 ⑵Al(OH) 3物理性质及用途:不溶于水的白色胶状物,
有吸附性,可作净水剂。Al(OH)3 +3H+=2Al3++3H2O
Al(OH)3 +OH-=[Al (OH) 4]-四羟基合铝酸根离子⑴两性氢氧化物:⑶Al(OH) 3制取方法:用铝盐溶液与氨水反应!Al3+ +3 NH 3 · H2O =Al(OH) 3 ↓+ 3 NH 4+思考:实验室为何不用可溶性铝盐与
氢氧化钠溶液反应制取氢氧化铝?氢氧化铝会溶于过量的氢氧化钠溶液!Al(OH)3 +NaOH=Na[Al (OH) 4]4、Al2O3性质Al2O3 +6H+=2Al3++3H2O
Al2O3 +2OH- +3H2O = 2[Al (OH) 4] -氧化铝的性质实验白色固
体溶解白色固
体溶解氧化铝溶于盐酸氧化铝跟氢氧化钠溶液结论:氧化铝即溶于盐酸又溶于氢氧
化钠溶液属于两性氧化物两性氧化物:即能与强酸反应,又能与
强碱反应的氧化物。 例Al2O3
桌面上有两堆白色粉末,已知它们分别是Al2O3和MgO,你能用什么方法加以鉴别? 你能写出相关的化学反应方程式吗?Al2O3+2NaOH+3H2O=2Na[Al(OH)4] 即学即练1.合金:由两种或两种以上金属(或金属与非金属)
熔合而成的具有金属特性的物质。例:钢
2.合金的特性:
①合金的硬度一般比它各成分金属的硬度大;
②合金的熔点一般比它的各成分金属的熔点低;
③合金性质并不是各成分物质性质的总和,
合金的性能一般优于纯金属。(二).铝合金及其制品(自学了解)回忆初中相关知识:阅读课本:了解铝合金及其制品的性质和用途?铝散热器铝合金及其制品 1、下列物质中不属于合金的是( )
A.不锈钢 B.黄铜
C.碳素钢 D.铜绿
2、有关合金的性质叙述不正确的是( )
A.合金的熔点比它的各成分的熔点低
B.合金一定是金属熔合而成
C.合金的硬度和强度一般比纯金属高
D.硬铝、青铜、硅钢均为合金学学练练√√二、金属与金属材料(自学知识)黑色金属材料:
有色金属材料:铁、铬、锰以及它们的
合金构成的材料。除黑色金属(铁、铬、锰)
以外的其他金属材料。阅读课本:
了解重要的黑色金属材料——钢铁的
性质和用途? 1.重要的黑色金属材料——钢铁 钢铁的制备:
铁矿石→生铁→普通钢→特种钢生铁
[含较多的
C等杂质]思考:⑴钢中加入铬镍用途?
⑵不锈钢的性质和用途?
不锈钢加入铬镍钢铁钢筋混疑土弹簧片
(硅、锰钢)医疗器械
(不锈钢)车轴、履带
(钨钢、锰钢)钢铁的用途: 柔软的,黄色的金
质地柔软的,银白色的银
硬度较小的,紫红色的铜 金银铜 2.几种有色金属材料——金、银、铜 (1)金、银、铜的性质(均不活泼)
①金属光泽:Au——黄色;
Ag——银白色;
Cu——紫红色。
②延展性:Au >Ag>Cu
③传热性:Ag>Cu>Au
④导电性:Ag>Cu>Au
⑤化学活动性:Cu>Ag>Au 2 Cu +O2 +H2O +CO2 ===Cu2(OH)2CO3
碱式碳酸铜(铜绿)(2)铜及铜的化合物的转化黑色红色蓝色白色②在加热或点燃条件下,同能与许多非金属反应。加热加热 ①铜的弱还原性:在潮湿的空气中会锈蚀。③铜及其化合物的转化(3)金、银、铜及其合金的应用 Au货币电子元件航空、航天装饰品Ag货币催化剂化学电源装饰品牙科材料
第 1 课时高中化学必修1:第四章第二节《铝 金属材料》课件联想·质疑金属单质的基本性质 我们已经学习过钠、镁、铁等金属单质的知识,
这些金属在性质上具有相似之处。 1、铝作为一种金属,它具有哪些性质?
2、铝是一种重要的金属材料,这可能与它 具有哪些性质有关?讨论1、铝的物理性质和相应用途易加工成各种形状,包装、装饰工艺,铝箔、铝丝、银粉涂料铝锅、铝壶等加热器具铝芯电线、电缆导热性能好导电性能较好(仅次于银、
铜和金)一、铝与铝合金金属 Al还原性例如:2Al + 3Cl2 == 2AlCl3
2Al+6H+=2Al3++3H2↑
2Al +3Cu2+=3Cu+2Al3+
2Al+3CuO==3Cu+Al2O3点燃思考探究:铝锅为什么可以用来煮饭?
不易被腐蚀?2、铝的化学性质用途:制燃烧弹、信号弹、火箭推进剂等铝在氧气中燃烧 实验 一、铝在氧气中燃烧剧烈燃烧,放出大量的热和耀眼的白光。常温下铝的表面被氧化,生
成一层致密氧化物薄膜。(1)、铝与非金属的反应因此铝具有抗腐蚀性。再如:2Al + 3S == Al2S3—铝表现出强的还原性点燃4Al+3O2==2Al2O3点燃实验探究实验 二现象:发出耀眼的光芒,有红色熔融物生成 将5g三氧化二铁粉末和2g铝粉
混合均匀放在 “纸漏斗”中,上面
加少量氯酸钾并在混合物中插一根
镁条,观察发生的现象。药品: Fe2O3、Al粉、
镁条、氯酸钾(2)、铝热反应铝热反应10页思考:问题探究1、引发此反应的操作是什么?
2、镁条、氯酸钾在这个反应中起
什么作用?
3、该反应的条件是什么?
4、此反应是放热反应还是吸热反应?
5、此反应属于什么反应类型?
6、铝和氧化镁是否反应?
7、铝热反应的用途?9页铝热反应的原理? Al在高温下表现出强还原性,把某些
金属从它的氧化物中置换出来。2Al + Fe2O3 == 2Fe + Al2O3铝热剂高温铝热反应用途
①冶炼难熔的金属 ②焊接钢轨
反应方程式:该反应叫铝热反应
写出Al与V2O5 、Cr2O3反应的化学方式。学以致用:铝是活泼金属,能与盐酸、稀硫酸等反应例如:3、铝与酸溶液反应4、铝与碱溶液反应2Al+2NaOH+6H2O==2 Na[ Al(OH)4 ] +3H2↑四羟基合铝酸钠o铝与氢氧化钠溶液反应注:铝在冷的浓硫酸、浓硝酸中发生钝化(5)与盐溶液反应 根据金属活动性顺序的应用,铝能把排在它后面的金属从它们的盐溶液中置换出来,如:2Al+3CuSO4 =3Cu+Al2(SO4)32Al+3Cu2+=3Cu+2Al3+【学用结合】:写出下列离子反应的离子方程式:
①铝丝与稀硫酸反应:
②铝片与氢氧化钠溶液反应:
2Al+6H+=2Al3++3H2↑2Al+2OHˉ+6H2O=2 [Al(OH)4] ˉ+ 3H2↑问题探究1、为什么铝制餐具不宜蒸煮或长期存放有酸性或碱性的食物? 2、Al与氨水反应能生成H2吗?Al能与酸或碱起反应不能! Al与强碱反应才能生成H2 ! 某课外活动小组做如下实验:往一铝制易拉罐内充满CO2,然后往罐内注入足量的NaOH溶液,立即用胶布严封罐口,过一段时间后,发现罐内凹而瘪,再过一段时间后,瘪了的罐壁重新鼓起,试解释:1、罐壁内凹而瘪的原因是 ,化学方程式为 .
罐壁再鼓起的原因是 ,
化学方程式为 . 2、如果用金属薄铁制易拉罐做上述实验,
出现的结果是 . 随堂练习CO2+2NaOH==Na2CO3+H2O2Al+6H2O+2NaOH==2 Na[Al(OH)4 ] +3H2↑CO2溶于与NaOH溶液,压强减小铝与与NaOH溶液反应生成H2,压强增大罐变瘪后不会再鼓起知识小结第2节铝 金属材料第2课时产生白色
胶状沉淀白色胶状
沉淀溶解白色胶状
沉淀溶解氢氧化铝溶于盐酸氢氧化铝溶于
氢氧化钠溶液可溶性铝盐遇碱
生成Al(OH)3沉淀。 3、氢氧化铝的性质氢氧化铝的性质实验结论:Al(OH) 3——即溶于盐酸又溶于氢氧化钠
溶液属于两性氢氧化物 既能与强酸反应,
又能与强碱反应的氢氧化物。
例:Al(OH) 3 ⑵Al(OH) 3物理性质及用途:不溶于水的白色胶状物,
有吸附性,可作净水剂。Al(OH)3 +3H+=2Al3++3H2O
Al(OH)3 +OH-=[Al (OH) 4]-四羟基合铝酸根离子⑴两性氢氧化物:⑶Al(OH) 3制取方法:用铝盐溶液与氨水反应!Al3+ +3 NH 3 · H2O =Al(OH) 3 ↓+ 3 NH 4+思考:实验室为何不用可溶性铝盐与
氢氧化钠溶液反应制取氢氧化铝?氢氧化铝会溶于过量的氢氧化钠溶液!Al(OH)3 +NaOH=Na[Al (OH) 4]4、Al2O3性质Al2O3 +6H+=2Al3++3H2O
Al2O3 +2OH- +3H2O = 2[Al (OH) 4] -氧化铝的性质实验白色固
体溶解白色固
体溶解氧化铝溶于盐酸氧化铝跟氢氧化钠溶液结论:氧化铝即溶于盐酸又溶于氢氧
化钠溶液属于两性氧化物两性氧化物:即能与强酸反应,又能与
强碱反应的氧化物。 例Al2O3
桌面上有两堆白色粉末,已知它们分别是Al2O3和MgO,你能用什么方法加以鉴别? 你能写出相关的化学反应方程式吗?Al2O3+2NaOH+3H2O=2Na[Al(OH)4] 即学即练1.合金:由两种或两种以上金属(或金属与非金属)
熔合而成的具有金属特性的物质。例:钢
2.合金的特性:
①合金的硬度一般比它各成分金属的硬度大;
②合金的熔点一般比它的各成分金属的熔点低;
③合金性质并不是各成分物质性质的总和,
合金的性能一般优于纯金属。(二).铝合金及其制品(自学了解)回忆初中相关知识:阅读课本:了解铝合金及其制品的性质和用途?铝散热器铝合金及其制品 1、下列物质中不属于合金的是( )
A.不锈钢 B.黄铜
C.碳素钢 D.铜绿
2、有关合金的性质叙述不正确的是( )
A.合金的熔点比它的各成分的熔点低
B.合金一定是金属熔合而成
C.合金的硬度和强度一般比纯金属高
D.硬铝、青铜、硅钢均为合金学学练练√√二、金属与金属材料(自学知识)黑色金属材料:
有色金属材料:铁、铬、锰以及它们的
合金构成的材料。除黑色金属(铁、铬、锰)
以外的其他金属材料。阅读课本:
了解重要的黑色金属材料——钢铁的
性质和用途? 1.重要的黑色金属材料——钢铁 钢铁的制备:
铁矿石→生铁→普通钢→特种钢生铁
[含较多的
C等杂质]思考:⑴钢中加入铬镍用途?
⑵不锈钢的性质和用途?
不锈钢加入铬镍钢铁钢筋混疑土弹簧片
(硅、锰钢)医疗器械
(不锈钢)车轴、履带
(钨钢、锰钢)钢铁的用途: 柔软的,黄色的金
质地柔软的,银白色的银
硬度较小的,紫红色的铜 金银铜 2.几种有色金属材料——金、银、铜 (1)金、银、铜的性质(均不活泼)
①金属光泽:Au——黄色;
Ag——银白色;
Cu——紫红色。
②延展性:Au >Ag>Cu
③传热性:Ag>Cu>Au
④导电性:Ag>Cu>Au
⑤化学活动性:Cu>Ag>Au 2 Cu +O2 +H2O +CO2 ===Cu2(OH)2CO3
碱式碳酸铜(铜绿)(2)铜及铜的化合物的转化黑色红色蓝色白色②在加热或点燃条件下,同能与许多非金属反应。加热加热 ①铜的弱还原性:在潮湿的空气中会锈蚀。③铜及其化合物的转化(3)金、银、铜及其合金的应用 Au货币电子元件航空、航天装饰品Ag货币催化剂化学电源装饰品牙科材料
