四川省绵阳市平武县2024-2025学年九年级(上)期末化学试卷(含答案)
文档属性
| 名称 | 四川省绵阳市平武县2024-2025学年九年级(上)期末化学试卷(含答案) |

|
|
| 格式 | docx | ||
| 文件大小 | 159.2KB | ||
| 资源类型 | 教案 | ||
| 版本资源 | 人教版 | ||
| 科目 | 化学 | ||
| 更新时间 | 2025-01-11 00:00:00 | ||
图片预览




文档简介
四川省绵阳市平武县2024-2025学年九年级(上)期末化学试卷
第I卷(选择题)
一、单选题:本大题共20小题,共40分。
1.环戊烷是一种新型发泡剂,可以替代氟利昂作为冰箱制冷剂。环戊烷的下列性质属于化学性质的是( )
A. 无色透明的液体 B. 不溶于水,能溶于乙醇
C. 有刺激性气味 D. 易燃烧
2.下列四种物质中,属于纯净物的是( )
A. 澄清的石灰水 B. 冰水混合物 C. 食盐水 D. 洁净的空气
3.年月日是第个世界环境日。我国环境日主题是“全面推进美丽中国建设”。下列做法不符合这一理念的是( )
A. 推广使用新能源汽车,减少汽车尾气的排放
B. 发展废旧电池回收技术,促进资源循环利用
C. 工业废水直接灌溉农田,重复利用水资源
D. 提升石油化工水平,实现绿色低碳转型
4.如图的简易净水器中,主要起到吸附作用的是( )
A. 小卵石 B. 石英砂 C. 活性炭 D. 蓬松棉
5.安全重于泰山。下表列出了常见的三种可燃性气体的爆炸极限。据此判断,下列说法正确的是 ( )
可燃性气体
爆炸极限体积分数
A. 可燃性气体在爆炸极限范围内,一定会爆炸
B. 使用比其他两种气体更安全
C. 验纯后的可燃性气体一定是纯净物
D. 和混合一定会爆炸
6.在日常生活中我们常接触到许多含氮的物质,如:、、、、、、、,则这八种物质中氮元素显示的化合价共有( )
A. 种 B. 种 C. 种 D. 种
7.用分子、原子的观点分析下列生活中的现象,其解释不合理的是( )
A. 水与酒精混合后,总体积小于--分子之间有间隔
B. 八月桂花香--分子在不断运动
C. 滴水中约含个水分子--分子很小
D. 水电解--分子不会发变成其他分子
8.有关氧气性质的实验现象中,描述错误的是( )
A. 木炭在氧气中燃烧,发出白光
B. 铁丝在氧气中燃烧,火星四射,生成黑色固体
C. 红磷在氧气中燃烧,产生大量白烟
D. 硫在氧气中燃烧,生成二氧化硫气体
9.下列化学符号中数字表示的意义正确的是( )
A. :“”表示一个二氧化硫分子含有两个氧原子
B. :“”表示两个镁元素
C. :“”表示钙离子带有两个单位正电荷
D. :“”表示氧元素的化合价为负二价
10.“碳海绵”是已知最轻的固体材料,其结构类似海绵,密度仅为,其主要成分是石墨烯和碳纳米管两种碳单质。下列关于“碳海绵”的推测不正确的是( )
A. 碳海绵常温下化学性质稳定 B. 碳海绵具有吸附性
C. 碳海绵没有可燃性 D. 碳海绵能浮在水面上
11.芯片可存储大量信息,如图是其中含有的某元素在元素周期表中的部分信息,下列关于该元素的说法中错误的是( )
A. 该元素的名称是硅 B. 该元素的原子核内有个质子
C. 该元素的一个原子的质量为 D. 该元素的原子核外有个电子
12.运用推理、归纳、类比、对比的方法得出下列结论,其中合理的是( )
A. 铝的金属活动性比铁强,则铝制品比铁制品更容易锈蚀
B. 同种元素的粒子具有相同的质子数,所以具有相同质子数的粒子一定属于同种元素
C. 同温下分解氯酸钾,加催化剂的反应速率快,说明催化剂可以改变反应速率
D. 、、最外层电子数均为,由此得出离子的最外层电子数均为
13.“归纳与比较”是化学学习的主要方法,下列关于与的不同点比较错误的是( )
A. 组成:一个二氧化碳分子比一个一氧化碳分子多一个氧原子
B. 性质:能溶于水,水溶液呈酸性;难溶于水,但能燃烧
C. 用途:可用于光合作用、灭火等;可作气体燃料,还可用于人工降雨
D. 危害:会造成“温室效应”;使用不当容易引起爆炸
14.下列燃料燃烧时,能实现二氧化碳零排放的是( )
A. 氢气 B. 柴草 C. 煤 D. 汽油
15.深海鱼油中的化学式为是一种特殊的不饱和脂肪酸,这种不饱和脂肪酸是大脑细胞形成、发育及运作不可缺少的物质基础。下列关于相关说法中正确的是( )
A. 属于氧化物
B. 中、、三种元素的质量比为::
C. 的相对分子质量为
D. 中氢元素和氧元素的质量分数相等
16.人工光合固碳装置通过电化学手段将二氧化碳转化为甲酸,该反应的微观示意图如图,下列说法正确的是 ( )
A. 反应过程中,分子种类未改变
B. 参加反应的两种物质的微粒个数比为:
C. 该反应有助于实现“碳中和”
D. 甲酸中碳元素和氢元素的质量比为:
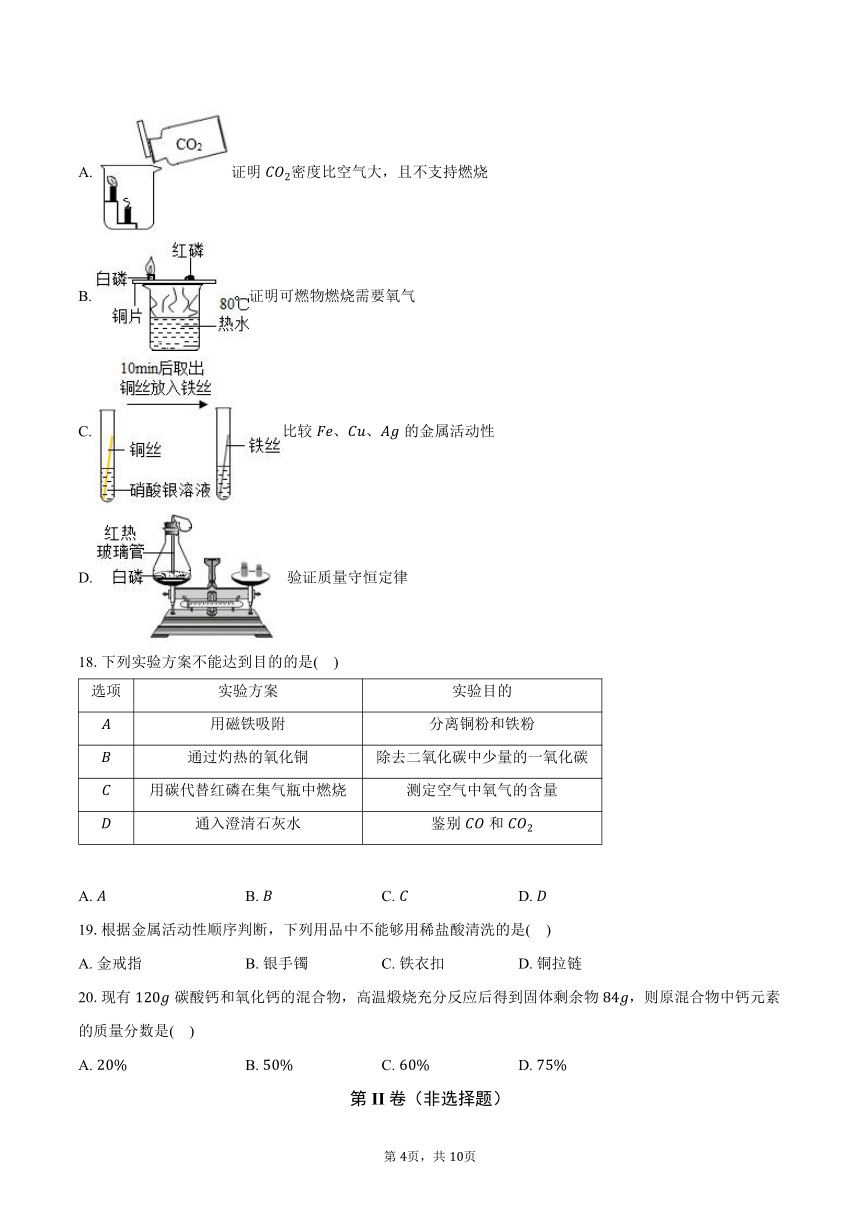
17.下列方案不能达到实验目的是( )
A. 证明密度比空气大,且不支持燃烧
B. 证明可燃物燃烧需要氧气
C. 比较、、的金属活动性
D. 验证质量守恒定律
18.下列实验方案不能达到目的的是( )
选项 实验方案 实验目的
用磁铁吸附 分离铜粉和铁粉
通过灼热的氧化铜 除去二氧化碳中少量的一氧化碳
用碳代替红磷在集气瓶中燃烧 测定空气中氧气的含量
通入澄清石灰水 鉴别和
A. B. C. D.
19.根据金属活动性顺序判断,下列用品中不能够用稀盐酸清洗的是( )
A. 金戒指 B. 银手镯 C. 铁衣扣 D. 铜拉链
20.现有碳酸钙和氧化钙的混合物,高温煅烧充分反应后得到固体剩余物,则原混合物中钙元素的质量分数是( )
A. B. C. D.
第II卷(非选择题)
二、填空题:本大题共3小题,共16分。
21.写出符合下列要求的化学符号。
保持氮气化学性质的最小粒子 ______ 。
两个锌离子 ______ 。
个钙原子 ______ 。
个五氧化二磷分子 ______ 。
氯化亚铁 ______ 。
22.火是人类文明的起源,水是人类生命之源。
取火有“术”:在汽油中添加乙醇可有效减缓石油危机,乙醇是一种 ______ 填“可”或“不可”再生能源。
防火有“法”:油锅起火时切记不要使用水来扑灭,灭火的有效方法之一是盖上锅盖,其灭火原理是 ______ 。
水之净:活性炭可以有效除去水中的色素和异味,是因为活性炭具有 ______ 性。
水之变:实验室常用电石主要成分为和水反应制取乙炔气体,同时生成一种常见的碱,请写出化学方程式 ______ 。
23.现在空气污染已经越来越受到人们的关注,为了减缓空气污染:
我们倡导减少使用煤、石油、 ______ 等化石燃料,其中煤燃烧会产生大气污染物 ______ ,它们排放于空气中会造成酸雨。
使用乙醇汽油可以节约石油资源。乙醇是一种可再生燃料,请写出它在空气中完全燃烧的化学方程式 ______ 。氢气是最清洁的能源,实验室制取氢气的常用化学反应方程式是 ______ 。
三、流程题:本大题共2小题,共10分。
24.我国科研团队发现“嫦娥五号”取回的月壤中含催化活性物质,它们能实现水、二氧化碳的高效转化如图所示,一为初中化学常见的物质,常温下为无色气体。
物质的化学式为 ______ 。
反应的化学反应类型为 ______ 。
反应的化学方程式为 ______ 。
物质的用途有 ______ 。
25.“海绵城市”理念是将城市建设成具有吸水、蓄水、净水和释水功能的海绵体,提高城市防洪排涝减灾能力。图为海绵城市雨水排放示意图:
下列有关海绵城市建设和水资源利用正确的是 ______ 。
A.建设海绵城市可减少水的流失
B.大量开采和使用地下水
C.水体有自净能力,雨水和生活污水不分流可任意排放
天然降雨是硬水还是软水,可用 ______ 检验。
透水砖是海绵城市的“海绵体”,水下渗过程相当于化学实验室中的 ______ 操作。
分解水可以制得未来最有发展前途的清洁能源氢气。如图,以太阳能为热源,经由铁氧化合物催化,进行循环分解水制的过程,该过程总反应的化学方程式为 ______ 。
四、实验题:本大题共1小题,共13分。
26.如图所示是初中化学常用的实验装置,请回答下列问题。
写出有标号仪器的名称: ______ 。
若用氯酸钾制取一瓶较纯净的氧气应选择的装置组合是 ______ 填序号;若用高锰酸钾制取氧气也选该装置组合,发生装置还需如何改进 ______ ;写出用其中任一药品制氧气的化学方程式 ______ 。
如果用装置或来制取氧气,发生反应的化学方程式是 ______ ;装置和对比,用装置进行实验的优点是 ______ 。
实验室制取二氧化碳的发生装置为 ______ 填序号,发生反应的化学方程式为 ______ 。可用于收集二氧化碳,验满的方法是 ______ 。
用图装置验证二氧化碳的性质,观察到的现象是 ______ 。
五、探究题:本大题共1小题,共6分。
27.兴趣小组同学模仿工业高炉炼铁原理,用图实验装置加热装置已省略探究冶炼铜的化学原理。实验操作过程如下:
将加水制成糊状,用毛笔刷在试管内壁,烘干;然后在试管底部加入一定量的焦炭,再向试管里通入干燥的,此时用仪器测得含量为,用气球密封试管口。
用酒精灯加热试管中的氧化铜部位一段时间,无明显现象,随后熄灭酒精灯。
高温加热焦炭部位一段时间,停止加热,用热成像仪拍摄图中虚线框部位,数据输出得到图。恢复至与相同的条件测得含量为。
再次用酒精灯加热氧化铜部位,分钟左右黑色固体变成紫红色。
操作中将加水制成糊状,用毛笔刷在试管内壁的目的是 ______ 。
操作中含量减小的原因是 ______ 。
操作中的化学方程式为 ______ 。
实验结束后,一般将装置内的气体灼烧处理,目的是 ______ 。
由图可知,刚停止加热后焦炭区温度降低更快,可能的原因是 ______ 。
六、计算题:本大题共1小题,共15分。
28.实验室常用过氧化氢溶液与二氧化锰混合制取氧气,现将二氧化锰放入盛有过氧化氢溶液的锥形瓶中,完全反应后,放出气体的质量与反应时间的关系如图所示。
试求:
完全反应后生成的氧气的质量为 ______ 。
反应结束后,过滤、洗涤并烘干滤渣,称得滤渣的质量为 ______ 。
1.
2.
3.
4.
5.
6.
7.
8.
9.
10.
11.
12.
13.
14.
15.
16.
17.
18.
19.
20.
21.
22.可 隔绝空气或氧气 吸附
23.天然气 二氧化硫、二氧化氮
24. 分解反应 灭火
25. 肥皂水 过滤
26.分液漏斗 试管口放一团棉花 或 可以控制反应的速率 或 把燃着的木条放在管口,木条熄灭,证明二氧化碳满了 下面的蜡烛先熄灭,上面的蜡烛后熄灭
27.增加接触面积,使反应更快更充分 高温条件下二氧化碳和碳发生反应 防止一氧化碳污染环境 焦炭和二氧化碳的反应为吸热反应
28.
第9页,共10页
第I卷(选择题)
一、单选题:本大题共20小题,共40分。
1.环戊烷是一种新型发泡剂,可以替代氟利昂作为冰箱制冷剂。环戊烷的下列性质属于化学性质的是( )
A. 无色透明的液体 B. 不溶于水,能溶于乙醇
C. 有刺激性气味 D. 易燃烧
2.下列四种物质中,属于纯净物的是( )
A. 澄清的石灰水 B. 冰水混合物 C. 食盐水 D. 洁净的空气
3.年月日是第个世界环境日。我国环境日主题是“全面推进美丽中国建设”。下列做法不符合这一理念的是( )
A. 推广使用新能源汽车,减少汽车尾气的排放
B. 发展废旧电池回收技术,促进资源循环利用
C. 工业废水直接灌溉农田,重复利用水资源
D. 提升石油化工水平,实现绿色低碳转型
4.如图的简易净水器中,主要起到吸附作用的是( )
A. 小卵石 B. 石英砂 C. 活性炭 D. 蓬松棉
5.安全重于泰山。下表列出了常见的三种可燃性气体的爆炸极限。据此判断,下列说法正确的是 ( )
可燃性气体
爆炸极限体积分数
A. 可燃性气体在爆炸极限范围内,一定会爆炸
B. 使用比其他两种气体更安全
C. 验纯后的可燃性气体一定是纯净物
D. 和混合一定会爆炸
6.在日常生活中我们常接触到许多含氮的物质,如:、、、、、、、,则这八种物质中氮元素显示的化合价共有( )
A. 种 B. 种 C. 种 D. 种
7.用分子、原子的观点分析下列生活中的现象,其解释不合理的是( )
A. 水与酒精混合后,总体积小于--分子之间有间隔
B. 八月桂花香--分子在不断运动
C. 滴水中约含个水分子--分子很小
D. 水电解--分子不会发变成其他分子
8.有关氧气性质的实验现象中,描述错误的是( )
A. 木炭在氧气中燃烧,发出白光
B. 铁丝在氧气中燃烧,火星四射,生成黑色固体
C. 红磷在氧气中燃烧,产生大量白烟
D. 硫在氧气中燃烧,生成二氧化硫气体
9.下列化学符号中数字表示的意义正确的是( )
A. :“”表示一个二氧化硫分子含有两个氧原子
B. :“”表示两个镁元素
C. :“”表示钙离子带有两个单位正电荷
D. :“”表示氧元素的化合价为负二价
10.“碳海绵”是已知最轻的固体材料,其结构类似海绵,密度仅为,其主要成分是石墨烯和碳纳米管两种碳单质。下列关于“碳海绵”的推测不正确的是( )
A. 碳海绵常温下化学性质稳定 B. 碳海绵具有吸附性
C. 碳海绵没有可燃性 D. 碳海绵能浮在水面上
11.芯片可存储大量信息,如图是其中含有的某元素在元素周期表中的部分信息,下列关于该元素的说法中错误的是( )
A. 该元素的名称是硅 B. 该元素的原子核内有个质子
C. 该元素的一个原子的质量为 D. 该元素的原子核外有个电子
12.运用推理、归纳、类比、对比的方法得出下列结论,其中合理的是( )
A. 铝的金属活动性比铁强,则铝制品比铁制品更容易锈蚀
B. 同种元素的粒子具有相同的质子数,所以具有相同质子数的粒子一定属于同种元素
C. 同温下分解氯酸钾,加催化剂的反应速率快,说明催化剂可以改变反应速率
D. 、、最外层电子数均为,由此得出离子的最外层电子数均为
13.“归纳与比较”是化学学习的主要方法,下列关于与的不同点比较错误的是( )
A. 组成:一个二氧化碳分子比一个一氧化碳分子多一个氧原子
B. 性质:能溶于水,水溶液呈酸性;难溶于水,但能燃烧
C. 用途:可用于光合作用、灭火等;可作气体燃料,还可用于人工降雨
D. 危害:会造成“温室效应”;使用不当容易引起爆炸
14.下列燃料燃烧时,能实现二氧化碳零排放的是( )
A. 氢气 B. 柴草 C. 煤 D. 汽油
15.深海鱼油中的化学式为是一种特殊的不饱和脂肪酸,这种不饱和脂肪酸是大脑细胞形成、发育及运作不可缺少的物质基础。下列关于相关说法中正确的是( )
A. 属于氧化物
B. 中、、三种元素的质量比为::
C. 的相对分子质量为
D. 中氢元素和氧元素的质量分数相等
16.人工光合固碳装置通过电化学手段将二氧化碳转化为甲酸,该反应的微观示意图如图,下列说法正确的是 ( )
A. 反应过程中,分子种类未改变
B. 参加反应的两种物质的微粒个数比为:
C. 该反应有助于实现“碳中和”
D. 甲酸中碳元素和氢元素的质量比为:
17.下列方案不能达到实验目的是( )
A. 证明密度比空气大,且不支持燃烧
B. 证明可燃物燃烧需要氧气
C. 比较、、的金属活动性
D. 验证质量守恒定律
18.下列实验方案不能达到目的的是( )
选项 实验方案 实验目的
用磁铁吸附 分离铜粉和铁粉
通过灼热的氧化铜 除去二氧化碳中少量的一氧化碳
用碳代替红磷在集气瓶中燃烧 测定空气中氧气的含量
通入澄清石灰水 鉴别和
A. B. C. D.
19.根据金属活动性顺序判断,下列用品中不能够用稀盐酸清洗的是( )
A. 金戒指 B. 银手镯 C. 铁衣扣 D. 铜拉链
20.现有碳酸钙和氧化钙的混合物,高温煅烧充分反应后得到固体剩余物,则原混合物中钙元素的质量分数是( )
A. B. C. D.
第II卷(非选择题)
二、填空题:本大题共3小题,共16分。
21.写出符合下列要求的化学符号。
保持氮气化学性质的最小粒子 ______ 。
两个锌离子 ______ 。
个钙原子 ______ 。
个五氧化二磷分子 ______ 。
氯化亚铁 ______ 。
22.火是人类文明的起源,水是人类生命之源。
取火有“术”:在汽油中添加乙醇可有效减缓石油危机,乙醇是一种 ______ 填“可”或“不可”再生能源。
防火有“法”:油锅起火时切记不要使用水来扑灭,灭火的有效方法之一是盖上锅盖,其灭火原理是 ______ 。
水之净:活性炭可以有效除去水中的色素和异味,是因为活性炭具有 ______ 性。
水之变:实验室常用电石主要成分为和水反应制取乙炔气体,同时生成一种常见的碱,请写出化学方程式 ______ 。
23.现在空气污染已经越来越受到人们的关注,为了减缓空气污染:
我们倡导减少使用煤、石油、 ______ 等化石燃料,其中煤燃烧会产生大气污染物 ______ ,它们排放于空气中会造成酸雨。
使用乙醇汽油可以节约石油资源。乙醇是一种可再生燃料,请写出它在空气中完全燃烧的化学方程式 ______ 。氢气是最清洁的能源,实验室制取氢气的常用化学反应方程式是 ______ 。
三、流程题:本大题共2小题,共10分。
24.我国科研团队发现“嫦娥五号”取回的月壤中含催化活性物质,它们能实现水、二氧化碳的高效转化如图所示,一为初中化学常见的物质,常温下为无色气体。
物质的化学式为 ______ 。
反应的化学反应类型为 ______ 。
反应的化学方程式为 ______ 。
物质的用途有 ______ 。
25.“海绵城市”理念是将城市建设成具有吸水、蓄水、净水和释水功能的海绵体,提高城市防洪排涝减灾能力。图为海绵城市雨水排放示意图:
下列有关海绵城市建设和水资源利用正确的是 ______ 。
A.建设海绵城市可减少水的流失
B.大量开采和使用地下水
C.水体有自净能力,雨水和生活污水不分流可任意排放
天然降雨是硬水还是软水,可用 ______ 检验。
透水砖是海绵城市的“海绵体”,水下渗过程相当于化学实验室中的 ______ 操作。
分解水可以制得未来最有发展前途的清洁能源氢气。如图,以太阳能为热源,经由铁氧化合物催化,进行循环分解水制的过程,该过程总反应的化学方程式为 ______ 。
四、实验题:本大题共1小题,共13分。
26.如图所示是初中化学常用的实验装置,请回答下列问题。
写出有标号仪器的名称: ______ 。
若用氯酸钾制取一瓶较纯净的氧气应选择的装置组合是 ______ 填序号;若用高锰酸钾制取氧气也选该装置组合,发生装置还需如何改进 ______ ;写出用其中任一药品制氧气的化学方程式 ______ 。
如果用装置或来制取氧气,发生反应的化学方程式是 ______ ;装置和对比,用装置进行实验的优点是 ______ 。
实验室制取二氧化碳的发生装置为 ______ 填序号,发生反应的化学方程式为 ______ 。可用于收集二氧化碳,验满的方法是 ______ 。
用图装置验证二氧化碳的性质,观察到的现象是 ______ 。
五、探究题:本大题共1小题,共6分。
27.兴趣小组同学模仿工业高炉炼铁原理,用图实验装置加热装置已省略探究冶炼铜的化学原理。实验操作过程如下:
将加水制成糊状,用毛笔刷在试管内壁,烘干;然后在试管底部加入一定量的焦炭,再向试管里通入干燥的,此时用仪器测得含量为,用气球密封试管口。
用酒精灯加热试管中的氧化铜部位一段时间,无明显现象,随后熄灭酒精灯。
高温加热焦炭部位一段时间,停止加热,用热成像仪拍摄图中虚线框部位,数据输出得到图。恢复至与相同的条件测得含量为。
再次用酒精灯加热氧化铜部位,分钟左右黑色固体变成紫红色。
操作中将加水制成糊状,用毛笔刷在试管内壁的目的是 ______ 。
操作中含量减小的原因是 ______ 。
操作中的化学方程式为 ______ 。
实验结束后,一般将装置内的气体灼烧处理,目的是 ______ 。
由图可知,刚停止加热后焦炭区温度降低更快,可能的原因是 ______ 。
六、计算题:本大题共1小题,共15分。
28.实验室常用过氧化氢溶液与二氧化锰混合制取氧气,现将二氧化锰放入盛有过氧化氢溶液的锥形瓶中,完全反应后,放出气体的质量与反应时间的关系如图所示。
试求:
完全反应后生成的氧气的质量为 ______ 。
反应结束后,过滤、洗涤并烘干滤渣,称得滤渣的质量为 ______ 。
1.
2.
3.
4.
5.
6.
7.
8.
9.
10.
11.
12.
13.
14.
15.
16.
17.
18.
19.
20.
21.
22.可 隔绝空气或氧气 吸附
23.天然气 二氧化硫、二氧化氮
24. 分解反应 灭火
25. 肥皂水 过滤
26.分液漏斗 试管口放一团棉花 或 可以控制反应的速率 或 把燃着的木条放在管口,木条熄灭,证明二氧化碳满了 下面的蜡烛先熄灭,上面的蜡烛后熄灭
27.增加接触面积,使反应更快更充分 高温条件下二氧化碳和碳发生反应 防止一氧化碳污染环境 焦炭和二氧化碳的反应为吸热反应
28.
第9页,共10页
同课章节目录
