北京市海淀区第二十中学2024-2025学年高一上学期期中考试化学试题(含答案)
文档属性
| 名称 | 北京市海淀区第二十中学2024-2025学年高一上学期期中考试化学试题(含答案) |  | |
| 格式 | docx | ||
| 文件大小 | 1.1MB | ||
| 资源类型 | 教案 | ||
| 版本资源 | 人教版(2019) | ||
| 科目 | 化学 | ||
| 更新时间 | 2025-01-15 19:08:23 | ||
图片预览




文档简介
北京市海淀区第二十中学2024-2025学年高一上学期期中考试化学试题
可能用到的相对原子质量:H-1,C-12,N-14,O-16,Na-23,Mg-24,S-32,C1-35.5,Ca-40,Fe-56,Cu-64,Zn-65,Ag-108,Ba-137
一、单选题:本大题共25小题,共75分。
1.人工智能在化学领域的应用正变得越来越广泛,尤其是在药物发现和材料科学中。我国在材料的开发和应用方面取得了举世瞩目的成就。下列属于金属材料的是
A.使用的碳纤维复合材料 B.盾构机钻头刀刃的硬质钨合金
C.浙大科学家用冰制作出的“冰光纤” D.卫星芯片使用的高纯硅
A.
A. B. C. D.
2.“酒香薰枕席,炉气暖轩除。岑参行军雪后月夜宴王卿家”诗人能闻到酒香的原因是
A. 分子很小 B. 分子在不断地运动 C. 分子之间有间隙 D. 分子是可分的
3.掌握好分类方法,可以帮助我们学习好化学,下列物质的分类不正确的是
A. 属于酸 B. 属于盐 C. 属于氧化物 D. 属于碱
4.下列物质的俗名与化学式对应关系正确的是
A. 干冰 B. 纯碱 C. 食盐 D. 烧碱
5.当光束通过下列分散系时,能观察到丁达尔效应的是
A. 盐酸 B. 食盐溶液 C. 氢氧化铁胶体 D. 碘的酒精溶液
6.下列关于金属钠的叙述中,说法正确的是
A. 少量的钠保存在酒精中 B. 钠的密度比水小
C. 钠是银白色金属,硬度大,熔点高 D. 钠着火时可以用泡末灭火剂扑灭
7.“纳米材料”是指微粒直径为几纳米到几十纳米的材料。据报道,科学家制造出了一种臂长只有纳米的纳米级镊子一种纳米材料,该镊子能够钳起分子或原子。下列说法正确的是
A. 该纳米级镊子钳起分子时发生了化学反应
B. 分子是化学反应中的最小微粒
C. 把该纳米级镊子分散到适当分散剂中可形成溶液
D. 把该纳米级镊子分散到适当分散剂中得到的混合物能产生丁达尔效应
8.下列叙述正确的是
A. 摩尔是七个基本物理量之一
B. 阿伏加德罗常数的符号为,近似为
C. 阿伏加德罗常数是中所含的碳原子数
D. 摩尔既是物质的量的单位,又是粒子数量的单位
9.下列有关气体摩尔体积的描述中正确的是
A. 在标准状况下,气体的摩尔体积约为
B. 在通常状况下,和所占的体积都约为
C. 单位物质的量的气体所占的体积就是气体摩尔体积
D. 相同物质的量的气体的气体摩尔体积相同
10.用表示阿伏加德罗常数的值,下列叙述中正确的是
A. 通常状况下,与的混合物所含氧原子数目一定为
B. 标准状况下,含有的分子数为
C. 的硫酸溶液中,的物质的量为
D. 铁和足量的盐酸反应,失去电子的数目为
11.下列电离方程式错误的是
A. B.
C. D.
12.下列叙述中,正确的是
A. 固体不导电,所以不是电解质
B. 铜丝、石墨均能导电,所以它们都是电解质
C. 熔融的能导电,所以是电解质
D. 溶于水,在通电条件下才能发生电离
13.下列各组中的离子,能在溶液中大量共存的是
A. B.
C. 、、、 D.
14.下列离子方程式中,书写正确的是
A. 氢氧化镁溶于盐酸中:
B. 将铁片插入硫酸铜溶液中:
C. 硫酸溶液与氢氧化钡溶液反应:
D. 氢氧化钡溶液与硝酸的反应:
15.下列各组中两种物质在溶液中的反应,能用同一离子方程式表示的是
A. ;
B. ;
C. ;
D. ;
16.酒精检测仪中装有重铬酸钾,该化合物中铬元素的化合价为
A. B. C. D.
17.下列物质转化中,一定需要加入氧化剂才能实现的是
A. B. C. D.
18.具有强氧化性,可发生反应:,下列说法不正确的是
A. 既是氧化产物,又是还原产物
B. 还原剂为
C. 生成转移电子
D. 氧化产物和还原产物的物质的量之比为:
19.下列反应中,水作氧化剂的是
A. B.
C. D.
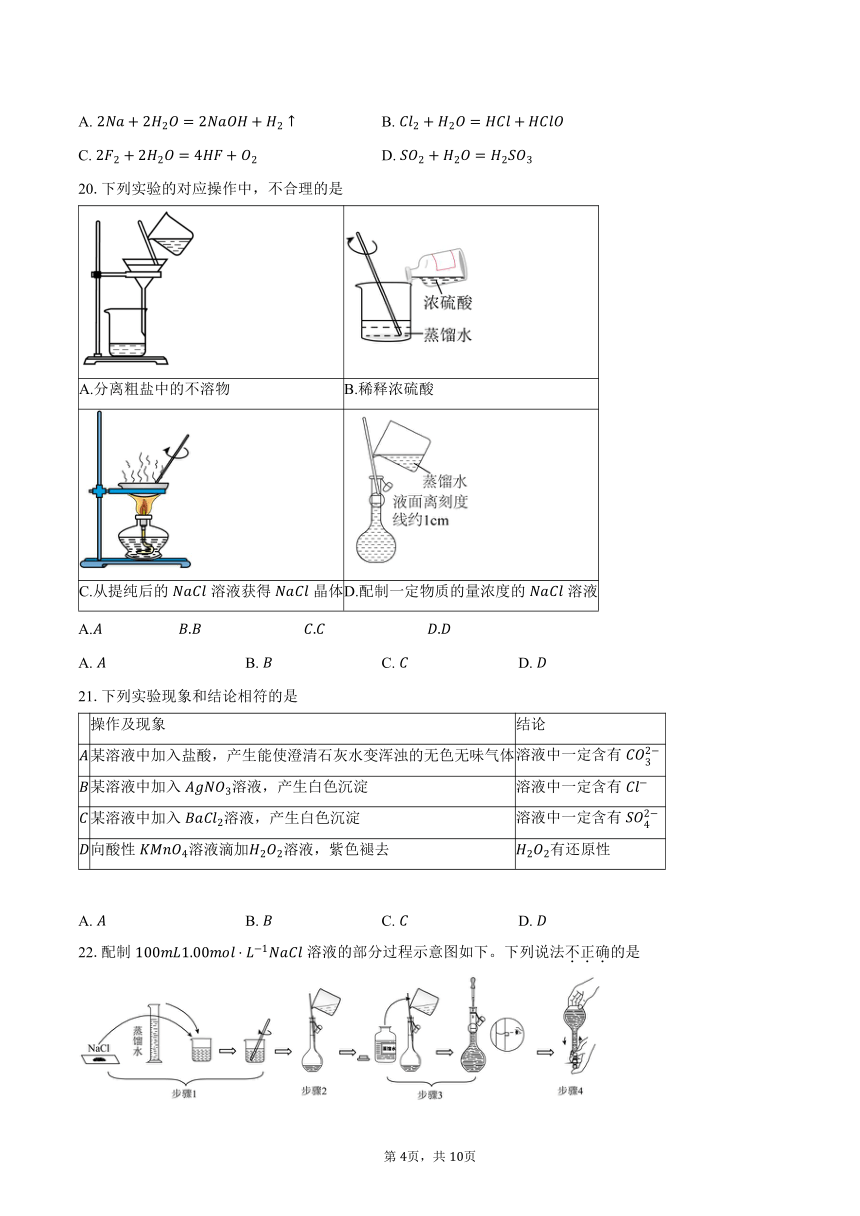
20.下列实验的对应操作中,不合理的是
A.分离粗盐中的不溶物 B.稀释浓硫酸
C.从提纯后的溶液获得晶体 D.配制一定物质的量浓度的溶液
A.
A. B. C. D.
21.下列实验现象和结论相符的是
操作及现象 结论
某溶液中加入盐酸,产生能使澄清石灰水变浑浊的无色无味气体 溶液中一定含有
某溶液中加入溶液,产生白色沉淀 溶液中一定含有
某溶液中加入溶液,产生白色沉淀 溶液中一定含有
向酸性溶液滴加溶液,紫色褪去 有还原性
A. B. C. D.
22.配制溶液的部分过程示意图如下。下列说法不正确的是
A. 步骤中用玻璃棒搅拌的目的是加快溶解
B. 步骤中需用少量蒸馏水洗涤烧杯内壁和玻璃棒次,并将洗涤液都注入容量瓶
C. 步骤中液面距容量瓶刻度线时,改用胶头滴管加蒸馏水至凹液面与刻度线相切
D. 步骤中摇匀后若容量瓶内液面下降,需加水至刻度线
23.气体与足量溶液完全反应后,再加入溶液,发生如下化学反应:
;
,
下列有关说法正确的是
A. 氧化性:
B. 若有参加反应,则最终消耗
C. 反应中,每有参加反应,转移电子的数目为
D. 由上述反应原理推断:不能将氧化成
24.在明代宋应星所著的天工开物中,有关火法炼锌的工艺记载:“每炉甘石炉甘石的主要成分是十斤,装载入一泥罐内,,然后逐层用煤炭饼垫盛,其底铺薪,发火煅红,罐中炉甘石熔化成团.”火法炼锌的反应为:,下列说法不正确的是
A. 的化学式是
B. 被氧化的物质是
C. 既是氧化剂又是还原剂
D. 参与反应,转移电子的物质的量为
25.某溶液可能由、、、、、、中的若干种离子组成。现取适量溶液进行如下实验:
根据以上实验判断,下列推断错误的是
A. 气体通入澄清石灰水中,溶液变浑浊
B. 滤液中加入碳酸钠溶液一定会产生沉淀
C. 原溶液中一定存在和 ,一定不存在
D. 白色沉淀中加稀硝酸,沉淀不溶解
二、填空题:本大题共5小题,共40分。
26.下表是生活生产中常见的物质:
编号
名称 酒精
请你对表中的物质进行分类填序号:属于电解质的是____;属于盐的是____。
写出电离方程式:的电离方程式是____;的电离方程式是____。
写出与在水溶液中反应的离子方程式:____。
27.物质的量是高中化学常用的物理量,请完成以下有关计算:回答下列问题:
的物质的量是____,含有____个质子。
中含____,____个。
某金属氯化物,含有,则该氯化物的摩尔质量为____。
标准状况中所含氢原子的数目为____。
分子中所含原子数与____分子中所含原子数相等,该气体在标准状况下的体积为____。
28.氧化还原反应是一类重要的反应,在工农业生产、日常生活中都有广泛的用途。请结合相关化学知识回答下列问题:
化工厂可用浓氨水来检验输送的管道是否泄漏。相关化学反应如下:
____________________
配平以上方程式____;
反应中被还原的物质是____填化学式。
可在野外作生氢剂,反应原理为,该反应中氧化产物和还原产物的质量比为____。
在汽车的排气管上装一个催化转化器,可有效降低氮氧化物的排放,其中一个反应为用单线桥法表示出电子转移的方向和数目:____。
根据反应,回答下列问题。
氧化剂与还原剂的分子数之比为____。
当有个参加反应时,转移的电子个数为____。
用双线桥的方法表示该反应的电子转移情况____。
29.为除去粗盐中的、、以及泥沙等杂质,某同学设计了一种制备精盐的实验方案,步骤如下用于沉淀的试剂稍过量:
请回答:
步骤需采用的主要物质分离提纯操作,名称是______,所需要的玻璃仪器除酒精灯、玻璃棒、烧杯外,还要______。
步骤加入过量的目的是______。
步骤需加入适量的___ 填试剂名称,所发生反应的化学方程式为_______。
30.A、、、为四种可溶性盐,它们的阳离子分别是、、、中的一种,阴离子分别是、、、中的一种离子在物质中不能重复出现。现做如下实验:
把四种盐分别溶于盛有蒸馏水的四支试管中,只有的溶液呈蓝色。
向的四支试管中分别加入盐酸,的溶液中有沉淀生成,的溶液中有无色无味的气体逸出。
根据实验现象回答下列问题:
写出、、的化学式:______,______,______。
写出盐酸与反应产生气体的离子方程式:______。
写出与溶液反应的离子方程式:______。
将含相同数目、、的溶液混合后,写出溶液中存在的离子______;在此溶液中加入锌粒,写出发生反应的离子方程式____。
三、简答题:本大题共1小题,共8分。
31.某化学研究小组在实验室中探究金属钠及其化合物的性质。
某同学夹取一块钠,用滤纸吸干后再切一小块放在如图所示装置上做钠的燃烧实验,反应的化学方程式为____。
该小组的同学将产生的固体投入水中,反应的方程式为:____。反应停止后,同学们观察到烧杯内有少许黑色固体物质,经检测为碳。
某同学分析碳可能是加热过程中钠与反应产生的,为此设计如下图所示装置进行验证。先取一块纯净的钠放入干燥的管中,然后打开的活塞,反应一段时间后,点燃处酒精灯。观察到钠剧烈燃烧,产生大量白烟,同时有黑色物质生成,冷却后有白色固体附着在管壁上。
中所盛试剂为饱和溶液,作用是____。若缺少装置,可能产生的影响是____用化学方程式表示。
中反应一段时间后,再点燃处酒精灯的目的是____。
装置中反应生成碳单质的化学方程式为____。
1.【答案】
2.【答案】
3.【答案】
4.【答案】
5.【答案】
6.【答案】
7.【答案】
8.【答案】
9.【答案】
10.【答案】
11.【答案】
12.【答案】
13.【答案】
14.【答案】
15.【答案】
16.【答案】
17.【答案】
18.【答案】
19.【答案】
20.【答案】
21.【答案】
22.【答案】
23.【答案】
24.【答案】
25.【答案】
26.【答案】
27.【答案】
28.【答案】
:
:
29.【答案】蒸发蒸发皿将溶液中的杂质离子钙离子以及多余的钡离子除去盐酸、
30.【答案】
31.【答案】
除去中的杂质 排除装置内的空气,防止钠与氧气反应 或
第2页,共10页
可能用到的相对原子质量:H-1,C-12,N-14,O-16,Na-23,Mg-24,S-32,C1-35.5,Ca-40,Fe-56,Cu-64,Zn-65,Ag-108,Ba-137
一、单选题:本大题共25小题,共75分。
1.人工智能在化学领域的应用正变得越来越广泛,尤其是在药物发现和材料科学中。我国在材料的开发和应用方面取得了举世瞩目的成就。下列属于金属材料的是
A.使用的碳纤维复合材料 B.盾构机钻头刀刃的硬质钨合金
C.浙大科学家用冰制作出的“冰光纤” D.卫星芯片使用的高纯硅
A.
A. B. C. D.
2.“酒香薰枕席,炉气暖轩除。岑参行军雪后月夜宴王卿家”诗人能闻到酒香的原因是
A. 分子很小 B. 分子在不断地运动 C. 分子之间有间隙 D. 分子是可分的
3.掌握好分类方法,可以帮助我们学习好化学,下列物质的分类不正确的是
A. 属于酸 B. 属于盐 C. 属于氧化物 D. 属于碱
4.下列物质的俗名与化学式对应关系正确的是
A. 干冰 B. 纯碱 C. 食盐 D. 烧碱
5.当光束通过下列分散系时,能观察到丁达尔效应的是
A. 盐酸 B. 食盐溶液 C. 氢氧化铁胶体 D. 碘的酒精溶液
6.下列关于金属钠的叙述中,说法正确的是
A. 少量的钠保存在酒精中 B. 钠的密度比水小
C. 钠是银白色金属,硬度大,熔点高 D. 钠着火时可以用泡末灭火剂扑灭
7.“纳米材料”是指微粒直径为几纳米到几十纳米的材料。据报道,科学家制造出了一种臂长只有纳米的纳米级镊子一种纳米材料,该镊子能够钳起分子或原子。下列说法正确的是
A. 该纳米级镊子钳起分子时发生了化学反应
B. 分子是化学反应中的最小微粒
C. 把该纳米级镊子分散到适当分散剂中可形成溶液
D. 把该纳米级镊子分散到适当分散剂中得到的混合物能产生丁达尔效应
8.下列叙述正确的是
A. 摩尔是七个基本物理量之一
B. 阿伏加德罗常数的符号为,近似为
C. 阿伏加德罗常数是中所含的碳原子数
D. 摩尔既是物质的量的单位,又是粒子数量的单位
9.下列有关气体摩尔体积的描述中正确的是
A. 在标准状况下,气体的摩尔体积约为
B. 在通常状况下,和所占的体积都约为
C. 单位物质的量的气体所占的体积就是气体摩尔体积
D. 相同物质的量的气体的气体摩尔体积相同
10.用表示阿伏加德罗常数的值,下列叙述中正确的是
A. 通常状况下,与的混合物所含氧原子数目一定为
B. 标准状况下,含有的分子数为
C. 的硫酸溶液中,的物质的量为
D. 铁和足量的盐酸反应,失去电子的数目为
11.下列电离方程式错误的是
A. B.
C. D.
12.下列叙述中,正确的是
A. 固体不导电,所以不是电解质
B. 铜丝、石墨均能导电,所以它们都是电解质
C. 熔融的能导电,所以是电解质
D. 溶于水,在通电条件下才能发生电离
13.下列各组中的离子,能在溶液中大量共存的是
A. B.
C. 、、、 D.
14.下列离子方程式中,书写正确的是
A. 氢氧化镁溶于盐酸中:
B. 将铁片插入硫酸铜溶液中:
C. 硫酸溶液与氢氧化钡溶液反应:
D. 氢氧化钡溶液与硝酸的反应:
15.下列各组中两种物质在溶液中的反应,能用同一离子方程式表示的是
A. ;
B. ;
C. ;
D. ;
16.酒精检测仪中装有重铬酸钾,该化合物中铬元素的化合价为
A. B. C. D.
17.下列物质转化中,一定需要加入氧化剂才能实现的是
A. B. C. D.
18.具有强氧化性,可发生反应:,下列说法不正确的是
A. 既是氧化产物,又是还原产物
B. 还原剂为
C. 生成转移电子
D. 氧化产物和还原产物的物质的量之比为:
19.下列反应中,水作氧化剂的是
A. B.
C. D.
20.下列实验的对应操作中,不合理的是
A.分离粗盐中的不溶物 B.稀释浓硫酸
C.从提纯后的溶液获得晶体 D.配制一定物质的量浓度的溶液
A.
A. B. C. D.
21.下列实验现象和结论相符的是
操作及现象 结论
某溶液中加入盐酸,产生能使澄清石灰水变浑浊的无色无味气体 溶液中一定含有
某溶液中加入溶液,产生白色沉淀 溶液中一定含有
某溶液中加入溶液,产生白色沉淀 溶液中一定含有
向酸性溶液滴加溶液,紫色褪去 有还原性
A. B. C. D.
22.配制溶液的部分过程示意图如下。下列说法不正确的是
A. 步骤中用玻璃棒搅拌的目的是加快溶解
B. 步骤中需用少量蒸馏水洗涤烧杯内壁和玻璃棒次,并将洗涤液都注入容量瓶
C. 步骤中液面距容量瓶刻度线时,改用胶头滴管加蒸馏水至凹液面与刻度线相切
D. 步骤中摇匀后若容量瓶内液面下降,需加水至刻度线
23.气体与足量溶液完全反应后,再加入溶液,发生如下化学反应:
;
,
下列有关说法正确的是
A. 氧化性:
B. 若有参加反应,则最终消耗
C. 反应中,每有参加反应,转移电子的数目为
D. 由上述反应原理推断:不能将氧化成
24.在明代宋应星所著的天工开物中,有关火法炼锌的工艺记载:“每炉甘石炉甘石的主要成分是十斤,装载入一泥罐内,,然后逐层用煤炭饼垫盛,其底铺薪,发火煅红,罐中炉甘石熔化成团.”火法炼锌的反应为:,下列说法不正确的是
A. 的化学式是
B. 被氧化的物质是
C. 既是氧化剂又是还原剂
D. 参与反应,转移电子的物质的量为
25.某溶液可能由、、、、、、中的若干种离子组成。现取适量溶液进行如下实验:
根据以上实验判断,下列推断错误的是
A. 气体通入澄清石灰水中,溶液变浑浊
B. 滤液中加入碳酸钠溶液一定会产生沉淀
C. 原溶液中一定存在和 ,一定不存在
D. 白色沉淀中加稀硝酸,沉淀不溶解
二、填空题:本大题共5小题,共40分。
26.下表是生活生产中常见的物质:
编号
名称 酒精
请你对表中的物质进行分类填序号:属于电解质的是____;属于盐的是____。
写出电离方程式:的电离方程式是____;的电离方程式是____。
写出与在水溶液中反应的离子方程式:____。
27.物质的量是高中化学常用的物理量,请完成以下有关计算:回答下列问题:
的物质的量是____,含有____个质子。
中含____,____个。
某金属氯化物,含有,则该氯化物的摩尔质量为____。
标准状况中所含氢原子的数目为____。
分子中所含原子数与____分子中所含原子数相等,该气体在标准状况下的体积为____。
28.氧化还原反应是一类重要的反应,在工农业生产、日常生活中都有广泛的用途。请结合相关化学知识回答下列问题:
化工厂可用浓氨水来检验输送的管道是否泄漏。相关化学反应如下:
____________________
配平以上方程式____;
反应中被还原的物质是____填化学式。
可在野外作生氢剂,反应原理为,该反应中氧化产物和还原产物的质量比为____。
在汽车的排气管上装一个催化转化器,可有效降低氮氧化物的排放,其中一个反应为用单线桥法表示出电子转移的方向和数目:____。
根据反应,回答下列问题。
氧化剂与还原剂的分子数之比为____。
当有个参加反应时,转移的电子个数为____。
用双线桥的方法表示该反应的电子转移情况____。
29.为除去粗盐中的、、以及泥沙等杂质,某同学设计了一种制备精盐的实验方案,步骤如下用于沉淀的试剂稍过量:
请回答:
步骤需采用的主要物质分离提纯操作,名称是______,所需要的玻璃仪器除酒精灯、玻璃棒、烧杯外,还要______。
步骤加入过量的目的是______。
步骤需加入适量的___ 填试剂名称,所发生反应的化学方程式为_______。
30.A、、、为四种可溶性盐,它们的阳离子分别是、、、中的一种,阴离子分别是、、、中的一种离子在物质中不能重复出现。现做如下实验:
把四种盐分别溶于盛有蒸馏水的四支试管中,只有的溶液呈蓝色。
向的四支试管中分别加入盐酸,的溶液中有沉淀生成,的溶液中有无色无味的气体逸出。
根据实验现象回答下列问题:
写出、、的化学式:______,______,______。
写出盐酸与反应产生气体的离子方程式:______。
写出与溶液反应的离子方程式:______。
将含相同数目、、的溶液混合后,写出溶液中存在的离子______;在此溶液中加入锌粒,写出发生反应的离子方程式____。
三、简答题:本大题共1小题,共8分。
31.某化学研究小组在实验室中探究金属钠及其化合物的性质。
某同学夹取一块钠,用滤纸吸干后再切一小块放在如图所示装置上做钠的燃烧实验,反应的化学方程式为____。
该小组的同学将产生的固体投入水中,反应的方程式为:____。反应停止后,同学们观察到烧杯内有少许黑色固体物质,经检测为碳。
某同学分析碳可能是加热过程中钠与反应产生的,为此设计如下图所示装置进行验证。先取一块纯净的钠放入干燥的管中,然后打开的活塞,反应一段时间后,点燃处酒精灯。观察到钠剧烈燃烧,产生大量白烟,同时有黑色物质生成,冷却后有白色固体附着在管壁上。
中所盛试剂为饱和溶液,作用是____。若缺少装置,可能产生的影响是____用化学方程式表示。
中反应一段时间后,再点燃处酒精灯的目的是____。
装置中反应生成碳单质的化学方程式为____。
1.【答案】
2.【答案】
3.【答案】
4.【答案】
5.【答案】
6.【答案】
7.【答案】
8.【答案】
9.【答案】
10.【答案】
11.【答案】
12.【答案】
13.【答案】
14.【答案】
15.【答案】
16.【答案】
17.【答案】
18.【答案】
19.【答案】
20.【答案】
21.【答案】
22.【答案】
23.【答案】
24.【答案】
25.【答案】
26.【答案】
27.【答案】
28.【答案】
:
:
29.【答案】蒸发蒸发皿将溶液中的杂质离子钙离子以及多余的钡离子除去盐酸、
30.【答案】
31.【答案】
除去中的杂质 排除装置内的空气,防止钠与氧气反应 或
第2页,共10页
同课章节目录
