辽宁省点石联考2024-2025学年高一(上)期末化学试卷(含答案)
文档属性
| 名称 | 辽宁省点石联考2024-2025学年高一(上)期末化学试卷(含答案) |  | |
| 格式 | docx | ||
| 文件大小 | 156.0KB | ||
| 资源类型 | 教案 | ||
| 版本资源 | 人教版(2019) | ||
| 科目 | 化学 | ||
| 更新时间 | 2025-01-15 19:09:38 | ||
图片预览



文档简介
辽宁省点石联考2024-2025学年高一(上)期末化学试卷
相对原子质量H:1 C:12 N:14 O:16 Na:23 Mg:24 A1:27 S:32 C1:35.5
Ca:40 Fe:56 Cu:64 Zn:65
一、单选题:本大题共15小题,共45分。
1.化学与生产、生活、科技、环境等关系密切。下列说法错误的是( )
A. 复方氢氧化铝片可作抗酸药
B. 孔雀石颜料主要成分为易被空气氧化
C. 稀土永磁材料是电子技术通信中的重要材料,稀土元素均为金属元素
D. 漂粉精既可作棉、麻、纸张的漂白剂,又可用作环境的消毒剂
2.如图是某反应的微观示意图,下列有关说法错误的是 ( )
A. 为还原剂
B. 发生还原反应
C. 该反应的化学方程式为
D. 每生成还原产物时,转移电子
3.下列叙述中,正确的是( )
A. “错把陈醋当成墨,写尽半生纸上酸”,陈醋是电解质
B. 牙膏中摩擦剂碳酸钙固体不导电,所以碳酸钙不是电解质
C. 碳量子点是一类具有荧光性能的碳纳米材料,属于胶体
D. “朝坛雾卷,曙岭烟沉”中的雾是一种气溶胶,能产生丁达尔效应
4.下列化学方程式或离子方程式不能准确解释事实的是( )
A. 溶液腐蚀铜板:
B. 溶液中通入过量:
C. 溶于强酸:
D. 呼吸面具中用吸收并供氧:
5.已知:。设为阿伏加德罗常数的值,下列说法正确的是( )
A. 的摩尔质量是
B. 标准状况下,的质量为
C. 的溶液中含有的原子数目为
D. 若反应中消耗,则该反应转移的电子数为
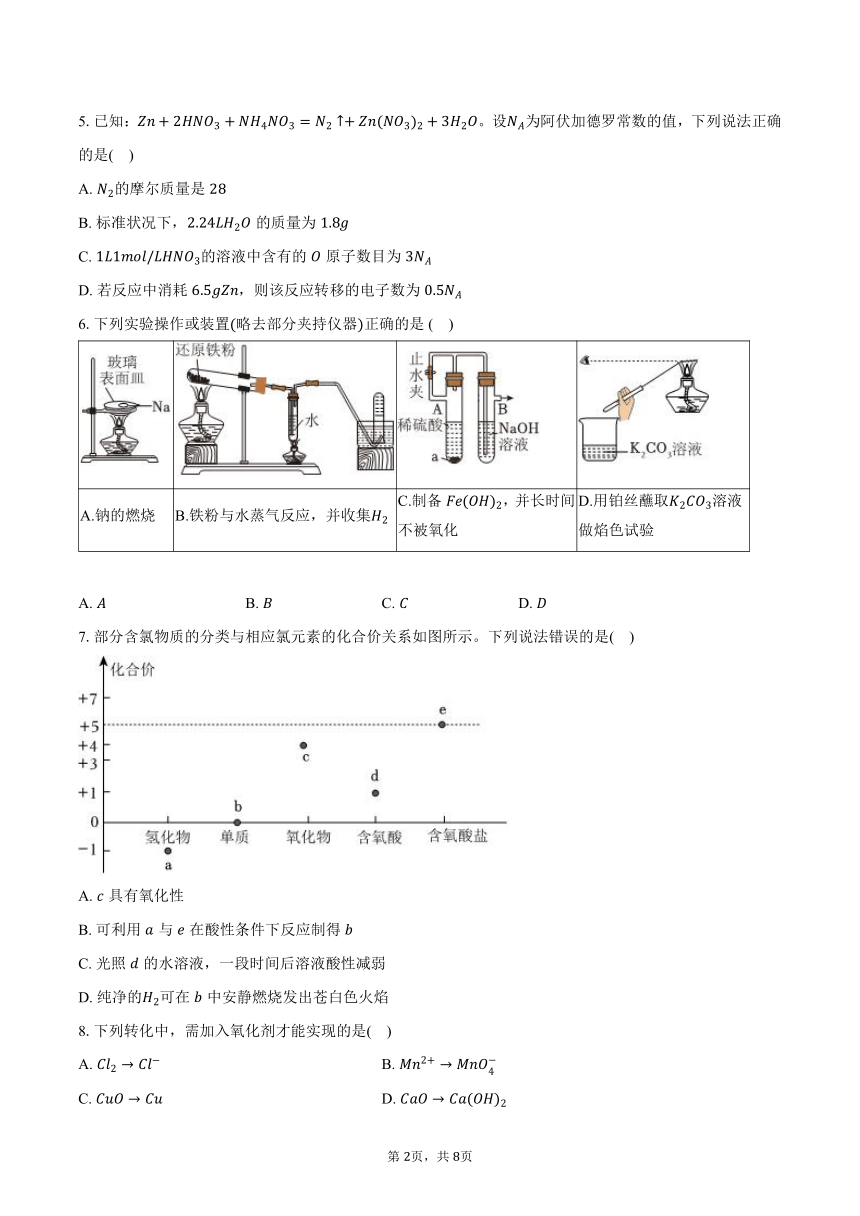
6.下列实验操作或装置略去部分夹持仪器正确的是 ( )
A.钠的燃烧 B.铁粉与水蒸气反应,并收集 C.制备,并长时间不被氧化 D.用铂丝蘸取溶液做焰色试验
A. B. C. D.
7.部分含氯物质的分类与相应氯元素的化合价关系如图所示。下列说法错误的是( )
A. 具有氧化性
B. 可利用与在酸性条件下反应制得
C. 光照的水溶液,一段时间后溶液酸性减弱
D. 纯净的可在中安静燃烧发出苍白色火焰
8.下列转化中,需加入氧化剂才能实现的是( )
A. B.
C. D.
9.常温下,下列各组离子在指定溶液中一定能大量共存的是( )
A. 澄清透明的溶液中:、、、
B. 溶液:、、、
C. 滴入酚酞呈红色的溶液:、、、
D. 能溶解并放出氢气的溶液:、、、
10.化学是以实验为基础的科学,下列实验方案设计中,能达到实验目的的是 ( )
选项 实验方案 实验目的
向某溶液中滴入适量稀硝酸无现象,再滴入溶液,生成白色沉淀 证明溶液中一定存在
取久置的粉末,向其中滴加过量的盐酸,产生无色气体 证明已变质
向某溶液滴入氯水后再滴溶液,溶液变红色 证明该溶液一定含
向较浓的溶液中滴入少量酸性溶液,观察到溶液紫色褪去 证明具有还原性
A. B. C. D.
11.高效净水剂高铁酸钾的制备流程如图所示,下列相关说法或离子方程式正确的是 ( )
A. 反应Ⅰ中可用澄清石灰水作尾气处理剂
B. 反应Ⅱ:
C. 反应Ⅲ:
D. 用净水时可生成胶体
12.下列实验现象与氧化还原反应无关的是( )
A. 在溶液中加入锌片,溶液变为无色
B. 向包有固体的棉花上滴几滴水,棉花立即燃烧
C. 将有色鲜花放入盛有干燥氯气的集气瓶中,鲜花褪色
D. 熔融的铁流入钢轨的裂缝,冷却后将钢轨牢牢地焊接在一起
13.已知某工业废水中含有大量的,还含有较多的、,以及部分污泥,通过下列流程可从该废水中回收晶体及固体单质。已知氧化性:。下列说法错误的是 ( )
A. 步骤、步骤和步骤的操作均为过滤
B. 若步骤中铁粉不足,将导致制备的晶体不纯
C. 步骤可确定含有,步骤中试剂为稀盐酸
D. 步骤中涉及的操作为蒸发浓缩、冷却结晶、过滤、洗涤
14.向、和的混合物中加入时,固体恰好完全溶解,所得溶液中不含。若用过量的在高温下还原相同质量的原混合物,所得固体质量是( )
A. B. C. D.
15.如图所示的恒温恒容密闭容器中间有自由滑动的隔板,将容器分成了两部分。当向左边的容器中充入,向右边的容器中充入由和组成的混合气体时,隔板处于如图所示位置,则混合气体中和的分子个数比( )
A. : B. : C. : D. :
二、流程题:本大题共1小题,共14分。
16.海洋是人类宝贵的自然资源,海水“晒盐”和海水“制碱”体现了人类利用和改造自然的智慧,请根据粗盐“制碱”的流程图回答问题:
选择适合用于步骤Ⅰ的除杂试剂,并按顺序填写 ______ 填标号。
A.稀硫酸
B.盐酸
C.烧碱
D.纯碱
步骤Ⅲ中向饱和食盐水中先通入的气体为 ______ ,再通入另一种气体。步骤Ⅲ中发生反应的化学方程式 ______ 。
为提高原料利用率,该流程中可以循环利用的物质为 ______ 填化学式。
某小组同学按下面设计的方案制备碳酸氢钠。实验装置如图所示夹持、固定用的仪器未画出。乙装置中盛放的是 ______ ,一段时间后丙装置中的反应现象为 ______ ,丁中倒置漏斗的作用是 ______ 。
三、实验题:本大题共2小题,共26分。
17.Ⅰ实验室有化学纯的浓硫酸,其试剂瓶上标签部分信息如下。现需配制的溶液,请回答下列问题:
硫酸化学纯
品名:硫酸
化学式:
相对分子质量:
密度:
质量分数:
需量取该浓硫酸的体积是 ______ 。
实验用到的玻璃仪器有烧杯、玻璃棒、胶头滴管、 ______ 填写仪器名称。
下列操作会使配制的溶液浓度偏低的有 ______ 填标号
A.溶液未冷却至室温就转移至容量瓶中进行定容
B.量取浓硫酸时俯视刻度线
C.溶解时有少量溶液洒出
D.摇匀后发现液面下降,未加水至刻度线
Ⅱ某“”消毒液部分标签如图所示,,请回答下列问题:
有效成分 质量分数
密度 净含量
注意事项
计算配制这样的一瓶“”消毒液需用托盘天平称量固体的质量为 ______ 保留小数点后一位。
如图为某同学配制该溶液的过程,该同学的操作步骤中错误的有 ______ 填标号。
A.
B.
C.
D.
含氯消毒剂的消毒能力可以用“有效氯”来表示,“有效氯”是指与含氯消毒剂氧化能力相当的氯气的质量。该溶液的“有效氯”是 ______ 。保留小数点后一位
18.铁有两种氯化物,都是重要的化工试剂。查阅有关资料如下:
:熔点为;易吸收空气中的水分而潮解。工业上采用向的铁粉中通入来制备无水。
:熔点为,易升华。工业上采用向炽热铁粉中通入来制备无水。
某化学活动小组用如图所示的装置部分夹持装置略去模拟工业生产制备无水铁粉足量。请回答下列问题:
仪器的名称为 ______ 。
在装置中,用与浓盐酸反应制取氯气,该反应的化学方程式为 ______ 。
中盛放的试剂是 ______ 。中盛放的碱石灰的作用是 ______ 答两条。
取装置中的少量产物溶于稀盐酸中配成稀溶液,经检测发现其中混有, ______ 填“能”或“不能”说明生成的同时还生成了,理由是 ______ 用离子方程式表示。
取装置中的产物,按以下步骤进行测定:
称取装置中的产物溶于过量的稀盐酸中;
加入足量溶液;
再加入足量溶液;
过滤、洗涤后干燥沉淀;
称量所得固体为。
则装置中的产物中铁元素的质量分数为 ______ 用带有和的式子表示。
四、简答题:本大题共1小题,共15分。
19.Ⅰ亚硝酸钠是一种用途广泛的工业盐,因其外观和食盐相似容易误食中毒。亚硝酸钠加热到以上会分解产生、和,亚硝酸钠水溶液呈碱性,能与溶液反应生成难溶于水、易溶于酸的。回答下列问题:
设计一种方法能用来区分固体和 ______ 。
误食会导致人体血红蛋白中的转化为而中毒,该过程中表现了 ______ 性填“氧化”或“还原”。服用柠檬可解毒,其原因是柠檬中含有的 ______ 将转化为填标号。
A.
B.
C.维生素
亚硝酸钠受热分解的化学方程式为,若反应中有气体生成,则转移电子的物质的量为 ______ 。
Ⅱ消毒剂是高效消毒灭菌剂。
制备的一种反应为:,该反应中还原性最强的物质是 ______ ,用单线桥标出其电子转移的方向和数目 ______ 。
实验室可用亚氯酸钠溶液与反应制的同时生成,此反应的离子方程式为 ______ ,氧化剂与还原剂物质的量之比为 ______ 。
1.【答案】
2.【答案】
3.【答案】
4.【答案】
5.【答案】
6.【答案】
7.【答案】
8.【答案】
9.【答案】
10.【答案】
11.【答案】
12.【答案】
13.【答案】
14.【答案】
15.【答案】
16.【答案】 、 饱和碳酸氢钠溶液 析出晶体 防止倒吸
17.【答案】 量筒和容量瓶
18.【答案】圆底烧瓶 浓 浓硫酸 尾气处理,防止污染空气;防止空气中的水蒸气进入中,造成氯化铁潮解 不能 或
19.【答案】分别加强热并收集气体或分别溶于水并滴加酚酞试液 氧化 :
第2页,共8页
相对原子质量H:1 C:12 N:14 O:16 Na:23 Mg:24 A1:27 S:32 C1:35.5
Ca:40 Fe:56 Cu:64 Zn:65
一、单选题:本大题共15小题,共45分。
1.化学与生产、生活、科技、环境等关系密切。下列说法错误的是( )
A. 复方氢氧化铝片可作抗酸药
B. 孔雀石颜料主要成分为易被空气氧化
C. 稀土永磁材料是电子技术通信中的重要材料,稀土元素均为金属元素
D. 漂粉精既可作棉、麻、纸张的漂白剂,又可用作环境的消毒剂
2.如图是某反应的微观示意图,下列有关说法错误的是 ( )
A. 为还原剂
B. 发生还原反应
C. 该反应的化学方程式为
D. 每生成还原产物时,转移电子
3.下列叙述中,正确的是( )
A. “错把陈醋当成墨,写尽半生纸上酸”,陈醋是电解质
B. 牙膏中摩擦剂碳酸钙固体不导电,所以碳酸钙不是电解质
C. 碳量子点是一类具有荧光性能的碳纳米材料,属于胶体
D. “朝坛雾卷,曙岭烟沉”中的雾是一种气溶胶,能产生丁达尔效应
4.下列化学方程式或离子方程式不能准确解释事实的是( )
A. 溶液腐蚀铜板:
B. 溶液中通入过量:
C. 溶于强酸:
D. 呼吸面具中用吸收并供氧:
5.已知:。设为阿伏加德罗常数的值,下列说法正确的是( )
A. 的摩尔质量是
B. 标准状况下,的质量为
C. 的溶液中含有的原子数目为
D. 若反应中消耗,则该反应转移的电子数为
6.下列实验操作或装置略去部分夹持仪器正确的是 ( )
A.钠的燃烧 B.铁粉与水蒸气反应,并收集 C.制备,并长时间不被氧化 D.用铂丝蘸取溶液做焰色试验
A. B. C. D.
7.部分含氯物质的分类与相应氯元素的化合价关系如图所示。下列说法错误的是( )
A. 具有氧化性
B. 可利用与在酸性条件下反应制得
C. 光照的水溶液,一段时间后溶液酸性减弱
D. 纯净的可在中安静燃烧发出苍白色火焰
8.下列转化中,需加入氧化剂才能实现的是( )
A. B.
C. D.
9.常温下,下列各组离子在指定溶液中一定能大量共存的是( )
A. 澄清透明的溶液中:、、、
B. 溶液:、、、
C. 滴入酚酞呈红色的溶液:、、、
D. 能溶解并放出氢气的溶液:、、、
10.化学是以实验为基础的科学,下列实验方案设计中,能达到实验目的的是 ( )
选项 实验方案 实验目的
向某溶液中滴入适量稀硝酸无现象,再滴入溶液,生成白色沉淀 证明溶液中一定存在
取久置的粉末,向其中滴加过量的盐酸,产生无色气体 证明已变质
向某溶液滴入氯水后再滴溶液,溶液变红色 证明该溶液一定含
向较浓的溶液中滴入少量酸性溶液,观察到溶液紫色褪去 证明具有还原性
A. B. C. D.
11.高效净水剂高铁酸钾的制备流程如图所示,下列相关说法或离子方程式正确的是 ( )
A. 反应Ⅰ中可用澄清石灰水作尾气处理剂
B. 反应Ⅱ:
C. 反应Ⅲ:
D. 用净水时可生成胶体
12.下列实验现象与氧化还原反应无关的是( )
A. 在溶液中加入锌片,溶液变为无色
B. 向包有固体的棉花上滴几滴水,棉花立即燃烧
C. 将有色鲜花放入盛有干燥氯气的集气瓶中,鲜花褪色
D. 熔融的铁流入钢轨的裂缝,冷却后将钢轨牢牢地焊接在一起
13.已知某工业废水中含有大量的,还含有较多的、,以及部分污泥,通过下列流程可从该废水中回收晶体及固体单质。已知氧化性:。下列说法错误的是 ( )
A. 步骤、步骤和步骤的操作均为过滤
B. 若步骤中铁粉不足,将导致制备的晶体不纯
C. 步骤可确定含有,步骤中试剂为稀盐酸
D. 步骤中涉及的操作为蒸发浓缩、冷却结晶、过滤、洗涤
14.向、和的混合物中加入时,固体恰好完全溶解,所得溶液中不含。若用过量的在高温下还原相同质量的原混合物,所得固体质量是( )
A. B. C. D.
15.如图所示的恒温恒容密闭容器中间有自由滑动的隔板,将容器分成了两部分。当向左边的容器中充入,向右边的容器中充入由和组成的混合气体时,隔板处于如图所示位置,则混合气体中和的分子个数比( )
A. : B. : C. : D. :
二、流程题:本大题共1小题,共14分。
16.海洋是人类宝贵的自然资源,海水“晒盐”和海水“制碱”体现了人类利用和改造自然的智慧,请根据粗盐“制碱”的流程图回答问题:
选择适合用于步骤Ⅰ的除杂试剂,并按顺序填写 ______ 填标号。
A.稀硫酸
B.盐酸
C.烧碱
D.纯碱
步骤Ⅲ中向饱和食盐水中先通入的气体为 ______ ,再通入另一种气体。步骤Ⅲ中发生反应的化学方程式 ______ 。
为提高原料利用率,该流程中可以循环利用的物质为 ______ 填化学式。
某小组同学按下面设计的方案制备碳酸氢钠。实验装置如图所示夹持、固定用的仪器未画出。乙装置中盛放的是 ______ ,一段时间后丙装置中的反应现象为 ______ ,丁中倒置漏斗的作用是 ______ 。
三、实验题:本大题共2小题,共26分。
17.Ⅰ实验室有化学纯的浓硫酸,其试剂瓶上标签部分信息如下。现需配制的溶液,请回答下列问题:
硫酸化学纯
品名:硫酸
化学式:
相对分子质量:
密度:
质量分数:
需量取该浓硫酸的体积是 ______ 。
实验用到的玻璃仪器有烧杯、玻璃棒、胶头滴管、 ______ 填写仪器名称。
下列操作会使配制的溶液浓度偏低的有 ______ 填标号
A.溶液未冷却至室温就转移至容量瓶中进行定容
B.量取浓硫酸时俯视刻度线
C.溶解时有少量溶液洒出
D.摇匀后发现液面下降,未加水至刻度线
Ⅱ某“”消毒液部分标签如图所示,,请回答下列问题:
有效成分 质量分数
密度 净含量
注意事项
计算配制这样的一瓶“”消毒液需用托盘天平称量固体的质量为 ______ 保留小数点后一位。
如图为某同学配制该溶液的过程,该同学的操作步骤中错误的有 ______ 填标号。
A.
B.
C.
D.
含氯消毒剂的消毒能力可以用“有效氯”来表示,“有效氯”是指与含氯消毒剂氧化能力相当的氯气的质量。该溶液的“有效氯”是 ______ 。保留小数点后一位
18.铁有两种氯化物,都是重要的化工试剂。查阅有关资料如下:
:熔点为;易吸收空气中的水分而潮解。工业上采用向的铁粉中通入来制备无水。
:熔点为,易升华。工业上采用向炽热铁粉中通入来制备无水。
某化学活动小组用如图所示的装置部分夹持装置略去模拟工业生产制备无水铁粉足量。请回答下列问题:
仪器的名称为 ______ 。
在装置中,用与浓盐酸反应制取氯气,该反应的化学方程式为 ______ 。
中盛放的试剂是 ______ 。中盛放的碱石灰的作用是 ______ 答两条。
取装置中的少量产物溶于稀盐酸中配成稀溶液,经检测发现其中混有, ______ 填“能”或“不能”说明生成的同时还生成了,理由是 ______ 用离子方程式表示。
取装置中的产物,按以下步骤进行测定:
称取装置中的产物溶于过量的稀盐酸中;
加入足量溶液;
再加入足量溶液;
过滤、洗涤后干燥沉淀;
称量所得固体为。
则装置中的产物中铁元素的质量分数为 ______ 用带有和的式子表示。
四、简答题:本大题共1小题,共15分。
19.Ⅰ亚硝酸钠是一种用途广泛的工业盐,因其外观和食盐相似容易误食中毒。亚硝酸钠加热到以上会分解产生、和,亚硝酸钠水溶液呈碱性,能与溶液反应生成难溶于水、易溶于酸的。回答下列问题:
设计一种方法能用来区分固体和 ______ 。
误食会导致人体血红蛋白中的转化为而中毒,该过程中表现了 ______ 性填“氧化”或“还原”。服用柠檬可解毒,其原因是柠檬中含有的 ______ 将转化为填标号。
A.
B.
C.维生素
亚硝酸钠受热分解的化学方程式为,若反应中有气体生成,则转移电子的物质的量为 ______ 。
Ⅱ消毒剂是高效消毒灭菌剂。
制备的一种反应为:,该反应中还原性最强的物质是 ______ ,用单线桥标出其电子转移的方向和数目 ______ 。
实验室可用亚氯酸钠溶液与反应制的同时生成,此反应的离子方程式为 ______ ,氧化剂与还原剂物质的量之比为 ______ 。
1.【答案】
2.【答案】
3.【答案】
4.【答案】
5.【答案】
6.【答案】
7.【答案】
8.【答案】
9.【答案】
10.【答案】
11.【答案】
12.【答案】
13.【答案】
14.【答案】
15.【答案】
16.【答案】 、 饱和碳酸氢钠溶液 析出晶体 防止倒吸
17.【答案】 量筒和容量瓶
18.【答案】圆底烧瓶 浓 浓硫酸 尾气处理,防止污染空气;防止空气中的水蒸气进入中,造成氯化铁潮解 不能 或
19.【答案】分别加强热并收集气体或分别溶于水并滴加酚酞试液 氧化 :
第2页,共8页
同课章节目录
