四川省泸州市泸县2024-2025学年高一上学期1月期末考试 化学试题(含答案)
文档属性
| 名称 | 四川省泸州市泸县2024-2025学年高一上学期1月期末考试 化学试题(含答案) |

|
|
| 格式 | docx | ||
| 文件大小 | 552.4KB | ||
| 资源类型 | 教案 | ||
| 版本资源 | 人教版(2019) | ||
| 科目 | 化学 | ||
| 更新时间 | 2025-01-17 00:00:00 | ||
图片预览


文档简介
泸州市泸县2024-2025学年上期高一高考文考期末测试题
化 学
注意事项:
1.答卷前,考生务必把自己的姓名、 准考证号填写在答题卡上。
2.考生作答时,选择题用2B铅笔将答题卡对应题目的答案标号涂黑,其余各题用0.5毫米黑色墨迹签字笔将答案写在答题卡上,在本试卷、草稿纸上答题无效。
3.全卷满分100分,考试时间75分钟。考试结束后,将本试卷和答题卡一并交回。
可能用到的相对原子质量:H=1 N=14 O=16 Na=23 Al=27 S=32 Fe=56 Cu=64
第一部分 选择题(共42分)
一、单项选择题:本题共14小题,每小题3分,共42分。在每小题给出的四个选项中,只有一项是符合题目要求的。
1.化学与生活密切相关,下列说法错误的是
A.高纯硅可用于制作光感电池
B.胃舒平(主要成分:氢氧化铝)可用于胃酸中和剂
C.铝合金大量用于高铁建设
D.生活中常用的玻璃、水泥和陶瓷材料均需用石灰石作工业原料生产
2.工业焊接钢管时常用进行“无损探伤”,下列数字表示的意义正确的是
A.“137”是指该原子的质子数
B.“55”是指该原子的中子数
C.该原子的电子数是82
D.“137”是指该原子的质量数
3.部分常见含氯物质的分类与相应化合价关系如图所示,下列推断不合理的是
A.a可以做氧化剂,也可以做还原剂
B.d的浓溶液与c的固体反应一定生成b与e
C.实验室可通过加热与d的浓溶液制得a
D.可存在a→c→e→d→b→a的循环转化关系
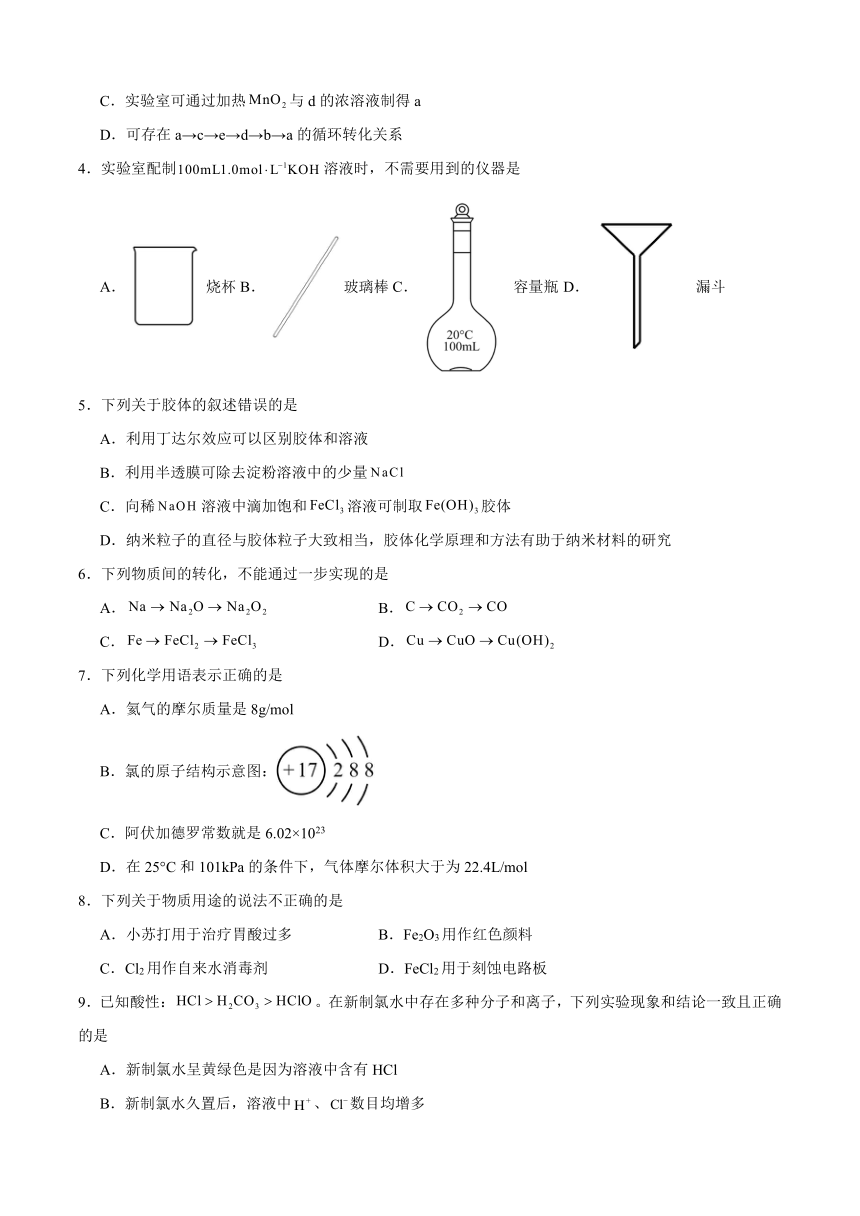
4.实验室配制溶液时,不需要用到的仪器是
A.烧杯B.玻璃棒C.容量瓶 D.漏斗
5.下列关于胶体的叙述错误的是
A.利用丁达尔效应可以区别胶体和溶液
B.利用半透膜可除去淀粉溶液中的少量
C.向稀溶液中滴加饱和溶液可制取胶体
D.纳米粒子的直径与胶体粒子大致相当,胶体化学原理和方法有助于纳米材料的研究
6.下列物质间的转化,不能通过一步实现的是
A. B.
C. D.
7.下列化学用语表示正确的是
A.氦气的摩尔质量是8g/mol
B.氯的原子结构示意图:
C.阿伏加德罗常数就是6.02×1023
D.在25°C和101kPa的条件下,气体摩尔体积大于为22.4L/mol
8.下列关于物质用途的说法不正确的是
A.小苏打用于治疗胃酸过多 B.Fe2O3用作红色颜料
C.Cl2用作自来水消毒剂 D.FeCl2用于刻蚀电路板
9.已知酸性:。在新制氯水中存在多种分子和离子,下列实验现象和结论一致且正确的是
A.新制氯水呈黄绿色是因为溶液中含有HCl
B.新制氯水久置后,溶液中、数目均增多
C.将KHCO3固体加入新制的氯水中,有气泡产生,说明氯水中有HClO
D.向紫色石蕊试液中加入氯水溶液先变蓝后褪色
10.下列各离子组在指定的溶液中能够大量共存的是
A.无色透明溶液中:
B.使紫色石蕊溶液呈红色的溶液中:
C.溶液加入铝片可以产生
D.使酚酞试液呈红色的溶液中:
11.如图所示,气缸的总体积一定,内部被活塞隔成Ⅰ、Ⅱ两部分,活塞可以自由移动,也可以固定。25℃时向Ⅰ中充入8gSO2,Ⅱ中充入8gO2,则下列说法正确的是
A.当活塞不再移动时,Ⅰ、Ⅱ两部分体积比为2∶1
B.当活塞不再移动时,Ⅰ、Ⅱ两部分密度比为1∶1
C.当活塞固定在气缸中间,Ⅰ、Ⅱ两部分压强比为2∶1
D.将气缸活塞去掉后,Ⅰ、Ⅱ中气体充分混合,混合气体对氢气的相对密度为
12.在铜的冶炼过程中有如下反应发生。关于此反应,下列说法正确的是
A.既是氧化产物,又是还原产物
B.5个发生反应,有14个电子转移
C.只作还原剂
D.产物中的有一部分是氧化产物
13.市售“84消毒液”显碱性,其有效成分是。下列分析错误的是
A.制备“84消毒液”的离子方程式:
B.加入溶液有沉淀生成,证明“84消毒液”中含有
C.消毒液作用于物体表面时适当放置一段时间效果更好
D.用次氯酸盐代替做消毒剂,存储更方便、使用更安全
14.根据下列实验操作与现象得出的结论正确的是
选项 实验操作及现象 结论
A 向某溶液中滴加AgNO3溶液,产生白色沉淀 该溶液中一定含Cl-
B 向某溶液中滴加澄清石灰水,产生白色沉淀 该溶液中一定含CO
C 取少量浓硫酸,加入水中,插入温度计,温度上升 浓硫酸溶于水放热
D 向某溶液中滴加BaCl2溶液,产生白色沉淀 该溶液中一定含SO
A.A B.B C.C D.D
第二部分 非选择题(共58分)
二、非选择题:本题共4小题,共58分。
15.(本题14分)由 Ca2+、Ag+、K+、Fe3+、NO、SO、Cl-、CO 这 8 种离子构成 A、B、C、D 四种可溶性盐(离子在物质中不能重复出现)。现做如下实验:
①把四种盐分别溶于盛有蒸馏水的四支试管中,只有C的溶液呈黄色;
②向①的四支试管中分别加入盐酸,A的溶液中有沉淀生成,B的溶液中有无色无味的气体逸出。
回答下列问题:
(1)写出A、C的化学式:A ,C
(2)写出足量盐酸与B反应的离子方程式: 。
(3)向C中滴入NaOH溶液的现象: 。
(4)与C含有同一种阳离子的氯化物M,配制M的饱和溶液并进行以下实验:
①在烧杯中加入40mL蒸馏水,加热至沸腾后,向沸水中加入制取的饱和M溶液5~6滴,继续煮沸至液体呈 色,停止加热,用激光笔照射烧杯中的液体,从垂直方向可以观察到液体中 。
②向步骤①的烧杯中逐滴加入足量的盐酸,可以观察到的现象: ,反应的离子方程式: 。
16.(本题14分)草酸晶体(H2C2O4·2H2O)熔点较低,受热时迅速熔化,在175°C分解成三种氧化物,某同学利用下列装置设计实验分别检验。回答下列问题:
(1)加热草酸晶体应选用上述装置 (填序号),其中发生反应的化学方程式为 。
(2)补充完整实验装置:混合气体→ →c→ →g→f。其中装置c的气体入口是 (填序号),仪器e中应装入试剂名称是 ,其作用是 。
(3)装置g中的现象是 。
(4)简述装置f末端导管口需要进行的操作是 。
17.(本题15分)通过海水晾晒可得粗盐,粗盐除NaCl外,还含有、、以及泥沙等杂质。以下是制备精盐的实验方案,各步操作流程如下:
(1)在第①步粗盐溶解操作中要用玻璃棒搅拌,作用是 。
(2)第②步操作的目的是除去粗盐中的 (填化学式,下同),第⑥步操作的目的是除去滤液中 和 。
(3)第⑤步“过滤”操作中得到沉淀的成分有:泥沙、、、 和 。
(4)在第③步操作中,选择的除杂的试剂不能用KOH代替NaOH,理由是 。
(5)过量溶液和过量溶液滴加顺序 (填可以或不可以)调换,理由是 。
(6)写出第③步一定能发生的离子反应方程 。
18.(本题15分)元素的价-类二维图是我们学习元素及其化合物相关知识的重要模型工具,也是发展证据推理与模型认知这一科学核心素养的重要途径。如图为氯元素的价-类二维图,回答下列问题:
(1)实验室用二氧化锰制取的离子方程式为 。
(2)物质的量均为的的和Fe充分反应,转移电子数为 。
(3)已知能与反应生成及等物质的量的另一种含氯物质,参考价类二维图,写出二者反应的离子方程式: 。
(4)亚氯酸钠是一种高效的漂白剂和消毒剂,它在酸性条件下生成并放出,有类似的性质。某兴趣小组探究亚氯酸钠的制备与性质。
Ⅰ.制备亚氯酸钠。关闭止水夹②,打开止水夹①,从进气口通入足量,充分反应生成。仪器a的名称为 ,仪器b的作用是 。
Ⅱ.探究亚氯酸钠的性质。停止通入气体,再通入空气一段时间后,关闭止水夹①,打开止水夹②,向A中滴入稀硫酸,装置B中的现象为 。
(5)城市饮用水处理,新技术用替代,其中氯元素都被还原为,如果以单位质量的氧化剂所得到的电子数来表示消毒效率,那么消毒杀菌剂的消毒效率是的 倍(结果保留两位小数)。
参考答案:
题号 1 2 3 4 5 6 7 8 9 10
答案 D D B D C D D D B D
题号 11 12 13 14
答案 D D B C
15.(1) AgNO3 Fe2(SO4)3
(2)
(3)生成红褐色沉淀
(4) 红褐 有一条光亮通路 先有红褐色沉淀后沉淀溶解
16.(1) b H2C2O4·2H2O CO↑+CO2↑+3H2O
(2) e d ② 球形干燥管 检验生成的水
(3)黑色粉末变红
(4)点燃未反应的一氧化碳使它转化为二氧化碳,防止污染空气。
17.(1)搅拌,加快溶解
(2) NaOH
(3)
(4)防止引入
(5) 不可以 为了确保钡离子被碳酸根离子除尽
(6)
18.(1)MnO2+2Cl-+4H+Cl2↑+Mn2++2H2O;
(2)2mol
(3)2ClO2+2OH-=+H2O
(4) 分液漏斗 吸收尾气并防倒吸 溶液变蓝
(5)1.57
化 学
注意事项:
1.答卷前,考生务必把自己的姓名、 准考证号填写在答题卡上。
2.考生作答时,选择题用2B铅笔将答题卡对应题目的答案标号涂黑,其余各题用0.5毫米黑色墨迹签字笔将答案写在答题卡上,在本试卷、草稿纸上答题无效。
3.全卷满分100分,考试时间75分钟。考试结束后,将本试卷和答题卡一并交回。
可能用到的相对原子质量:H=1 N=14 O=16 Na=23 Al=27 S=32 Fe=56 Cu=64
第一部分 选择题(共42分)
一、单项选择题:本题共14小题,每小题3分,共42分。在每小题给出的四个选项中,只有一项是符合题目要求的。
1.化学与生活密切相关,下列说法错误的是
A.高纯硅可用于制作光感电池
B.胃舒平(主要成分:氢氧化铝)可用于胃酸中和剂
C.铝合金大量用于高铁建设
D.生活中常用的玻璃、水泥和陶瓷材料均需用石灰石作工业原料生产
2.工业焊接钢管时常用进行“无损探伤”,下列数字表示的意义正确的是
A.“137”是指该原子的质子数
B.“55”是指该原子的中子数
C.该原子的电子数是82
D.“137”是指该原子的质量数
3.部分常见含氯物质的分类与相应化合价关系如图所示,下列推断不合理的是
A.a可以做氧化剂,也可以做还原剂
B.d的浓溶液与c的固体反应一定生成b与e
C.实验室可通过加热与d的浓溶液制得a
D.可存在a→c→e→d→b→a的循环转化关系
4.实验室配制溶液时,不需要用到的仪器是
A.烧杯B.玻璃棒C.容量瓶 D.漏斗
5.下列关于胶体的叙述错误的是
A.利用丁达尔效应可以区别胶体和溶液
B.利用半透膜可除去淀粉溶液中的少量
C.向稀溶液中滴加饱和溶液可制取胶体
D.纳米粒子的直径与胶体粒子大致相当,胶体化学原理和方法有助于纳米材料的研究
6.下列物质间的转化,不能通过一步实现的是
A. B.
C. D.
7.下列化学用语表示正确的是
A.氦气的摩尔质量是8g/mol
B.氯的原子结构示意图:
C.阿伏加德罗常数就是6.02×1023
D.在25°C和101kPa的条件下,气体摩尔体积大于为22.4L/mol
8.下列关于物质用途的说法不正确的是
A.小苏打用于治疗胃酸过多 B.Fe2O3用作红色颜料
C.Cl2用作自来水消毒剂 D.FeCl2用于刻蚀电路板
9.已知酸性:。在新制氯水中存在多种分子和离子,下列实验现象和结论一致且正确的是
A.新制氯水呈黄绿色是因为溶液中含有HCl
B.新制氯水久置后,溶液中、数目均增多
C.将KHCO3固体加入新制的氯水中,有气泡产生,说明氯水中有HClO
D.向紫色石蕊试液中加入氯水溶液先变蓝后褪色
10.下列各离子组在指定的溶液中能够大量共存的是
A.无色透明溶液中:
B.使紫色石蕊溶液呈红色的溶液中:
C.溶液加入铝片可以产生
D.使酚酞试液呈红色的溶液中:
11.如图所示,气缸的总体积一定,内部被活塞隔成Ⅰ、Ⅱ两部分,活塞可以自由移动,也可以固定。25℃时向Ⅰ中充入8gSO2,Ⅱ中充入8gO2,则下列说法正确的是
A.当活塞不再移动时,Ⅰ、Ⅱ两部分体积比为2∶1
B.当活塞不再移动时,Ⅰ、Ⅱ两部分密度比为1∶1
C.当活塞固定在气缸中间,Ⅰ、Ⅱ两部分压强比为2∶1
D.将气缸活塞去掉后,Ⅰ、Ⅱ中气体充分混合,混合气体对氢气的相对密度为
12.在铜的冶炼过程中有如下反应发生。关于此反应,下列说法正确的是
A.既是氧化产物,又是还原产物
B.5个发生反应,有14个电子转移
C.只作还原剂
D.产物中的有一部分是氧化产物
13.市售“84消毒液”显碱性,其有效成分是。下列分析错误的是
A.制备“84消毒液”的离子方程式:
B.加入溶液有沉淀生成,证明“84消毒液”中含有
C.消毒液作用于物体表面时适当放置一段时间效果更好
D.用次氯酸盐代替做消毒剂,存储更方便、使用更安全
14.根据下列实验操作与现象得出的结论正确的是
选项 实验操作及现象 结论
A 向某溶液中滴加AgNO3溶液,产生白色沉淀 该溶液中一定含Cl-
B 向某溶液中滴加澄清石灰水,产生白色沉淀 该溶液中一定含CO
C 取少量浓硫酸,加入水中,插入温度计,温度上升 浓硫酸溶于水放热
D 向某溶液中滴加BaCl2溶液,产生白色沉淀 该溶液中一定含SO
A.A B.B C.C D.D
第二部分 非选择题(共58分)
二、非选择题:本题共4小题,共58分。
15.(本题14分)由 Ca2+、Ag+、K+、Fe3+、NO、SO、Cl-、CO 这 8 种离子构成 A、B、C、D 四种可溶性盐(离子在物质中不能重复出现)。现做如下实验:
①把四种盐分别溶于盛有蒸馏水的四支试管中,只有C的溶液呈黄色;
②向①的四支试管中分别加入盐酸,A的溶液中有沉淀生成,B的溶液中有无色无味的气体逸出。
回答下列问题:
(1)写出A、C的化学式:A ,C
(2)写出足量盐酸与B反应的离子方程式: 。
(3)向C中滴入NaOH溶液的现象: 。
(4)与C含有同一种阳离子的氯化物M,配制M的饱和溶液并进行以下实验:
①在烧杯中加入40mL蒸馏水,加热至沸腾后,向沸水中加入制取的饱和M溶液5~6滴,继续煮沸至液体呈 色,停止加热,用激光笔照射烧杯中的液体,从垂直方向可以观察到液体中 。
②向步骤①的烧杯中逐滴加入足量的盐酸,可以观察到的现象: ,反应的离子方程式: 。
16.(本题14分)草酸晶体(H2C2O4·2H2O)熔点较低,受热时迅速熔化,在175°C分解成三种氧化物,某同学利用下列装置设计实验分别检验。回答下列问题:
(1)加热草酸晶体应选用上述装置 (填序号),其中发生反应的化学方程式为 。
(2)补充完整实验装置:混合气体→ →c→ →g→f。其中装置c的气体入口是 (填序号),仪器e中应装入试剂名称是 ,其作用是 。
(3)装置g中的现象是 。
(4)简述装置f末端导管口需要进行的操作是 。
17.(本题15分)通过海水晾晒可得粗盐,粗盐除NaCl外,还含有、、以及泥沙等杂质。以下是制备精盐的实验方案,各步操作流程如下:
(1)在第①步粗盐溶解操作中要用玻璃棒搅拌,作用是 。
(2)第②步操作的目的是除去粗盐中的 (填化学式,下同),第⑥步操作的目的是除去滤液中 和 。
(3)第⑤步“过滤”操作中得到沉淀的成分有:泥沙、、、 和 。
(4)在第③步操作中,选择的除杂的试剂不能用KOH代替NaOH,理由是 。
(5)过量溶液和过量溶液滴加顺序 (填可以或不可以)调换,理由是 。
(6)写出第③步一定能发生的离子反应方程 。
18.(本题15分)元素的价-类二维图是我们学习元素及其化合物相关知识的重要模型工具,也是发展证据推理与模型认知这一科学核心素养的重要途径。如图为氯元素的价-类二维图,回答下列问题:
(1)实验室用二氧化锰制取的离子方程式为 。
(2)物质的量均为的的和Fe充分反应,转移电子数为 。
(3)已知能与反应生成及等物质的量的另一种含氯物质,参考价类二维图,写出二者反应的离子方程式: 。
(4)亚氯酸钠是一种高效的漂白剂和消毒剂,它在酸性条件下生成并放出,有类似的性质。某兴趣小组探究亚氯酸钠的制备与性质。
Ⅰ.制备亚氯酸钠。关闭止水夹②,打开止水夹①,从进气口通入足量,充分反应生成。仪器a的名称为 ,仪器b的作用是 。
Ⅱ.探究亚氯酸钠的性质。停止通入气体,再通入空气一段时间后,关闭止水夹①,打开止水夹②,向A中滴入稀硫酸,装置B中的现象为 。
(5)城市饮用水处理,新技术用替代,其中氯元素都被还原为,如果以单位质量的氧化剂所得到的电子数来表示消毒效率,那么消毒杀菌剂的消毒效率是的 倍(结果保留两位小数)。
参考答案:
题号 1 2 3 4 5 6 7 8 9 10
答案 D D B D C D D D B D
题号 11 12 13 14
答案 D D B C
15.(1) AgNO3 Fe2(SO4)3
(2)
(3)生成红褐色沉淀
(4) 红褐 有一条光亮通路 先有红褐色沉淀后沉淀溶解
16.(1) b H2C2O4·2H2O CO↑+CO2↑+3H2O
(2) e d ② 球形干燥管 检验生成的水
(3)黑色粉末变红
(4)点燃未反应的一氧化碳使它转化为二氧化碳,防止污染空气。
17.(1)搅拌,加快溶解
(2) NaOH
(3)
(4)防止引入
(5) 不可以 为了确保钡离子被碳酸根离子除尽
(6)
18.(1)MnO2+2Cl-+4H+Cl2↑+Mn2++2H2O;
(2)2mol
(3)2ClO2+2OH-=+H2O
(4) 分液漏斗 吸收尾气并防倒吸 溶液变蓝
(5)1.57
同课章节目录
