河南省三门峡市2024-2025学年高一上学期1月期末化学试题(图片版,无答案)
文档属性
| 名称 | 河南省三门峡市2024-2025学年高一上学期1月期末化学试题(图片版,无答案) |  | |
| 格式 | docx | ||
| 文件大小 | 4.8MB | ||
| 资源类型 | 教案 | ||
| 版本资源 | 人教版(2019) | ||
| 科目 | 化学 | ||
| 更新时间 | 2025-01-18 12:47:30 | ||
图片预览


文档简介
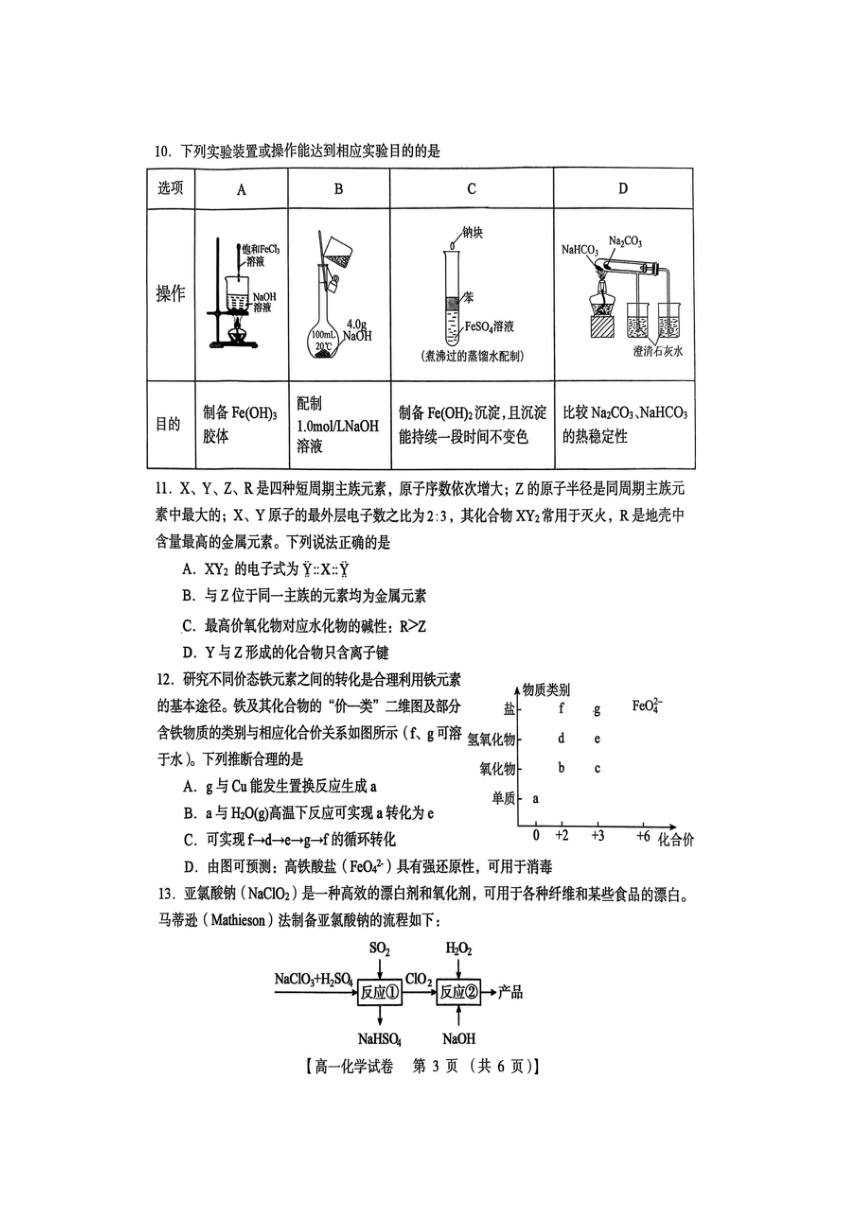
下列说法错误的是
A.反应①阶段,参加反应的NaCIO3和S02的个数之比为2:1
B.反应①中NaCIO,是氧化剂,NaHSO4是氧化产物
C.反应②条件下,C102的氧化性大于H02
D.反应②中的H02可用NaCl04代替
14.某溶液X中可能含有下列离子中的若干种:S042、C、HC0、Na、Mg2、Ba2+,所含
离子的浓度均相同。为了确定该溶液的组成,某同学取上述溶液X,进行了如下实验:
①向溶液X中加入足量的Ba(OD2溶液,得到白色沉淀:
②将①的反应混合液过滤,在沉淀中加人足量稀盐酸,沉淀部分溶解且产生气体。
下列说法正确的是
A.①中得到的白色沉淀是BaCO3和BaSO4的混合物
B.溶液X中一定不存在Ba2+、C
C.溶液X中一定存在S042、HC03,可能存在Mg
D.无法确定溶液X中是否含有Na,需要做焰色试验才能确定
第Ⅱ卷(非选择题共58分)
二、非选择题(本题包含4道小题,共58分)
15.(16分)下表为元素周期表的一部分,请参照元素①~⑨在表中的位置,用相应化学用语
回答下列问题:
族
IA
0
周期
①
IA
ⅢA
IVA
VA
VIA
VIIA
②
③
④
⑤
⑥
⑦
⑧
⑨
(1)②的原子结构示意图为
写出它与原子半径最小的原子形成10电子且为正四
面体结构的化合物的电子式
;用电子式表示⑤和⑧形成化合物的过程
(2)④⑤⑧形成的简单离子半径由大到小的顺序为
(填离子符号):③⑦⑨的最高
价氧化物对应水化物的酸性由强到弱的顺序为
(填化学式)。
(3)这些元素形成的氧化物中,不溶于水,但既能与强酸又能与强碱反应的是
(填化
学式),写出它与⑤的最高价氧化物对应水化物发生反应的离子方程式:
0
(4)④与⑤能形成谈黄色化合物A,②与④能形成一种常见的气体B,则A与B反应的
化学方程式为
0
【高一化学试卷第4页(共6页)】
16.(12分)化学与生产、生活息息相关。回答下列问题:
(1)小苏打在面包行业,不仅可以做膨松剂,还可以调节酸度。写出用小苏打调节盐酸酸度
时发生反应的离子方程式:
0
(2)过氧化钠常用作供氧剂,其与水反应的离子方程式为
0
(3)有人误把洁厕灵(主要成分为盐酸)和“84”消毒液(主要成分为NaC10)一起倒在马
桶里,结果产生大量的黄绿色气体。该反应的离子方程式为
(4)我国“四大发明”在人类发展史上起到了非常重要的作用,其中黑火药的爆炸反应
2KN03+S+3C=KS+N2+3C02↑。该反应中被还原的元素是
(填元素符号)。
(5)安全气囊弹出时发生反应:10NaN3+2KNO3=K20+5Na20+16N2t,该反应中氧化产物与还
原产物的物质的量之比为
。标准状况下生成44.8LN2时转移电子个数为NA
(Na为阿伏加德罗常数的值)。
17.(16分)实验室用如图所示装置(夹持仪器略)验证C2的漂白性并制备无水FCl3。查阅
相关资料得知:无水FCL3在空气中易与水反应,加热易升华。
浓盐酸
铁月
碱石灰
收集器
饱和食盐水
冷水
D
回答下列问题:
(1)仪器a的名称为
,仪器b中发生反应的离子方程式为
(2)实验开始时,应先点燃
(填“A”或“D”)处酒精灯。
(3)装置B中饱和食盐水的作用是
同时还用作安全瓶(监测实验时装置C中
是否发生堵塞),若装置C发生堵塞,则装置B中将观察到的现象是
(4)装置C的作用是验证氯气是否具有漂白性,为此,实验时装置C中I、Ⅱ、Ⅲ处依次放
入的物质是
。(填“甲”“乙”“丙”或“丁”。
装置
I
Ⅲ
甲
干燥的有色布条
碱石灰
湿润的有色布条
乙
湿润的有色布条
无水氯化钙
干燥的有色布条
丙
干燥的有色布条
无水氯化钙
湿润的有色布条
湿润的有色布条
浓硫酸
干燥的有色布条
【高一化学试卷
第5页(共6页)】
A.反应①阶段,参加反应的NaCIO3和S02的个数之比为2:1
B.反应①中NaCIO,是氧化剂,NaHSO4是氧化产物
C.反应②条件下,C102的氧化性大于H02
D.反应②中的H02可用NaCl04代替
14.某溶液X中可能含有下列离子中的若干种:S042、C、HC0、Na、Mg2、Ba2+,所含
离子的浓度均相同。为了确定该溶液的组成,某同学取上述溶液X,进行了如下实验:
①向溶液X中加入足量的Ba(OD2溶液,得到白色沉淀:
②将①的反应混合液过滤,在沉淀中加人足量稀盐酸,沉淀部分溶解且产生气体。
下列说法正确的是
A.①中得到的白色沉淀是BaCO3和BaSO4的混合物
B.溶液X中一定不存在Ba2+、C
C.溶液X中一定存在S042、HC03,可能存在Mg
D.无法确定溶液X中是否含有Na,需要做焰色试验才能确定
第Ⅱ卷(非选择题共58分)
二、非选择题(本题包含4道小题,共58分)
15.(16分)下表为元素周期表的一部分,请参照元素①~⑨在表中的位置,用相应化学用语
回答下列问题:
族
IA
0
周期
①
IA
ⅢA
IVA
VA
VIA
VIIA
②
③
④
⑤
⑥
⑦
⑧
⑨
(1)②的原子结构示意图为
写出它与原子半径最小的原子形成10电子且为正四
面体结构的化合物的电子式
;用电子式表示⑤和⑧形成化合物的过程
(2)④⑤⑧形成的简单离子半径由大到小的顺序为
(填离子符号):③⑦⑨的最高
价氧化物对应水化物的酸性由强到弱的顺序为
(填化学式)。
(3)这些元素形成的氧化物中,不溶于水,但既能与强酸又能与强碱反应的是
(填化
学式),写出它与⑤的最高价氧化物对应水化物发生反应的离子方程式:
0
(4)④与⑤能形成谈黄色化合物A,②与④能形成一种常见的气体B,则A与B反应的
化学方程式为
0
【高一化学试卷第4页(共6页)】
16.(12分)化学与生产、生活息息相关。回答下列问题:
(1)小苏打在面包行业,不仅可以做膨松剂,还可以调节酸度。写出用小苏打调节盐酸酸度
时发生反应的离子方程式:
0
(2)过氧化钠常用作供氧剂,其与水反应的离子方程式为
0
(3)有人误把洁厕灵(主要成分为盐酸)和“84”消毒液(主要成分为NaC10)一起倒在马
桶里,结果产生大量的黄绿色气体。该反应的离子方程式为
(4)我国“四大发明”在人类发展史上起到了非常重要的作用,其中黑火药的爆炸反应
2KN03+S+3C=KS+N2+3C02↑。该反应中被还原的元素是
(填元素符号)。
(5)安全气囊弹出时发生反应:10NaN3+2KNO3=K20+5Na20+16N2t,该反应中氧化产物与还
原产物的物质的量之比为
。标准状况下生成44.8LN2时转移电子个数为NA
(Na为阿伏加德罗常数的值)。
17.(16分)实验室用如图所示装置(夹持仪器略)验证C2的漂白性并制备无水FCl3。查阅
相关资料得知:无水FCL3在空气中易与水反应,加热易升华。
浓盐酸
铁月
碱石灰
收集器
饱和食盐水
冷水
D
回答下列问题:
(1)仪器a的名称为
,仪器b中发生反应的离子方程式为
(2)实验开始时,应先点燃
(填“A”或“D”)处酒精灯。
(3)装置B中饱和食盐水的作用是
同时还用作安全瓶(监测实验时装置C中
是否发生堵塞),若装置C发生堵塞,则装置B中将观察到的现象是
(4)装置C的作用是验证氯气是否具有漂白性,为此,实验时装置C中I、Ⅱ、Ⅲ处依次放
入的物质是
。(填“甲”“乙”“丙”或“丁”。
装置
I
Ⅲ
甲
干燥的有色布条
碱石灰
湿润的有色布条
乙
湿润的有色布条
无水氯化钙
干燥的有色布条
丙
干燥的有色布条
无水氯化钙
湿润的有色布条
湿润的有色布条
浓硫酸
干燥的有色布条
【高一化学试卷
第5页(共6页)】
同课章节目录
