山东省淄博市2024-2025学年高一上学期1月期末化学试题(无答案)
文档属性
| 名称 | 山东省淄博市2024-2025学年高一上学期1月期末化学试题(无答案) |  | |
| 格式 | docx | ||
| 文件大小 | 866.8KB | ||
| 资源类型 | 教案 | ||
| 版本资源 | 人教版(2019) | ||
| 科目 | 化学 | ||
| 更新时间 | 2025-01-18 12:55:21 | ||
图片预览



文档简介
参照秘密级管理★启用前
2024—2025学年度第一学期高一教学质量检测
化 学
注意事项:
1.答卷前,考生务必将自己的姓名,准考证号等填写在答题卡上。
2回答选择题时,选出每小题答案后,用铅笔把答题卡上对应题目的答案标号涂黑。如需改动,用橡皮擦干净后,再选涂其他答案标号。回答非选择题时,将答案写在答题卡上。写在本试卷上无效。
3考试结束后,将本试卷和答题卡一并交回。
可能用到的相对原子质量:H 1 C 12 O 16 Mn 55 Na 23 Al 27 Cl 35.5
一、选择题:本题共10小题,每小题2分,共20分. 每小题只有1个选项是符合题目要求。
1. 下列应用中不涉及氧化还原反应的是
A. 用作饮用水消毒剂 B. 用作食品干燥剂
C. 用作潜水艇的供氧剂 D. 溶液用作覆铜板腐蚀液
2. 实验安全至关重要, 下列实验操作、事故处理方法错误的是
A. 未用完的钠、钾、白磷需放回原试剂瓶
B. 火灾现场有大量活泼金属时需用潮湿的沙土来灭火
C. 皮肤溅上碱液,先用大量水冲洗,再用 2%的硼酸溶液冲洗
D. 氯气泄漏时, 应用浸有小苏打水的毛巾捂住口鼻向高处撤离
3. 下列化学用语或图示正确的是
A. 的结构式:
B. 的离子结构示意图:
C. 用电子式表示 的形成过程:
D. 在水中的电离方程式:
4. 下列图示实验中, 操作正确且能达到实验目的的是
A. 收集 B. 加热试管中的液体 C. 制取 胶体 D.制取
5. 下列物质均为离子化合物, 且化学键类型相同的是
A. 与 B. 与
C. 与 D. 与
6. 约里奥-居里夫妇用 粒子轰击 ,获得了首个人工放射性核素 ,其反应为
。下列说法错误的是
A. B. 与 互为同位素
C. 中子数为 14 D. 与 互为同素异形体
7. 设 为阿伏加德罗常数的值。下列说法错误的是
A. 溶液中含有的离子数为
B. 与足量 反应生成 的分子数为
C. 与足量铁粉充分反应转移的电子数为
D. 标准状况下, 与 混合气体中含有的原子数为
8. 下列有关说法错误的是
A. 钠、氧化钠、过氧化钠长期放置在空气中最终产物相同
B. 铁的化学性质比较活泼, 自然界中铁元素仅以化合态存在
C. 铝合金比铝硬度大的原因是原子层之间的相对滑动变得困难
D. 氢气在氯气中燃烧, 发出苍白色火焰, 瓶口上方有白雾生成
9. 工业上将 通入冷的 溶液中制得漂白液,下列说法错误的是
A. 溶液比 溶液稳定 B. 漂白液需在阴凉处避光保存
C. 通入 后的漂白液消毒能力增强 D. 漂白液的有效成分是 和
10. 实验室中利用下图装置验证铁与水蒸气的反应。下列说法错误的是
A. 酒精灯点燃的顺序:先①后②
B. 用火柴点燃肥皂泡检验生成的
C. 反应为
D. 由此可知炽热的铁水注入模具之前, 模具须干燥
二、选择题:本题共5小题,每小题4分,共20分。每小题只有一个或两个选项符合题意,全部选对得4分,选对但不全对的得2分,有选错的得0分。
11. 对下列粒子组在溶液中能否大量共存的判断和分析均正确的是
粒子组 判断和分析
A 不能大量共存, 因发生反应:
B 不能大量共存,因发生反应:
C 能大量共存, 粒子间不反应
D 能大量共存, 粒子间不反应
12. W、X、Y、Z 为原子序数依次增大的短周期主族元素,且最外层电子数之和为 20 , 与 同族, 是地壳中含量最多的元素。下列说法错误的是
A. 简单氢化物的稳定性:
B. 组成的化合物有还原性
C. 组成的化合物能与水反应
D. 最高价氧化物的水化物的酸性:
13. 根据实验操作和现象所得结论错误的是
实验操作和现象 结论
A 向待测液中滴加 溶液和稀 ,产生白色沉淀 待测液中含有
B 向 溶液中滴加几滴酸性 溶液,紫红色消失 具有还原性
C 向 溶液中滴加几滴新制氯水,溶液变为橙黄色 非金属性:
D 和 中均分别加入 溶液和盐酸, 只溶于盐酸, 都能溶 碱性:
14. 亚氯酸钠 是一种高效消毒剂,其制备流程如下。下列说法正确的是
A. 由反应①可知还原性:
B. 反应①中生成 转移 电子
C. 反应②中 做氧化剂, 是氧化产物
D. 理论上,制得 消耗 与 物质的量之和为
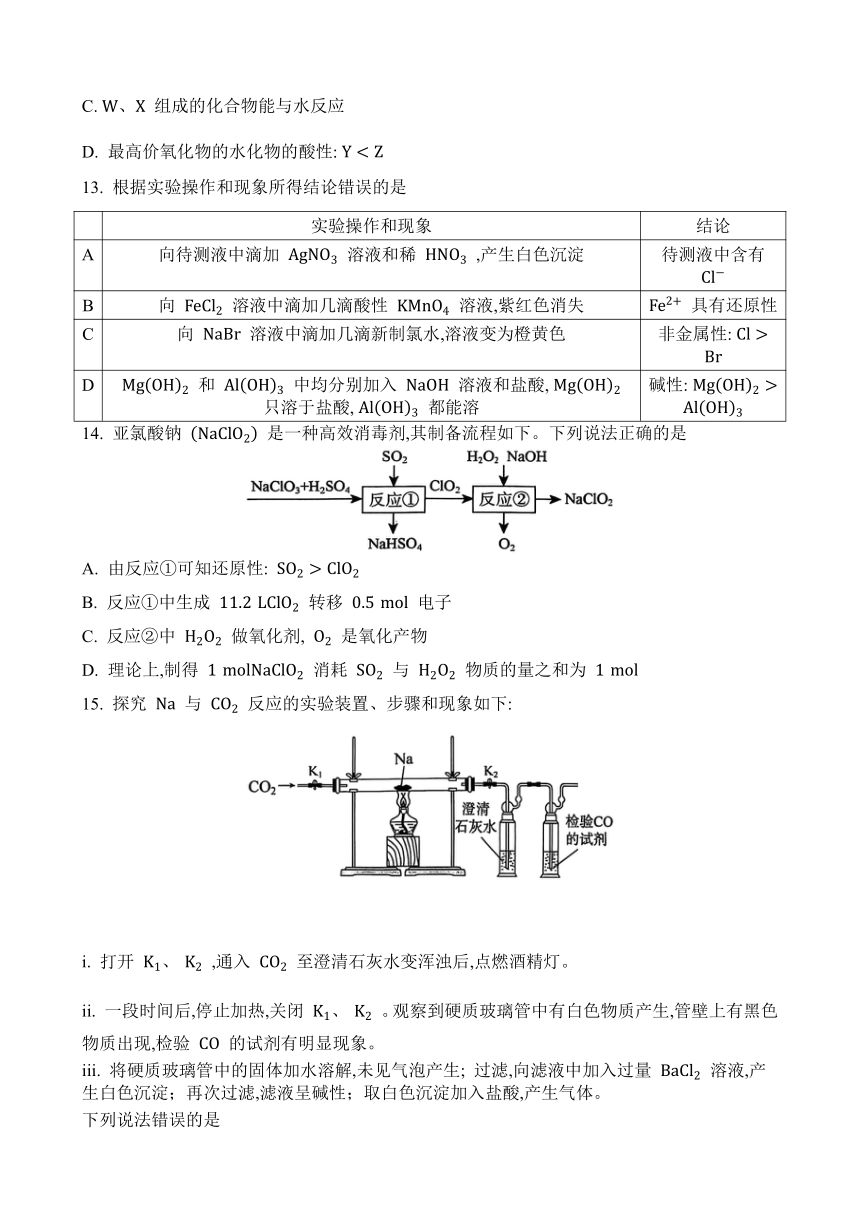
15. 探究 与 反应的实验装置、步骤和现象如下:
i. 打开 ,通入 至澄清石灰水变浑浊后,点燃酒精灯。
ii. 一段时间后,停止加热,关闭 。观察到硬质玻璃管中有白色物质产生,管壁上有黑色物质出现,检验 的试剂有明显现象。
iii. 将硬质玻璃管中的固体加水溶解,未见气泡产生; 过滤,向滤液中加入过量 溶液,产生白色沉淀;再次过滤,滤液呈碱性;取白色沉淀加入盐酸,产生气体。
下列说法错误的是
A. 步骤 的目的是排除 和水蒸气的干扰
B. 步骤 ii 中的黑色物质可能是碳单质
C. 步骤 iii 中的现象说明步骤 ii 中生成的白色物质为
D. 与 反应的产物可能为
三、非选择题:本题共5小题,共60分。
16. (12 分) “价一类”二维图是学习化学的一种重要工具。由原子序数依次增大的 X、Y、Z、M、Q 五种短周期元素形成的部分化合物甲、乙、丙的“价一类”二维图如图所示,甲的焰色试验呈黄色。
回答下列问题:
(1)Q 在元素周期表中位于第_____周期第_____族;五种元素中,原子半径最大的是_____(填元素符号,下同),非金属性最强的是_____。
(2)X 与 Y 形成的 10 个电子的分子为_____(填化学式),与 Q 的单质反应的离子方程式为_____。
(3)Y 与 Z 形成的既含离子键又含非极性键的化合物的电子式为_____。甲与乙反应的离子方程式为_____。
(4)R 为与 M 同周期相邻主族的金属元素,下列说法正确的是_____(填标号)。
A. 的单质可与热水反应 B. 的最高价氧化物的水化物为强碱
C. 金属性: D. 的单质能从 的盐溶液中置换出 的单质
17. (12 分)我国化学家侯德榜发明的 “联合制碱法” 为世界制碱工业做出了巨大贡献, 联合制碱法主要过程和部分物质的溶解度曲线如图所示。
回答下列问题:
(1)生产过程涉及的部分物质 ④饱和食盐水中,属于电解质的是_____(填序号,下同),能导电的是_____;沉淀池中发生反应的化学方程式为_____。
(2)物质 X 的化学式为_____;循环_____(填 "I" 或 "II" )使原料 NaCl 的利用率从 70%提高到 90% 以上。为测定煅烧后固体中的 含量,将煅烧后固体充分加热,产生的气体先通过足量浓硫酸,再通过足量 增重 ,则固体中 的质量为_____g。
(3)向母液中加入 可促进副产品 的生成,根据 和 的溶解度曲线,为使 充分析出,需控制的适宜温度为_____(填标号)。
A. B. C. D.
(4)关于 和 的下列说法中,错误的是_____(填标号)。
A. 可利用 溶液使 转化为
B. “联合制碱法” 是利用 与其它物质的溶解度差异
C. 利用二者的热稳定性差异,可从它们的固体混合物中除去
D. 相同条件下,等质量的 和 与足量盐酸反应, 产生 多
18. (12 分) 乳酸亚铁是一种补铁剂,易溶于水,难溶于乙醇,可由乳酸与 反应制得。工业上以废料铁泥(主要成分是 ,含少量 )为原料制备乳酸亚铁的工艺流程如下:
已知: 与硫酸不反应,难溶于水。
回答下列问题:
(1)滤渣 1 的主要成分为_____(填化学式);“酸浸”时 发生反应的离子方程式为_____。
(2)"还原"时, Fe +发生反应的离子方程式为_____,可用_____(填试剂的化学式)检验 已经完全反应。
(3)滤渣 3 的主要成分为_____(填化学式)。“沉铁” 过程中发生反应的离子方程式为_____。
(4)"合成"过程中加入足量乳酸充分反应,同时加入少量铁粉,加入铁粉的作用是_____。获得乳酸亚铁晶体的系列操作是:溶液隔绝空气低温蒸发,冷却结晶,过滤, 用_____(填“水”或“乙醇”)洗涤晶体 次,干燥,制得乳酸亚铁晶体。
19. (12 分) 磺酰氯 是一种重要的化工原料,实验室用 和 催化制备 并检验 性质的装置如图所示,“ ”表示气体流向。
已知:① 的熔点为 ,沸点为 ,遇水剧烈反应。
② 和 反应过程中放出热量。
回答下列问题:
(1)仪器 A 的名称为_____,装置甲中发生反应的化学方程式为_____。
(2)装置乙中盛放试剂为_____,其作用为_____。
(3)实验过程中观察到装置丙中溶液颜色呈现如下图所示变化。对导致变色的物质
I、II、III 的正确判断是_____(填标号)。
A. B.
C. D.
丙装置实验体现了氯气的_____(填“氧化性”、“还原性”或“氧化性和还原性”)。
(4)冰水浴的作用是_____,戊装置中发生反应的化学方程式为_____,图示装置存在的一处缺陷是_____。 20. 胃舒平的有效成分为 ,测定其中 含量的操作如下(设该药片中的其它成分不与盐酸或 溶液反应)。
①加入 稀盐酸;
②用移液管量取 胃舒平悬浊液于锥形瓶中;
③ 配制 稀盐酸和 溶液;
④取 5 粒药片(0.10g/片),研碎,加入 蒸馏水充分搅拌;
⑤用 溶液中和过量的稀盐酸,记录所消耗 溶液的体积。 回答下列问题:
(1)正确的操作顺序是③④_____(填序号)。
(2)测定过程中发生反应的离子方程式为_____、_____。
(3)该测定实验共进行了 4 次。实验室现有 、 、 、 四种规格的容量瓶,则配制盐酸应选用的容量瓶规格最好为_____mL。用密度为 、质量分数为 36.5%的浓盐酸配制实验中所需稀盐酸,需用量筒量取浓盐酸的体积为_____mL。
配制溶液过程中,关于容量瓶的操作,正确的是_____(填标号)。
A. 查漏 B. 转移 C. 定容 D. 摇匀
(4)某同学 4 次测定所消耗的 溶液的体积如下:
实验序号 1 2 3 4
消耗 溶液体积/mL 15.90 17.30 16.10 16.00
胃舒平中 的质量分数为_____ (保留 3 位有效数字)。
(5)用 固体配制实验中所需的 溶液时,下列操作会使胃舒平中 含量测定值偏高的是_____。
A. 固体中含有 杂质
B. 定容时俯视容量瓶刻度线
C. 溶液未冷却至室温即进行定容
D. 摇匀后发现液面低于刻度线, 再加蒸馏水至刻度线
2024—2025学年度第一学期高一教学质量检测
化 学
注意事项:
1.答卷前,考生务必将自己的姓名,准考证号等填写在答题卡上。
2回答选择题时,选出每小题答案后,用铅笔把答题卡上对应题目的答案标号涂黑。如需改动,用橡皮擦干净后,再选涂其他答案标号。回答非选择题时,将答案写在答题卡上。写在本试卷上无效。
3考试结束后,将本试卷和答题卡一并交回。
可能用到的相对原子质量:H 1 C 12 O 16 Mn 55 Na 23 Al 27 Cl 35.5
一、选择题:本题共10小题,每小题2分,共20分. 每小题只有1个选项是符合题目要求。
1. 下列应用中不涉及氧化还原反应的是
A. 用作饮用水消毒剂 B. 用作食品干燥剂
C. 用作潜水艇的供氧剂 D. 溶液用作覆铜板腐蚀液
2. 实验安全至关重要, 下列实验操作、事故处理方法错误的是
A. 未用完的钠、钾、白磷需放回原试剂瓶
B. 火灾现场有大量活泼金属时需用潮湿的沙土来灭火
C. 皮肤溅上碱液,先用大量水冲洗,再用 2%的硼酸溶液冲洗
D. 氯气泄漏时, 应用浸有小苏打水的毛巾捂住口鼻向高处撤离
3. 下列化学用语或图示正确的是
A. 的结构式:
B. 的离子结构示意图:
C. 用电子式表示 的形成过程:
D. 在水中的电离方程式:
4. 下列图示实验中, 操作正确且能达到实验目的的是
A. 收集 B. 加热试管中的液体 C. 制取 胶体 D.制取
5. 下列物质均为离子化合物, 且化学键类型相同的是
A. 与 B. 与
C. 与 D. 与
6. 约里奥-居里夫妇用 粒子轰击 ,获得了首个人工放射性核素 ,其反应为
。下列说法错误的是
A. B. 与 互为同位素
C. 中子数为 14 D. 与 互为同素异形体
7. 设 为阿伏加德罗常数的值。下列说法错误的是
A. 溶液中含有的离子数为
B. 与足量 反应生成 的分子数为
C. 与足量铁粉充分反应转移的电子数为
D. 标准状况下, 与 混合气体中含有的原子数为
8. 下列有关说法错误的是
A. 钠、氧化钠、过氧化钠长期放置在空气中最终产物相同
B. 铁的化学性质比较活泼, 自然界中铁元素仅以化合态存在
C. 铝合金比铝硬度大的原因是原子层之间的相对滑动变得困难
D. 氢气在氯气中燃烧, 发出苍白色火焰, 瓶口上方有白雾生成
9. 工业上将 通入冷的 溶液中制得漂白液,下列说法错误的是
A. 溶液比 溶液稳定 B. 漂白液需在阴凉处避光保存
C. 通入 后的漂白液消毒能力增强 D. 漂白液的有效成分是 和
10. 实验室中利用下图装置验证铁与水蒸气的反应。下列说法错误的是
A. 酒精灯点燃的顺序:先①后②
B. 用火柴点燃肥皂泡检验生成的
C. 反应为
D. 由此可知炽热的铁水注入模具之前, 模具须干燥
二、选择题:本题共5小题,每小题4分,共20分。每小题只有一个或两个选项符合题意,全部选对得4分,选对但不全对的得2分,有选错的得0分。
11. 对下列粒子组在溶液中能否大量共存的判断和分析均正确的是
粒子组 判断和分析
A 不能大量共存, 因发生反应:
B 不能大量共存,因发生反应:
C 能大量共存, 粒子间不反应
D 能大量共存, 粒子间不反应
12. W、X、Y、Z 为原子序数依次增大的短周期主族元素,且最外层电子数之和为 20 , 与 同族, 是地壳中含量最多的元素。下列说法错误的是
A. 简单氢化物的稳定性:
B. 组成的化合物有还原性
C. 组成的化合物能与水反应
D. 最高价氧化物的水化物的酸性:
13. 根据实验操作和现象所得结论错误的是
实验操作和现象 结论
A 向待测液中滴加 溶液和稀 ,产生白色沉淀 待测液中含有
B 向 溶液中滴加几滴酸性 溶液,紫红色消失 具有还原性
C 向 溶液中滴加几滴新制氯水,溶液变为橙黄色 非金属性:
D 和 中均分别加入 溶液和盐酸, 只溶于盐酸, 都能溶 碱性:
14. 亚氯酸钠 是一种高效消毒剂,其制备流程如下。下列说法正确的是
A. 由反应①可知还原性:
B. 反应①中生成 转移 电子
C. 反应②中 做氧化剂, 是氧化产物
D. 理论上,制得 消耗 与 物质的量之和为
15. 探究 与 反应的实验装置、步骤和现象如下:
i. 打开 ,通入 至澄清石灰水变浑浊后,点燃酒精灯。
ii. 一段时间后,停止加热,关闭 。观察到硬质玻璃管中有白色物质产生,管壁上有黑色物质出现,检验 的试剂有明显现象。
iii. 将硬质玻璃管中的固体加水溶解,未见气泡产生; 过滤,向滤液中加入过量 溶液,产生白色沉淀;再次过滤,滤液呈碱性;取白色沉淀加入盐酸,产生气体。
下列说法错误的是
A. 步骤 的目的是排除 和水蒸气的干扰
B. 步骤 ii 中的黑色物质可能是碳单质
C. 步骤 iii 中的现象说明步骤 ii 中生成的白色物质为
D. 与 反应的产物可能为
三、非选择题:本题共5小题,共60分。
16. (12 分) “价一类”二维图是学习化学的一种重要工具。由原子序数依次增大的 X、Y、Z、M、Q 五种短周期元素形成的部分化合物甲、乙、丙的“价一类”二维图如图所示,甲的焰色试验呈黄色。
回答下列问题:
(1)Q 在元素周期表中位于第_____周期第_____族;五种元素中,原子半径最大的是_____(填元素符号,下同),非金属性最强的是_____。
(2)X 与 Y 形成的 10 个电子的分子为_____(填化学式),与 Q 的单质反应的离子方程式为_____。
(3)Y 与 Z 形成的既含离子键又含非极性键的化合物的电子式为_____。甲与乙反应的离子方程式为_____。
(4)R 为与 M 同周期相邻主族的金属元素,下列说法正确的是_____(填标号)。
A. 的单质可与热水反应 B. 的最高价氧化物的水化物为强碱
C. 金属性: D. 的单质能从 的盐溶液中置换出 的单质
17. (12 分)我国化学家侯德榜发明的 “联合制碱法” 为世界制碱工业做出了巨大贡献, 联合制碱法主要过程和部分物质的溶解度曲线如图所示。
回答下列问题:
(1)生产过程涉及的部分物质 ④饱和食盐水中,属于电解质的是_____(填序号,下同),能导电的是_____;沉淀池中发生反应的化学方程式为_____。
(2)物质 X 的化学式为_____;循环_____(填 "I" 或 "II" )使原料 NaCl 的利用率从 70%提高到 90% 以上。为测定煅烧后固体中的 含量,将煅烧后固体充分加热,产生的气体先通过足量浓硫酸,再通过足量 增重 ,则固体中 的质量为_____g。
(3)向母液中加入 可促进副产品 的生成,根据 和 的溶解度曲线,为使 充分析出,需控制的适宜温度为_____(填标号)。
A. B. C. D.
(4)关于 和 的下列说法中,错误的是_____(填标号)。
A. 可利用 溶液使 转化为
B. “联合制碱法” 是利用 与其它物质的溶解度差异
C. 利用二者的热稳定性差异,可从它们的固体混合物中除去
D. 相同条件下,等质量的 和 与足量盐酸反应, 产生 多
18. (12 分) 乳酸亚铁是一种补铁剂,易溶于水,难溶于乙醇,可由乳酸与 反应制得。工业上以废料铁泥(主要成分是 ,含少量 )为原料制备乳酸亚铁的工艺流程如下:
已知: 与硫酸不反应,难溶于水。
回答下列问题:
(1)滤渣 1 的主要成分为_____(填化学式);“酸浸”时 发生反应的离子方程式为_____。
(2)"还原"时, Fe +发生反应的离子方程式为_____,可用_____(填试剂的化学式)检验 已经完全反应。
(3)滤渣 3 的主要成分为_____(填化学式)。“沉铁” 过程中发生反应的离子方程式为_____。
(4)"合成"过程中加入足量乳酸充分反应,同时加入少量铁粉,加入铁粉的作用是_____。获得乳酸亚铁晶体的系列操作是:溶液隔绝空气低温蒸发,冷却结晶,过滤, 用_____(填“水”或“乙醇”)洗涤晶体 次,干燥,制得乳酸亚铁晶体。
19. (12 分) 磺酰氯 是一种重要的化工原料,实验室用 和 催化制备 并检验 性质的装置如图所示,“ ”表示气体流向。
已知:① 的熔点为 ,沸点为 ,遇水剧烈反应。
② 和 反应过程中放出热量。
回答下列问题:
(1)仪器 A 的名称为_____,装置甲中发生反应的化学方程式为_____。
(2)装置乙中盛放试剂为_____,其作用为_____。
(3)实验过程中观察到装置丙中溶液颜色呈现如下图所示变化。对导致变色的物质
I、II、III 的正确判断是_____(填标号)。
A. B.
C. D.
丙装置实验体现了氯气的_____(填“氧化性”、“还原性”或“氧化性和还原性”)。
(4)冰水浴的作用是_____,戊装置中发生反应的化学方程式为_____,图示装置存在的一处缺陷是_____。 20. 胃舒平的有效成分为 ,测定其中 含量的操作如下(设该药片中的其它成分不与盐酸或 溶液反应)。
①加入 稀盐酸;
②用移液管量取 胃舒平悬浊液于锥形瓶中;
③ 配制 稀盐酸和 溶液;
④取 5 粒药片(0.10g/片),研碎,加入 蒸馏水充分搅拌;
⑤用 溶液中和过量的稀盐酸,记录所消耗 溶液的体积。 回答下列问题:
(1)正确的操作顺序是③④_____(填序号)。
(2)测定过程中发生反应的离子方程式为_____、_____。
(3)该测定实验共进行了 4 次。实验室现有 、 、 、 四种规格的容量瓶,则配制盐酸应选用的容量瓶规格最好为_____mL。用密度为 、质量分数为 36.5%的浓盐酸配制实验中所需稀盐酸,需用量筒量取浓盐酸的体积为_____mL。
配制溶液过程中,关于容量瓶的操作,正确的是_____(填标号)。
A. 查漏 B. 转移 C. 定容 D. 摇匀
(4)某同学 4 次测定所消耗的 溶液的体积如下:
实验序号 1 2 3 4
消耗 溶液体积/mL 15.90 17.30 16.10 16.00
胃舒平中 的质量分数为_____ (保留 3 位有效数字)。
(5)用 固体配制实验中所需的 溶液时,下列操作会使胃舒平中 含量测定值偏高的是_____。
A. 固体中含有 杂质
B. 定容时俯视容量瓶刻度线
C. 溶液未冷却至室温即进行定容
D. 摇匀后发现液面低于刻度线, 再加蒸馏水至刻度线
同课章节目录
