8.2.2 稀酸的化学性质 课件(共21张PPT内嵌视频) 2024-2025学年化学科粤版九年级下册
文档属性
| 名称 | 8.2.2 稀酸的化学性质 课件(共21张PPT内嵌视频) 2024-2025学年化学科粤版九年级下册 |

|
|
| 格式 | pptx | ||
| 文件大小 | 42.0MB | ||
| 资源类型 | 试卷 | ||
| 版本资源 | 科粤版 | ||
| 科目 | 化学 | ||
| 更新时间 | 2025-01-20 00:00:00 | ||
图片预览








文档简介
(共21张PPT)
1.知道常见酸有相似的化学性质,了解一些反应的发生所需的条件。
2.通过对酸、碱的性质的开放性探究,养成“先个别后一般”的认识物质的科学方法,进一步发展科学探究能力。
工人师傅在电焊时,通常先用稀盐酸或稀硫酸对焊接面进行清洗,以使焊接后的接头更牢固。为什么用稀盐酸、稀硫酸清洗而不用水清洗呢
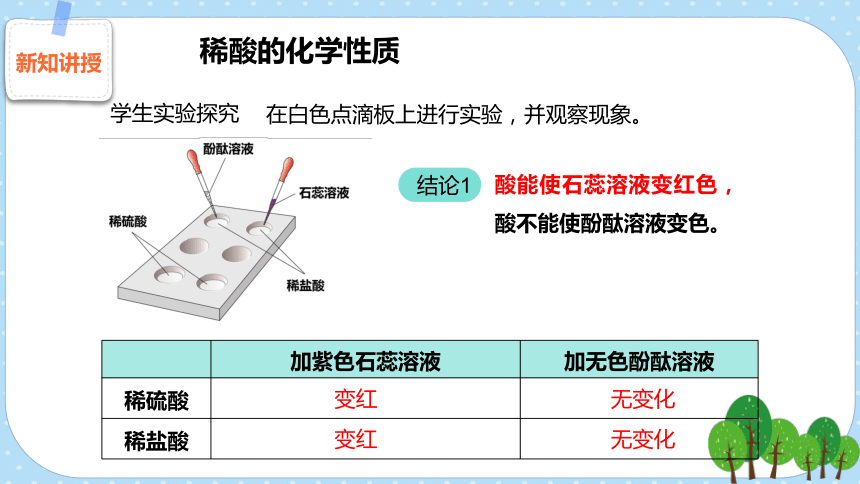
在白色点滴板上进行实验,并观察现象。
学生实验探究
加紫色石蕊溶液 加无色酚酞溶液
稀硫酸
稀盐酸
变红
无变化
变红
无变化
酸能使石蕊溶液变红色,酸不能使酚酞溶液变色。
结论1
稀酸的化学性质
回顾稀酸与较活泼金属的反应,写出化学方程式。
学生实验探究
与稀盐酸反应 与稀硫酸反应
镁
锌
铁
Mg +2HCl = MgCl2 + H2↑
Zn + 2HCl = ZnCl2 + H2↑
Zn + H2SO4 = ZnSO4 + H2↑
Mg + H2SO4 = MgSO4 + H2↑
Fe + H2SO4 = FeSO4 + H2↑
Fe + 2HCl = FeCl2 + H2↑
结论2
酸能与较活泼的金属(排在H前的金属)反应产生氢气。
上述金属与足量酸反应产生氢气最快的是 ,
相同质量的金属产生氢气最多的是 。
Mg
Al
实验8-7
在盛有稀盐酸和稀硫酸的试管里分别放入一根生锈(铁锈的主要成分是Fe2O3)的铁钉,观察现象。
用于金属表面除铁锈
酸能与某些金属氧化物反应生成水和该金属的化合物。
结论3
注意:反应前后化合价不变!
铁锈+稀盐酸 铁锈+稀硫酸
现象
化学方程式
铁锈逐渐消失,铁钉变得光亮,溶液由无色变为黄色
铁锈逐渐消失,铁钉变得光亮,溶液由无色变为黄色
Fe2O3+6HCl=FeCl3+3H2O
Fe2O3+3H2SO4=Fe2(SO4)3+3H2O
将铜丝和氧化铜固体加入稀硫酸中,发生的化学反应有
_______________________________________________
未打磨的镁条放入足量盐酸中,发生的化学反应
6 2AlCl3+3H2O
Al2O3 + HCl=______________
MgO +2HCl==MgCl2+ H2O Mg +2HCl==MgCl2+H2↑
CuO +H2SO4=CuSO4+ H2O
与金属氧化物反应,反应前后化合价不变;
与金属活动性无关。
现象:黑色粉末溶解,溶液由无色变蓝色。
小 组 讨 论
2.利用酸清除铁锈时,能否将金属制品长时间浸泡在酸中,为什么?
1.以上反应的生成物有什么共同之处?
酸 + 金属氧化物 → 盐 + 水
不能。
当铁钉表面的铁锈被清除完,酸将与铁发生反应。
如盐酸: Fe+2HCl=== FeCl2+H2↑
碳酸钙用于实验室制取二氧化碳
CaCO3 + 2HCl == CaCl2 + H2CO3
H2CO3 == H2O + CO2↑
CaCO3 + 2HCl == CaCl2 + H2O + CO2↑
交流讨论:根据上述反应,推断一下Na2CO3和NaHCO3能否与稀盐酸反应?如果能反应,它们又会生成什么物质?
碳酸钠(或碳酸氢钠)与稀盐酸的反应
实验8-8
碳酸钠(或碳酸氢钠)与稀盐酸的反应
碳酸钠+盐酸 碳酸氢钠+盐酸
现象 产生大量_______,澄清石灰水__________
分析 碳酸钠/碳酸氢钠与盐酸反应生成了_______气体
气泡
2 =2NaCl+CO2↑+H2O
变浑浊
CO2
= NaCl+CO2↑+H2O
盐 + 酸 = 新盐+新酸
Na2CO3+ HCl
NaHCO3+HCl
CaCO3+2HCl = CaCl2+ CO2 ↑ +H2O
结论4
1.写出下列反应的化学方程式:
(1) 硫酸跟氧化镁反应, 生成硫酸镁和水。
(2) 硫酸跟氯化钡反应, 生成硫酸钡和盐酸。
(3) 稀硫酸跟锌反应, 生成硫酸锌和氢气。
2.举例说明以下转变关系 (参照上题, 把题号填在下面的括号内):
例如 ( )
例如 ( )
例如 ( )
酸
+
较活泼金属 →氢气
金属氧化物 →水
盐→新酸
+ 盐
3
1
2
Zn+H2SO4=ZnSO4+H2↑
H2SO4+BaSO4=BaSO4+2HCl
H2SO4+MgO=MgSO4+H2O
1.酸能使紫色石蕊试液变红,不能使无色酚酞变色;
2.酸 + 金属 → 盐 + H2
(注:浓硫酸、硝酸除外;金属活动性排在H之前,除了钾、钙、钠)
3. 酸+金属氧化物→盐+ H2O
4. 酸+盐→新盐+新酸
稀酸的化学性质
1. 小明想除去卫生间瓷砖上的铁锈痕迹,在用清水洗涤之前,他从家中选择了一种最合适的物质对铁锈进行处理,这种物质是( )
A.汽油 B.食盐水
C.白醋 D.米酒
C
2.下列关于酸的说法错误的是( )
A.浓硫酸具有吸水性,浓盐酸具有挥发性
B.稀盐酸和稀硫酸都可用于金属除锈
C.稀盐酸能够使紫色石蕊溶液和无色酚酞溶液变红色
D.稀硫酸能够与活泼金属反应制取氢气
C
3.下列物质与稀盐酸反应的化学方程式正确的是( )
A
4.将生锈的铁钉放在盐酸中,最先看到的现象是铁锈逐渐溶解,溶液由无色变成黄色,反应的化学方程式为: ,当时间稍长时,又看到有气泡产生,其反应方程式为: 。
Fe2O3+6HCl=2FeCl3+3H2O
Fe+2HCl=FeCl2+H2↑
5.盐酸是一种重要的化工产品,也是实验室中重要的化学试剂。
(1)增大压强,HCl由气态变为液态,从微观的角度分析该变化过程中改变的是______________ 。
(2)在盐酸中加入过量的铁粉充分反应。
①可以看到的现象是_______________________________________________。
②下图表示该反应前后溶液中存在的主要离子,请写出每种图形代表的离子(填离子符号):
H+ Cl- Fe2+
分子的间隔
固体部分溶解,溶液由无色变为浅绿色,有气泡产生
1.知道常见酸有相似的化学性质,了解一些反应的发生所需的条件。
2.通过对酸、碱的性质的开放性探究,养成“先个别后一般”的认识物质的科学方法,进一步发展科学探究能力。
工人师傅在电焊时,通常先用稀盐酸或稀硫酸对焊接面进行清洗,以使焊接后的接头更牢固。为什么用稀盐酸、稀硫酸清洗而不用水清洗呢
在白色点滴板上进行实验,并观察现象。
学生实验探究
加紫色石蕊溶液 加无色酚酞溶液
稀硫酸
稀盐酸
变红
无变化
变红
无变化
酸能使石蕊溶液变红色,酸不能使酚酞溶液变色。
结论1
稀酸的化学性质
回顾稀酸与较活泼金属的反应,写出化学方程式。
学生实验探究
与稀盐酸反应 与稀硫酸反应
镁
锌
铁
Mg +2HCl = MgCl2 + H2↑
Zn + 2HCl = ZnCl2 + H2↑
Zn + H2SO4 = ZnSO4 + H2↑
Mg + H2SO4 = MgSO4 + H2↑
Fe + H2SO4 = FeSO4 + H2↑
Fe + 2HCl = FeCl2 + H2↑
结论2
酸能与较活泼的金属(排在H前的金属)反应产生氢气。
上述金属与足量酸反应产生氢气最快的是 ,
相同质量的金属产生氢气最多的是 。
Mg
Al
实验8-7
在盛有稀盐酸和稀硫酸的试管里分别放入一根生锈(铁锈的主要成分是Fe2O3)的铁钉,观察现象。
用于金属表面除铁锈
酸能与某些金属氧化物反应生成水和该金属的化合物。
结论3
注意:反应前后化合价不变!
铁锈+稀盐酸 铁锈+稀硫酸
现象
化学方程式
铁锈逐渐消失,铁钉变得光亮,溶液由无色变为黄色
铁锈逐渐消失,铁钉变得光亮,溶液由无色变为黄色
Fe2O3+6HCl=FeCl3+3H2O
Fe2O3+3H2SO4=Fe2(SO4)3+3H2O
将铜丝和氧化铜固体加入稀硫酸中,发生的化学反应有
_______________________________________________
未打磨的镁条放入足量盐酸中,发生的化学反应
6 2AlCl3+3H2O
Al2O3 + HCl=______________
MgO +2HCl==MgCl2+ H2O Mg +2HCl==MgCl2+H2↑
CuO +H2SO4=CuSO4+ H2O
与金属氧化物反应,反应前后化合价不变;
与金属活动性无关。
现象:黑色粉末溶解,溶液由无色变蓝色。
小 组 讨 论
2.利用酸清除铁锈时,能否将金属制品长时间浸泡在酸中,为什么?
1.以上反应的生成物有什么共同之处?
酸 + 金属氧化物 → 盐 + 水
不能。
当铁钉表面的铁锈被清除完,酸将与铁发生反应。
如盐酸: Fe+2HCl=== FeCl2+H2↑
碳酸钙用于实验室制取二氧化碳
CaCO3 + 2HCl == CaCl2 + H2CO3
H2CO3 == H2O + CO2↑
CaCO3 + 2HCl == CaCl2 + H2O + CO2↑
交流讨论:根据上述反应,推断一下Na2CO3和NaHCO3能否与稀盐酸反应?如果能反应,它们又会生成什么物质?
碳酸钠(或碳酸氢钠)与稀盐酸的反应
实验8-8
碳酸钠(或碳酸氢钠)与稀盐酸的反应
碳酸钠+盐酸 碳酸氢钠+盐酸
现象 产生大量_______,澄清石灰水__________
分析 碳酸钠/碳酸氢钠与盐酸反应生成了_______气体
气泡
2 =2NaCl+CO2↑+H2O
变浑浊
CO2
= NaCl+CO2↑+H2O
盐 + 酸 = 新盐+新酸
Na2CO3+ HCl
NaHCO3+HCl
CaCO3+2HCl = CaCl2+ CO2 ↑ +H2O
结论4
1.写出下列反应的化学方程式:
(1) 硫酸跟氧化镁反应, 生成硫酸镁和水。
(2) 硫酸跟氯化钡反应, 生成硫酸钡和盐酸。
(3) 稀硫酸跟锌反应, 生成硫酸锌和氢气。
2.举例说明以下转变关系 (参照上题, 把题号填在下面的括号内):
例如 ( )
例如 ( )
例如 ( )
酸
+
较活泼金属 →氢气
金属氧化物 →水
盐→新酸
+ 盐
3
1
2
Zn+H2SO4=ZnSO4+H2↑
H2SO4+BaSO4=BaSO4+2HCl
H2SO4+MgO=MgSO4+H2O
1.酸能使紫色石蕊试液变红,不能使无色酚酞变色;
2.酸 + 金属 → 盐 + H2
(注:浓硫酸、硝酸除外;金属活动性排在H之前,除了钾、钙、钠)
3. 酸+金属氧化物→盐+ H2O
4. 酸+盐→新盐+新酸
稀酸的化学性质
1. 小明想除去卫生间瓷砖上的铁锈痕迹,在用清水洗涤之前,他从家中选择了一种最合适的物质对铁锈进行处理,这种物质是( )
A.汽油 B.食盐水
C.白醋 D.米酒
C
2.下列关于酸的说法错误的是( )
A.浓硫酸具有吸水性,浓盐酸具有挥发性
B.稀盐酸和稀硫酸都可用于金属除锈
C.稀盐酸能够使紫色石蕊溶液和无色酚酞溶液变红色
D.稀硫酸能够与活泼金属反应制取氢气
C
3.下列物质与稀盐酸反应的化学方程式正确的是( )
A
4.将生锈的铁钉放在盐酸中,最先看到的现象是铁锈逐渐溶解,溶液由无色变成黄色,反应的化学方程式为: ,当时间稍长时,又看到有气泡产生,其反应方程式为: 。
Fe2O3+6HCl=2FeCl3+3H2O
Fe+2HCl=FeCl2+H2↑
5.盐酸是一种重要的化工产品,也是实验室中重要的化学试剂。
(1)增大压强,HCl由气态变为液态,从微观的角度分析该变化过程中改变的是______________ 。
(2)在盐酸中加入过量的铁粉充分反应。
①可以看到的现象是_______________________________________________。
②下图表示该反应前后溶液中存在的主要离子,请写出每种图形代表的离子(填离子符号):
H+ Cl- Fe2+
分子的间隔
固体部分溶解,溶液由无色变为浅绿色,有气泡产生
