(人教版)2016年中考化学知识点冲刺课件:第1讲-分子、原子、离子(12页)
文档属性
| 名称 | (人教版)2016年中考化学知识点冲刺课件:第1讲-分子、原子、离子(12页) |

|
|
| 格式 | zip | ||
| 文件大小 | 241.5KB | ||
| 资源类型 | 教案 | ||
| 版本资源 | 人教版(新课程标准) | ||
| 科目 | 化学 | ||
| 更新时间 | 2016-04-21 00:00:00 | ||
图片预览





文档简介
课件12张PPT。第1讲 构成物质的微粒——分子、原子、离子2.原子
(1)定义:原子是_________中的最小粒子。
(2)特点:在化学变化中,原子不能再分。
(3)物质构成:由原子构成的物质包括金属单质、稀有气体、某些固态非金属(例如______、_______)等。
(4)表示方法:原子用___________表示。例如:2个氧原子______.
3.离子
(1)定义:离子是带电荷的原子或原子团,带正电荷的离子叫________,带负电荷的离子叫________。
(2)物质构成:由离子构成的物质包括金属氧化物、碱类、盐类等。要求掌握氯化钠是由________构成。
(3)表示方法:在元素符号右上角标出离子所带的电荷及电性。例如:2个钠离子____________,1个硫酸根离子____________
4.分子和原子的比较
化学变化铜 氦元素符号2O阳离子阴离子离子SO42-2Na+第1讲 构成物质的微粒——分子、原子、离子5.原子和离子的比较小于原子化学等于大于第1讲 构成物质的微粒——分子、原子、离子二、原子的构成(1)在原子中:核电荷数=_______ =________,所以原子不显电性。
(2)原子核内质子数不一定等于核内中子数。
(3)普通氢原子核内无中子。
(4)原子的质量集中在________上。
(5)在化学变化中原子的种类不变,是指原子核没有发生变化,但核外电子数可以得失。负质子正中子中子不带电荷质子数 电子数原子核电子第1讲 构成物质的微粒——分子、原子、离子三、核外电子排布的初步知识
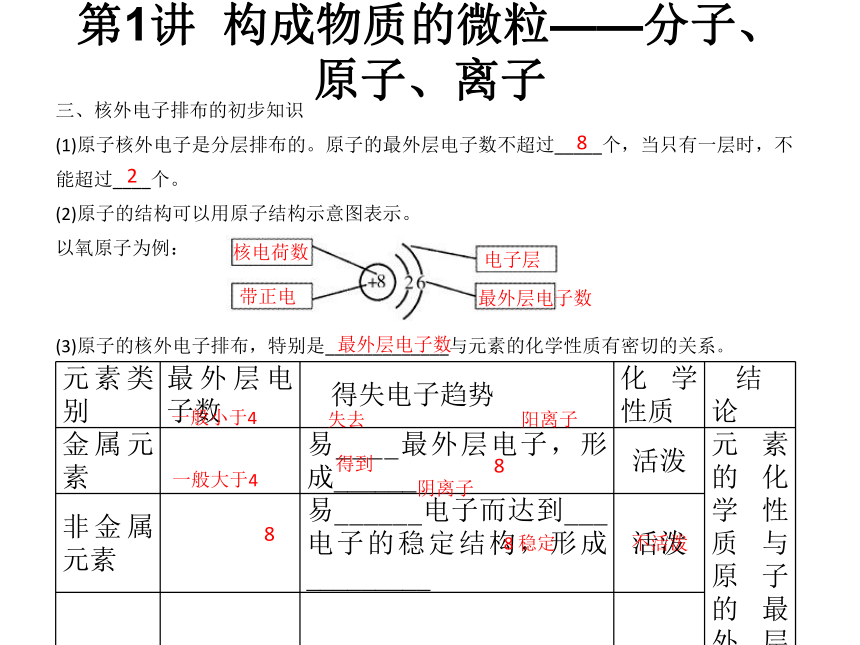
(1)原子核外电子是分层排布的。原子的最外层电子数不超过_____个,当只有一层时,不能超过____个。
(2)原子的结构可以用原子结构示意图表示。
以氧原子为例:(3)原子的核外电子排布,特别是_____________与元素的化学性质有密切的关系。8 稳定82核电荷数带正电电子层最外层电子数最外层电子数一般小于4失去阳离子一般大于48得到8阴离子不活泼第1讲 构成物质的微粒——分子、原子、离子[例题分析]
[例1]:原子的构成示意图如右图,下列叙述正确的是
A.原子是实心球体
B.原子、中子、电子均匀分布在原子中
C.质子与电子 质量相等
D.整个原子的质量主要集中在原子核上
【思路点拨】A、原子由带正电的原子核和核外带负电的电子构成,原子核又是由带正电的质子和不带电的中子构成,原子不是不可分割的实心球体,故A错误;
B、质子、中子、电子不是均匀分布在原子中,故B错误;
C、质子与电子质量不相等,故C错误;
D、原子质量主要集中在原子核上,故D正确.
【解答】D.第1讲 构成物质的微粒——分子、原子、离子 [例2]:右图是两种元素在周期表中的信息。请回答:
(1)氧元素的原子序数是 。
(2)若铝离子的结构示意图为: ,则Y= 。
(3)写出铝与氧气发生化合反应的化学方程式 。
【思路点拨】由元素周期表中元素的信息可知氧元素的原子序数为8,图中所说的是离子,可知是稳定结构,Y为8,铝与氧气发生化合反应的化学方程式的书写要正确,必须把氧化铝的化学式书写正确,并且会配平。
【解答】(1)8 (2)8 (3)4Al+3O2==2Al2O3(条件写加热、点燃也可)第1讲 构成物质的微粒——分子、原子、离子强化训练
A组
1.大树菠萝是湛江特产,它是世界上最重的水果.切开大树菠萝闻到阵阵果香,原因是( )
A.分子在不断运动 B.分子很大 C.分子之间有间隙 D.分子分解成原子
2.2014年5月,德国亥姆霍兹重离子研究中心再次成功合成117号元素。该元素已获正式名称“Ununseptium”,元素符号为Uus。该原子的原子核内有ll7个质子,原子质量约是氢原子质量的29倍,是目前获得正式承认的最重的原子。该原子的原子核外电子数为( )
A .1l7 B.174 C.291 D.408
3.现代客机外壳主要材料是铝锂合金。锂的原子结构示意图为 ,下列关于锂的说法错误的是( )
A.锂元素属于金属元素 B. 锂原子的质子数为3
C.锂元素在化合物中通常显+3价 D. 锂原子在化学反应中容易失去电子AAC第1讲 构成物质的微粒——分子、原子、离子4.右图是R原子结构示意图和磷元素的相关信息,下列说法错误的是( )
A.X=8
B.磷元素的相对原子质量为15
C.两种元素可形成化学式为P2R5的化合物
D.磷可以在R的单质中剧烈燃烧
5、将40mL水与40mL酒精混合,所得溶液体积小于80mL.下列对此现象的解释最合理的是( )
A.分子间是有间隔的 B.分子是由原子构成的
C.分子的质量和体积都很小 D.分子是不断运动的
6.下列对宏观事实的微观解释正确的是 ( )BAB第1讲 构成物质的微粒——分子、原子、离子7.下列物质中,含有氧分子的是( )
A.O2 B.MnO2 C.CO2 D.H2O2
8.下列现象用分子的相关知识解释不正确的是( )
A. 石油气经加压后贮存在钢罐中,说明分子间有间隔
B. 水冷却成冰后体积变大,说明分子的大小发生了改变
C. 湿衣服在太阳下晾晒干得快,说明分子运动速率与温度有关
D. 水在通电情况下分解成氢气和氧气,说明分子在化学变化中可分
9.用微粒的观点回答下列问题:
(1)保持水的化学性质的微粒是 。
(2)水通电分解过程中,不变的微粒是 。
(3)用湿抹布擦过的桌面,一段时间后变干的原因是 。
(4)一定质量的水蒸气冷凝成水时,其体积变小的原因是 。
10.用化学符号或者化学式填写:
(1)2个氢原子 。 (2) 五氧化二氮分子 。
(3)食盐水中的溶质 。(4)地壳中含量最高的金属元素 。Al分子原子水分子热运动水分子间间距减小2HN2O5NaClAB第1讲 构成物质的微粒——分子、原子、离子B组
11下面是钠元素和氯元素在元素周期表中的信息和3种粒子的结构示意图。请回答下列问题:
(1)氯原子的核电荷数是 ;钠原子与氯原子的最本质区别是 。
(2)在钠和氯气生成氯化钠的反应中,得到电子的是 原子;Na+的结构示意图
是 (填字母)。
12. (4分)根据下列粒子结构示意图,回答问题。
(1)上图A、B、C、D四种粒子共表示 种元素。
(2)D原子在化学反应中易 (填“得到”或“失去”)电子。
(3)由B元素和D元素组成的化合物的化学式为 。
(4)E粒子带1个单位正电荷,则X= 。17核电荷数(或质子数)不同氯(或Cl)A三得到MgCl211第1讲 构成物质的微粒——分子、原子、离子13.6分)在“宏观—微观—符号”之间建立联系,是学习化学的一种重要思维方式。下图是元素周期表中部分元素的原子结构示意图,根据所学知识回答下列问题。
(1)上图四种元素中,属于非金属元素的是 (填元素符号)。
(2)2个镁离子的符号为 ,铝原子的核电荷数X为 ,硅的氧化物的化学式为 。
(3)相对原子质量与原子真实质量之间存在紧密的关系(见下表),根据下表判断6.02×1023个钠原子的质量y为 。请归纳下表中的规律: 。 6.02×1023个原子的质量在数值上等于该原子的相对原子质量(或6.02×1023个不同原子的质量之比等于对应原子的相对原子质量之比)Si2Mg2+13SiO223g
(1)定义:原子是_________中的最小粒子。
(2)特点:在化学变化中,原子不能再分。
(3)物质构成:由原子构成的物质包括金属单质、稀有气体、某些固态非金属(例如______、_______)等。
(4)表示方法:原子用___________表示。例如:2个氧原子______.
3.离子
(1)定义:离子是带电荷的原子或原子团,带正电荷的离子叫________,带负电荷的离子叫________。
(2)物质构成:由离子构成的物质包括金属氧化物、碱类、盐类等。要求掌握氯化钠是由________构成。
(3)表示方法:在元素符号右上角标出离子所带的电荷及电性。例如:2个钠离子____________,1个硫酸根离子____________
4.分子和原子的比较
化学变化铜 氦元素符号2O阳离子阴离子离子SO42-2Na+第1讲 构成物质的微粒——分子、原子、离子5.原子和离子的比较小于原子化学等于大于第1讲 构成物质的微粒——分子、原子、离子二、原子的构成(1)在原子中:核电荷数=_______ =________,所以原子不显电性。
(2)原子核内质子数不一定等于核内中子数。
(3)普通氢原子核内无中子。
(4)原子的质量集中在________上。
(5)在化学变化中原子的种类不变,是指原子核没有发生变化,但核外电子数可以得失。负质子正中子中子不带电荷质子数 电子数原子核电子第1讲 构成物质的微粒——分子、原子、离子三、核外电子排布的初步知识
(1)原子核外电子是分层排布的。原子的最外层电子数不超过_____个,当只有一层时,不能超过____个。
(2)原子的结构可以用原子结构示意图表示。
以氧原子为例:(3)原子的核外电子排布,特别是_____________与元素的化学性质有密切的关系。8 稳定82核电荷数带正电电子层最外层电子数最外层电子数一般小于4失去阳离子一般大于48得到8阴离子不活泼第1讲 构成物质的微粒——分子、原子、离子[例题分析]
[例1]:原子的构成示意图如右图,下列叙述正确的是
A.原子是实心球体
B.原子、中子、电子均匀分布在原子中
C.质子与电子 质量相等
D.整个原子的质量主要集中在原子核上
【思路点拨】A、原子由带正电的原子核和核外带负电的电子构成,原子核又是由带正电的质子和不带电的中子构成,原子不是不可分割的实心球体,故A错误;
B、质子、中子、电子不是均匀分布在原子中,故B错误;
C、质子与电子质量不相等,故C错误;
D、原子质量主要集中在原子核上,故D正确.
【解答】D.第1讲 构成物质的微粒——分子、原子、离子 [例2]:右图是两种元素在周期表中的信息。请回答:
(1)氧元素的原子序数是 。
(2)若铝离子的结构示意图为: ,则Y= 。
(3)写出铝与氧气发生化合反应的化学方程式 。
【思路点拨】由元素周期表中元素的信息可知氧元素的原子序数为8,图中所说的是离子,可知是稳定结构,Y为8,铝与氧气发生化合反应的化学方程式的书写要正确,必须把氧化铝的化学式书写正确,并且会配平。
【解答】(1)8 (2)8 (3)4Al+3O2==2Al2O3(条件写加热、点燃也可)第1讲 构成物质的微粒——分子、原子、离子强化训练
A组
1.大树菠萝是湛江特产,它是世界上最重的水果.切开大树菠萝闻到阵阵果香,原因是( )
A.分子在不断运动 B.分子很大 C.分子之间有间隙 D.分子分解成原子
2.2014年5月,德国亥姆霍兹重离子研究中心再次成功合成117号元素。该元素已获正式名称“Ununseptium”,元素符号为Uus。该原子的原子核内有ll7个质子,原子质量约是氢原子质量的29倍,是目前获得正式承认的最重的原子。该原子的原子核外电子数为( )
A .1l7 B.174 C.291 D.408
3.现代客机外壳主要材料是铝锂合金。锂的原子结构示意图为 ,下列关于锂的说法错误的是( )
A.锂元素属于金属元素 B. 锂原子的质子数为3
C.锂元素在化合物中通常显+3价 D. 锂原子在化学反应中容易失去电子AAC第1讲 构成物质的微粒——分子、原子、离子4.右图是R原子结构示意图和磷元素的相关信息,下列说法错误的是( )
A.X=8
B.磷元素的相对原子质量为15
C.两种元素可形成化学式为P2R5的化合物
D.磷可以在R的单质中剧烈燃烧
5、将40mL水与40mL酒精混合,所得溶液体积小于80mL.下列对此现象的解释最合理的是( )
A.分子间是有间隔的 B.分子是由原子构成的
C.分子的质量和体积都很小 D.分子是不断运动的
6.下列对宏观事实的微观解释正确的是 ( )BAB第1讲 构成物质的微粒——分子、原子、离子7.下列物质中,含有氧分子的是( )
A.O2 B.MnO2 C.CO2 D.H2O2
8.下列现象用分子的相关知识解释不正确的是( )
A. 石油气经加压后贮存在钢罐中,说明分子间有间隔
B. 水冷却成冰后体积变大,说明分子的大小发生了改变
C. 湿衣服在太阳下晾晒干得快,说明分子运动速率与温度有关
D. 水在通电情况下分解成氢气和氧气,说明分子在化学变化中可分
9.用微粒的观点回答下列问题:
(1)保持水的化学性质的微粒是 。
(2)水通电分解过程中,不变的微粒是 。
(3)用湿抹布擦过的桌面,一段时间后变干的原因是 。
(4)一定质量的水蒸气冷凝成水时,其体积变小的原因是 。
10.用化学符号或者化学式填写:
(1)2个氢原子 。 (2) 五氧化二氮分子 。
(3)食盐水中的溶质 。(4)地壳中含量最高的金属元素 。Al分子原子水分子热运动水分子间间距减小2HN2O5NaClAB第1讲 构成物质的微粒——分子、原子、离子B组
11下面是钠元素和氯元素在元素周期表中的信息和3种粒子的结构示意图。请回答下列问题:
(1)氯原子的核电荷数是 ;钠原子与氯原子的最本质区别是 。
(2)在钠和氯气生成氯化钠的反应中,得到电子的是 原子;Na+的结构示意图
是 (填字母)。
12. (4分)根据下列粒子结构示意图,回答问题。
(1)上图A、B、C、D四种粒子共表示 种元素。
(2)D原子在化学反应中易 (填“得到”或“失去”)电子。
(3)由B元素和D元素组成的化合物的化学式为 。
(4)E粒子带1个单位正电荷,则X= 。17核电荷数(或质子数)不同氯(或Cl)A三得到MgCl211第1讲 构成物质的微粒——分子、原子、离子13.6分)在“宏观—微观—符号”之间建立联系,是学习化学的一种重要思维方式。下图是元素周期表中部分元素的原子结构示意图,根据所学知识回答下列问题。
(1)上图四种元素中,属于非金属元素的是 (填元素符号)。
(2)2个镁离子的符号为 ,铝原子的核电荷数X为 ,硅的氧化物的化学式为 。
(3)相对原子质量与原子真实质量之间存在紧密的关系(见下表),根据下表判断6.02×1023个钠原子的质量y为 。请归纳下表中的规律: 。 6.02×1023个原子的质量在数值上等于该原子的相对原子质量(或6.02×1023个不同原子的质量之比等于对应原子的相对原子质量之比)Si2Mg2+13SiO223g
同课章节目录
