江苏省无锡市2024-2025学年届高三上学期期终教学质量调研测试化学试卷(图片版,含答案)
文档属性
| 名称 | 江苏省无锡市2024-2025学年届高三上学期期终教学质量调研测试化学试卷(图片版,含答案) |
|
|
| 格式 | docx | ||
| 文件大小 | 1.1MB | ||
| 资源类型 | 教案 | ||
| 版本资源 | 通用版 | ||
| 科目 | 化学 | ||
| 更新时间 | 2025-01-21 00:00:00 | ||
图片预览



文档简介
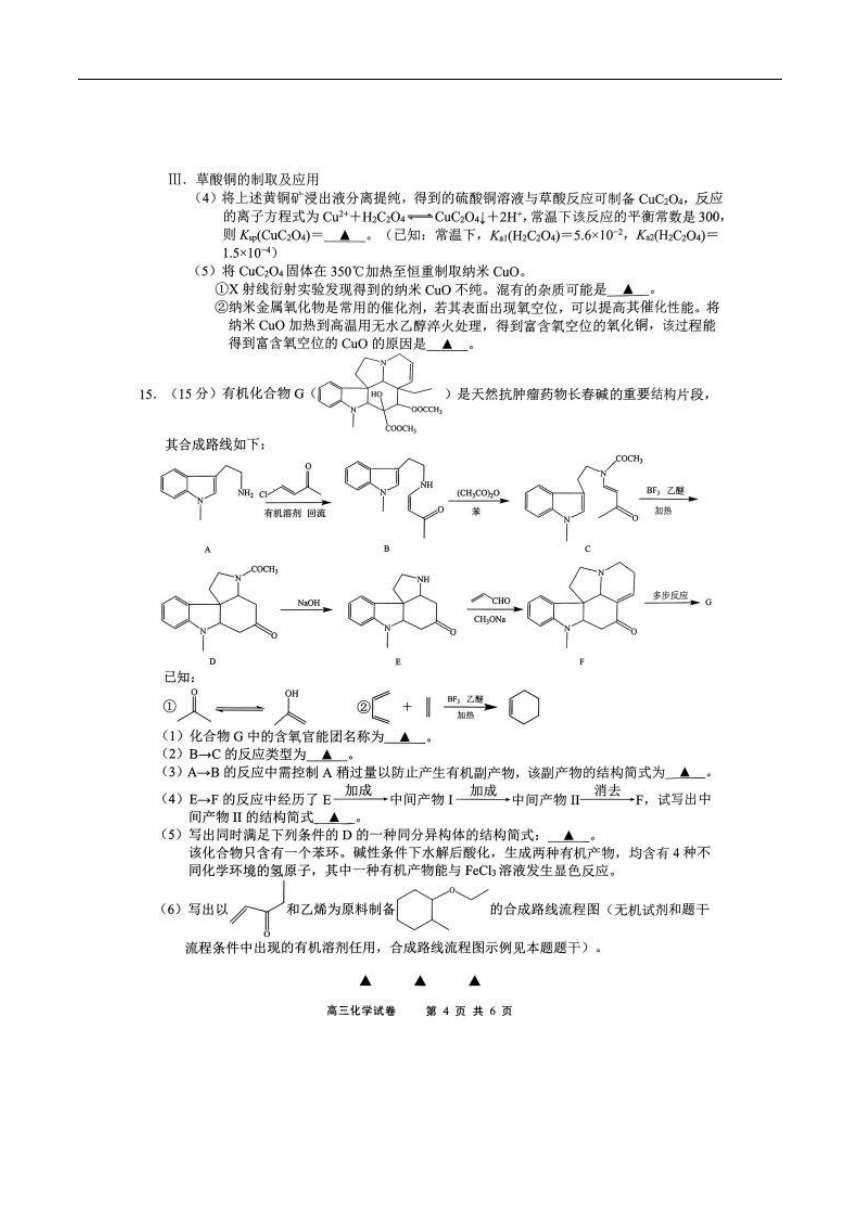
Ⅲ.草酸铜的制取及应用
(4)将上述黄铜矿浸出液分离提纯,得到的硫酸铜溶液与草酸反应可制备CC2O4,反应
的离子方程式为Cu2+十HC204一CuC204!十2H,常温下该反应的平衡常数是300,
则Kp(CuC204)=▲一。(已知:常温下,K1(HC204)=5.6×102,K(HC204)=
1.5×10-4)
(5)将CuC2O4固体在350℃加热至恒重制取纳米Cu0。
①X射线衍射实验发现得到的纳米CO不纯。混有的杂质可能是▲。
②纳米金属氧化物是常用的催化剂,若其表面出现氧空位,可以提高其催化性能。将
纳米C0加热到高温用无水乙醇淬火处理,得到富含氧空位的氧化铜,该过程能
得到富含氧空位的CO的原因是▲。
15.(15分)有机化合物G
)是天然抗肿瘤药物长春碱的重要结构片段,
0●H
COOCH
其合成路线如下:
COCH
(CH COO
BF乙醇
有机溶剂回流
加热
多步反应。G
已知:
OH
①
②+1
F,乙
(1)化合物G中的含氧官能团名称为▲一。
(2)B→C的反应类型为▲。
(3)A→B的反应中需控制A稍过量以防止产生有机副产物,该副产物的结构简式为▲。
(4)E一F的反应中经历了E加成中间产物1加成中间产物Ⅱ消去F,试写出中
间产物Ⅱ的结构简式▲一。
(5)写出同时满足下列条件的D的一种同分异构体的结构简式:▲。
该化合物只含有一个苯环。碱性条件下水解后酸化,生成两种有机产物,均含有4种不
同化学环境的氢原子,其中一种有机产物能与FC溶液发生显色反应。
(6)写出以
和乙烯为原料制备
的合成路线流程图(无机试剂和题干
流程条件中出现的有机溶剂任用,合成路线流程图示例见本题题干)。
▲
▲
▲
高三化学试卷第4页共6页
16.(15分)回收错铁合金抛光废料(含Fe和少量Pr及杂质),可制备Pr6O1和Pr(OH,错
铁合金抛光废料经除铁、萃取、反萃取可得PC3溶液。Pr的常见化合价为十3和十4。
(1)沉淀Pr3+。搅拌下,将一定量的PCl溶液与沉淀剂NaCO,溶液充分反应,过滤得到
Pr(COh8H0沉淀,发生反应的化学方程式为▲。沉淀剂用Na2CO3溶液比用
NHHCO3溶液得到的沉淀颗粒更加致密,可能的原因是▲一。
(2)PrOu的制备和性质。
①将P2(C0)38H0置于空气中灼烧,测得剩余固体质量与起始固体质量的比值随温度变
化的曲线如题16图所示。制备P6O最适宜的温度为▲(写出计算过程)
②将0.5gPr6011加入到20mL30%H0z酸性溶液中产生大量气泡,反应后错元素仅以
P+的形式存在。该反应的离子方程式为▲。
100
皮
90
脑
80
(280,76.23)
70
(560.61.72)
60
(755,56.22)
50
(1200,54.46)
200400
60080010001200
温度/℃
题16图
(3)Pr(OHD3的制备。
用萃取剂P507HA月苯取PP的原理:P3A
萃取
3H+PHA2为(有机层)。
已知:①P507对Pr3+和Fc3+、Fe2*都有萃取作用,对杂质离子无萃取作用。
②Pr3+开始沉淀的pH为8,Fe+完全沉淀的pH为3.7,Fe2完全沉淀的pH为9.7。
为获得较高纯度P(OHD5,请补充完整实验方案:将一定量错铁合金抛光废料加入到稀
盐酸中,▲,浓缩后得PrC溶液,向溶液中滴加l.0 mol'L-I NaOH溶液至不再产
生沉淀,过滤,用蒸馏水洗涤,将固体干燥,得到P(OH)。
(须选用的试剂和仪器:1.0molL1HCl溶液、1.0molL-1NaOH溶液、1.0mol-L1HzO2
溶液、P507、分液漏斗)·
17.(16分)C02的分离回收和资源化利用具有重要意义。
I.C02的分离回收
乙醇胺类水溶液对C02气体具有优良的吸收性能。在20~40℃条件下,单乙醇胺
(HOCH2CH2NH)水溶液吸收CO2生成单乙醇氨基碳酸盐,升温至较高温度可实现吸收剂
的再生。在吸收过程中,部分单乙醇胺会与CO2反应生成单乙醇氨基甲酸盐,对设备有
强腐蚀性。N甲基二乙醇胺[(CH)N(CH2CH2OH]水溶液吸收CO2时,生成氨基碳酸氢
盐,较低温度即可实现吸收剂再生。
(1)单乙醇胺水溶液吸收CO2生成单乙醇氨基碳酸盐的反应是▲(填“吸热”或“放
热”)反应。
(2)利用20%单乙醇胺水溶液吸收C02,测得高于40℃时,单乙醇胺水溶液吸收C02
的吸收率随温度升高呈现下降趋势,其主要原因是▲。
(3)单乙醇胺与CO2反应生成单乙醇氨基甲酸盐,该过程分两步进行:
HOCH,CHNH2CGO X HOCH.CHHY(单乙醇氨基甲酸盐)
①
③
其中第①步反应类型为▲。
(4)与N甲基二乙醇胺相比,单乙醇胺作为CO2吸收剂的缺点是▲。
高三化学试卷
第5页共6页
(4)将上述黄铜矿浸出液分离提纯,得到的硫酸铜溶液与草酸反应可制备CC2O4,反应
的离子方程式为Cu2+十HC204一CuC204!十2H,常温下该反应的平衡常数是300,
则Kp(CuC204)=▲一。(已知:常温下,K1(HC204)=5.6×102,K(HC204)=
1.5×10-4)
(5)将CuC2O4固体在350℃加热至恒重制取纳米Cu0。
①X射线衍射实验发现得到的纳米CO不纯。混有的杂质可能是▲。
②纳米金属氧化物是常用的催化剂,若其表面出现氧空位,可以提高其催化性能。将
纳米C0加热到高温用无水乙醇淬火处理,得到富含氧空位的氧化铜,该过程能
得到富含氧空位的CO的原因是▲。
15.(15分)有机化合物G
)是天然抗肿瘤药物长春碱的重要结构片段,
0●H
COOCH
其合成路线如下:
COCH
(CH COO
BF乙醇
有机溶剂回流
加热
多步反应。G
已知:
OH
①
②+1
F,乙
(1)化合物G中的含氧官能团名称为▲一。
(2)B→C的反应类型为▲。
(3)A→B的反应中需控制A稍过量以防止产生有机副产物,该副产物的结构简式为▲。
(4)E一F的反应中经历了E加成中间产物1加成中间产物Ⅱ消去F,试写出中
间产物Ⅱ的结构简式▲一。
(5)写出同时满足下列条件的D的一种同分异构体的结构简式:▲。
该化合物只含有一个苯环。碱性条件下水解后酸化,生成两种有机产物,均含有4种不
同化学环境的氢原子,其中一种有机产物能与FC溶液发生显色反应。
(6)写出以
和乙烯为原料制备
的合成路线流程图(无机试剂和题干
流程条件中出现的有机溶剂任用,合成路线流程图示例见本题题干)。
▲
▲
▲
高三化学试卷第4页共6页
16.(15分)回收错铁合金抛光废料(含Fe和少量Pr及杂质),可制备Pr6O1和Pr(OH,错
铁合金抛光废料经除铁、萃取、反萃取可得PC3溶液。Pr的常见化合价为十3和十4。
(1)沉淀Pr3+。搅拌下,将一定量的PCl溶液与沉淀剂NaCO,溶液充分反应,过滤得到
Pr(COh8H0沉淀,发生反应的化学方程式为▲。沉淀剂用Na2CO3溶液比用
NHHCO3溶液得到的沉淀颗粒更加致密,可能的原因是▲一。
(2)PrOu的制备和性质。
①将P2(C0)38H0置于空气中灼烧,测得剩余固体质量与起始固体质量的比值随温度变
化的曲线如题16图所示。制备P6O最适宜的温度为▲(写出计算过程)
②将0.5gPr6011加入到20mL30%H0z酸性溶液中产生大量气泡,反应后错元素仅以
P+的形式存在。该反应的离子方程式为▲。
100
皮
90
脑
80
(280,76.23)
70
(560.61.72)
60
(755,56.22)
50
(1200,54.46)
200400
60080010001200
温度/℃
题16图
(3)Pr(OHD3的制备。
用萃取剂P507HA月苯取PP的原理:P3A
萃取
3H+PHA2为(有机层)。
已知:①P507对Pr3+和Fc3+、Fe2*都有萃取作用,对杂质离子无萃取作用。
②Pr3+开始沉淀的pH为8,Fe+完全沉淀的pH为3.7,Fe2完全沉淀的pH为9.7。
为获得较高纯度P(OHD5,请补充完整实验方案:将一定量错铁合金抛光废料加入到稀
盐酸中,▲,浓缩后得PrC溶液,向溶液中滴加l.0 mol'L-I NaOH溶液至不再产
生沉淀,过滤,用蒸馏水洗涤,将固体干燥,得到P(OH)。
(须选用的试剂和仪器:1.0molL1HCl溶液、1.0molL-1NaOH溶液、1.0mol-L1HzO2
溶液、P507、分液漏斗)·
17.(16分)C02的分离回收和资源化利用具有重要意义。
I.C02的分离回收
乙醇胺类水溶液对C02气体具有优良的吸收性能。在20~40℃条件下,单乙醇胺
(HOCH2CH2NH)水溶液吸收CO2生成单乙醇氨基碳酸盐,升温至较高温度可实现吸收剂
的再生。在吸收过程中,部分单乙醇胺会与CO2反应生成单乙醇氨基甲酸盐,对设备有
强腐蚀性。N甲基二乙醇胺[(CH)N(CH2CH2OH]水溶液吸收CO2时,生成氨基碳酸氢
盐,较低温度即可实现吸收剂再生。
(1)单乙醇胺水溶液吸收CO2生成单乙醇氨基碳酸盐的反应是▲(填“吸热”或“放
热”)反应。
(2)利用20%单乙醇胺水溶液吸收C02,测得高于40℃时,单乙醇胺水溶液吸收C02
的吸收率随温度升高呈现下降趋势,其主要原因是▲。
(3)单乙醇胺与CO2反应生成单乙醇氨基甲酸盐,该过程分两步进行:
HOCH,CHNH2CGO X HOCH.CHHY(单乙醇氨基甲酸盐)
①
③
其中第①步反应类型为▲。
(4)与N甲基二乙醇胺相比,单乙醇胺作为CO2吸收剂的缺点是▲。
高三化学试卷
第5页共6页
同课章节目录
