2024-2025学年高二下学期化学人教版(2019)选择性必修3 有机化学专项训练(含答案)
文档属性
| 名称 | 2024-2025学年高二下学期化学人教版(2019)选择性必修3 有机化学专项训练(含答案) |
|
|
| 格式 | docx | ||
| 文件大小 | 988.2KB | ||
| 资源类型 | 教案 | ||
| 版本资源 | 人教版(2019) | ||
| 科目 | 化学 | ||
| 更新时间 | 2025-02-06 00:00:00 | ||
图片预览

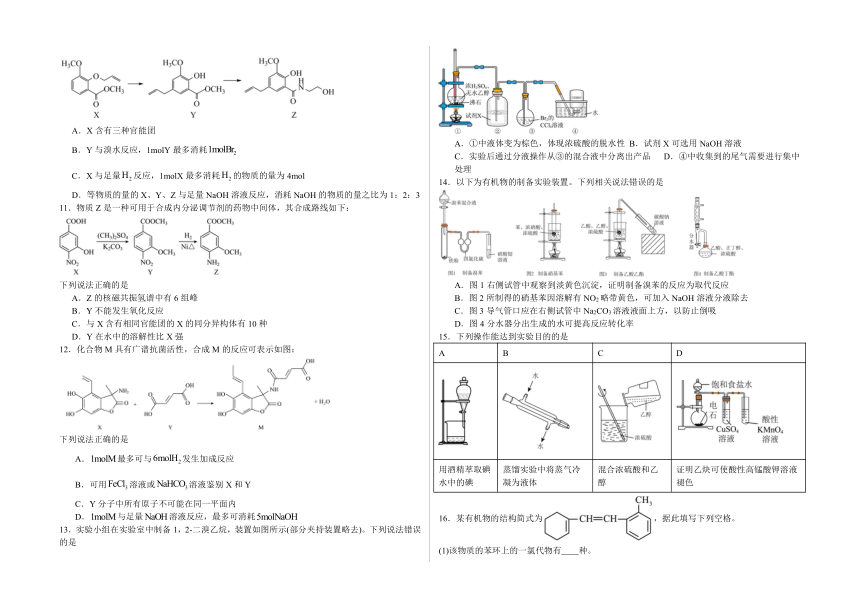

文档简介
高二化学有机化学专项训练
1.文房四宝是中华传统文化的瑰宝。下列有关叙述错误的是
A.羊毛可用于制毛笔,主要成分为蛋白质
B.松木可用于制墨,墨的主要成分是单质碳
C.竹子可用于造纸,纸的主要成分是纤维素
D.大理石可用于制砚台,主要成分为硅酸盐
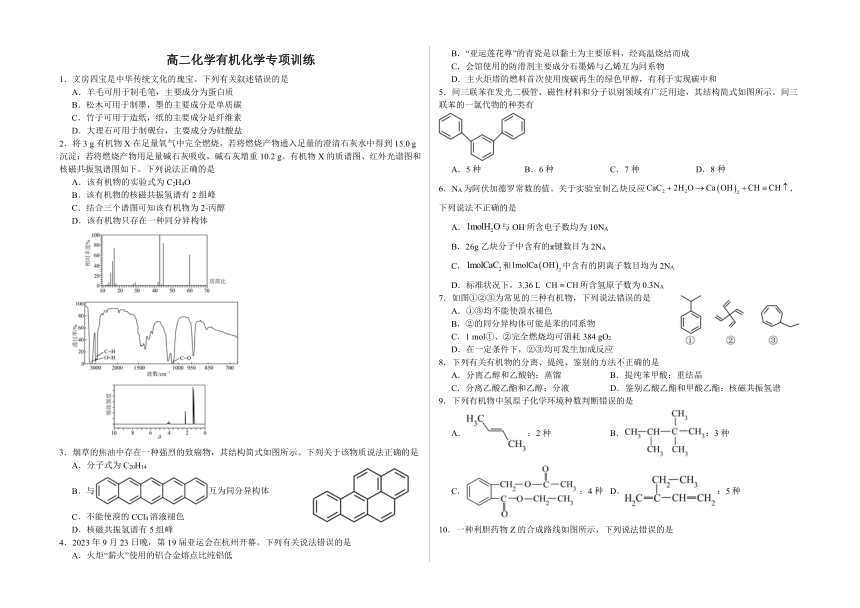
2.将3 g有机物X在足量氧气中完全燃烧,若将燃烧产物通入足量的澄清石灰水中得到15.0 g沉淀;若将燃烧产物用足量碱石灰吸收,碱石灰增重10.2 g。有机物X的质谱图、红外光谱图和核磁共振氢谱图如下。下列说法正确的是
A.该有机物的实验式为C2H4O
B.该有机物的核磁共振氢谱有2组峰
C.结合三个谱图可知该有机物为2-丙醇
D.该有机物只存在一种同分异构体
3.烟草的焦油中存在一种强烈的致癌物,其结构简式如图所示。下列关于该物质说法正确的是
A.分子式为C20H14
B.与互为同分异构体
C.不能使溴的CCl4溶液褪色
D.核磁共振氢谱有5组峰
4.2023年9月23日晚,第19届亚运会在杭州开幕。下列有关说法错误的是
A.火炬“薪火”使用的铝合金熔点比纯铝低
B.“亚运莲花尊”的青瓷是以黏土为主要原料,经高温烧结而成
C.会馆使用的防滑剂主要成分石墨烯与乙烯互为同系物
D.主火炬塔的燃料首次使用废碳再生的绿色甲醇,有利于实现碳中和
5.间三联苯在发光二极管、磁性材料和分子识别领域有广泛用途,其结构简式如图所示。间三联苯的一氯代物的种类有
A.5种 B.6种 C.7种 D.8种
6.NA为阿伏加德罗常数的值。关于实验室制乙炔反应,下列说法不正确的是
A.与OH-所含电子数均为10NA
B.26g乙炔分子中含有的π键数目为2NA
C.和中含有的阴离子数目均为2NA
D.标准状况下,3.36 L 所含氢原子数为0.3NA
7.如图①②③为常见的三种有机物,下列说法错误的是
A.①③均不能使溴水褪色
B.②的同分异构体可能是苯的同系物
C.1 mol①、②完全燃烧均可消耗384 gO2
D.在一定条件下,②③均可发生加成反应
8.下列有关有机物的分离、提纯、鉴别的方法不正确的是
A.分离乙醇和乙酸钠:蒸馏 B.提纯苯甲酸:重结晶
C.分离乙酸乙酯和乙醇:分液 D.鉴别乙酸乙酯和甲酸乙酯:核磁共振氢谱
9.下列有机物中氢原子化学环境种数判断错误的是
A.:2种 B.:3种
C.:4种 D.:5种
10.一种利胆药物Z的合成路线如图所示,下列说法错误的是
A.X含有三种官能团
B.Y与溴水反应,1molY最多消耗
C.X与足量反应,1molX最多消耗的物质的量为4mol
D.等物质的量的X、Y、Z与足量NaOH溶液反应,消耗NaOH的物质的量之比为1:2:3
11.物质Z是一种可用于合成内分泌调节剂的药物中间体,其合成路线如下:
下列说法正确的是
A.Z的核磁共振氢谱中有6组峰
B.Y不能发生氧化反应
C.与X含有相同官能团的X的同分异构体有10种
D.Y在水中的溶解性比X强
12.化合物M具有广谱抗菌活性,合成M的反应可表示如图:
下列说法正确的是
A.最多可与发生加成反应
B.可用溶液或溶液鉴别X和Y
C.Y分子中所有原子不可能在同一平面内
D.与足量溶液反应,最多可消耗
13.实验小组在实验室中制备1,2-二溴乙烷,装置如图所示(部分夹持装置略去)。下列说法错误的是
A.①中液体变为棕色,体现浓硫酸的脱水性 B.试剂X可选用NaOH溶液
C.实验后通过分液操作从③的混合液中分离出产品 D.④中收集到的尾气需要进行集中处理
14.以下为有机物的制备实验装置。下列相关说法错误的是
A.图1右侧试管中观察到淡黄色沉淀,证明制备溴苯的反应为取代反应
B.图2所制得的硝基苯因溶解有NO2略带黄色,可加入NaOH溶液分液除去
C.图3导气管口应在右侧试管中Na2CO3溶液液面上方,以防止倒吸
D.图4分水器分出生成的水可提高反应转化率
15.下列操作能达到实验目的的是
A B C D
用酒精萃取碘水中的碘 蒸馏实验中将蒸气冷凝为液体 混合浓硫酸和乙醇 证明乙炔可使酸性高锰酸钾溶液褪色
16.某有机物的结构简式为,据此填写下列空格。
(1)该物质的苯环上的一氯代物有 种。
(2)1 mol 该物质和溴水混合,消耗Br2的物质的量为 mol。
(3)1 mol 该物质和H2加成需H2 mol。
(4)下列说法不正确的是 (填字母) 。
A.此物质可发生加成、取代、氧化等反应 B.和甲苯互为同系物
(5)电器包装中大量使用的泡沫塑料的主要成分是聚苯乙烯(),它是由 (写结构简式)聚合而成的。
(6)CH2=CHCl与聚苯乙烯的单体在一定条件下可发生加聚反应,所得产物的结构简式为 。
17.二氧化碳的转化与综合利用是实现“碳达峰”“碳中和”战略的重要途径。近期,我国学者以电催化反应为关键步骤,用CO2作原料,实现了重要医药中间体——阿托酸的合成,其合成路线如下:
(1)阿托酸所含官能团名称为碳碳双键、 。
(2)A→B的反应类型为 。
(3)A的含有苯环且能发生银镜反应的同分异构体数目为 ,其中在核磁共振氢谱中呈现四组峰的结构简式为 。
(4)写出B→C反应方程式: 。
(5)C→D反应所需试剂及条件为 。
(6)在D→E反应中,用Mg作阳极、Pt作阴极进行电解,则CO2与D的反应在 (填“阳极”或“阴极”)上进行。
(7)下列关于E的叙述错误的是 (填序号)。
a.可发生聚合反应
b.分子内9个碳原子共平面
c.分子内含有1个手性碳原子
d.可形成分子内氢键和分子间氢键
(8)结合题干信息,完成以下合成路线: 。
( )
18.一种以甲苯为原料合成有机物M的设计路线如下:
已知:R-Br
回答下列问题:
(1)B所含官能团的名称是 。
(2)A的名称是 ,A→B中加入Fe的目的是 。
(3)甲苯→A的反应类型是 ,甲苯→C的化学方程式为 。
(4)在制药行业中常用“成盐修饰”改善物质的理化性质,若用饱和溶液对E进行“成盐修饰”,可将E转化为 (用结构简式表示)。
(5)用结构简式表示满足下列条件的D的同分异构体 。
①苯环上只有两个取代基;
②核磁共振氢谱中有6组吸收峰;
③分子中只含有1个手性碳原子
(6)根据已有知识并结合上述合成路线图的相关信息,写出以乙烯为原料,选用必要的无机试剂,合成高分子物质 的路线图(请用结构简式表示有机物,用“→”表示转化关系,并在“→”上注明试剂和反应条件) 。
19.乙酸正丁酯在香料、色谱分析、塑料加工、制药等领域中均有广泛应用。实验室中按照下列流程制取乙酸正丁酯并测定其结构。有关物质的部分性质如下表:
物质 相对分子质量 密度 沸点(℃) 水溶性
乙酸 60 1.045 118.1 互溶
正丁醇 74 0.80 118.0 可溶
乙酸正丁酯 116 0.882 126.1 微溶
Ⅰ.用如图所示装置合成乙酸正丁酯粗产品
将乙酸、正丁醇、3~4滴浓硫酸依次加入A中,混匀后投入沸石,接通冷却水,加热至反应完全,得到乙酸正丁酯粗产品。
(1)仪器A的名称是 ;冷却水由 (填“a”或“b”)通入更合理。
(2)制备乙酸正丁酯的化学方程式为 。
(3)从平衡移动的角度分析,分水器的作用是 。
Ⅱ.通过下列步骤精制粗产品
(4)操作1的名称是 ;饱和溶液的作用 、 以及降低乙酸正丁酯的溶解度便于分层。
(5)下列各组物质的分离或提纯过程也需要用到“操作2”的是_____(填字母)。
A.除去乙烷气体中的乙烯 B.除去苯甲酸中的氯化钠
C.分离邻二甲苯和水 D.分离三氯甲烷和四氯化碳
(6)通过上述步骤最终获得乙酸正丁酯,则乙酸正丁酯的产率为 。
20.心血管药物缬沙坦中间体(F)的两条合成路线如下:
已知:
Ⅰ.+
Ⅱ.R1CHOR1CH2NHR2
回答下列问题:
(1)A结构简式为 ;B→C反应类型为 。
(2)C+D→F化学方程式为 。
(3)E中含氧官能团名称为 ;F中手性碳原子有 个。
(4)D的一种同分异构体含硝基和3种不同化学环境的氢原子(个数比为6∶6∶1),其结构简式为 。
(5)C→E的合成路线设计如下:
CG(C14H11NO)E
试剂X为 (填化学式);试剂Y不能选用KMnO4,原因是
。
21.吡咯类化合物在导电聚合物、化学传感器及药物制剂上有着广泛应用,一种合成1-(4-甲氧基苯基)-2,5-二甲基吡咯(用吡咯X表示)的反应和方法如下:
实验装置如图所示,将100 mmol己-2,5-二酮(熔点:-5.5 ℃,密度:0.737 g·cm-3)与100 mmol 4-甲氧基苯胺(熔点:57 ℃)放入①中,搅拌。待反应完成后,加入50%的乙醇溶液,析出浅棕色固体。加热至65 ℃,至固体溶解,加入脱色剂,回流20 min,趁热过滤。滤液静置至室温,冰水浴冷却,有大量白色固体析出。经过滤、洗涤、干燥得到产品。
回答下列问题:
(1)量取己-2,5-二酮应使用的仪器为 (填名称)。
(2)仪器①用铁夹固定在③上,③的名称是 ;仪器②的名称是 。
(3)“搅拌”的作用是 。
(4)“加热”方式为 。
(5)使用的“脱色剂”是 。
(6)“趁热过滤”的目的是 ;
用 洗涤白色固体。
(7)若需进一步提纯产品,可采用的方法是 。
高二化学参考答案:
1-5.DCCCB 6-10.CACCD 11-15.ABCBD
16.(1)4 (2)2 (3)5 (4)B (5)
(6)、、、
17.(1)羧基 (2)加成反应(或还原反应) (3) 4
(4)+H2O
(5)O2,△/催化剂 (6)阴极 (7)b
(8)。
18.(1)氨基
(2) 对硝基甲苯(或1-甲基-4-硝基苯或4-硝基甲苯 ) 将硝基还原为氨基
(3) 取代反应或硝化反应 +Br2 +HBr
(4) (5)
(6)
19.(1) 圆底烧瓶 b
(2)
(3)将水分离出体系,促进平衡向正反应方向移动,进而提高酯的产率
(4) 分液 除去乙酸 溶解正丁醇 (5)D (6)80%
20.(1) 取代反应
(2)+HBr+
(3)醛基 1
(4)
(5)NaOH G中的—CH2OH会被KMnO4氧化为—COOH,无法得到E
21.(1)酸式滴定管 (2)铁架台 球形冷凝管 (3)加快反应速率 (4)水浴加热 (5)活性炭 (6)减少产品损失 50%的乙醇溶液 (7)重结晶
1.文房四宝是中华传统文化的瑰宝。下列有关叙述错误的是
A.羊毛可用于制毛笔,主要成分为蛋白质
B.松木可用于制墨,墨的主要成分是单质碳
C.竹子可用于造纸,纸的主要成分是纤维素
D.大理石可用于制砚台,主要成分为硅酸盐
2.将3 g有机物X在足量氧气中完全燃烧,若将燃烧产物通入足量的澄清石灰水中得到15.0 g沉淀;若将燃烧产物用足量碱石灰吸收,碱石灰增重10.2 g。有机物X的质谱图、红外光谱图和核磁共振氢谱图如下。下列说法正确的是
A.该有机物的实验式为C2H4O
B.该有机物的核磁共振氢谱有2组峰
C.结合三个谱图可知该有机物为2-丙醇
D.该有机物只存在一种同分异构体
3.烟草的焦油中存在一种强烈的致癌物,其结构简式如图所示。下列关于该物质说法正确的是
A.分子式为C20H14
B.与互为同分异构体
C.不能使溴的CCl4溶液褪色
D.核磁共振氢谱有5组峰
4.2023年9月23日晚,第19届亚运会在杭州开幕。下列有关说法错误的是
A.火炬“薪火”使用的铝合金熔点比纯铝低
B.“亚运莲花尊”的青瓷是以黏土为主要原料,经高温烧结而成
C.会馆使用的防滑剂主要成分石墨烯与乙烯互为同系物
D.主火炬塔的燃料首次使用废碳再生的绿色甲醇,有利于实现碳中和
5.间三联苯在发光二极管、磁性材料和分子识别领域有广泛用途,其结构简式如图所示。间三联苯的一氯代物的种类有
A.5种 B.6种 C.7种 D.8种
6.NA为阿伏加德罗常数的值。关于实验室制乙炔反应,下列说法不正确的是
A.与OH-所含电子数均为10NA
B.26g乙炔分子中含有的π键数目为2NA
C.和中含有的阴离子数目均为2NA
D.标准状况下,3.36 L 所含氢原子数为0.3NA
7.如图①②③为常见的三种有机物,下列说法错误的是
A.①③均不能使溴水褪色
B.②的同分异构体可能是苯的同系物
C.1 mol①、②完全燃烧均可消耗384 gO2
D.在一定条件下,②③均可发生加成反应
8.下列有关有机物的分离、提纯、鉴别的方法不正确的是
A.分离乙醇和乙酸钠:蒸馏 B.提纯苯甲酸:重结晶
C.分离乙酸乙酯和乙醇:分液 D.鉴别乙酸乙酯和甲酸乙酯:核磁共振氢谱
9.下列有机物中氢原子化学环境种数判断错误的是
A.:2种 B.:3种
C.:4种 D.:5种
10.一种利胆药物Z的合成路线如图所示,下列说法错误的是
A.X含有三种官能团
B.Y与溴水反应,1molY最多消耗
C.X与足量反应,1molX最多消耗的物质的量为4mol
D.等物质的量的X、Y、Z与足量NaOH溶液反应,消耗NaOH的物质的量之比为1:2:3
11.物质Z是一种可用于合成内分泌调节剂的药物中间体,其合成路线如下:
下列说法正确的是
A.Z的核磁共振氢谱中有6组峰
B.Y不能发生氧化反应
C.与X含有相同官能团的X的同分异构体有10种
D.Y在水中的溶解性比X强
12.化合物M具有广谱抗菌活性,合成M的反应可表示如图:
下列说法正确的是
A.最多可与发生加成反应
B.可用溶液或溶液鉴别X和Y
C.Y分子中所有原子不可能在同一平面内
D.与足量溶液反应,最多可消耗
13.实验小组在实验室中制备1,2-二溴乙烷,装置如图所示(部分夹持装置略去)。下列说法错误的是
A.①中液体变为棕色,体现浓硫酸的脱水性 B.试剂X可选用NaOH溶液
C.实验后通过分液操作从③的混合液中分离出产品 D.④中收集到的尾气需要进行集中处理
14.以下为有机物的制备实验装置。下列相关说法错误的是
A.图1右侧试管中观察到淡黄色沉淀,证明制备溴苯的反应为取代反应
B.图2所制得的硝基苯因溶解有NO2略带黄色,可加入NaOH溶液分液除去
C.图3导气管口应在右侧试管中Na2CO3溶液液面上方,以防止倒吸
D.图4分水器分出生成的水可提高反应转化率
15.下列操作能达到实验目的的是
A B C D
用酒精萃取碘水中的碘 蒸馏实验中将蒸气冷凝为液体 混合浓硫酸和乙醇 证明乙炔可使酸性高锰酸钾溶液褪色
16.某有机物的结构简式为,据此填写下列空格。
(1)该物质的苯环上的一氯代物有 种。
(2)1 mol 该物质和溴水混合,消耗Br2的物质的量为 mol。
(3)1 mol 该物质和H2加成需H2 mol。
(4)下列说法不正确的是 (填字母) 。
A.此物质可发生加成、取代、氧化等反应 B.和甲苯互为同系物
(5)电器包装中大量使用的泡沫塑料的主要成分是聚苯乙烯(),它是由 (写结构简式)聚合而成的。
(6)CH2=CHCl与聚苯乙烯的单体在一定条件下可发生加聚反应,所得产物的结构简式为 。
17.二氧化碳的转化与综合利用是实现“碳达峰”“碳中和”战略的重要途径。近期,我国学者以电催化反应为关键步骤,用CO2作原料,实现了重要医药中间体——阿托酸的合成,其合成路线如下:
(1)阿托酸所含官能团名称为碳碳双键、 。
(2)A→B的反应类型为 。
(3)A的含有苯环且能发生银镜反应的同分异构体数目为 ,其中在核磁共振氢谱中呈现四组峰的结构简式为 。
(4)写出B→C反应方程式: 。
(5)C→D反应所需试剂及条件为 。
(6)在D→E反应中,用Mg作阳极、Pt作阴极进行电解,则CO2与D的反应在 (填“阳极”或“阴极”)上进行。
(7)下列关于E的叙述错误的是 (填序号)。
a.可发生聚合反应
b.分子内9个碳原子共平面
c.分子内含有1个手性碳原子
d.可形成分子内氢键和分子间氢键
(8)结合题干信息,完成以下合成路线: 。
( )
18.一种以甲苯为原料合成有机物M的设计路线如下:
已知:R-Br
回答下列问题:
(1)B所含官能团的名称是 。
(2)A的名称是 ,A→B中加入Fe的目的是 。
(3)甲苯→A的反应类型是 ,甲苯→C的化学方程式为 。
(4)在制药行业中常用“成盐修饰”改善物质的理化性质,若用饱和溶液对E进行“成盐修饰”,可将E转化为 (用结构简式表示)。
(5)用结构简式表示满足下列条件的D的同分异构体 。
①苯环上只有两个取代基;
②核磁共振氢谱中有6组吸收峰;
③分子中只含有1个手性碳原子
(6)根据已有知识并结合上述合成路线图的相关信息,写出以乙烯为原料,选用必要的无机试剂,合成高分子物质 的路线图(请用结构简式表示有机物,用“→”表示转化关系,并在“→”上注明试剂和反应条件) 。
19.乙酸正丁酯在香料、色谱分析、塑料加工、制药等领域中均有广泛应用。实验室中按照下列流程制取乙酸正丁酯并测定其结构。有关物质的部分性质如下表:
物质 相对分子质量 密度 沸点(℃) 水溶性
乙酸 60 1.045 118.1 互溶
正丁醇 74 0.80 118.0 可溶
乙酸正丁酯 116 0.882 126.1 微溶
Ⅰ.用如图所示装置合成乙酸正丁酯粗产品
将乙酸、正丁醇、3~4滴浓硫酸依次加入A中,混匀后投入沸石,接通冷却水,加热至反应完全,得到乙酸正丁酯粗产品。
(1)仪器A的名称是 ;冷却水由 (填“a”或“b”)通入更合理。
(2)制备乙酸正丁酯的化学方程式为 。
(3)从平衡移动的角度分析,分水器的作用是 。
Ⅱ.通过下列步骤精制粗产品
(4)操作1的名称是 ;饱和溶液的作用 、 以及降低乙酸正丁酯的溶解度便于分层。
(5)下列各组物质的分离或提纯过程也需要用到“操作2”的是_____(填字母)。
A.除去乙烷气体中的乙烯 B.除去苯甲酸中的氯化钠
C.分离邻二甲苯和水 D.分离三氯甲烷和四氯化碳
(6)通过上述步骤最终获得乙酸正丁酯,则乙酸正丁酯的产率为 。
20.心血管药物缬沙坦中间体(F)的两条合成路线如下:
已知:
Ⅰ.+
Ⅱ.R1CHOR1CH2NHR2
回答下列问题:
(1)A结构简式为 ;B→C反应类型为 。
(2)C+D→F化学方程式为 。
(3)E中含氧官能团名称为 ;F中手性碳原子有 个。
(4)D的一种同分异构体含硝基和3种不同化学环境的氢原子(个数比为6∶6∶1),其结构简式为 。
(5)C→E的合成路线设计如下:
CG(C14H11NO)E
试剂X为 (填化学式);试剂Y不能选用KMnO4,原因是
。
21.吡咯类化合物在导电聚合物、化学传感器及药物制剂上有着广泛应用,一种合成1-(4-甲氧基苯基)-2,5-二甲基吡咯(用吡咯X表示)的反应和方法如下:
实验装置如图所示,将100 mmol己-2,5-二酮(熔点:-5.5 ℃,密度:0.737 g·cm-3)与100 mmol 4-甲氧基苯胺(熔点:57 ℃)放入①中,搅拌。待反应完成后,加入50%的乙醇溶液,析出浅棕色固体。加热至65 ℃,至固体溶解,加入脱色剂,回流20 min,趁热过滤。滤液静置至室温,冰水浴冷却,有大量白色固体析出。经过滤、洗涤、干燥得到产品。
回答下列问题:
(1)量取己-2,5-二酮应使用的仪器为 (填名称)。
(2)仪器①用铁夹固定在③上,③的名称是 ;仪器②的名称是 。
(3)“搅拌”的作用是 。
(4)“加热”方式为 。
(5)使用的“脱色剂”是 。
(6)“趁热过滤”的目的是 ;
用 洗涤白色固体。
(7)若需进一步提纯产品,可采用的方法是 。
高二化学参考答案:
1-5.DCCCB 6-10.CACCD 11-15.ABCBD
16.(1)4 (2)2 (3)5 (4)B (5)
(6)、、、
17.(1)羧基 (2)加成反应(或还原反应) (3) 4
(4)+H2O
(5)O2,△/催化剂 (6)阴极 (7)b
(8)。
18.(1)氨基
(2) 对硝基甲苯(或1-甲基-4-硝基苯或4-硝基甲苯 ) 将硝基还原为氨基
(3) 取代反应或硝化反应 +Br2 +HBr
(4) (5)
(6)
19.(1) 圆底烧瓶 b
(2)
(3)将水分离出体系,促进平衡向正反应方向移动,进而提高酯的产率
(4) 分液 除去乙酸 溶解正丁醇 (5)D (6)80%
20.(1) 取代反应
(2)+HBr+
(3)醛基 1
(4)
(5)NaOH G中的—CH2OH会被KMnO4氧化为—COOH,无法得到E
21.(1)酸式滴定管 (2)铁架台 球形冷凝管 (3)加快反应速率 (4)水浴加热 (5)活性炭 (6)减少产品损失 50%的乙醇溶液 (7)重结晶
