第1章 认识化学科学 寒假演练题 2024--2025学年高一上学期化学鲁科版(2019)必修第一册(含答案)
文档属性
| 名称 | 第1章 认识化学科学 寒假演练题 2024--2025学年高一上学期化学鲁科版(2019)必修第一册(含答案) |  | |
| 格式 | docx | ||
| 文件大小 | 227.1KB | ||
| 资源类型 | 教案 | ||
| 版本资源 | 鲁科版(2019) | ||
| 科目 | 化学 | ||
| 更新时间 | 2025-02-06 21:26:43 | ||
图片预览




文档简介
第1章 认识化学科学 寒假演练题2024--2025学年高一上学期化学鲁科版(2019)必修第一册
一、选择题。(18题)
1、化学科学史上每一次重大的发现都极大地推进了科学的发展,对于人类文明的进步发挥了巨大的推动作用,如合成氨技术,制造出能促进粮食增产的大量氮肥,使成千上万的人免除饥饿的威胁。下列对化学史的描述不正确的是( )
A.侯德榜联合制碱法中制得的碱是烧碱
B.道尔顿提出了原子论
C.阿伏加德罗提出了分子学说
D.拉瓦锡提出了燃烧的氧化学说
2、下列说法不正确的是( )
A.84消毒液和过氧乙酸常用于环境消毒,消毒原理相同
B.自来水厂常用明矾消毒、净化水质
C.咳嗽产生的飞沫分散到空气中形成气溶胶
D.亚硝酸盐中毒和CO中毒的原理不相同
3、某同学按如图所示实验装置进行钠与水反应的实验,据此判断下列说法正确的是( )
A.打开右端活塞,将一小块金属钠加入煤油中,反应前片刻,钠的位置在a处
B.开始反应后,能观察到的实验现象是钠在b处液面以下的水中反应
C.反应一段时间后,左端液面上升进入长颈漏斗,b处有无色气体产生
D.若用酒精来代替煤油,可观察到相同的实验现象
4、当足量的Cl2或盐酸分别与下列金属反应时,均有MCl2型化合物生成的是( )
A.Fe B.Mg C.Cu D.Ag
5、在自来水的生产中,常通入适量氯气进行杀菌消毒,氯气与水反应的产物之一是盐酸。市场上有些不法商贩为牟取暴利,利用自来水冒充纯净水桶装出售。为辨别真伪,可用下列哪一种试剂来鉴别( )
A.酚酞试液 B.氯化钡溶液
C.氢氧化钠溶液 D.硝酸银溶液
6、某容器真空时,称量其质量为60.4 g,此容器充满N2时总质量为66.0 g,在相同状况下,充满另一气体时,总质量为74.6 g,那么该气体可能是( )
A.Cl2 B.O2 C.SO2 D.HCl
7、下列溶液中,与200mL0.5mol/LNa2SO4溶液所含物质的量浓度相同的是( )
A.200mL0.25mol/LNaCl溶液 B.100mL1mol/LNaCl溶液
C.100mL0.5mol/LNaOH溶液 D.100mL2mol/LNaOH溶液
8、下列各气体:①0.5molHe;②9.0gNO;③3.4g的NH3;④3.01×1023个CO2。四种物质所含的原子总数最多是( )
A.① B.② C.③ D.④
9、某溶液含有①②③④⑤等五种阴离子,向其中加入少量的过氧化钠固体后,溶液中的离子浓度基本保持不变的是(忽略溶液体积变化)( )
A.① B.①⑤ C.①④⑤ D.①③⑤
10、对危险化学品要在包装标签上印有警示性标志。氢氧化钠溶液应选用的标志是( )
A B C D
爆炸品 氧化剂 剧毒品 腐蚀品
A.A B.B C.C D.D
11、下列实验操作中错误的是( )
A.蒸馏操作时,应使温度计水银球靠近蒸馏烧瓶的支管口处
B.蒸发操作时,当蒸发皿中的水分只残留少许时,停止加热,利用余热将剩余水分蒸干
C.称量时,将NaOH固体放在称量纸上置于托盘天平的左盘,将砝码放在托盘天平的右盘
D.溶解操作时,玻璃棒作用是搅拌以加速溶解;过滤操作时,玻璃棒作用是引流,防止溶液溅出
12、下列物质的转化不能通过一步反应实现的是( )
A.Na→NaOH B.Na→Na2CO3
C.Na2O→NaOH D.Na2O2→Na2CO3
13、使用容量瓶配制溶液过程中,下列操作会使所配制的溶液浓度不发生变化的是( )
A.溶液转移到容量瓶后,烧杯内壁及玻璃棒未用蒸馏水洗涤
B.转移溶液前,容量瓶内存有少量蒸馏水
C.定容时,俯视容量瓶的刻度线
D.定容后摇匀,发现液面降低,又补加少量蒸馏水重新达到刻度线
14、将一定物质的量的Na2CO3、NaHCO3组成的混合物溶于水,配成1L溶液,取出50mL溶液然后滴加一定物质的量浓度的盐酸得到的图像如图所示,下列说法正确的是( )
A.标注NaCl的直线代表产生的CO2的物质的量
B.原混合物中Na2CO3与NaHCO3的物质的量之比为1:2
C.盐酸的浓度是0.05mol·L-1
D.盐酸加到
15、用NA表示阿伏加 德罗常数的值,下列叙述正确的是( )
①22gT2O含有电子数为10NA
②0.44gC3H8中含有的共价键总数目为0.1NA
③1molNa2O2与CO2完全反应时转移电子数为2NA
④28g硅晶体中含有2NA个Si—Si键
⑤11.2LCl2通入足量的NaOH溶液中充分反应,转移的电子数等于0.5NA
⑥200mL1mol·L-1Al2(SO4)3溶液中Al3+和SO42-的数目总和是NA
A.①②③ B.②④⑥ C.①③⑤ D.①②④
16、在化学实验中,玻璃棒一般不用于( )
A.捣碎块状固体 B.转移引流液体 C.蘸取少量溶液 D.搅拌加速溶解
17、已知浓盐酸和次氯酸钙能发生如下反应:Ca(ClO)2+4HCl(浓) ===CaCl2+2Cl2↑+2H2O。用贮存很久的漂白粉与浓盐酸反应制得的氯气中,可能含有的杂质气体是( )
①CO2 ②HCl ③H2O ④O2
A.①②③ B.②③④ C.②③ D.①④
18、同温同压下,具有相同分子数的气体一定具有( )
A.相同的体积 B.相同的质量
C.相同的分子量 D.相同的密度
二、填空题。(3题)
19、环保部门检测到某工厂的工业废水中含有大量的FeSO4、较多的Cu2+和少量的Na+。为了减少污染并变废为宝,要求该工厂从该废水中回收硫酸亚铁和金属铜。该工厂设计了如下流程图,完成回收硫酸亚铁和铜的简单实验方案。
回答下列问题
(1)填写试剂A的化学式 _______________
(2)假如加入2mol D刚好完全反应,此步转移的电子的物质的量为 __________
(3)写出加入A的离子方程式: _________________
(4)操作Ⅱ和III 的名称分别是 ___________、 ____________、________
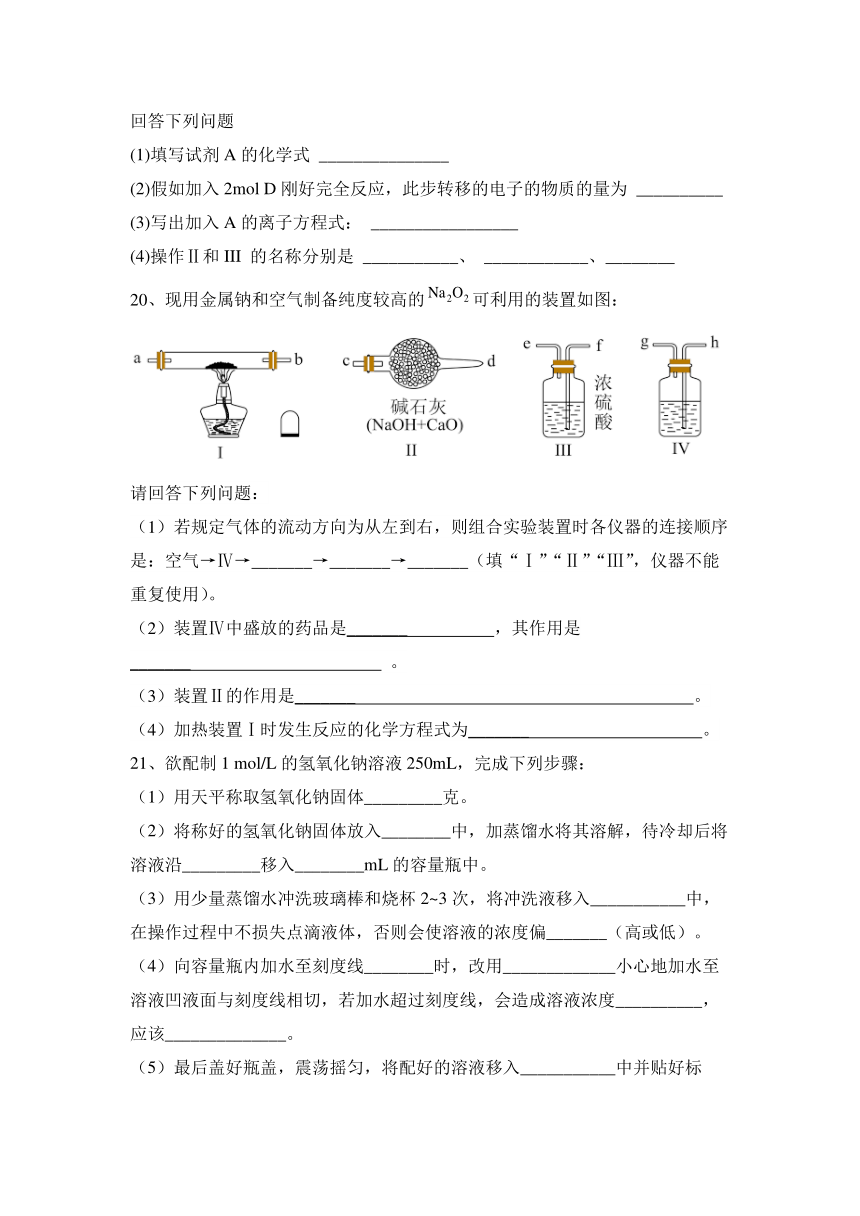
20、现用金属钠和空气制备纯度较高的可利用的装置如图:
请回答下列问题:
(1)若规定气体的流动方向为从左到右,则组合实验装置时各仪器的连接顺序是:空气→Ⅳ→_______→_______→_______(填“Ⅰ”“Ⅱ”“Ⅲ”,仪器不能重复使用)。
(2)装置Ⅳ中盛放的药品是_______ ,其作用是_______ 。
(3)装置Ⅱ的作用是_______ 。
(4)加热装置Ⅰ时发生反应的化学方程式为_______ 。
21、欲配制1 mol/L的氢氧化钠溶液250mL,完成下列步骤:
(1)用天平称取氢氧化钠固体_________克。
(2)将称好的氢氧化钠固体放入________中,加蒸馏水将其溶解,待冷却后将溶液沿_________移入________mL的容量瓶中。
(3)用少量蒸馏水冲洗玻璃棒和烧杯2~3次,将冲洗液移入___________中,在操作过程中不损失点滴液体,否则会使溶液的浓度偏_______(高或低)。
(4)向容量瓶内加水至刻度线________时,改用_____________小心地加水至溶液凹液面与刻度线相切,若加水超过刻度线,会造成溶液浓度__________,应该______________。
(5)最后盖好瓶盖,震荡摇匀,将配好的溶液移入___________中并贴好标签。
三、实验题。(2题)
22、在课堂上,老师演示了金属钠与CuSO4溶液反应的实验,同学们观察到该反应中生成了蓝色的Cu(OH)2沉淀和气泡,而没有发现铜单质。某同学想,会不会是因为生成的铜较少而被蓝色沉淀所覆盖从而没有被发现呢?于是他想课后到实验室继续探究,希望进一步用实验来验证自己的猜测是否正确。
(1)假如你是该同学,请你写一份实验准备单交给老师,要求老师提供必需的用品。
①实验探究的目的:_______________________________________________。
②探究所依据的化学原理:_________________________________________。
③实验必需的仪器或用品:小刀、玻璃片、滤纸、______________和烧杯;药品:金属钠、CuSO4溶液和______________。
(2)该同学在探究实验中意外地发现了生成的蓝色沉淀中混有少量的黑色难溶物,而所使用的药品均没有问题,你认为该黑色难溶物是____________(填化学式),生成该黑色难溶物的原因是(结合化学方程式和必要的文字作答)
_________________________________________________________________ 。
23、某同学在实验室进行如图所示的过氧化钠性质实验。请回答下列问题:
(1)如图所示实验,滴入几滴水,整个过程现象是___________。实验结束后,向试管所得溶液中滴加酚酞溶液,现象是___________。
(2)过氧化钠与水反应的化学方程式为___________。
(3)若用嘴通过导管向附着少量Na2O2粉末的脱脂棉吹气,棉花燃烧。原因是Na2O2与H2O和CO2反应,写出其中Na2O2与CO2反应的化学方程式为___________。
第1章 认识化学科学 寒假演练题2024--2025学年高一上学期化学鲁科版(2019)必修第一册
一、选择题。(18题)
1、化学科学史上每一次重大的发现都极大地推进了科学的发展,对于人类文明的进步发挥了巨大的推动作用,如合成氨技术,制造出能促进粮食增产的大量氮肥,使成千上万的人免除饥饿的威胁。下列对化学史的描述不正确的是( )
A.侯德榜联合制碱法中制得的碱是烧碱
B.道尔顿提出了原子论
C.阿伏加德罗提出了分子学说
D.拉瓦锡提出了燃烧的氧化学说
【答案】A
2、下列说法不正确的是( )
A.84消毒液和过氧乙酸常用于环境消毒,消毒原理相同
B.自来水厂常用明矾消毒、净化水质
C.咳嗽产生的飞沫分散到空气中形成气溶胶
D.亚硝酸盐中毒和CO中毒的原理不相同
【答案】B
3、某同学按如图所示实验装置进行钠与水反应的实验,据此判断下列说法正确的是( )
A.打开右端活塞,将一小块金属钠加入煤油中,反应前片刻,钠的位置在a处
B.开始反应后,能观察到的实验现象是钠在b处液面以下的水中反应
C.反应一段时间后,左端液面上升进入长颈漏斗,b处有无色气体产生
D.若用酒精来代替煤油,可观察到相同的实验现象
【答案】C
4、当足量的Cl2或盐酸分别与下列金属反应时,均有MCl2型化合物生成的是( )
A.Fe B.Mg C.Cu D.Ag
【答案】B
5、在自来水的生产中,常通入适量氯气进行杀菌消毒,氯气与水反应的产物之一是盐酸。市场上有些不法商贩为牟取暴利,利用自来水冒充纯净水桶装出售。为辨别真伪,可用下列哪一种试剂来鉴别( )
A.酚酞试液 B.氯化钡溶液
C.氢氧化钠溶液 D.硝酸银溶液
【答案】D
6、某容器真空时,称量其质量为60.4 g,此容器充满N2时总质量为66.0 g,在相同状况下,充满另一气体时,总质量为74.6 g,那么该气体可能是( )
A.Cl2 B.O2 C.SO2 D.HCl
【答案】A
7、下列溶液中,与200mL0.5mol/LNa2SO4溶液所含物质的量浓度相同的是( )
A.200mL0.25mol/LNaCl溶液 B.100mL1mol/LNaCl溶液
C.100mL0.5mol/LNaOH溶液 D.100mL2mol/LNaOH溶液
【答案】B
8、下列各气体:①0.5molHe;②9.0gNO;③3.4g的NH3;④3.01×1023个CO2。四种物质所含的原子总数最多是( )
A.① B.② C.③ D.④
【答案】D
9、某溶液含有①②③④⑤等五种阴离子,向其中加入少量的过氧化钠固体后,溶液中的离子浓度基本保持不变的是(忽略溶液体积变化)( )
A.① B.①⑤ C.①④⑤ D.①③⑤
【答案】A
10、对危险化学品要在包装标签上印有警示性标志。氢氧化钠溶液应选用的标志是( )
A B C D
爆炸品 氧化剂 剧毒品 腐蚀品
A.A B.B C.C D.D
【答案】D
11、下列实验操作中错误的是( )
A.蒸馏操作时,应使温度计水银球靠近蒸馏烧瓶的支管口处
B.蒸发操作时,当蒸发皿中的水分只残留少许时,停止加热,利用余热将剩余水分蒸干
C.称量时,将NaOH固体放在称量纸上置于托盘天平的左盘,将砝码放在托盘天平的右盘
D.溶解操作时,玻璃棒作用是搅拌以加速溶解;过滤操作时,玻璃棒作用是引流,防止溶液溅出
【答案】C
12、下列物质的转化不能通过一步反应实现的是( )
A.Na→NaOH B.Na→Na2CO3
C.Na2O→NaOH D.Na2O2→Na2CO3
【答案】B
13、使用容量瓶配制溶液过程中,下列操作会使所配制的溶液浓度不发生变化的是( )
A.溶液转移到容量瓶后,烧杯内壁及玻璃棒未用蒸馏水洗涤
B.转移溶液前,容量瓶内存有少量蒸馏水
C.定容时,俯视容量瓶的刻度线
D.定容后摇匀,发现液面降低,又补加少量蒸馏水重新达到刻度线
【答案】B
14、将一定物质的量的Na2CO3、NaHCO3组成的混合物溶于水,配成1L溶液,取出50mL溶液然后滴加一定物质的量浓度的盐酸得到的图像如图所示,下列说法正确的是( )
A.标注NaCl的直线代表产生的CO2的物质的量
B.原混合物中Na2CO3与NaHCO3的物质的量之比为1:2
C.盐酸的浓度是0.05mol·L-1
D.盐酸加到
15、用NA表示阿伏加 德罗常数的值,下列叙述正确的是( )
①22gT2O含有电子数为10NA
②0.44gC3H8中含有的共价键总数目为0.1NA
③1molNa2O2与CO2完全反应时转移电子数为2NA
④28g硅晶体中含有2NA个Si—Si键
⑤11.2LCl2通入足量的NaOH溶液中充分反应,转移的电子数等于0.5NA
⑥200mL1mol·L-1Al2(SO4)3溶液中Al3+和SO42-的数目总和是NA
A.①②③ B.②④⑥ C.①③⑤ D.①②④
【答案】D
16、在化学实验中,玻璃棒一般不用于( )
A.捣碎块状固体 B.转移引流液体 C.蘸取少量溶液 D.搅拌加速溶解
【答案】A
17、已知浓盐酸和次氯酸钙能发生如下反应:Ca(ClO)2+4HCl(浓) ===CaCl2+2Cl2↑+2H2O。用贮存很久的漂白粉与浓盐酸反应制得的氯气中,可能含有的杂质气体是( )
①CO2 ②HCl ③H2O ④O2
A.①②③ B.②③④ C.②③ D.①④
【答案】A
18、同温同压下,具有相同分子数的气体一定具有( )
A.相同的体积 B.相同的质量
C.相同的分子量 D.相同的密度
【答案】A
二、填空题。(3题)
19、环保部门检测到某工厂的工业废水中含有大量的FeSO4、较多的Cu2+和少量的Na+。为了减少污染并变废为宝,要求该工厂从该废水中回收硫酸亚铁和金属铜。该工厂设计了如下流程图,完成回收硫酸亚铁和铜的简单实验方案。
回答下列问题
(1)填写试剂A的化学式 _______________
(2)假如加入2mol D刚好完全反应,此步转移的电子的物质的量为 __________
(3)写出加入A的离子方程式: _________________
(4)操作Ⅱ和III 的名称分别是 ___________、 ____________、________
【答案】(1)Fe (2)4mol (3)Fe+Cu2+=Fe2++Cu
(4)过滤 蒸发浓缩 冷却结晶
20、现用金属钠和空气制备纯度较高的可利用的装置如图:
请回答下列问题:
(1)若规定气体的流动方向为从左到右,则组合实验装置时各仪器的连接顺序是:空气→Ⅳ→_______→_______→_______(填“Ⅰ”“Ⅱ”“Ⅲ”,仪器不能重复使用)。
(2)装置Ⅳ中盛放的药品是_______ ,其作用是_______ 。
(3)装置Ⅱ的作用是_______ 。
(4)加热装置Ⅰ时发生反应的化学方程式为_______ 。
【答案】(1)Ⅲ;Ⅰ;Ⅱ
(2)氢氧化钠溶液;吸收通入空气中的二氧化碳
(3)防止空气中的水蒸气和二氧化碳进入装置Ⅰ
(4)
21、欲配制1 mol/L的氢氧化钠溶液250mL,完成下列步骤:
(1)用天平称取氢氧化钠固体_________克。
(2)将称好的氢氧化钠固体放入________中,加蒸馏水将其溶解,待冷却后将溶液沿_________移入________mL的容量瓶中。
(3)用少量蒸馏水冲洗玻璃棒和烧杯2~3次,将冲洗液移入___________中,在操作过程中不损失点滴液体,否则会使溶液的浓度偏_______(高或低)。
(4)向容量瓶内加水至刻度线________时,改用_____________小心地加水至溶液凹液面与刻度线相切,若加水超过刻度线,会造成溶液浓度__________,应该______________。
(5)最后盖好瓶盖,震荡摇匀,将配好的溶液移入___________中并贴好标签。
【答案】10.0 烧杯 玻璃棒 250 250mL容量瓶 低 1cm~2cm 胶头滴管 低 重新配制 试剂瓶
三、实验题。
22、在课堂上,老师演示了金属钠与CuSO4溶液反应的实验,同学们观察到该反应中生成了蓝色的Cu(OH)2沉淀和气泡,而没有发现铜单质。某同学想,会不会是因为生成的铜较少而被蓝色沉淀所覆盖从而没有被发现呢?于是他想课后到实验室继续探究,希望进一步用实验来验证自己的猜测是否正确。
(1)假如你是该同学,请你写一份实验准备单交给老师,要求老师提供必需的用品。
①实验探究的目的:_______________________________________________。
②探究所依据的化学原理:_________________________________________。
③实验必需的仪器或用品:小刀、玻璃片、滤纸、______________和烧杯;药品:金属钠、CuSO4溶液和______________。
(2)该同学在探究实验中意外地发现了生成的蓝色沉淀中混有少量的黑色难溶物,而所使用的药品均没有问题,你认为该黑色难溶物是____________(填化学式),生成该黑色难溶物的原因是(结合化学方程式和必要的文字作答)
_________________________________________________________________ 。
【答案】(1)①验证钠与硫酸铜溶液反应是否有铜生成
②氢氧化铜可溶于盐酸而铜不溶
③镊子 稀盐酸(或稀硫酸)
(2)CuO 钠与水反应放出的热使生成的Cu(OH)2部分发生分解,
Cu(OH)2CuO+H2O
23、某同学在实验室进行如图所示的过氧化钠性质实验。请回答下列问题:
(1)如图所示实验,滴入几滴水,整个过程现象是___________。实验结束后,向试管所得溶液中滴加酚酞溶液,现象是___________。
(2)过氧化钠与水反应的化学方程式为___________。
(3)若用嘴通过导管向附着少量Na2O2粉末的脱脂棉吹气,棉花燃烧。原因是Na2O2与H2O和CO2反应,写出其中Na2O2与CO2反应的化学方程式为___________。
【答案】(1) 有大量气泡产生,使带火星的木条复燃 溶液先变红后褪色
(2)2Na2O2+2H2O=4NaOH+O2↑
(3)2Na2O2+2CO2=2Na2CO3+O2
一、选择题。(18题)
1、化学科学史上每一次重大的发现都极大地推进了科学的发展,对于人类文明的进步发挥了巨大的推动作用,如合成氨技术,制造出能促进粮食增产的大量氮肥,使成千上万的人免除饥饿的威胁。下列对化学史的描述不正确的是( )
A.侯德榜联合制碱法中制得的碱是烧碱
B.道尔顿提出了原子论
C.阿伏加德罗提出了分子学说
D.拉瓦锡提出了燃烧的氧化学说
2、下列说法不正确的是( )
A.84消毒液和过氧乙酸常用于环境消毒,消毒原理相同
B.自来水厂常用明矾消毒、净化水质
C.咳嗽产生的飞沫分散到空气中形成气溶胶
D.亚硝酸盐中毒和CO中毒的原理不相同
3、某同学按如图所示实验装置进行钠与水反应的实验,据此判断下列说法正确的是( )
A.打开右端活塞,将一小块金属钠加入煤油中,反应前片刻,钠的位置在a处
B.开始反应后,能观察到的实验现象是钠在b处液面以下的水中反应
C.反应一段时间后,左端液面上升进入长颈漏斗,b处有无色气体产生
D.若用酒精来代替煤油,可观察到相同的实验现象
4、当足量的Cl2或盐酸分别与下列金属反应时,均有MCl2型化合物生成的是( )
A.Fe B.Mg C.Cu D.Ag
5、在自来水的生产中,常通入适量氯气进行杀菌消毒,氯气与水反应的产物之一是盐酸。市场上有些不法商贩为牟取暴利,利用自来水冒充纯净水桶装出售。为辨别真伪,可用下列哪一种试剂来鉴别( )
A.酚酞试液 B.氯化钡溶液
C.氢氧化钠溶液 D.硝酸银溶液
6、某容器真空时,称量其质量为60.4 g,此容器充满N2时总质量为66.0 g,在相同状况下,充满另一气体时,总质量为74.6 g,那么该气体可能是( )
A.Cl2 B.O2 C.SO2 D.HCl
7、下列溶液中,与200mL0.5mol/LNa2SO4溶液所含物质的量浓度相同的是( )
A.200mL0.25mol/LNaCl溶液 B.100mL1mol/LNaCl溶液
C.100mL0.5mol/LNaOH溶液 D.100mL2mol/LNaOH溶液
8、下列各气体:①0.5molHe;②9.0gNO;③3.4g的NH3;④3.01×1023个CO2。四种物质所含的原子总数最多是( )
A.① B.② C.③ D.④
9、某溶液含有①②③④⑤等五种阴离子,向其中加入少量的过氧化钠固体后,溶液中的离子浓度基本保持不变的是(忽略溶液体积变化)( )
A.① B.①⑤ C.①④⑤ D.①③⑤
10、对危险化学品要在包装标签上印有警示性标志。氢氧化钠溶液应选用的标志是( )
A B C D
爆炸品 氧化剂 剧毒品 腐蚀品
A.A B.B C.C D.D
11、下列实验操作中错误的是( )
A.蒸馏操作时,应使温度计水银球靠近蒸馏烧瓶的支管口处
B.蒸发操作时,当蒸发皿中的水分只残留少许时,停止加热,利用余热将剩余水分蒸干
C.称量时,将NaOH固体放在称量纸上置于托盘天平的左盘,将砝码放在托盘天平的右盘
D.溶解操作时,玻璃棒作用是搅拌以加速溶解;过滤操作时,玻璃棒作用是引流,防止溶液溅出
12、下列物质的转化不能通过一步反应实现的是( )
A.Na→NaOH B.Na→Na2CO3
C.Na2O→NaOH D.Na2O2→Na2CO3
13、使用容量瓶配制溶液过程中,下列操作会使所配制的溶液浓度不发生变化的是( )
A.溶液转移到容量瓶后,烧杯内壁及玻璃棒未用蒸馏水洗涤
B.转移溶液前,容量瓶内存有少量蒸馏水
C.定容时,俯视容量瓶的刻度线
D.定容后摇匀,发现液面降低,又补加少量蒸馏水重新达到刻度线
14、将一定物质的量的Na2CO3、NaHCO3组成的混合物溶于水,配成1L溶液,取出50mL溶液然后滴加一定物质的量浓度的盐酸得到的图像如图所示,下列说法正确的是( )
A.标注NaCl的直线代表产生的CO2的物质的量
B.原混合物中Na2CO3与NaHCO3的物质的量之比为1:2
C.盐酸的浓度是0.05mol·L-1
D.盐酸加到
15、用NA表示阿伏加 德罗常数的值,下列叙述正确的是( )
①22gT2O含有电子数为10NA
②0.44gC3H8中含有的共价键总数目为0.1NA
③1molNa2O2与CO2完全反应时转移电子数为2NA
④28g硅晶体中含有2NA个Si—Si键
⑤11.2LCl2通入足量的NaOH溶液中充分反应,转移的电子数等于0.5NA
⑥200mL1mol·L-1Al2(SO4)3溶液中Al3+和SO42-的数目总和是NA
A.①②③ B.②④⑥ C.①③⑤ D.①②④
16、在化学实验中,玻璃棒一般不用于( )
A.捣碎块状固体 B.转移引流液体 C.蘸取少量溶液 D.搅拌加速溶解
17、已知浓盐酸和次氯酸钙能发生如下反应:Ca(ClO)2+4HCl(浓) ===CaCl2+2Cl2↑+2H2O。用贮存很久的漂白粉与浓盐酸反应制得的氯气中,可能含有的杂质气体是( )
①CO2 ②HCl ③H2O ④O2
A.①②③ B.②③④ C.②③ D.①④
18、同温同压下,具有相同分子数的气体一定具有( )
A.相同的体积 B.相同的质量
C.相同的分子量 D.相同的密度
二、填空题。(3题)
19、环保部门检测到某工厂的工业废水中含有大量的FeSO4、较多的Cu2+和少量的Na+。为了减少污染并变废为宝,要求该工厂从该废水中回收硫酸亚铁和金属铜。该工厂设计了如下流程图,完成回收硫酸亚铁和铜的简单实验方案。
回答下列问题
(1)填写试剂A的化学式 _______________
(2)假如加入2mol D刚好完全反应,此步转移的电子的物质的量为 __________
(3)写出加入A的离子方程式: _________________
(4)操作Ⅱ和III 的名称分别是 ___________、 ____________、________
20、现用金属钠和空气制备纯度较高的可利用的装置如图:
请回答下列问题:
(1)若规定气体的流动方向为从左到右,则组合实验装置时各仪器的连接顺序是:空气→Ⅳ→_______→_______→_______(填“Ⅰ”“Ⅱ”“Ⅲ”,仪器不能重复使用)。
(2)装置Ⅳ中盛放的药品是_______ ,其作用是_______ 。
(3)装置Ⅱ的作用是_______ 。
(4)加热装置Ⅰ时发生反应的化学方程式为_______ 。
21、欲配制1 mol/L的氢氧化钠溶液250mL,完成下列步骤:
(1)用天平称取氢氧化钠固体_________克。
(2)将称好的氢氧化钠固体放入________中,加蒸馏水将其溶解,待冷却后将溶液沿_________移入________mL的容量瓶中。
(3)用少量蒸馏水冲洗玻璃棒和烧杯2~3次,将冲洗液移入___________中,在操作过程中不损失点滴液体,否则会使溶液的浓度偏_______(高或低)。
(4)向容量瓶内加水至刻度线________时,改用_____________小心地加水至溶液凹液面与刻度线相切,若加水超过刻度线,会造成溶液浓度__________,应该______________。
(5)最后盖好瓶盖,震荡摇匀,将配好的溶液移入___________中并贴好标签。
三、实验题。(2题)
22、在课堂上,老师演示了金属钠与CuSO4溶液反应的实验,同学们观察到该反应中生成了蓝色的Cu(OH)2沉淀和气泡,而没有发现铜单质。某同学想,会不会是因为生成的铜较少而被蓝色沉淀所覆盖从而没有被发现呢?于是他想课后到实验室继续探究,希望进一步用实验来验证自己的猜测是否正确。
(1)假如你是该同学,请你写一份实验准备单交给老师,要求老师提供必需的用品。
①实验探究的目的:_______________________________________________。
②探究所依据的化学原理:_________________________________________。
③实验必需的仪器或用品:小刀、玻璃片、滤纸、______________和烧杯;药品:金属钠、CuSO4溶液和______________。
(2)该同学在探究实验中意外地发现了生成的蓝色沉淀中混有少量的黑色难溶物,而所使用的药品均没有问题,你认为该黑色难溶物是____________(填化学式),生成该黑色难溶物的原因是(结合化学方程式和必要的文字作答)
_________________________________________________________________ 。
23、某同学在实验室进行如图所示的过氧化钠性质实验。请回答下列问题:
(1)如图所示实验,滴入几滴水,整个过程现象是___________。实验结束后,向试管所得溶液中滴加酚酞溶液,现象是___________。
(2)过氧化钠与水反应的化学方程式为___________。
(3)若用嘴通过导管向附着少量Na2O2粉末的脱脂棉吹气,棉花燃烧。原因是Na2O2与H2O和CO2反应,写出其中Na2O2与CO2反应的化学方程式为___________。
第1章 认识化学科学 寒假演练题2024--2025学年高一上学期化学鲁科版(2019)必修第一册
一、选择题。(18题)
1、化学科学史上每一次重大的发现都极大地推进了科学的发展,对于人类文明的进步发挥了巨大的推动作用,如合成氨技术,制造出能促进粮食增产的大量氮肥,使成千上万的人免除饥饿的威胁。下列对化学史的描述不正确的是( )
A.侯德榜联合制碱法中制得的碱是烧碱
B.道尔顿提出了原子论
C.阿伏加德罗提出了分子学说
D.拉瓦锡提出了燃烧的氧化学说
【答案】A
2、下列说法不正确的是( )
A.84消毒液和过氧乙酸常用于环境消毒,消毒原理相同
B.自来水厂常用明矾消毒、净化水质
C.咳嗽产生的飞沫分散到空气中形成气溶胶
D.亚硝酸盐中毒和CO中毒的原理不相同
【答案】B
3、某同学按如图所示实验装置进行钠与水反应的实验,据此判断下列说法正确的是( )
A.打开右端活塞,将一小块金属钠加入煤油中,反应前片刻,钠的位置在a处
B.开始反应后,能观察到的实验现象是钠在b处液面以下的水中反应
C.反应一段时间后,左端液面上升进入长颈漏斗,b处有无色气体产生
D.若用酒精来代替煤油,可观察到相同的实验现象
【答案】C
4、当足量的Cl2或盐酸分别与下列金属反应时,均有MCl2型化合物生成的是( )
A.Fe B.Mg C.Cu D.Ag
【答案】B
5、在自来水的生产中,常通入适量氯气进行杀菌消毒,氯气与水反应的产物之一是盐酸。市场上有些不法商贩为牟取暴利,利用自来水冒充纯净水桶装出售。为辨别真伪,可用下列哪一种试剂来鉴别( )
A.酚酞试液 B.氯化钡溶液
C.氢氧化钠溶液 D.硝酸银溶液
【答案】D
6、某容器真空时,称量其质量为60.4 g,此容器充满N2时总质量为66.0 g,在相同状况下,充满另一气体时,总质量为74.6 g,那么该气体可能是( )
A.Cl2 B.O2 C.SO2 D.HCl
【答案】A
7、下列溶液中,与200mL0.5mol/LNa2SO4溶液所含物质的量浓度相同的是( )
A.200mL0.25mol/LNaCl溶液 B.100mL1mol/LNaCl溶液
C.100mL0.5mol/LNaOH溶液 D.100mL2mol/LNaOH溶液
【答案】B
8、下列各气体:①0.5molHe;②9.0gNO;③3.4g的NH3;④3.01×1023个CO2。四种物质所含的原子总数最多是( )
A.① B.② C.③ D.④
【答案】D
9、某溶液含有①②③④⑤等五种阴离子,向其中加入少量的过氧化钠固体后,溶液中的离子浓度基本保持不变的是(忽略溶液体积变化)( )
A.① B.①⑤ C.①④⑤ D.①③⑤
【答案】A
10、对危险化学品要在包装标签上印有警示性标志。氢氧化钠溶液应选用的标志是( )
A B C D
爆炸品 氧化剂 剧毒品 腐蚀品
A.A B.B C.C D.D
【答案】D
11、下列实验操作中错误的是( )
A.蒸馏操作时,应使温度计水银球靠近蒸馏烧瓶的支管口处
B.蒸发操作时,当蒸发皿中的水分只残留少许时,停止加热,利用余热将剩余水分蒸干
C.称量时,将NaOH固体放在称量纸上置于托盘天平的左盘,将砝码放在托盘天平的右盘
D.溶解操作时,玻璃棒作用是搅拌以加速溶解;过滤操作时,玻璃棒作用是引流,防止溶液溅出
【答案】C
12、下列物质的转化不能通过一步反应实现的是( )
A.Na→NaOH B.Na→Na2CO3
C.Na2O→NaOH D.Na2O2→Na2CO3
【答案】B
13、使用容量瓶配制溶液过程中,下列操作会使所配制的溶液浓度不发生变化的是( )
A.溶液转移到容量瓶后,烧杯内壁及玻璃棒未用蒸馏水洗涤
B.转移溶液前,容量瓶内存有少量蒸馏水
C.定容时,俯视容量瓶的刻度线
D.定容后摇匀,发现液面降低,又补加少量蒸馏水重新达到刻度线
【答案】B
14、将一定物质的量的Na2CO3、NaHCO3组成的混合物溶于水,配成1L溶液,取出50mL溶液然后滴加一定物质的量浓度的盐酸得到的图像如图所示,下列说法正确的是( )
A.标注NaCl的直线代表产生的CO2的物质的量
B.原混合物中Na2CO3与NaHCO3的物质的量之比为1:2
C.盐酸的浓度是0.05mol·L-1
D.盐酸加到
15、用NA表示阿伏加 德罗常数的值,下列叙述正确的是( )
①22gT2O含有电子数为10NA
②0.44gC3H8中含有的共价键总数目为0.1NA
③1molNa2O2与CO2完全反应时转移电子数为2NA
④28g硅晶体中含有2NA个Si—Si键
⑤11.2LCl2通入足量的NaOH溶液中充分反应,转移的电子数等于0.5NA
⑥200mL1mol·L-1Al2(SO4)3溶液中Al3+和SO42-的数目总和是NA
A.①②③ B.②④⑥ C.①③⑤ D.①②④
【答案】D
16、在化学实验中,玻璃棒一般不用于( )
A.捣碎块状固体 B.转移引流液体 C.蘸取少量溶液 D.搅拌加速溶解
【答案】A
17、已知浓盐酸和次氯酸钙能发生如下反应:Ca(ClO)2+4HCl(浓) ===CaCl2+2Cl2↑+2H2O。用贮存很久的漂白粉与浓盐酸反应制得的氯气中,可能含有的杂质气体是( )
①CO2 ②HCl ③H2O ④O2
A.①②③ B.②③④ C.②③ D.①④
【答案】A
18、同温同压下,具有相同分子数的气体一定具有( )
A.相同的体积 B.相同的质量
C.相同的分子量 D.相同的密度
【答案】A
二、填空题。(3题)
19、环保部门检测到某工厂的工业废水中含有大量的FeSO4、较多的Cu2+和少量的Na+。为了减少污染并变废为宝,要求该工厂从该废水中回收硫酸亚铁和金属铜。该工厂设计了如下流程图,完成回收硫酸亚铁和铜的简单实验方案。
回答下列问题
(1)填写试剂A的化学式 _______________
(2)假如加入2mol D刚好完全反应,此步转移的电子的物质的量为 __________
(3)写出加入A的离子方程式: _________________
(4)操作Ⅱ和III 的名称分别是 ___________、 ____________、________
【答案】(1)Fe (2)4mol (3)Fe+Cu2+=Fe2++Cu
(4)过滤 蒸发浓缩 冷却结晶
20、现用金属钠和空气制备纯度较高的可利用的装置如图:
请回答下列问题:
(1)若规定气体的流动方向为从左到右,则组合实验装置时各仪器的连接顺序是:空气→Ⅳ→_______→_______→_______(填“Ⅰ”“Ⅱ”“Ⅲ”,仪器不能重复使用)。
(2)装置Ⅳ中盛放的药品是_______ ,其作用是_______ 。
(3)装置Ⅱ的作用是_______ 。
(4)加热装置Ⅰ时发生反应的化学方程式为_______ 。
【答案】(1)Ⅲ;Ⅰ;Ⅱ
(2)氢氧化钠溶液;吸收通入空气中的二氧化碳
(3)防止空气中的水蒸气和二氧化碳进入装置Ⅰ
(4)
21、欲配制1 mol/L的氢氧化钠溶液250mL,完成下列步骤:
(1)用天平称取氢氧化钠固体_________克。
(2)将称好的氢氧化钠固体放入________中,加蒸馏水将其溶解,待冷却后将溶液沿_________移入________mL的容量瓶中。
(3)用少量蒸馏水冲洗玻璃棒和烧杯2~3次,将冲洗液移入___________中,在操作过程中不损失点滴液体,否则会使溶液的浓度偏_______(高或低)。
(4)向容量瓶内加水至刻度线________时,改用_____________小心地加水至溶液凹液面与刻度线相切,若加水超过刻度线,会造成溶液浓度__________,应该______________。
(5)最后盖好瓶盖,震荡摇匀,将配好的溶液移入___________中并贴好标签。
【答案】10.0 烧杯 玻璃棒 250 250mL容量瓶 低 1cm~2cm 胶头滴管 低 重新配制 试剂瓶
三、实验题。
22、在课堂上,老师演示了金属钠与CuSO4溶液反应的实验,同学们观察到该反应中生成了蓝色的Cu(OH)2沉淀和气泡,而没有发现铜单质。某同学想,会不会是因为生成的铜较少而被蓝色沉淀所覆盖从而没有被发现呢?于是他想课后到实验室继续探究,希望进一步用实验来验证自己的猜测是否正确。
(1)假如你是该同学,请你写一份实验准备单交给老师,要求老师提供必需的用品。
①实验探究的目的:_______________________________________________。
②探究所依据的化学原理:_________________________________________。
③实验必需的仪器或用品:小刀、玻璃片、滤纸、______________和烧杯;药品:金属钠、CuSO4溶液和______________。
(2)该同学在探究实验中意外地发现了生成的蓝色沉淀中混有少量的黑色难溶物,而所使用的药品均没有问题,你认为该黑色难溶物是____________(填化学式),生成该黑色难溶物的原因是(结合化学方程式和必要的文字作答)
_________________________________________________________________ 。
【答案】(1)①验证钠与硫酸铜溶液反应是否有铜生成
②氢氧化铜可溶于盐酸而铜不溶
③镊子 稀盐酸(或稀硫酸)
(2)CuO 钠与水反应放出的热使生成的Cu(OH)2部分发生分解,
Cu(OH)2CuO+H2O
23、某同学在实验室进行如图所示的过氧化钠性质实验。请回答下列问题:
(1)如图所示实验,滴入几滴水,整个过程现象是___________。实验结束后,向试管所得溶液中滴加酚酞溶液,现象是___________。
(2)过氧化钠与水反应的化学方程式为___________。
(3)若用嘴通过导管向附着少量Na2O2粉末的脱脂棉吹气,棉花燃烧。原因是Na2O2与H2O和CO2反应,写出其中Na2O2与CO2反应的化学方程式为___________。
【答案】(1) 有大量气泡产生,使带火星的木条复燃 溶液先变红后褪色
(2)2Na2O2+2H2O=4NaOH+O2↑
(3)2Na2O2+2CO2=2Na2CO3+O2
