第九单元课题1溶液及其应用课件(共43张PPT 内嵌视频)-2024-2025学年九年级化学人教版(2024)下册
文档属性
| 名称 | 第九单元课题1溶液及其应用课件(共43张PPT 内嵌视频)-2024-2025学年九年级化学人教版(2024)下册 |  | |
| 格式 | pptx | ||
| 文件大小 | 72.5MB | ||
| 资源类型 | 教案 | ||
| 版本资源 | 人教版 | ||
| 科目 | 化学 | ||
| 更新时间 | 2025-02-07 20:09:00 | ||
图片预览








文档简介
(共43张PPT)
第九单元 溶液
课题1 溶液及其应用
学习目标
1.通过物质在水中溶解的观察和分析,知道溶液、溶质、溶剂的概念。
2.通过实验探究知道物质在溶解过程中通常伴随着热量的变化。
3.了解溶液在日常生活、工农业生产、科学研究和医疗等领域的应用。
4.在体验科学探究的过程中培养独立思考、合作交流的能力,形成科学严谨的探究意识,提高科学素养。
CONTENT 目录
溶液的形成
Ⅰ
Ⅱ
溶液的应用
海的味道
你知道吗?
海水中溶解了许多物质,它是一种混合物,也是我们常见的一种溶液,主要含有氯化钠,除此还含有氯化镁、硫酸镁等物质。
什么是溶液?溶液又是怎样形成的?
实验9-1:蔗糖在水中的溶解
蔗糖
烧杯
玻璃棒
玻璃棒搅拌,
加快溶解
蒸馏水
实验视频:蔗糖在水中的溶解
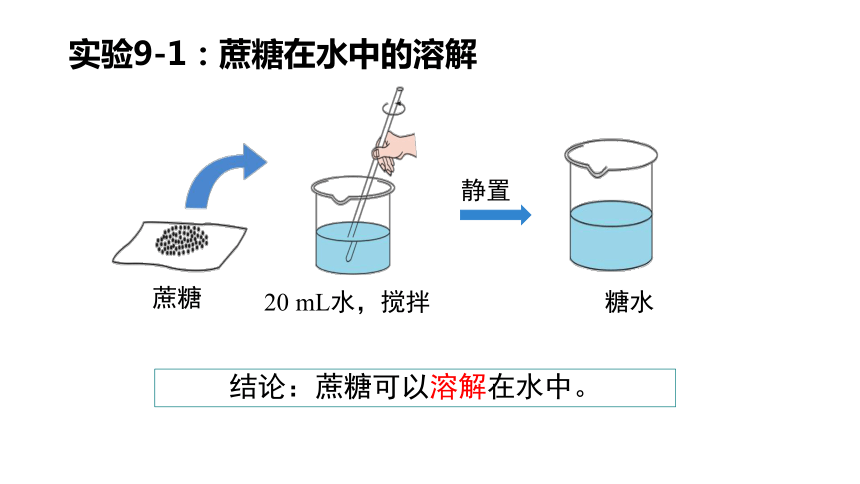
实验9-1:蔗糖在水中的溶解
蔗糖
20 mL水,搅拌
糖水
静置
结论:蔗糖可以溶解在水中。
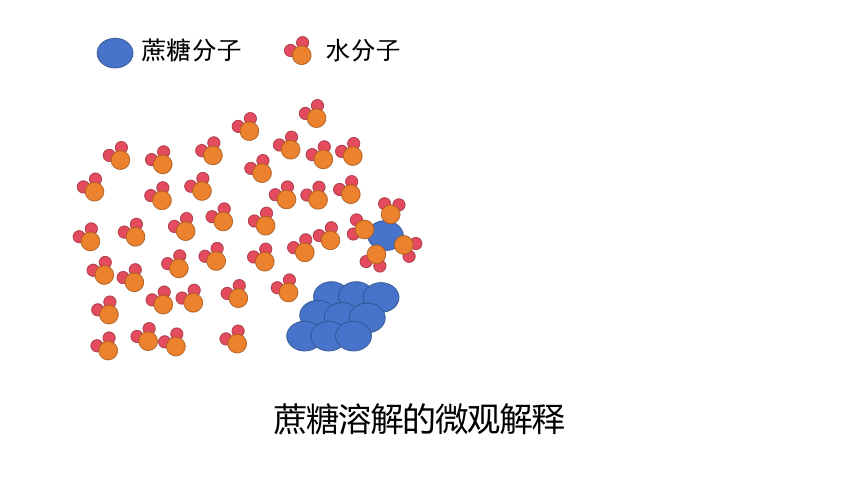
蔗糖分子
水分子
蔗糖溶解的微观解释
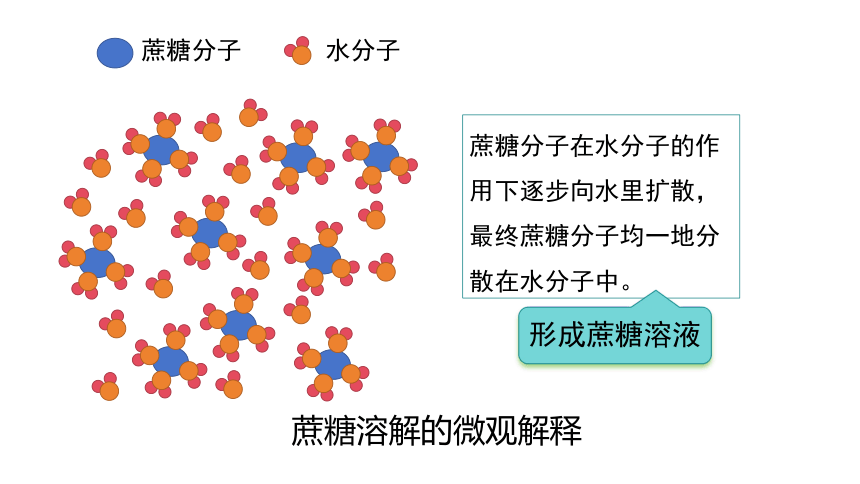
蔗糖分子
水分子
蔗糖分子在水分子的作用下逐步向水里扩散,最终蔗糖分子均一地分散在水分子中。
形成蔗糖溶液
蔗糖溶解的微观解释
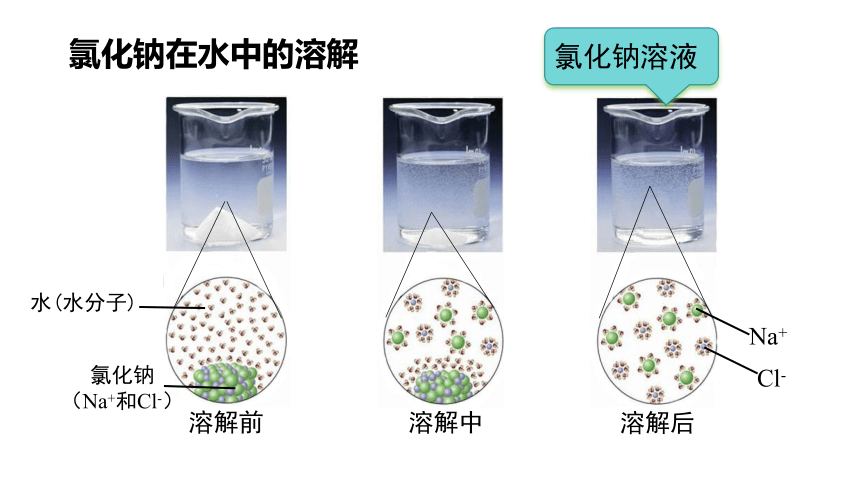
溶解前
溶解中
溶解后
水(水分子)
氯化钠(Na+和Cl-)
氯化钠在水中的溶解
氯化钠溶液
Na+
Cl-
定义:一种或几种物质分散到另一种物质里,形成均一的、稳定的混合物。
1、溶液
不是“反应”
蔗糖溶液
均一性:任一部分的组成和性质完全相同(指密度、浓度、性质等)
稳定性:在外界条件(温度、压强等)不变时,溶质不会从溶剂中分离出来
交流讨论:把溶液密封保存,在外界条件不变的情况下,溶液会出现分层或沉淀吗?将泥土或食用油加入水中能形成溶液吗?
泥土不溶解,沉降
食用油浮在水面上
硫酸铜溶液
稳定性
不是溶液
紫红色
蓝色
浅绿色
黄色
氯化铁溶液
硫酸铜溶液
高锰酸钾溶液
氯化亚铁溶液
交流讨论:水是溶液吗?溶液都是无色的吗?
水
纯净物,不是溶液
2、溶液的组成
硫酸铜晶体
硫酸铜溶液
水
溶质
溶剂
溶液
【溶剂】能溶解其他物质的物质叫做溶剂,如:水。
【溶质】被溶解的物质叫做溶质,如:蔗糖、氯化钠。
交流讨论:分析下列溶液中的溶质和溶剂。
蔗糖溶液
氯化钠溶液
氯化铁溶液
蔗糖和氯化钠的混合溶液
溶质:蔗糖
蔗糖+水
氯化钠+水
氯化铁+水
蔗糖+氯化钠+水
溶剂:水
溶质:氯化钠
溶剂:水
溶质:氯化铁
溶剂:水
溶质:蔗糖+ 氯化钠
溶剂:水
溶液、溶质和溶剂之间量的关系
1.溶液的质量
=溶质的质量+溶剂的质量
2.溶液的体积
≠溶质的体积+溶剂的体积
碘
水
碘
汽油
高锰酸钾
水
高锰酸钾
汽油
实验9-2:探究影响物质溶解性的因素
对照实验
任务:观看实验视频,观察并分析实验现象
溶剂 水 汽油 水 汽油
溶质 碘 碘 高锰酸钾 高锰酸钾
现象
实验9-2:探究影响物质溶解性的因素
无明显变化
结论:同一物质在不同溶剂中的溶解性是不同的,
不同物质在同一溶剂中的溶解性也是不同的。
溶解,
呈紫红色
溶解,
呈红棕色
无明显变化
溶质和溶剂
实验9-3:乙醇能溶解在水中
在盛有2mL水的试管中滴入两滴红墨水(用红墨水是为了显色,便于观察),振荡。然后将管倾斜,用滴管沿试管内壁(注意:滴管不要接触试管壁)缓缓加入2mL乙醇,不要振荡,观察液体是否分层,然后振荡,静置几分钟,观察现象。
实验内容 现象 结论
加入乙醇,不振荡
加入乙醇后振荡 静置 乙醇与水分层
均匀混合,不分层
不分层
酒精能溶于水
乙醇的水溶液
一般读作:溶质的溶剂溶液
若溶剂为水,可省略溶剂
乙醇,俗名酒精
C2H5OH
实验9-3:乙醇能溶解在水中
体系 溶质 溶剂
气+液
固+液
液+液 无水
有水
气体 液体
固体 液体
量少 量多
非水物质 水
溶液中溶质和溶剂的判断
溶 液 溶 质 溶 剂 说明
硫酸铜溶液
稀盐酸 稀/浓硫酸(98%) 医用酒精(75%) 生理盐水 碘 酒 双氧水 澄清石灰水 糖盐水 硫酸铜(CuSO4)
水
氯化氢(HCl)气体
水
氢氧化钙(Ca(OH)2)
水
乙醇(C2H5OH)液体
水
氯化钠(NaCl)
水
碘( I2 )
乙醇
硫酸(H2SO4)
过氧化氢(H2O2)
水
水
1.只要有水,水就是溶剂,不管多少;
2.一种溶液中溶剂只有一种,但溶质可以有多种。
3.溶质可以为固体、液体、气体
蔗糖、氯化钠
水
小结
提出问题
物质溶解的过程中是否有热量的变化?
猜想与假设
①有热量变化
②无热量变化
——吸热或放热
——温度不变
设计实验
向三个烧杯中各注入100mL水,用温度计测出水的温度。取NaCl、NH4NO3、NaOH固体各两药匙,分别加入上述三个烧杯中,用玻璃棒搅拌至固体全部溶解,再用温度计分别测量三种溶液的温度,记录并分析测量所得数据。
注意:氢氧化钠有强烈的腐蚀性,使用时必须十分小心,防止溅到眼睛、皮肤、衣服等上面。实验时戴好护目镜。
实验9-4:溶解过程能量变化
实验9-4:溶解过程能量变化
水中加入的溶质 NaCl NH4NO3 NaOH
加入溶质前水的温度/℃
溶质溶解后溶液的温度/℃
结论 实验记录与分析
22℃ 22℃ 22℃
22℃ 19℃ 33.8℃
得出结论
NH4NO3
NaOH
NaCl
温度降低
温度升高
温度变化不明显
吸收热量
放出热量
几乎无热量变化
物质在溶解过程中常伴随着热量的变化。
1.氢氧化钠固体
2.硝酸铵晶体
3.氯化钠晶体
1.氢氧化钠固体
2.硝酸铵晶体
3.氯化钠晶体
交流讨论:用下图所示装置进行实验,向锥形瓶中加入一定量的下列物质,判断气球如何变化。
气球鼓起
气球变瘪
气球不变
气球变瘪
气球鼓起
气球不变
溶液吸放热的应用
硝酸铵制冷
二、溶液的应用
生长在营养液中的植物
医疗注射液
硫酸铜溶液
稀盐酸
化学实验使用的溶液
医药制剂
二、溶液的应用
溶液的应用
无土栽培营养液
化学溶液试剂
食品饮料
生物体内的溶液
【思考】化学反应常在溶液中进行的原因 。
加快反应速率
二、溶液的应用
乙醚提取青蒿素
青蒿素是治疗疟疾耐药性效果最好的药物,在屠呦呦及其团队的努力下,最终利用青蒿素能溶解于乙醚溶剂中,成功提取青蒿素。不仅拯救了世界上数百万人的生命,更是中国历史上第一个诺贝尔奖!
屠呦呦
振荡植物油与水的混合物,可以得到乳状浑浊的液体。在这种液体里分散着不溶于水的、由许多分子集合而成的小液滴,这种液体叫作乳浊液。把少量泥土放入水中搅拌,也会得到一种浑浊的液体。在这种液体里悬浮着很多不溶于水的固体小颗粒,使液体呈现浑浊状态,这种液体叫作悬浊液。
乳浊液和悬浊液
油不能溶于水
搅拌
乳浊液
静置
分层
乳浊液和悬浊液
乳浊液和悬浊液具有广泛的用途。例如,用X射线检查肠胃病时,让患者服用的钡餐就是硫酸钡的悬浊液。粉刷墙壁用的乳胶漆的主要原料--合成树脂乳液是乳浊液。在农业上,为了合理使用农药,常把不溶于水的固体或液体农药配制成悬浊液或乳浊液,用来喷酒遭受病虫害的农作物。这样农药药液散失得少,附着在面上的多,药液喷洒均匀,既节省农药,又提高药效,使用还很方便。
课堂小结
一种或几
种物质
分散
水是
常用
溶剂
溶剂
固
液
气
溶质
另一种
物质
均一稳定的
混合物
溶液
应用
形成过程中的热量变化
课堂练习
1. 下列生活中常见的物质中,属于溶液的是( )
A. 冰水混合物 B. 医用酒精
C. 泥水 D. 石灰浆
2.下列有关碘酒的说法错误的是( )
A.碘酒是混合物 B.碘酒是溶液
C.碘是溶质 D.酒精是溶质
B
D
课堂练习
3.下列关于溶液的说法正确的是( )
A.溶液中一定含有水
B.均一、稳定的液体一定是溶液
C.只有固体和液体可以作为溶质
D.当外界条件不变时,密封溶液不论放置多长时间,溶质也不会从溶剂中分离出来
D
课堂练习
4.下列实验探究影响物质溶解性的因素。实验现象:
①A中几乎不溶
②B中固体可溶
③C中固体可溶。
现象________(填序号)说明不同的物质在同一溶剂中的溶解性不同。
AC
课堂练习
5.将一定量的下列固体放入适量水中,能形成溶液且温度明显升高的是( )
A.CaCO3 B.NaOH C.NaCl D.NH4NO3
C
B
课堂练习
6.如图所示,在试管中加入水,然后向试管中加入下列哪种物质,U型管中液面左边明显上升,右边下降( )
A. 氯化钠 B. 硝酸铵
C. 蔗糖 D. 氢氧化钠
B
第九单元 溶液
课题1 溶液及其应用
学习目标
1.通过物质在水中溶解的观察和分析,知道溶液、溶质、溶剂的概念。
2.通过实验探究知道物质在溶解过程中通常伴随着热量的变化。
3.了解溶液在日常生活、工农业生产、科学研究和医疗等领域的应用。
4.在体验科学探究的过程中培养独立思考、合作交流的能力,形成科学严谨的探究意识,提高科学素养。
CONTENT 目录
溶液的形成
Ⅰ
Ⅱ
溶液的应用
海的味道
你知道吗?
海水中溶解了许多物质,它是一种混合物,也是我们常见的一种溶液,主要含有氯化钠,除此还含有氯化镁、硫酸镁等物质。
什么是溶液?溶液又是怎样形成的?
实验9-1:蔗糖在水中的溶解
蔗糖
烧杯
玻璃棒
玻璃棒搅拌,
加快溶解
蒸馏水
实验视频:蔗糖在水中的溶解
实验9-1:蔗糖在水中的溶解
蔗糖
20 mL水,搅拌
糖水
静置
结论:蔗糖可以溶解在水中。
蔗糖分子
水分子
蔗糖溶解的微观解释
蔗糖分子
水分子
蔗糖分子在水分子的作用下逐步向水里扩散,最终蔗糖分子均一地分散在水分子中。
形成蔗糖溶液
蔗糖溶解的微观解释
溶解前
溶解中
溶解后
水(水分子)
氯化钠(Na+和Cl-)
氯化钠在水中的溶解
氯化钠溶液
Na+
Cl-
定义:一种或几种物质分散到另一种物质里,形成均一的、稳定的混合物。
1、溶液
不是“反应”
蔗糖溶液
均一性:任一部分的组成和性质完全相同(指密度、浓度、性质等)
稳定性:在外界条件(温度、压强等)不变时,溶质不会从溶剂中分离出来
交流讨论:把溶液密封保存,在外界条件不变的情况下,溶液会出现分层或沉淀吗?将泥土或食用油加入水中能形成溶液吗?
泥土不溶解,沉降
食用油浮在水面上
硫酸铜溶液
稳定性
不是溶液
紫红色
蓝色
浅绿色
黄色
氯化铁溶液
硫酸铜溶液
高锰酸钾溶液
氯化亚铁溶液
交流讨论:水是溶液吗?溶液都是无色的吗?
水
纯净物,不是溶液
2、溶液的组成
硫酸铜晶体
硫酸铜溶液
水
溶质
溶剂
溶液
【溶剂】能溶解其他物质的物质叫做溶剂,如:水。
【溶质】被溶解的物质叫做溶质,如:蔗糖、氯化钠。
交流讨论:分析下列溶液中的溶质和溶剂。
蔗糖溶液
氯化钠溶液
氯化铁溶液
蔗糖和氯化钠的混合溶液
溶质:蔗糖
蔗糖+水
氯化钠+水
氯化铁+水
蔗糖+氯化钠+水
溶剂:水
溶质:氯化钠
溶剂:水
溶质:氯化铁
溶剂:水
溶质:蔗糖+ 氯化钠
溶剂:水
溶液、溶质和溶剂之间量的关系
1.溶液的质量
=溶质的质量+溶剂的质量
2.溶液的体积
≠溶质的体积+溶剂的体积
碘
水
碘
汽油
高锰酸钾
水
高锰酸钾
汽油
实验9-2:探究影响物质溶解性的因素
对照实验
任务:观看实验视频,观察并分析实验现象
溶剂 水 汽油 水 汽油
溶质 碘 碘 高锰酸钾 高锰酸钾
现象
实验9-2:探究影响物质溶解性的因素
无明显变化
结论:同一物质在不同溶剂中的溶解性是不同的,
不同物质在同一溶剂中的溶解性也是不同的。
溶解,
呈紫红色
溶解,
呈红棕色
无明显变化
溶质和溶剂
实验9-3:乙醇能溶解在水中
在盛有2mL水的试管中滴入两滴红墨水(用红墨水是为了显色,便于观察),振荡。然后将管倾斜,用滴管沿试管内壁(注意:滴管不要接触试管壁)缓缓加入2mL乙醇,不要振荡,观察液体是否分层,然后振荡,静置几分钟,观察现象。
实验内容 现象 结论
加入乙醇,不振荡
加入乙醇后振荡 静置 乙醇与水分层
均匀混合,不分层
不分层
酒精能溶于水
乙醇的水溶液
一般读作:溶质的溶剂溶液
若溶剂为水,可省略溶剂
乙醇,俗名酒精
C2H5OH
实验9-3:乙醇能溶解在水中
体系 溶质 溶剂
气+液
固+液
液+液 无水
有水
气体 液体
固体 液体
量少 量多
非水物质 水
溶液中溶质和溶剂的判断
溶 液 溶 质 溶 剂 说明
硫酸铜溶液
稀盐酸 稀/浓硫酸(98%) 医用酒精(75%) 生理盐水 碘 酒 双氧水 澄清石灰水 糖盐水 硫酸铜(CuSO4)
水
氯化氢(HCl)气体
水
氢氧化钙(Ca(OH)2)
水
乙醇(C2H5OH)液体
水
氯化钠(NaCl)
水
碘( I2 )
乙醇
硫酸(H2SO4)
过氧化氢(H2O2)
水
水
1.只要有水,水就是溶剂,不管多少;
2.一种溶液中溶剂只有一种,但溶质可以有多种。
3.溶质可以为固体、液体、气体
蔗糖、氯化钠
水
小结
提出问题
物质溶解的过程中是否有热量的变化?
猜想与假设
①有热量变化
②无热量变化
——吸热或放热
——温度不变
设计实验
向三个烧杯中各注入100mL水,用温度计测出水的温度。取NaCl、NH4NO3、NaOH固体各两药匙,分别加入上述三个烧杯中,用玻璃棒搅拌至固体全部溶解,再用温度计分别测量三种溶液的温度,记录并分析测量所得数据。
注意:氢氧化钠有强烈的腐蚀性,使用时必须十分小心,防止溅到眼睛、皮肤、衣服等上面。实验时戴好护目镜。
实验9-4:溶解过程能量变化
实验9-4:溶解过程能量变化
水中加入的溶质 NaCl NH4NO3 NaOH
加入溶质前水的温度/℃
溶质溶解后溶液的温度/℃
结论 实验记录与分析
22℃ 22℃ 22℃
22℃ 19℃ 33.8℃
得出结论
NH4NO3
NaOH
NaCl
温度降低
温度升高
温度变化不明显
吸收热量
放出热量
几乎无热量变化
物质在溶解过程中常伴随着热量的变化。
1.氢氧化钠固体
2.硝酸铵晶体
3.氯化钠晶体
1.氢氧化钠固体
2.硝酸铵晶体
3.氯化钠晶体
交流讨论:用下图所示装置进行实验,向锥形瓶中加入一定量的下列物质,判断气球如何变化。
气球鼓起
气球变瘪
气球不变
气球变瘪
气球鼓起
气球不变
溶液吸放热的应用
硝酸铵制冷
二、溶液的应用
生长在营养液中的植物
医疗注射液
硫酸铜溶液
稀盐酸
化学实验使用的溶液
医药制剂
二、溶液的应用
溶液的应用
无土栽培营养液
化学溶液试剂
食品饮料
生物体内的溶液
【思考】化学反应常在溶液中进行的原因 。
加快反应速率
二、溶液的应用
乙醚提取青蒿素
青蒿素是治疗疟疾耐药性效果最好的药物,在屠呦呦及其团队的努力下,最终利用青蒿素能溶解于乙醚溶剂中,成功提取青蒿素。不仅拯救了世界上数百万人的生命,更是中国历史上第一个诺贝尔奖!
屠呦呦
振荡植物油与水的混合物,可以得到乳状浑浊的液体。在这种液体里分散着不溶于水的、由许多分子集合而成的小液滴,这种液体叫作乳浊液。把少量泥土放入水中搅拌,也会得到一种浑浊的液体。在这种液体里悬浮着很多不溶于水的固体小颗粒,使液体呈现浑浊状态,这种液体叫作悬浊液。
乳浊液和悬浊液
油不能溶于水
搅拌
乳浊液
静置
分层
乳浊液和悬浊液
乳浊液和悬浊液具有广泛的用途。例如,用X射线检查肠胃病时,让患者服用的钡餐就是硫酸钡的悬浊液。粉刷墙壁用的乳胶漆的主要原料--合成树脂乳液是乳浊液。在农业上,为了合理使用农药,常把不溶于水的固体或液体农药配制成悬浊液或乳浊液,用来喷酒遭受病虫害的农作物。这样农药药液散失得少,附着在面上的多,药液喷洒均匀,既节省农药,又提高药效,使用还很方便。
课堂小结
一种或几
种物质
分散
水是
常用
溶剂
溶剂
固
液
气
溶质
另一种
物质
均一稳定的
混合物
溶液
应用
形成过程中的热量变化
课堂练习
1. 下列生活中常见的物质中,属于溶液的是( )
A. 冰水混合物 B. 医用酒精
C. 泥水 D. 石灰浆
2.下列有关碘酒的说法错误的是( )
A.碘酒是混合物 B.碘酒是溶液
C.碘是溶质 D.酒精是溶质
B
D
课堂练习
3.下列关于溶液的说法正确的是( )
A.溶液中一定含有水
B.均一、稳定的液体一定是溶液
C.只有固体和液体可以作为溶质
D.当外界条件不变时,密封溶液不论放置多长时间,溶质也不会从溶剂中分离出来
D
课堂练习
4.下列实验探究影响物质溶解性的因素。实验现象:
①A中几乎不溶
②B中固体可溶
③C中固体可溶。
现象________(填序号)说明不同的物质在同一溶剂中的溶解性不同。
AC
课堂练习
5.将一定量的下列固体放入适量水中,能形成溶液且温度明显升高的是( )
A.CaCO3 B.NaOH C.NaCl D.NH4NO3
C
B
课堂练习
6.如图所示,在试管中加入水,然后向试管中加入下列哪种物质,U型管中液面左边明显上升,右边下降( )
A. 氯化钠 B. 硝酸铵
C. 蔗糖 D. 氢氧化钠
B
同课章节目录
