陕西省西安市长安区2024-2025学年高一(上)期末化学试卷(含答案)
文档属性
| 名称 | 陕西省西安市长安区2024-2025学年高一(上)期末化学试卷(含答案) |

|
|
| 格式 | docx | ||
| 文件大小 | 161.7KB | ||
| 资源类型 | 教案 | ||
| 版本资源 | 人教版(2019) | ||
| 科目 | 化学 | ||
| 更新时间 | 2025-02-11 00:00:00 | ||
图片预览


文档简介
陕西省西安市长安区2024-2025学年高一(上)期末化学试卷
一、单选题:本大题共14小题,共42分。
1.自主创新是我国成为世界科技强国的关键支点。下列说法错误的是( )
A. 钛合金可用于飞机发动机压气机部件,合金中可以含有非金属元素
B. “鸿蒙”操作系统载体芯片的主体材料硅属于电解质
C. 我国首次获得公斤级丰度的产品,与互为同位素
D. “神舟十九”号飞船的热控保温材料纳米气凝胶,可产生丁达尔效应
2.钇在新能源电池中有着重要的应用,钇的一种核素为,该核素的中子数为( )
A. B. C. D.
3.下列古代技术的工作原理不涉及氧化还原反应的是( )
A. 冶炼金属 B. 火药爆炸 C. 粮食酿酒 D. 活字印刷
4.下列化学用语或图示表示错误的是( )
A. 的结构式:
B. 原子的结构示意图:
C. 用电子式表示氯化镁的形成过程:
D. 的电离方程式:
5.某实验需要溶液,配制该溶液的部分实验操作如图所示,列说法错误的是 ( )
A. 此实验应用托盘天平称取固体
B. 进行操作时,若俯视容量瓶的刻度线,则所配制的溶液浓度偏高
C. 进行操作时,待固体在烧杯中完全溶解后,立即转移到容量瓶中
D. 上述实验操作的先后顺序是
6.下列各组离子在指定溶液中能大量共存的是( )
A. 澄清透明的溶液中:、、、
B. 使紫色石蕊试液呈红色的溶液中:、、、
C. 浓度为的溶液中:、、、
D. 含有大量的溶液中:、、、
7.设为阿伏加德罗常数的值,下列说法正确的是( )
A. 溶液中含离子总数为
B. 与足量铁粉反应转移的电子数为
C. 标况下和混合气体中含有的氧原子数为
D. 中含有的非极性键数目为
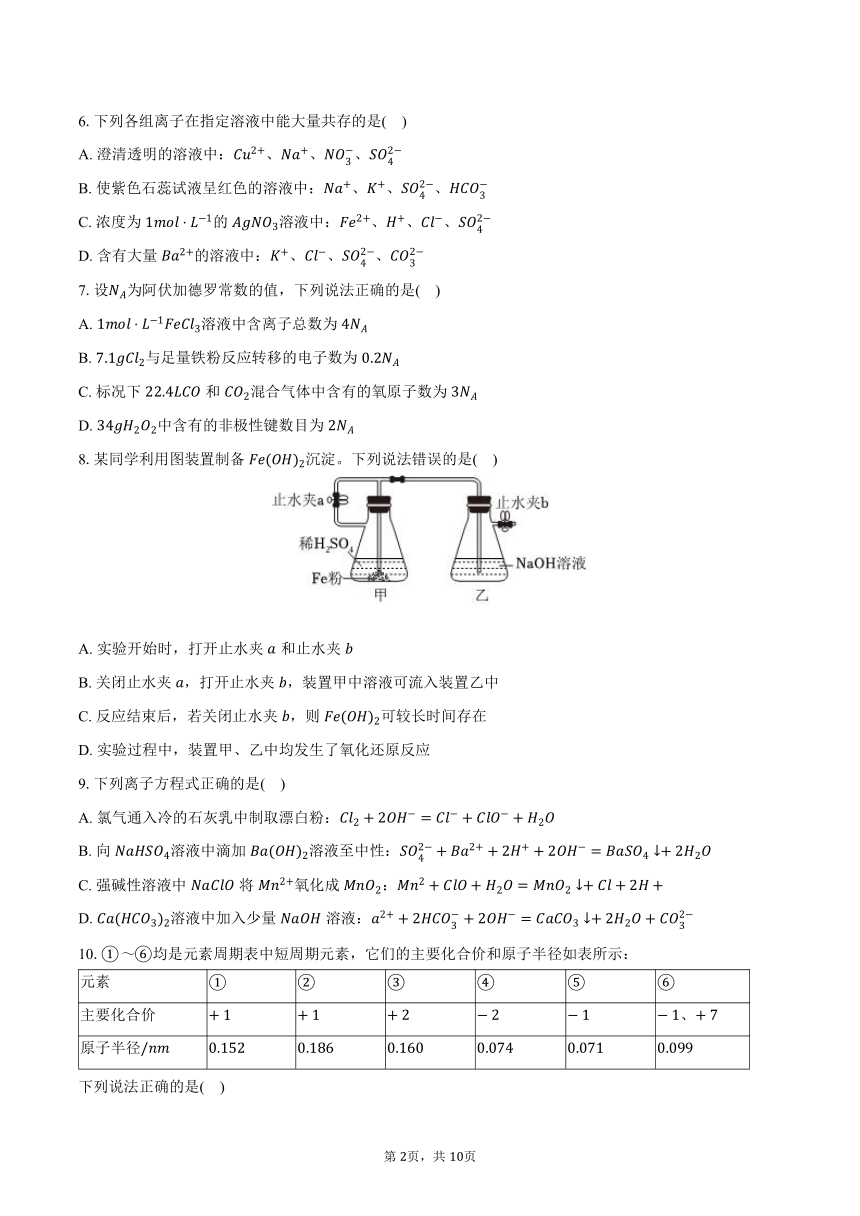
8.某同学利用图装置制备沉淀。下列说法错误的是( )
A. 实验开始时,打开止水夹和止水夹
B. 关闭止水夹,打开止水夹,装置甲中溶液可流入装置乙中
C. 反应结束后,若关闭止水夹,则可较长时间存在
D. 实验过程中,装置甲、乙中均发生了氧化还原反应
9.下列离子方程式正确的是( )
A. 氯气通入冷的石灰乳中制取漂白粉:
B. 向溶液中滴加溶液至中性:
C. 强碱性溶液中将氧化成:
D. 溶液中加入少量溶液:
10.均是元素周期表中短周期元素,它们的主要化合价和原子半径如表所示:
元素
主要化合价 、
原子半径
下列说法正确的是( )
A. 的原子半径在与它同主族的原子中最小 B. 的最高价氧化物对应的水化物是强酸
C. 与形成的化合物属于共价化合物 D. 、的单质在暗处就能与氢气反应
11.称取在空气中部分变质的粉末样品溶于水中,收集到气体,然后向水溶液中加入质量分数为的盐酸恰好完全反应,则发生变质的与未变质的的质量比为( )
A. : B. : C. : D. :
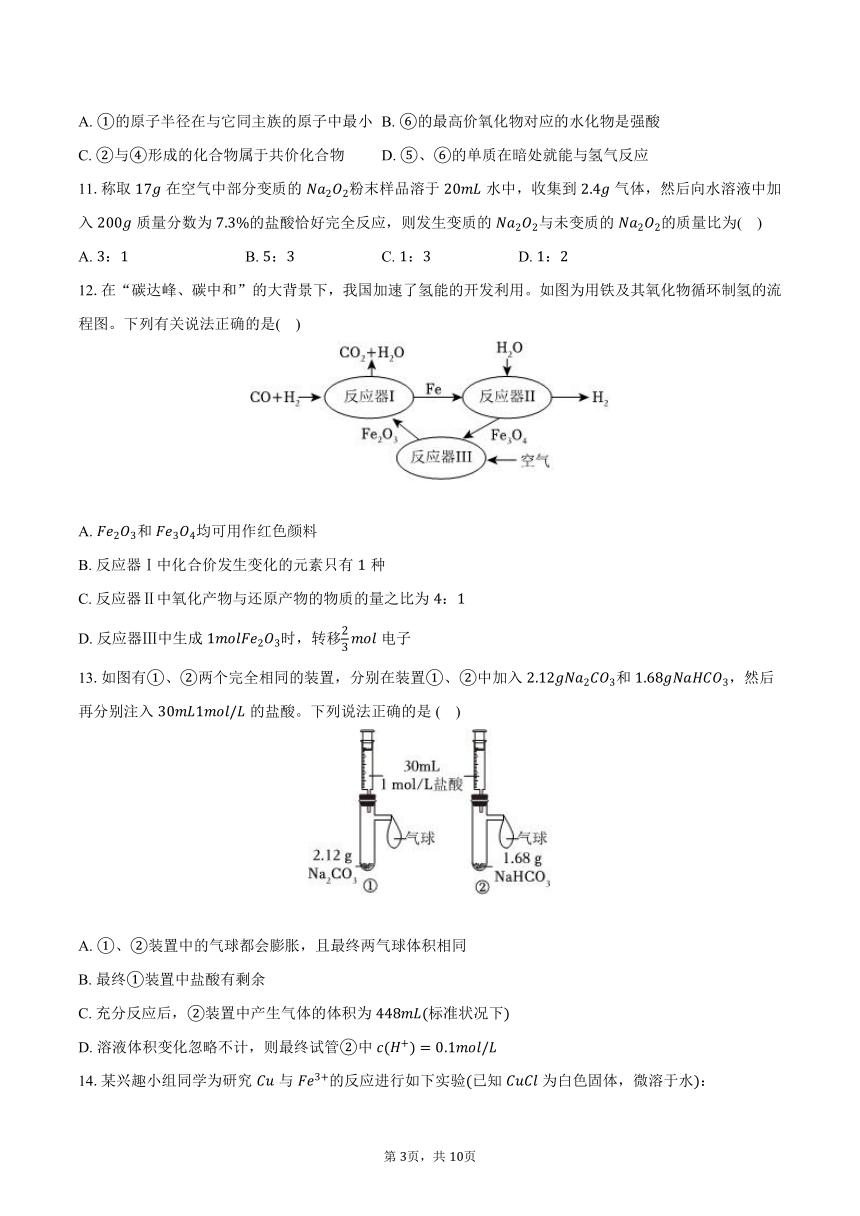
12.在“碳达峰、碳中和”的大背景下,我国加速了氢能的开发利用。如图为用铁及其氧化物循环制氢的流程图。下列有关说法正确的是( )
A. 和均可用作红色颜料
B. 反应器Ⅰ中化合价发生变化的元素只有种
C. 反应器Ⅱ中氧化产物与还原产物的物质的量之比为:
D. 反应器Ⅲ中生成时,转移电子
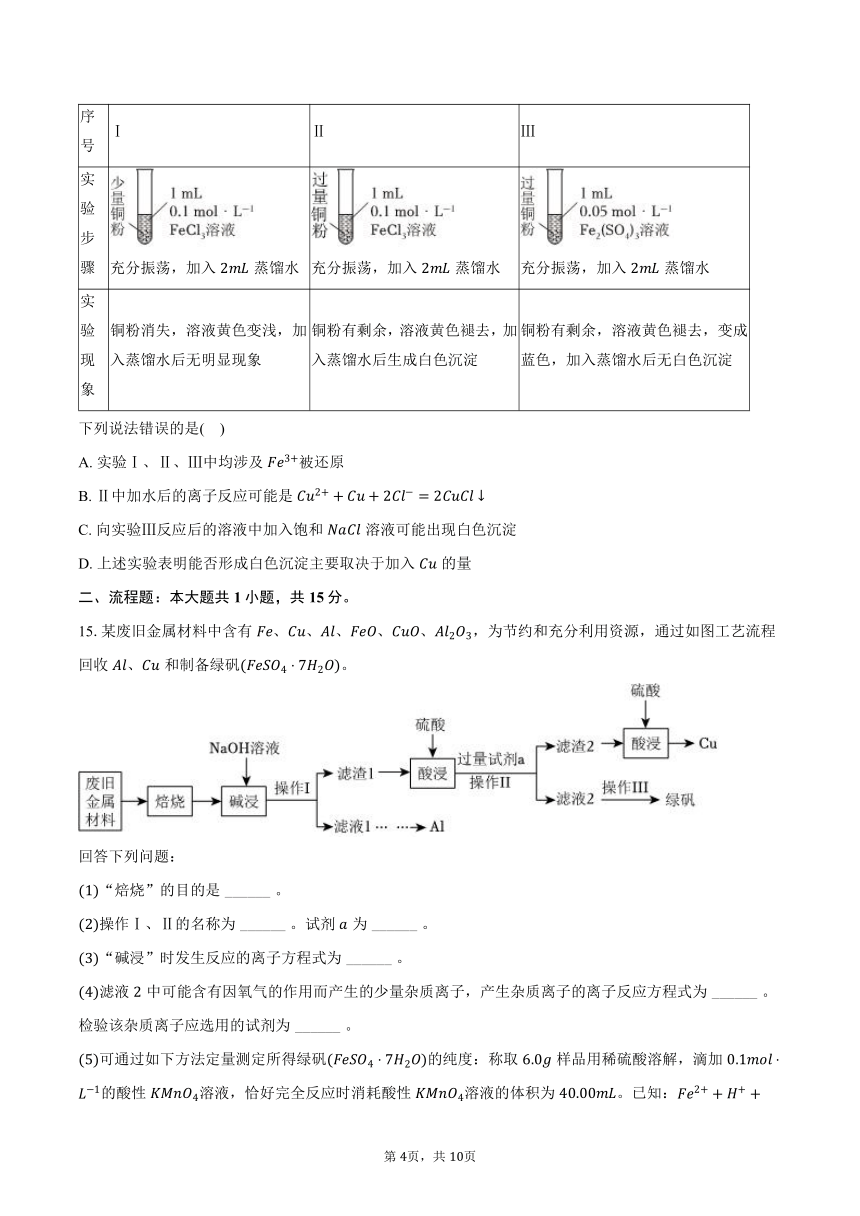
13.如图有、两个完全相同的装置,分别在装置、中加入和,然后再分别注入的盐酸。下列说法正确的是 ( )
A. 、装置中的气球都会膨胀,且最终两气球体积相同
B. 最终装置中盐酸有剩余
C. 充分反应后,装置中产生气体的体积为标准状况下
D. 溶液体积变化忽略不计,则最终试管中
14.某兴趣小组同学为研究与的反应进行如下实验已知为白色固体,微溶于水:
序号 Ⅰ Ⅱ Ⅲ
实验步骤
充分振荡,加入蒸馏水
充分振荡,加入蒸馏水
充分振荡,加入蒸馏水
实验现象 铜粉消失,溶液黄色变浅,加入蒸馏水后无明显现象 铜粉有剩余,溶液黄色褪去,加入蒸馏水后生成白色沉淀 铜粉有剩余,溶液黄色褪去,变成蓝色,加入蒸馏水后无白色沉淀
下列说法错误的是( )
A. 实验Ⅰ、Ⅱ、Ⅲ中均涉及被还原
B. Ⅱ中加水后的离子反应可能是
C. 向实验Ⅲ反应后的溶液中加入饱和溶液可能出现白色沉淀
D. 上述实验表明能否形成白色沉淀主要取决于加入的量
二、流程题:本大题共1小题,共15分。
15.某废旧金属材料中含有、、、、、,为节约和充分利用资源,通过如图工艺流程回收、和制备绿矾。
回答下列问题:
“焙烧”的目的是 ______ 。
操作Ⅰ、Ⅱ的名称为 ______ 。试剂为 ______ 。
“碱浸”时发生反应的离子方程式为 ______ 。
滤液中可能含有因氧气的作用而产生的少量杂质离子,产生杂质离子的离子反应方程式为 ______ 。检验该杂质离子应选用的试剂为 ______ 。
可通过如下方法定量测定所得绿矾的纯度:称取样品用稀硫酸溶解,滴加的酸性溶液,恰好完全反应时消耗酸性溶液的体积为。已知:未配平。计算绿矾的纯度为 ______ 精确到。
绿矾隔绝空气受热分解生成多种化合物过程的热重曲线残留样品质量随温度变化的曲线如图所示。
温度为时,固体物质的化学式为 ______ 。
在隔绝空气的条件下,由得到的化学方程式为 ______ 。
三、实验题:本大题共1小题,共15分。
16.含氯物质在生产、生活中有重要作用。化学小组同学为研究氯气的制备和性质进行了如图实验:
盛装的仪器名称为 ______ 。
实验室欲制备并收集干燥、纯净的,则实验装置接口的连接顺序为 ______ 用小写字母表示,写出浓盐酸与发生反应的离子方程式: ______ 。
饱和食盐水的作用是 ______ 。
若用与足量浓盐酸充分反应,则生成的在标准状况下的体积为 ______ 。
为验证卤素单质氧化性的相对强弱,某小组利用收集的进行了如下实验。夹持仪器已略去,装置气密性良好
已知:装置Ⅰ中可反应生成淀粉遇变蓝色;稀溴水呈黄色,浓溴水呈红棕色。
实验步骤:
打开弹簧夹和活塞,滴加浓盐酸。
当装置Ⅱ和装置Ⅲ分液漏斗中的溶液都变为黄色时,夹紧弹簧夹。
当装置Ⅱ中溶液由黄色变为红棕色时,关闭活塞。
证明单质的氧化性强于的实验现象是 ______ 。
装置Ⅱ中溶液发生反应的离子方程式为 ______ 。
为验证的氧化性强于,步骤的操作是 ______ 。
、、的氧化性逐渐减弱的本质原因是 ______ 。
四、简答题:本大题共2小题,共28分。
17.从古至今,金属及其化合物在人类的生产生活中都起到了巨大的作用。
我国古代四大发明之一指南针是由天然磁石制成的,该磁石的主要成分是 ______ 填化学式。
宋代洗冤集录中记载有“银针探毒”,其原理为。该反应的还原剂是 ______ ,用双线桥法标出该反应中转移电子的方向和数目: ______ 。
过氧化钠可用作呼吸面具、潜水艇的供氧剂,写出和反应的化学方程式: ______ 。
厨房中常用小苏打做膨松剂,使馒头变得更加松软,其原理是 ______ 用化学方程式表示。
现代工业常用的氯化铁溶液腐蚀覆在绝缘板上的铜箔,制作印刷电路板。为了使废液主要成分为、和进行回收再利用,设计了如图流程:
“滤渣”的主要成分是 ______ 填化学式,下同,“滤液”的主要成分为 ______ 。
写出通入时发生反应的离子方程式: ______ 。
18.是原子序数依次增大的五种短周期主族元素,其相关信息如表。
元素 特征
该元素的某种原子不含中子
简单氢化物的分子结构模型为
位于第周期Ⅴ族
该元素形成的化合物灼烧时火焰呈现黄色
该元素形成的单质常温下是黄绿色的有毒气体
请回答下列问题:
元素的化学符号为 ______ ,、对应的简单氢化物的稳定性强弱顺序为 ______ 用化学式表示。
元素与元素形成化合物的电子式为 ______ ,其含有的化学键类型为 ______ 填“极性”或“非极性”共价键。
的单质与的单质在加热条件下反应的化学方程式为 ______ 。
是中学化学常用的强氧化剂,可与还原剂发生反应。化学兴趣小组为探究与的反应,设计了如图所示装置进行实验。
上述装置中,碱石灰的作用是 ______ 。
实验过程中观察到熔化后,很快变成白色粉末,但干燥管内无水硫酸铜并未变成蓝色。则与反应的化学方程式为 ______ ,将产物放入含有酚酞的溶液中,若 ______ 填现象,说明没有完全反应。
装置乙为启普发生器,下列有关说法错误的是 ______ 填字母。
A.使用装置乙不需要检查装置气密性
B.为加快反应速率,可以对装置乙进行加热
C.若要使反应停止,应关闭活塞
D.装置乙也可用于高锰酸钾和浓盐酸制备氯气
答案和解析
1.【答案】
2.【答案】
3.【答案】
4.【答案】
5.【答案】
6.【答案】
7.【答案】
8.【答案】
9.【答案】
10.【答案】
11.【答案】
12.【答案】
13.【答案】
14.【答案】
15.【答案】将金属单质转化为氧化物 过滤
16.【答案】蒸馏烧瓶 除去杂质气体 湿润的淀粉试纸变蓝 打开活塞,将少量分液漏斗中溶液滴入溶液中,关闭活塞,取下试管,振荡,静置后加入层溶液变为紫红色 同主族元素从上到下,原子半径增大,对核外电子的吸引能力减弱,得电子能力逐渐减弱
17.【答案】 、
18.【答案】 极性 吸收中的水蒸气 溶液先变为红色、后迅速褪色
第8页,共9页
一、单选题:本大题共14小题,共42分。
1.自主创新是我国成为世界科技强国的关键支点。下列说法错误的是( )
A. 钛合金可用于飞机发动机压气机部件,合金中可以含有非金属元素
B. “鸿蒙”操作系统载体芯片的主体材料硅属于电解质
C. 我国首次获得公斤级丰度的产品,与互为同位素
D. “神舟十九”号飞船的热控保温材料纳米气凝胶,可产生丁达尔效应
2.钇在新能源电池中有着重要的应用,钇的一种核素为,该核素的中子数为( )
A. B. C. D.
3.下列古代技术的工作原理不涉及氧化还原反应的是( )
A. 冶炼金属 B. 火药爆炸 C. 粮食酿酒 D. 活字印刷
4.下列化学用语或图示表示错误的是( )
A. 的结构式:
B. 原子的结构示意图:
C. 用电子式表示氯化镁的形成过程:
D. 的电离方程式:
5.某实验需要溶液,配制该溶液的部分实验操作如图所示,列说法错误的是 ( )
A. 此实验应用托盘天平称取固体
B. 进行操作时,若俯视容量瓶的刻度线,则所配制的溶液浓度偏高
C. 进行操作时,待固体在烧杯中完全溶解后,立即转移到容量瓶中
D. 上述实验操作的先后顺序是
6.下列各组离子在指定溶液中能大量共存的是( )
A. 澄清透明的溶液中:、、、
B. 使紫色石蕊试液呈红色的溶液中:、、、
C. 浓度为的溶液中:、、、
D. 含有大量的溶液中:、、、
7.设为阿伏加德罗常数的值,下列说法正确的是( )
A. 溶液中含离子总数为
B. 与足量铁粉反应转移的电子数为
C. 标况下和混合气体中含有的氧原子数为
D. 中含有的非极性键数目为
8.某同学利用图装置制备沉淀。下列说法错误的是( )
A. 实验开始时,打开止水夹和止水夹
B. 关闭止水夹,打开止水夹,装置甲中溶液可流入装置乙中
C. 反应结束后,若关闭止水夹,则可较长时间存在
D. 实验过程中,装置甲、乙中均发生了氧化还原反应
9.下列离子方程式正确的是( )
A. 氯气通入冷的石灰乳中制取漂白粉:
B. 向溶液中滴加溶液至中性:
C. 强碱性溶液中将氧化成:
D. 溶液中加入少量溶液:
10.均是元素周期表中短周期元素,它们的主要化合价和原子半径如表所示:
元素
主要化合价 、
原子半径
下列说法正确的是( )
A. 的原子半径在与它同主族的原子中最小 B. 的最高价氧化物对应的水化物是强酸
C. 与形成的化合物属于共价化合物 D. 、的单质在暗处就能与氢气反应
11.称取在空气中部分变质的粉末样品溶于水中,收集到气体,然后向水溶液中加入质量分数为的盐酸恰好完全反应,则发生变质的与未变质的的质量比为( )
A. : B. : C. : D. :
12.在“碳达峰、碳中和”的大背景下,我国加速了氢能的开发利用。如图为用铁及其氧化物循环制氢的流程图。下列有关说法正确的是( )
A. 和均可用作红色颜料
B. 反应器Ⅰ中化合价发生变化的元素只有种
C. 反应器Ⅱ中氧化产物与还原产物的物质的量之比为:
D. 反应器Ⅲ中生成时,转移电子
13.如图有、两个完全相同的装置,分别在装置、中加入和,然后再分别注入的盐酸。下列说法正确的是 ( )
A. 、装置中的气球都会膨胀,且最终两气球体积相同
B. 最终装置中盐酸有剩余
C. 充分反应后,装置中产生气体的体积为标准状况下
D. 溶液体积变化忽略不计,则最终试管中
14.某兴趣小组同学为研究与的反应进行如下实验已知为白色固体,微溶于水:
序号 Ⅰ Ⅱ Ⅲ
实验步骤
充分振荡,加入蒸馏水
充分振荡,加入蒸馏水
充分振荡,加入蒸馏水
实验现象 铜粉消失,溶液黄色变浅,加入蒸馏水后无明显现象 铜粉有剩余,溶液黄色褪去,加入蒸馏水后生成白色沉淀 铜粉有剩余,溶液黄色褪去,变成蓝色,加入蒸馏水后无白色沉淀
下列说法错误的是( )
A. 实验Ⅰ、Ⅱ、Ⅲ中均涉及被还原
B. Ⅱ中加水后的离子反应可能是
C. 向实验Ⅲ反应后的溶液中加入饱和溶液可能出现白色沉淀
D. 上述实验表明能否形成白色沉淀主要取决于加入的量
二、流程题:本大题共1小题,共15分。
15.某废旧金属材料中含有、、、、、,为节约和充分利用资源,通过如图工艺流程回收、和制备绿矾。
回答下列问题:
“焙烧”的目的是 ______ 。
操作Ⅰ、Ⅱ的名称为 ______ 。试剂为 ______ 。
“碱浸”时发生反应的离子方程式为 ______ 。
滤液中可能含有因氧气的作用而产生的少量杂质离子,产生杂质离子的离子反应方程式为 ______ 。检验该杂质离子应选用的试剂为 ______ 。
可通过如下方法定量测定所得绿矾的纯度:称取样品用稀硫酸溶解,滴加的酸性溶液,恰好完全反应时消耗酸性溶液的体积为。已知:未配平。计算绿矾的纯度为 ______ 精确到。
绿矾隔绝空气受热分解生成多种化合物过程的热重曲线残留样品质量随温度变化的曲线如图所示。
温度为时,固体物质的化学式为 ______ 。
在隔绝空气的条件下,由得到的化学方程式为 ______ 。
三、实验题:本大题共1小题,共15分。
16.含氯物质在生产、生活中有重要作用。化学小组同学为研究氯气的制备和性质进行了如图实验:
盛装的仪器名称为 ______ 。
实验室欲制备并收集干燥、纯净的,则实验装置接口的连接顺序为 ______ 用小写字母表示,写出浓盐酸与发生反应的离子方程式: ______ 。
饱和食盐水的作用是 ______ 。
若用与足量浓盐酸充分反应,则生成的在标准状况下的体积为 ______ 。
为验证卤素单质氧化性的相对强弱,某小组利用收集的进行了如下实验。夹持仪器已略去,装置气密性良好
已知:装置Ⅰ中可反应生成淀粉遇变蓝色;稀溴水呈黄色,浓溴水呈红棕色。
实验步骤:
打开弹簧夹和活塞,滴加浓盐酸。
当装置Ⅱ和装置Ⅲ分液漏斗中的溶液都变为黄色时,夹紧弹簧夹。
当装置Ⅱ中溶液由黄色变为红棕色时,关闭活塞。
证明单质的氧化性强于的实验现象是 ______ 。
装置Ⅱ中溶液发生反应的离子方程式为 ______ 。
为验证的氧化性强于,步骤的操作是 ______ 。
、、的氧化性逐渐减弱的本质原因是 ______ 。
四、简答题:本大题共2小题,共28分。
17.从古至今,金属及其化合物在人类的生产生活中都起到了巨大的作用。
我国古代四大发明之一指南针是由天然磁石制成的,该磁石的主要成分是 ______ 填化学式。
宋代洗冤集录中记载有“银针探毒”,其原理为。该反应的还原剂是 ______ ,用双线桥法标出该反应中转移电子的方向和数目: ______ 。
过氧化钠可用作呼吸面具、潜水艇的供氧剂,写出和反应的化学方程式: ______ 。
厨房中常用小苏打做膨松剂,使馒头变得更加松软,其原理是 ______ 用化学方程式表示。
现代工业常用的氯化铁溶液腐蚀覆在绝缘板上的铜箔,制作印刷电路板。为了使废液主要成分为、和进行回收再利用,设计了如图流程:
“滤渣”的主要成分是 ______ 填化学式,下同,“滤液”的主要成分为 ______ 。
写出通入时发生反应的离子方程式: ______ 。
18.是原子序数依次增大的五种短周期主族元素,其相关信息如表。
元素 特征
该元素的某种原子不含中子
简单氢化物的分子结构模型为
位于第周期Ⅴ族
该元素形成的化合物灼烧时火焰呈现黄色
该元素形成的单质常温下是黄绿色的有毒气体
请回答下列问题:
元素的化学符号为 ______ ,、对应的简单氢化物的稳定性强弱顺序为 ______ 用化学式表示。
元素与元素形成化合物的电子式为 ______ ,其含有的化学键类型为 ______ 填“极性”或“非极性”共价键。
的单质与的单质在加热条件下反应的化学方程式为 ______ 。
是中学化学常用的强氧化剂,可与还原剂发生反应。化学兴趣小组为探究与的反应,设计了如图所示装置进行实验。
上述装置中,碱石灰的作用是 ______ 。
实验过程中观察到熔化后,很快变成白色粉末,但干燥管内无水硫酸铜并未变成蓝色。则与反应的化学方程式为 ______ ,将产物放入含有酚酞的溶液中,若 ______ 填现象,说明没有完全反应。
装置乙为启普发生器,下列有关说法错误的是 ______ 填字母。
A.使用装置乙不需要检查装置气密性
B.为加快反应速率,可以对装置乙进行加热
C.若要使反应停止,应关闭活塞
D.装置乙也可用于高锰酸钾和浓盐酸制备氯气
答案和解析
1.【答案】
2.【答案】
3.【答案】
4.【答案】
5.【答案】
6.【答案】
7.【答案】
8.【答案】
9.【答案】
10.【答案】
11.【答案】
12.【答案】
13.【答案】
14.【答案】
15.【答案】将金属单质转化为氧化物 过滤
16.【答案】蒸馏烧瓶 除去杂质气体 湿润的淀粉试纸变蓝 打开活塞,将少量分液漏斗中溶液滴入溶液中,关闭活塞,取下试管,振荡,静置后加入层溶液变为紫红色 同主族元素从上到下,原子半径增大,对核外电子的吸引能力减弱,得电子能力逐渐减弱
17.【答案】 、
18.【答案】 极性 吸收中的水蒸气 溶液先变为红色、后迅速褪色
第8页,共9页
同课章节目录
