3.3.3 共价晶体 课时跟踪检测(学生版+教师版)(含解析)2025年高中化学 选择性必修2 (苏教版2019)
文档属性
| 名称 | 3.3.3 共价晶体 课时跟踪检测(学生版+教师版)(含解析)2025年高中化学 选择性必修2 (苏教版2019) |

|
|
| 格式 | docx | ||
| 文件大小 | 369.3KB | ||
| 资源类型 | 教案 | ||
| 版本资源 | 苏教版(2019) | ||
| 科目 | 化学 | ||
| 更新时间 | 2025-02-12 00:00:00 | ||
图片预览




文档简介
第三课时 共价晶体
题组一 共价晶体
1.(2024·连云港高二检测)晶体硅在信息技术产业中有重要应用。下列关于晶体硅的说法不正确的是( )
A.可制半导体芯片 B.可制光导纤维
C.属于无机非金属材料 D.属于共价晶体
2.下列有关叙述错误的是( )
A.金刚石晶体和二氧化硅晶体的最小结构单元都是正四面体
B.1 mol金刚石中C—C键的数目是4NA(设NA为阿伏加德罗常数的值)
C.水晶在熔化时,晶体中的共价键会断裂
D.SiO2晶体是共价晶体,其中不存在分子
3.(2024·扬州高二检测)碳化硅(SiC)晶体结构与金刚石相似,俗称金刚砂。下列说法正确的是( )
A.SiC晶体中,硅、碳元素的质量比为1∶1
B.SiC晶体的熔点较高
C.SiC晶体的硬度较小
D.SiC属于分子晶体
4.下表是某些共价晶体的熔点和硬度。
共价晶体 金刚石 氮化硼 碳化硅 石英 晶体硅 晶体锗
熔点/ ℃ 大于 3 500 3 000 2 830 1 710 1 412 1 211
硬度 10 9.5 9 7 7 6
分析表中的数据,下列叙述正确的是( )
A.构成共价晶体的原子种类越多,晶体的熔点越高
B.构成共价晶体的原子间的共价键键能越大,晶体的熔点越低
C.构成共价晶体的原子的半径越大,晶体的硬度越大
D.构成共价晶体的原子的半径越小,晶体的硬度越大
题组二 常见共价晶体的结构
5.如图是金刚石晶体结构模型,下列关于金刚石的说法正确的是( )
A.金刚石晶体中碳碳键之间的夹角为120°
B.金刚石晶胞中六元环中的碳原子在同一平面内
C.每个碳原子与其他4个最近的碳原子相连形成正四面体结构
D.金刚石晶体中碳原子与碳碳键数目之比为1∶4
6.(2024·无锡高二检测)晶体硼的结构如图所示,熔点2 573 K。已知晶体硼结构单元是由硼原子组成的正二十面体,其中有20个等边三角形的面和一定数目的顶点,每个顶点上各有1个B原子。下列有关说法不正确的是( )
A.每个结构单元含有20个硼原子 B.1 mol晶体硼中含有30NA个B—B键
C.晶体硼中键角是60° D.晶体硼是共价晶体
7.“天问一号”采用了我国自主研制的高性能碳化硅增强铝基复合材料。碳化硅也叫金刚砂,硬度大,具有耐热性、耐氧化性和耐腐蚀性等性能,结构如图所示,下列叙述不正确的是( )
A.碳化硅为共价晶体
B.碳化硅的熔点比金刚石低
C.1 mol碳化硅中含2 mol Si—C键
D.碳原子和硅原子与其紧邻原子形成的空间结构相同
题组三 投影图
8.有一种氮化硼晶体的结构与金刚石相似,其晶胞如图所示。
氮化硼晶胞的俯视投影图是( )
9.InP晶体属于立方晶系,其晶胞结构如图1所示,晶胞参数为a nm,若沿y轴方向观察该晶胞,可得投影图如图2所示。已知NA为阿伏加德罗常数的值,下列说法不正确的是( )
A.晶体中In的配位数为4 B.晶胞中,1、2原子间间距与2、4相等
C.晶体密度为×1021 g·cm-3 D.P原子与In原子之间的最近距离为 nm
10.(2024·泰州高二检测)氮化硼(BN)是一种重要的功能陶瓷材料。以天然硼砂为起始物,经过一系列反应可以得到BF3和BN,如图1所示。下列叙述错误的是( )
A.H3BO3在水溶液中发生反应:H3BO3+H2OH++[B(OH4)]-,可知H3BO3是一元弱酸
B.六方氮化硼在高温、高压下,可以转化为立方氮化硼,其晶胞结构如图2,立方氮化硼晶胞中含有4个氮原子、4个硼原子
C.由B2O3可制备晶体硼,晶体硼的熔点为2 573 K,沸点为2 823 K,硬度大,属于共价晶体
D.NH4BF4(氟硼酸铵)是合成氮化硼纳米管的原料之一,1 mol NH4BF4含有配位键的数目为NA
11.一种广谱性熏蒸杀虫剂,其晶体熔点约为2 000 ℃,晶胞结构如图所示。已知该晶体的密度为ρ g·cm-3,NA表示阿伏加德罗常数的值。下列有关该晶体的说法错误的是( )
A.化学式为AlP B.晶体类型为共价晶体
C.晶胞中Al原子的配位数为8 D.两个P原子间的最近核间距为××1010 pm
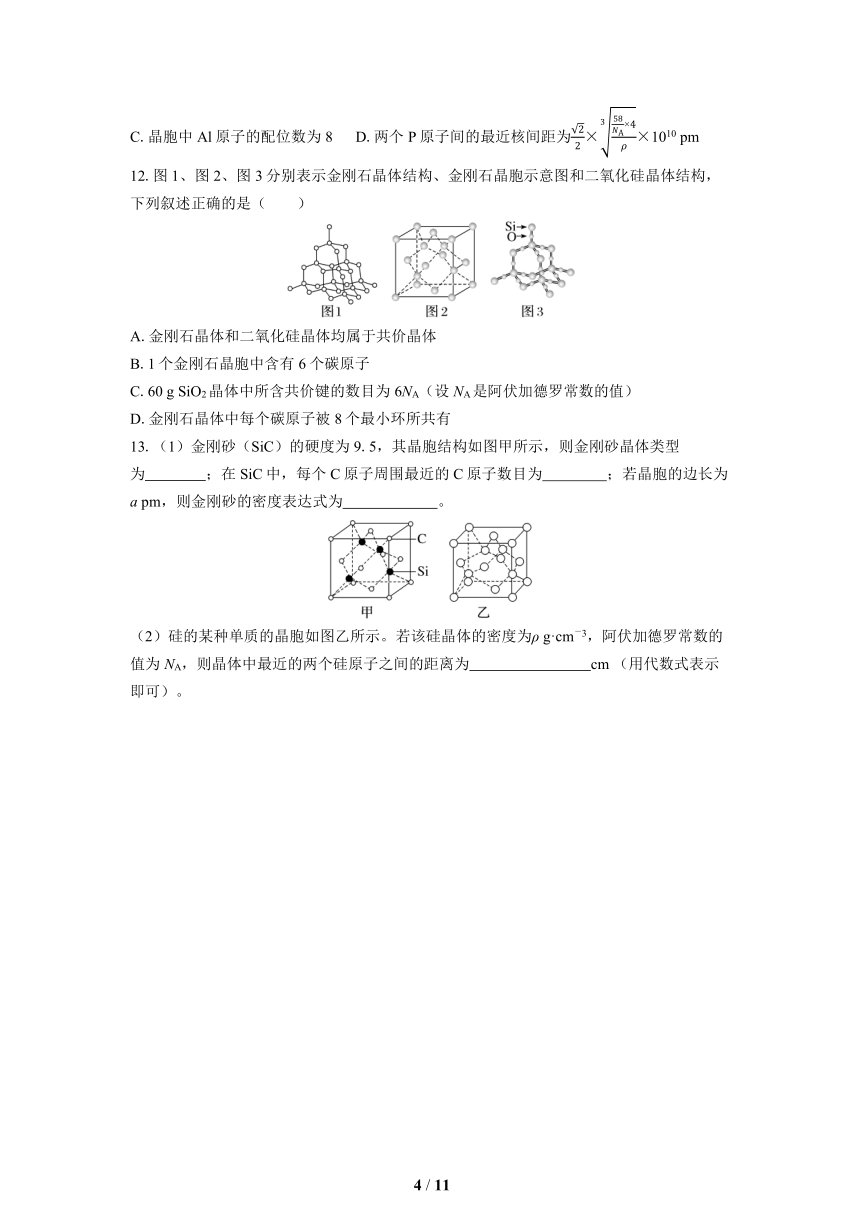
12.图1、图2、图3分别表示金刚石晶体结构、金刚石晶胞示意图和二氧化硅晶体结构,下列叙述正确的是( )
A.金刚石晶体和二氧化硅晶体均属于共价晶体
B.1个金刚石晶胞中含有6个碳原子
C.60 g SiO2晶体中所含共价键的数目为6NA(设NA是阿伏加德罗常数的值)
D.金刚石晶体中每个碳原子被8个最小环所共有
13.(1)金刚砂(SiC)的硬度为9.5,其晶胞结构如图甲所示,则金刚砂晶体类型为 ;在SiC中,每个C原子周围最近的C原子数目为 ;若晶胞的边长为a pm,则金刚砂的密度表达式为 。
(2)硅的某种单质的晶胞如图乙所示。若该硅晶体的密度为ρ g·cm-3,阿伏加德罗常数的值为NA,则晶体中最近的两个硅原子之间的距离为 cm (用代数式表示即可)。
题组一 共价晶体
1.(2024·连云港高二检测)晶体硅在信息技术产业中有重要应用。下列关于晶体硅的说法不正确的是( )
A.可制半导体芯片
B.可制光导纤维
C.属于无机非金属材料
D.属于共价晶体
解析:B 晶体硅是熔沸点高、硬度大的共价晶体,属于性能优良的无机非金属材料,可用于制半导体芯片,但不能用于制光导纤维,选B。
2.下列有关叙述错误的是( )
A.金刚石晶体和二氧化硅晶体的最小结构单元都是正四面体
B.1 mol金刚石中C—C键的数目是4NA(设NA为阿伏加德罗常数的值)
C.水晶在熔化时,晶体中的共价键会断裂
D.SiO2晶体是共价晶体,其中不存在分子
解析:B 金刚石晶体中,1个中心C原子连接4个C原子,二氧化硅晶体中,1个中心Si原子连接4个O原子,二者的最小结构单元均为正四面体,A项正确;金刚石中1个C—C键为2个C原子所有,1个C原子占有个C—C键,1 mol金刚石中C—C键的数目为4NA×=2NA,B项错误;水晶在熔化时,共价键会断裂,C项正确;SiO2是由Si原子和O原子构成的共价晶体,所以SiO2晶体中不含分子,D项正确。
3.(2024·扬州高二检测)碳化硅(SiC)晶体结构与金刚石相似,俗称金刚砂。下列说法正确的是( )
A.SiC晶体中,硅、碳元素的质量比为1∶1
B.SiC晶体的熔点较高
C.SiC晶体的硬度较小
D.SiC属于分子晶体
解析:B SiC晶体中,硅、碳元素的质量比为28∶12=7∶3,A项错误;SiC晶体结构与金刚石相似,属于共价晶体,熔点较高,B项正确,D项错误;SiC晶体属于共价晶体,硬度较大,C项错误。
4.下表是某些共价晶体的熔点和硬度。
共价晶体 金刚石 氮化硼 碳化硅 石英 晶体硅 晶体锗
熔点/ ℃ 大于 3 500 3 000 2 830 1 710 1 412 1 211
硬度 10 9.5 9 7 7 6
分析表中的数据,下列叙述正确的是( )
A.构成共价晶体的原子种类越多,晶体的熔点越高
B.构成共价晶体的原子间的共价键键能越大,晶体的熔点越低
C.构成共价晶体的原子的半径越大,晶体的硬度越大
D.构成共价晶体的原子的半径越小,晶体的硬度越大
解析:D 共价晶体的熔点和硬度与构成共价晶体的原子间的共价键键能有关,而原子间的共价键键能与原子半径的大小有关,原子半径越小,键能越大,共价晶体的熔点越高,硬度越大。
题组二 常见共价晶体的结构
5.如图是金刚石晶体结构模型,下列关于金刚石的说法正确的是( )
A.金刚石晶体中碳碳键之间的夹角为120°
B.金刚石晶胞中六元环中的碳原子在同一平面内
C.每个碳原子与其他4个最近的碳原子相连形成正四面体结构
D.金刚石晶体中碳原子与碳碳键数目之比为1∶4
解析:C 金刚石晶体中每个碳原子与周围四个碳原子形成共价键,形成立体网状结构,碳碳键之间的夹角为109°28',A错误;金刚石晶胞中最小的环为六元环,每个环中有4个碳原子在同一平面内,B错误;每个碳原子与其他4个最近的碳原子相连,形成正四面体结构,C正确;金刚石晶体中每个碳原子和周围4个碳形成碳碳键,碳原子与碳碳键数目之比为1∶=1∶2,D错误。
6.(2024·无锡高二检测)晶体硼的结构如图所示,熔点2 573 K。已知晶体硼结构单元是由硼原子组成的正二十面体,其中有20个等边三角形的面和一定数目的顶点,每个顶点上各有1个B原子。下列有关说法不正确的是( )
A.每个结构单元含有20个硼原子
B.1 mol晶体硼中含有30NA个B—B键
C.晶体硼中键角是60°
D.晶体硼是共价晶体
解析:A 根据图示可知,每个顶点被5个三角形共用,因此B原子个数=20×3×=12,即每个结构单元含有12个硼原子,A错误;三角形的边即B—B键,因此每个结构单元中B—B键个数=20×3×=30,因此1 mol晶体硼中含有30NA个B—B键,B正确;结构单元中每一面都是正三角形,因此晶体硼中键角是60°,C正确;该晶体由B原子之间以共价键结合形成空间立体结构,因此是共价晶体,D正确。
7.“天问一号”采用了我国自主研制的高性能碳化硅增强铝基复合材料。碳化硅也叫金刚砂,硬度大,具有耐热性、耐氧化性和耐腐蚀性等性能,结构如图所示,下列叙述不正确的是( )
A.碳化硅为共价晶体
B.碳化硅的熔点比金刚石低
C.1 mol碳化硅中含2 mol Si—C键
D.碳原子和硅原子与其紧邻原子形成的空间结构相同
解析:C 碳化硅也叫金刚砂,硬度大,具有耐热性,碳化硅为共价晶体,A正确;碳化硅和金刚石都是共价晶体,Si原子半径大于C原子,Si—C键的键长比C—C键的长,键能小,故碳化硅的熔点比金刚石低,B正确;碳化硅中,1个C和4个Si形成4个Si—C键,故1 mol碳化硅中含4 mol Si—C键,C错误;碳化硅中,碳原子和硅原子都通过4个键与紧邻的原子形成四面体结构,D正确。
题组三 投影图
8.有一种氮化硼晶体的结构与金刚石相似,其晶胞如图所示。
氮化硼晶胞的俯视投影图是( )
解析:B 氮化硼晶体的结构与金刚石相似,从题图可知,氮原子位于晶胞顶角和面心上,硼原子处在体对角线的处,两个在离顶面较近的体对角线处,且在相对位置,另外两个在离底面较近的体对角线处,且在相对位置,上两个原子与下两个原子互相错开,即两个原子的连线呈交叉状,故氮化硼晶胞的俯视投影图是B。
9.InP晶体属于立方晶系,其晶胞结构如图1所示,晶胞参数为a nm,若沿y轴方向观察该晶胞,可得投影图如图2所示。已知NA为阿伏加德罗常数的值,下列说法不正确的是( )
A.晶体中In的配位数为4
B.晶胞中,1、2原子间间距与2、4相等
C.晶体密度为×1021 g·cm-3
D.P原子与In原子之间的最近距离为 nm
解析:D 晶体中In和P的配位数相同,与P最近且等距离的In有4个,故In的配位数为4,A正确;图2中,1、2、3、4为晶体内的P原子,1、2原子间间距与2、4相等,B正确;1个晶胞中有4个InP,晶体密度为g·cm-3=×1021 g·cm-3,C正确;P原子与In原子之间的最近距离为晶胞体对角线长的,即nm,D错误。
10.(2024·泰州高二检测)氮化硼(BN)是一种重要的功能陶瓷材料。以天然硼砂为起始物,经过一系列反应可以得到BF3和BN,如图1所示。下列叙述错误的是( )
A.H3BO3在水溶液中发生反应:H3BO3+H2OH++[B(OH4)]-,可知H3BO3是一元弱酸
B.六方氮化硼在高温、高压下,可以转化为立方氮化硼,其晶胞结构如图2,立方氮化硼晶胞中含有4个氮原子、4个硼原子
C.由B2O3可制备晶体硼,晶体硼的熔点为2 573 K,沸点为2 823 K,硬度大,属于共价晶体
D.NH4BF4(氟硼酸铵)是合成氮化硼纳米管的原料之一,1 mol NH4BF4含有配位键的数目为NA
解析:D 由H3BO3在水溶液中发生反应:H3BO3+H2OH++[B(OH)4]-,可知H3BO3是一元弱酸,A正确;由题图2可以看出,立方氮化硼结构与金刚石相似,金刚石晶胞中,8个顶点有8个碳原子,6个面心有6个碳原子,立方体内部还有4个碳原子,金刚石的一个晶胞中含有的碳原子数为8×+6×+4=8,由氮化硼化学式可知晶体中N、B原子个数比为1∶1,故其晶胞中应该含有4个N原子和4个B原子,B正确;共价晶体通常具有很高的熔、沸点和很大的硬度,晶体硼的熔点为2 573 K,沸点为2 823 K,硬度大,说明其属于共价晶体,C项正确;N中含有氮氢配位键,B中含有硼氟配位键,则 1 mol NH4BF4含有配位键的数目为2NA,D错误。
11.一种广谱性熏蒸杀虫剂,其晶体熔点约为2 000 ℃,晶胞结构如图所示。已知该晶体的密度为ρ g·cm-3,NA表示阿伏加德罗常数的值。下列有关该晶体的说法错误的是( )
A.化学式为AlP
B.晶体类型为共价晶体
C.晶胞中Al原子的配位数为8
D.两个P原子间的最近核间距为××
1010 pm
解析:C 该晶胞中含有4个Al原子,8×+6×=4个P原子,化学式为AlP,A正确;根据题干信息,该晶体熔点高约2 000 ℃,应为共价晶体,B正确;Al原子的配位数为4,C错误;由立方晶胞密度计算公式可得晶胞体积为cm3,得到晶胞的边长为×1010pm,两个P原子间的最近核间距为面对角线长度的一半,即××1010pm,D正确。
12.图1、图2、图3分别表示金刚石晶体结构、金刚石晶胞示意图和二氧化硅晶体结构,下列叙述正确的是( )
A.金刚石晶体和二氧化硅晶体均属于共价晶体
B.1个金刚石晶胞中含有6个碳原子
C.60 g SiO2晶体中所含共价键的数目为6NA(设NA是阿伏加德罗常数的值)
D.金刚石晶体中每个碳原子被8个最小环所共有
解析:A 金刚石晶体和二氧化硅晶体均属于共价晶体,A项正确;1个金刚石晶胞中含有碳原子的个数为8×+6×+4=8,B项错误;60 g SiO2晶体的物质的量为1 mol,SiO2晶体中,1个Si原子与4个O原子形成4个Si—O键,故1 mol SiO2中含4NA个Si—O键,C项错误;金刚石晶体中每个碳原子被12个最小环所共有,D项错误。
13.(1)金刚砂(SiC)的硬度为9.5,其晶胞结构如图甲所示,则金刚砂晶体类型为共价晶体;在SiC中,每个C原子周围最近的C原子数目为12;若晶胞的边长为a pm,则金刚砂的密度表达式为。
(2)硅的某种单质的晶胞如图乙所示。若该硅晶体的密度为ρ g·cm-3,阿伏加德罗常数的值为NA,则晶体中最近的两个硅原子之间的距离为×cm (用代数式表示即可)。
解析:(1)金刚砂(SiC)的硬度为9.5,硬度大,属于共价晶体;在SiC中,每个碳原子周围最近的碳原子数目为12;该晶胞中C原子个数为8×+6×=4,Si原子个数为4,晶胞边长为a×10-10 cm,体积V=(a×10-10 cm)3,ρ==。
(2)由图乙的晶胞结构可知,晶体Si的一个晶胞中含有Si原子的数目是8×+6×+4=8,根据晶胞的密度ρ=可知,V=cm3= cm3,晶胞的边长a== cm,在晶胞中最近的两个Si原子之间的距离为晶胞体对角线长的,即× cm。
3 / 4
题组一 共价晶体
1.(2024·连云港高二检测)晶体硅在信息技术产业中有重要应用。下列关于晶体硅的说法不正确的是( )
A.可制半导体芯片 B.可制光导纤维
C.属于无机非金属材料 D.属于共价晶体
2.下列有关叙述错误的是( )
A.金刚石晶体和二氧化硅晶体的最小结构单元都是正四面体
B.1 mol金刚石中C—C键的数目是4NA(设NA为阿伏加德罗常数的值)
C.水晶在熔化时,晶体中的共价键会断裂
D.SiO2晶体是共价晶体,其中不存在分子
3.(2024·扬州高二检测)碳化硅(SiC)晶体结构与金刚石相似,俗称金刚砂。下列说法正确的是( )
A.SiC晶体中,硅、碳元素的质量比为1∶1
B.SiC晶体的熔点较高
C.SiC晶体的硬度较小
D.SiC属于分子晶体
4.下表是某些共价晶体的熔点和硬度。
共价晶体 金刚石 氮化硼 碳化硅 石英 晶体硅 晶体锗
熔点/ ℃ 大于 3 500 3 000 2 830 1 710 1 412 1 211
硬度 10 9.5 9 7 7 6
分析表中的数据,下列叙述正确的是( )
A.构成共价晶体的原子种类越多,晶体的熔点越高
B.构成共价晶体的原子间的共价键键能越大,晶体的熔点越低
C.构成共价晶体的原子的半径越大,晶体的硬度越大
D.构成共价晶体的原子的半径越小,晶体的硬度越大
题组二 常见共价晶体的结构
5.如图是金刚石晶体结构模型,下列关于金刚石的说法正确的是( )
A.金刚石晶体中碳碳键之间的夹角为120°
B.金刚石晶胞中六元环中的碳原子在同一平面内
C.每个碳原子与其他4个最近的碳原子相连形成正四面体结构
D.金刚石晶体中碳原子与碳碳键数目之比为1∶4
6.(2024·无锡高二检测)晶体硼的结构如图所示,熔点2 573 K。已知晶体硼结构单元是由硼原子组成的正二十面体,其中有20个等边三角形的面和一定数目的顶点,每个顶点上各有1个B原子。下列有关说法不正确的是( )
A.每个结构单元含有20个硼原子 B.1 mol晶体硼中含有30NA个B—B键
C.晶体硼中键角是60° D.晶体硼是共价晶体
7.“天问一号”采用了我国自主研制的高性能碳化硅增强铝基复合材料。碳化硅也叫金刚砂,硬度大,具有耐热性、耐氧化性和耐腐蚀性等性能,结构如图所示,下列叙述不正确的是( )
A.碳化硅为共价晶体
B.碳化硅的熔点比金刚石低
C.1 mol碳化硅中含2 mol Si—C键
D.碳原子和硅原子与其紧邻原子形成的空间结构相同
题组三 投影图
8.有一种氮化硼晶体的结构与金刚石相似,其晶胞如图所示。
氮化硼晶胞的俯视投影图是( )
9.InP晶体属于立方晶系,其晶胞结构如图1所示,晶胞参数为a nm,若沿y轴方向观察该晶胞,可得投影图如图2所示。已知NA为阿伏加德罗常数的值,下列说法不正确的是( )
A.晶体中In的配位数为4 B.晶胞中,1、2原子间间距与2、4相等
C.晶体密度为×1021 g·cm-3 D.P原子与In原子之间的最近距离为 nm
10.(2024·泰州高二检测)氮化硼(BN)是一种重要的功能陶瓷材料。以天然硼砂为起始物,经过一系列反应可以得到BF3和BN,如图1所示。下列叙述错误的是( )
A.H3BO3在水溶液中发生反应:H3BO3+H2OH++[B(OH4)]-,可知H3BO3是一元弱酸
B.六方氮化硼在高温、高压下,可以转化为立方氮化硼,其晶胞结构如图2,立方氮化硼晶胞中含有4个氮原子、4个硼原子
C.由B2O3可制备晶体硼,晶体硼的熔点为2 573 K,沸点为2 823 K,硬度大,属于共价晶体
D.NH4BF4(氟硼酸铵)是合成氮化硼纳米管的原料之一,1 mol NH4BF4含有配位键的数目为NA
11.一种广谱性熏蒸杀虫剂,其晶体熔点约为2 000 ℃,晶胞结构如图所示。已知该晶体的密度为ρ g·cm-3,NA表示阿伏加德罗常数的值。下列有关该晶体的说法错误的是( )
A.化学式为AlP B.晶体类型为共价晶体
C.晶胞中Al原子的配位数为8 D.两个P原子间的最近核间距为××1010 pm
12.图1、图2、图3分别表示金刚石晶体结构、金刚石晶胞示意图和二氧化硅晶体结构,下列叙述正确的是( )
A.金刚石晶体和二氧化硅晶体均属于共价晶体
B.1个金刚石晶胞中含有6个碳原子
C.60 g SiO2晶体中所含共价键的数目为6NA(设NA是阿伏加德罗常数的值)
D.金刚石晶体中每个碳原子被8个最小环所共有
13.(1)金刚砂(SiC)的硬度为9.5,其晶胞结构如图甲所示,则金刚砂晶体类型为 ;在SiC中,每个C原子周围最近的C原子数目为 ;若晶胞的边长为a pm,则金刚砂的密度表达式为 。
(2)硅的某种单质的晶胞如图乙所示。若该硅晶体的密度为ρ g·cm-3,阿伏加德罗常数的值为NA,则晶体中最近的两个硅原子之间的距离为 cm (用代数式表示即可)。
题组一 共价晶体
1.(2024·连云港高二检测)晶体硅在信息技术产业中有重要应用。下列关于晶体硅的说法不正确的是( )
A.可制半导体芯片
B.可制光导纤维
C.属于无机非金属材料
D.属于共价晶体
解析:B 晶体硅是熔沸点高、硬度大的共价晶体,属于性能优良的无机非金属材料,可用于制半导体芯片,但不能用于制光导纤维,选B。
2.下列有关叙述错误的是( )
A.金刚石晶体和二氧化硅晶体的最小结构单元都是正四面体
B.1 mol金刚石中C—C键的数目是4NA(设NA为阿伏加德罗常数的值)
C.水晶在熔化时,晶体中的共价键会断裂
D.SiO2晶体是共价晶体,其中不存在分子
解析:B 金刚石晶体中,1个中心C原子连接4个C原子,二氧化硅晶体中,1个中心Si原子连接4个O原子,二者的最小结构单元均为正四面体,A项正确;金刚石中1个C—C键为2个C原子所有,1个C原子占有个C—C键,1 mol金刚石中C—C键的数目为4NA×=2NA,B项错误;水晶在熔化时,共价键会断裂,C项正确;SiO2是由Si原子和O原子构成的共价晶体,所以SiO2晶体中不含分子,D项正确。
3.(2024·扬州高二检测)碳化硅(SiC)晶体结构与金刚石相似,俗称金刚砂。下列说法正确的是( )
A.SiC晶体中,硅、碳元素的质量比为1∶1
B.SiC晶体的熔点较高
C.SiC晶体的硬度较小
D.SiC属于分子晶体
解析:B SiC晶体中,硅、碳元素的质量比为28∶12=7∶3,A项错误;SiC晶体结构与金刚石相似,属于共价晶体,熔点较高,B项正确,D项错误;SiC晶体属于共价晶体,硬度较大,C项错误。
4.下表是某些共价晶体的熔点和硬度。
共价晶体 金刚石 氮化硼 碳化硅 石英 晶体硅 晶体锗
熔点/ ℃ 大于 3 500 3 000 2 830 1 710 1 412 1 211
硬度 10 9.5 9 7 7 6
分析表中的数据,下列叙述正确的是( )
A.构成共价晶体的原子种类越多,晶体的熔点越高
B.构成共价晶体的原子间的共价键键能越大,晶体的熔点越低
C.构成共价晶体的原子的半径越大,晶体的硬度越大
D.构成共价晶体的原子的半径越小,晶体的硬度越大
解析:D 共价晶体的熔点和硬度与构成共价晶体的原子间的共价键键能有关,而原子间的共价键键能与原子半径的大小有关,原子半径越小,键能越大,共价晶体的熔点越高,硬度越大。
题组二 常见共价晶体的结构
5.如图是金刚石晶体结构模型,下列关于金刚石的说法正确的是( )
A.金刚石晶体中碳碳键之间的夹角为120°
B.金刚石晶胞中六元环中的碳原子在同一平面内
C.每个碳原子与其他4个最近的碳原子相连形成正四面体结构
D.金刚石晶体中碳原子与碳碳键数目之比为1∶4
解析:C 金刚石晶体中每个碳原子与周围四个碳原子形成共价键,形成立体网状结构,碳碳键之间的夹角为109°28',A错误;金刚石晶胞中最小的环为六元环,每个环中有4个碳原子在同一平面内,B错误;每个碳原子与其他4个最近的碳原子相连,形成正四面体结构,C正确;金刚石晶体中每个碳原子和周围4个碳形成碳碳键,碳原子与碳碳键数目之比为1∶=1∶2,D错误。
6.(2024·无锡高二检测)晶体硼的结构如图所示,熔点2 573 K。已知晶体硼结构单元是由硼原子组成的正二十面体,其中有20个等边三角形的面和一定数目的顶点,每个顶点上各有1个B原子。下列有关说法不正确的是( )
A.每个结构单元含有20个硼原子
B.1 mol晶体硼中含有30NA个B—B键
C.晶体硼中键角是60°
D.晶体硼是共价晶体
解析:A 根据图示可知,每个顶点被5个三角形共用,因此B原子个数=20×3×=12,即每个结构单元含有12个硼原子,A错误;三角形的边即B—B键,因此每个结构单元中B—B键个数=20×3×=30,因此1 mol晶体硼中含有30NA个B—B键,B正确;结构单元中每一面都是正三角形,因此晶体硼中键角是60°,C正确;该晶体由B原子之间以共价键结合形成空间立体结构,因此是共价晶体,D正确。
7.“天问一号”采用了我国自主研制的高性能碳化硅增强铝基复合材料。碳化硅也叫金刚砂,硬度大,具有耐热性、耐氧化性和耐腐蚀性等性能,结构如图所示,下列叙述不正确的是( )
A.碳化硅为共价晶体
B.碳化硅的熔点比金刚石低
C.1 mol碳化硅中含2 mol Si—C键
D.碳原子和硅原子与其紧邻原子形成的空间结构相同
解析:C 碳化硅也叫金刚砂,硬度大,具有耐热性,碳化硅为共价晶体,A正确;碳化硅和金刚石都是共价晶体,Si原子半径大于C原子,Si—C键的键长比C—C键的长,键能小,故碳化硅的熔点比金刚石低,B正确;碳化硅中,1个C和4个Si形成4个Si—C键,故1 mol碳化硅中含4 mol Si—C键,C错误;碳化硅中,碳原子和硅原子都通过4个键与紧邻的原子形成四面体结构,D正确。
题组三 投影图
8.有一种氮化硼晶体的结构与金刚石相似,其晶胞如图所示。
氮化硼晶胞的俯视投影图是( )
解析:B 氮化硼晶体的结构与金刚石相似,从题图可知,氮原子位于晶胞顶角和面心上,硼原子处在体对角线的处,两个在离顶面较近的体对角线处,且在相对位置,另外两个在离底面较近的体对角线处,且在相对位置,上两个原子与下两个原子互相错开,即两个原子的连线呈交叉状,故氮化硼晶胞的俯视投影图是B。
9.InP晶体属于立方晶系,其晶胞结构如图1所示,晶胞参数为a nm,若沿y轴方向观察该晶胞,可得投影图如图2所示。已知NA为阿伏加德罗常数的值,下列说法不正确的是( )
A.晶体中In的配位数为4
B.晶胞中,1、2原子间间距与2、4相等
C.晶体密度为×1021 g·cm-3
D.P原子与In原子之间的最近距离为 nm
解析:D 晶体中In和P的配位数相同,与P最近且等距离的In有4个,故In的配位数为4,A正确;图2中,1、2、3、4为晶体内的P原子,1、2原子间间距与2、4相等,B正确;1个晶胞中有4个InP,晶体密度为g·cm-3=×1021 g·cm-3,C正确;P原子与In原子之间的最近距离为晶胞体对角线长的,即nm,D错误。
10.(2024·泰州高二检测)氮化硼(BN)是一种重要的功能陶瓷材料。以天然硼砂为起始物,经过一系列反应可以得到BF3和BN,如图1所示。下列叙述错误的是( )
A.H3BO3在水溶液中发生反应:H3BO3+H2OH++[B(OH4)]-,可知H3BO3是一元弱酸
B.六方氮化硼在高温、高压下,可以转化为立方氮化硼,其晶胞结构如图2,立方氮化硼晶胞中含有4个氮原子、4个硼原子
C.由B2O3可制备晶体硼,晶体硼的熔点为2 573 K,沸点为2 823 K,硬度大,属于共价晶体
D.NH4BF4(氟硼酸铵)是合成氮化硼纳米管的原料之一,1 mol NH4BF4含有配位键的数目为NA
解析:D 由H3BO3在水溶液中发生反应:H3BO3+H2OH++[B(OH)4]-,可知H3BO3是一元弱酸,A正确;由题图2可以看出,立方氮化硼结构与金刚石相似,金刚石晶胞中,8个顶点有8个碳原子,6个面心有6个碳原子,立方体内部还有4个碳原子,金刚石的一个晶胞中含有的碳原子数为8×+6×+4=8,由氮化硼化学式可知晶体中N、B原子个数比为1∶1,故其晶胞中应该含有4个N原子和4个B原子,B正确;共价晶体通常具有很高的熔、沸点和很大的硬度,晶体硼的熔点为2 573 K,沸点为2 823 K,硬度大,说明其属于共价晶体,C项正确;N中含有氮氢配位键,B中含有硼氟配位键,则 1 mol NH4BF4含有配位键的数目为2NA,D错误。
11.一种广谱性熏蒸杀虫剂,其晶体熔点约为2 000 ℃,晶胞结构如图所示。已知该晶体的密度为ρ g·cm-3,NA表示阿伏加德罗常数的值。下列有关该晶体的说法错误的是( )
A.化学式为AlP
B.晶体类型为共价晶体
C.晶胞中Al原子的配位数为8
D.两个P原子间的最近核间距为××
1010 pm
解析:C 该晶胞中含有4个Al原子,8×+6×=4个P原子,化学式为AlP,A正确;根据题干信息,该晶体熔点高约2 000 ℃,应为共价晶体,B正确;Al原子的配位数为4,C错误;由立方晶胞密度计算公式可得晶胞体积为cm3,得到晶胞的边长为×1010pm,两个P原子间的最近核间距为面对角线长度的一半,即××1010pm,D正确。
12.图1、图2、图3分别表示金刚石晶体结构、金刚石晶胞示意图和二氧化硅晶体结构,下列叙述正确的是( )
A.金刚石晶体和二氧化硅晶体均属于共价晶体
B.1个金刚石晶胞中含有6个碳原子
C.60 g SiO2晶体中所含共价键的数目为6NA(设NA是阿伏加德罗常数的值)
D.金刚石晶体中每个碳原子被8个最小环所共有
解析:A 金刚石晶体和二氧化硅晶体均属于共价晶体,A项正确;1个金刚石晶胞中含有碳原子的个数为8×+6×+4=8,B项错误;60 g SiO2晶体的物质的量为1 mol,SiO2晶体中,1个Si原子与4个O原子形成4个Si—O键,故1 mol SiO2中含4NA个Si—O键,C项错误;金刚石晶体中每个碳原子被12个最小环所共有,D项错误。
13.(1)金刚砂(SiC)的硬度为9.5,其晶胞结构如图甲所示,则金刚砂晶体类型为共价晶体;在SiC中,每个C原子周围最近的C原子数目为12;若晶胞的边长为a pm,则金刚砂的密度表达式为。
(2)硅的某种单质的晶胞如图乙所示。若该硅晶体的密度为ρ g·cm-3,阿伏加德罗常数的值为NA,则晶体中最近的两个硅原子之间的距离为×cm (用代数式表示即可)。
解析:(1)金刚砂(SiC)的硬度为9.5,硬度大,属于共价晶体;在SiC中,每个碳原子周围最近的碳原子数目为12;该晶胞中C原子个数为8×+6×=4,Si原子个数为4,晶胞边长为a×10-10 cm,体积V=(a×10-10 cm)3,ρ==。
(2)由图乙的晶胞结构可知,晶体Si的一个晶胞中含有Si原子的数目是8×+6×+4=8,根据晶胞的密度ρ=可知,V=cm3= cm3,晶胞的边长a== cm,在晶胞中最近的两个Si原子之间的距离为晶胞体对角线长的,即× cm。
3 / 4
