宁夏银川市贺兰县第四中学九年级化学人教版下册8-2金属化学性质课件(共28张PPT)
文档属性
| 名称 | 宁夏银川市贺兰县第四中学九年级化学人教版下册8-2金属化学性质课件(共28张PPT) |

|
|
| 格式 | zip | ||
| 文件大小 | 688.3KB | ||
| 资源类型 | 教案 | ||
| 版本资源 | 人教版(新课程标准) | ||
| 科目 | 化学 | ||
| 更新时间 | 2016-04-29 00:00:00 | ||
图片预览








文档简介
课件28张PPT。课题2 金属的化学性质
(共2课时)1、知道镁、锌、铁、铜等金属与氧气的反应及剧烈程度
2、探究不同金属与稀盐酸、稀硫酸及某些金属化合物(盐)溶液的反应
3、初步了解一些常见金属的活动性强弱顺序学习目标想一想2008年5月10日,“路人”捡到一条“金项链”,要与马老汉平分,马老汉非常高兴,3人商量中,在“捡项链者”的忽悠下,马老汉拿出了38300元钱将“金项链”买下。可是下午经银行鉴定之后,金项链被“确诊”为黄铜项链 现假黄金多为黄铜(铜、锌合金),根据你所学知识,能不能初步鉴定“真黄金”与“假黄金”?新闻:海口六旬老汉3.8万元买了条假金项链回 顾 已 知 “真金不怕火炼”是指什么意思?镁、铝比较活泼,铁、铜次之,金最不活泼。(Mg 、Al > Fe 、Cu > Au)一.金属与氧气的反应结论:1.不同的金属与氧气的反应
条件不同. 2.与氧气反应条件的不同,说明金属
的化学活动性不同. 铝的化学性质比铁活泼,为什么我们通常看见铁生锈而没有看到铝生锈? 思考 在清洗铝制品(如铝锅)时应注意什么?答:铝在空气中能与氧气反应,使其表面生成一层致密的氧化铝薄膜, 从而阻止里层的铝进一步被氧化,所以铝器本身有良好的抗腐蚀性能;
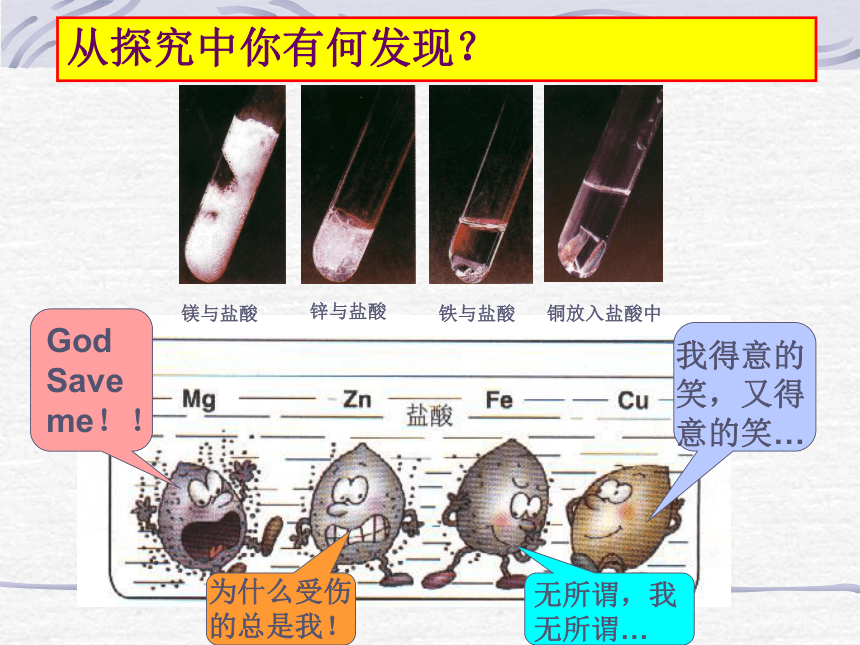
而铁在潮湿的空气中易生锈,疏松的铁锈不能阻止里层的铁继续被氧化,所以铁器需要涂油漆来防锈。二、金属活动性顺序活动与探究一在试管中分别加入稀盐酸和稀硫酸,然后分别加入铜丝、铁丝、锌粒、铝片、镁条,观察现象。从探究中你有何发现?镁与盐酸锌与盐酸铁与盐酸铜放入盐酸中活动与探究(1)反应剧烈,
放出大量的无色气体反应较剧烈,
放出大量的无色气体反应较慢,
有无色气体放出没有明显变化Mg+2HCl=MgCl2+H2↑Zn+2HCl =ZnCl2 +H2↑Fe +2HCl =FeCl2 + H2↑Fe +H2SO4 =FeSO4 +H2↑Mg+H2SO4=MgSO4+H2↑Zn +H2SO4 =ZnSO4 +H2↑ 二.金属活动性顺序1、能与盐酸,稀硫酸反应的金属是 、 、
它们反应的剧烈程度依次是 > > .
2、不能与盐酸,稀硫酸反应的金属是 3、镁、锌、铁、铜四种金属的活动性顺序是
> > > .
4、将镁、锌、铁、铜四种金属分为两类:
活泼金属 : .
不活泼金属: .
分类的依据是: .ZnFeMgZnCuMgMgZnFeCuMgZnFeFeCu是否与酸反应讨论得出单质化合物化合物单质小结:
这种由一种单质与一种化合物反应,生成了另一种单质和另一种化合物的反应叫做置换反应。
讨论: 对于以上的反应,从反应物和生成物的角度
分析,这些反应有何特点?将这一类反应与化合反
应、分解反应进行比较。
Mg + 2HCl = MgCl2 + H2 ↑
Zn + 2HCl = ZnCl2 + H2 ↑
Fe + 2HCl = FeCl2 + H2 ↑+ = +下列反应是否是置换反应? 判断H2 + CuO = Cu + H2OC + 2CuO = 2Cu + CO2 ↑CO + CuO = Cu + CO2C2H5OH + 3O2 = 2CO2 + 3H2O2H2O2 → 2H2O+O2↑1. 请归纳出金属的化学性质 小 结 (1)大多数金属在一定条件下可以和氧气反应;(2)活泼金属可以和酸反应生成氢气;2. 判断常见金属活泼性的方法(1)金属与氧气反应的难易程度(2)金属与酸反应的剧烈程度来找茬1、判断下列反应的正误2Fe + 6HCl = 2FeCl3 + 3H2↑Cu + 2HCl = CuCl2 + H2↑来找茬2、判断下列说法的正误,并举例说明(1)只要有单质和化合物参加的反应一定是置换反应 ( )(2)只要有单质和化合物生成的反应一定是置换反应 ( )(3)还原氧化铜的反应一定是置换反应 ( )╳╳╳选一选 有X、Y、Z三种金属,如果把这三种金属均投入到稀硫酸中,X、Y表面均无明显现象,Z表面有大量气泡产生。若将X、Y这两种金属放在氧气中加热,X表面无明显现象,Y表面发黑。则这三种金属活动性顺序为 ( )A、X>Y>Z B、Z>Y>X
C、Y>X>Z D、Z>X>YB再想想能不能设计一个鉴定“真黄金”与“假黄金”的方法?探究活动二金属与某些化合物溶液的反应实验步骤:
1.把一根用砂纸打磨过的铝丝浸入硫酸铜溶液中,一会取出,观察。
2.把一洁净铜丝浸入硝酸银溶液中,一会取出,观察。
3.把另一根洁净铜丝浸入硫酸铝溶液中,一会取出,观察。
实验现象填于下面表格中铝丝浸入硫酸铜溶液中 铜丝浸入硝酸银溶液中 金属与金属化合物溶液铝丝上有红色物质生成,溶液颜色逐渐变淡
铜丝上有银白色
物质生成,溶液
由无色逐渐变为
淡蓝色
没有明显变化Cu+2AgNO3 = 2Ag+Cu(NO3)22Al+3CuCl2 = 3Cu+2AlCl3
铝、铜、银三种金属的活动性顺序是
讨论得出AlCuAg>>规律学习 通过无数的科学探究,科学家总结出一个 重要规律:金属活动性顺序
K Ca Na Mg Al Zn Fe Sn Pb(H)Cu Hg Ag Pt Au
金属活动性由强逐渐减弱
判断常见金属活泼性的方法(1)金属能否与酸反应及反应的剧烈程度(2)金属能否与金属化合物(盐)溶液反应
1、在金属活动性顺序里,金属的位置越靠前,它的活动性就越强。
2、在金属活动性顺序里,位于氢前面的金属能置换出盐酸,稀硫酸中的氢
3、在金属活动顺序里,位于前面的金属(钾、钙、钠除外) 能把位于后面的金属从它们化合物的溶液中置换出来。
金属活动性顺序的应用1.根据金属活动性顺序,下列能发生反应的是( )
A. Ag 和 H2SO4 溶液 B. Fe 和 CuSO4 溶液
C. Cu 和 AgCl D. Zn 和 NaCl 溶液
2.将X. Y. Z三种金属分别浸入稀硫酸中, Z溶解, X. Y
不溶解;将X浸入Y的化合物溶液中,在X的表面析出Y.
则 X. Y. Z三种金属的活动性由强到弱的顺序为( )
A. Z>Y>X B. Y>Z>X
C. Z>X>Y D. Y>X>Z
练 习 巩 固BC1、大多数金属能与氧气发生反应,但反应的难易和剧烈程度不同。
2、活泼金属都能和稀盐酸、稀硫酸反应,但反应的难易和剧烈程度不同。
3、排在前面的金属可以和排在后面金属化合物(盐)的溶液反应。
4、金属的活动性顺序
K Ca Na Mg Al Zn Fe Sn Pb(H)Cu Hg Ag Pt Au
金属活动性由强逐渐减弱
金属的化学性质
归 纳 小 结
在CuCl2和MgCl2的混合溶液中加入过量Zn粉,充分反应后过滤,留在滤纸上的物质是( )
A. Zn B. Cu
C. Cu和Zn D. Mg和Cu 拓 展 延 伸C祝大家开心快乐!!
(共2课时)1、知道镁、锌、铁、铜等金属与氧气的反应及剧烈程度
2、探究不同金属与稀盐酸、稀硫酸及某些金属化合物(盐)溶液的反应
3、初步了解一些常见金属的活动性强弱顺序学习目标想一想2008年5月10日,“路人”捡到一条“金项链”,要与马老汉平分,马老汉非常高兴,3人商量中,在“捡项链者”的忽悠下,马老汉拿出了38300元钱将“金项链”买下。可是下午经银行鉴定之后,金项链被“确诊”为黄铜项链 现假黄金多为黄铜(铜、锌合金),根据你所学知识,能不能初步鉴定“真黄金”与“假黄金”?新闻:海口六旬老汉3.8万元买了条假金项链回 顾 已 知 “真金不怕火炼”是指什么意思?镁、铝比较活泼,铁、铜次之,金最不活泼。(Mg 、Al > Fe 、Cu > Au)一.金属与氧气的反应结论:1.不同的金属与氧气的反应
条件不同. 2.与氧气反应条件的不同,说明金属
的化学活动性不同. 铝的化学性质比铁活泼,为什么我们通常看见铁生锈而没有看到铝生锈? 思考 在清洗铝制品(如铝锅)时应注意什么?答:铝在空气中能与氧气反应,使其表面生成一层致密的氧化铝薄膜, 从而阻止里层的铝进一步被氧化,所以铝器本身有良好的抗腐蚀性能;
而铁在潮湿的空气中易生锈,疏松的铁锈不能阻止里层的铁继续被氧化,所以铁器需要涂油漆来防锈。二、金属活动性顺序活动与探究一在试管中分别加入稀盐酸和稀硫酸,然后分别加入铜丝、铁丝、锌粒、铝片、镁条,观察现象。从探究中你有何发现?镁与盐酸锌与盐酸铁与盐酸铜放入盐酸中活动与探究(1)反应剧烈,
放出大量的无色气体反应较剧烈,
放出大量的无色气体反应较慢,
有无色气体放出没有明显变化Mg+2HCl=MgCl2+H2↑Zn+2HCl =ZnCl2 +H2↑Fe +2HCl =FeCl2 + H2↑Fe +H2SO4 =FeSO4 +H2↑Mg+H2SO4=MgSO4+H2↑Zn +H2SO4 =ZnSO4 +H2↑ 二.金属活动性顺序1、能与盐酸,稀硫酸反应的金属是 、 、
它们反应的剧烈程度依次是 > > .
2、不能与盐酸,稀硫酸反应的金属是 3、镁、锌、铁、铜四种金属的活动性顺序是
> > > .
4、将镁、锌、铁、铜四种金属分为两类:
活泼金属 : .
不活泼金属: .
分类的依据是: .ZnFeMgZnCuMgMgZnFeCuMgZnFeFeCu是否与酸反应讨论得出单质化合物化合物单质小结:
这种由一种单质与一种化合物反应,生成了另一种单质和另一种化合物的反应叫做置换反应。
讨论: 对于以上的反应,从反应物和生成物的角度
分析,这些反应有何特点?将这一类反应与化合反
应、分解反应进行比较。
Mg + 2HCl = MgCl2 + H2 ↑
Zn + 2HCl = ZnCl2 + H2 ↑
Fe + 2HCl = FeCl2 + H2 ↑+ = +下列反应是否是置换反应? 判断H2 + CuO = Cu + H2OC + 2CuO = 2Cu + CO2 ↑CO + CuO = Cu + CO2C2H5OH + 3O2 = 2CO2 + 3H2O2H2O2 → 2H2O+O2↑1. 请归纳出金属的化学性质 小 结 (1)大多数金属在一定条件下可以和氧气反应;(2)活泼金属可以和酸反应生成氢气;2. 判断常见金属活泼性的方法(1)金属与氧气反应的难易程度(2)金属与酸反应的剧烈程度来找茬1、判断下列反应的正误2Fe + 6HCl = 2FeCl3 + 3H2↑Cu + 2HCl = CuCl2 + H2↑来找茬2、判断下列说法的正误,并举例说明(1)只要有单质和化合物参加的反应一定是置换反应 ( )(2)只要有单质和化合物生成的反应一定是置换反应 ( )(3)还原氧化铜的反应一定是置换反应 ( )╳╳╳选一选 有X、Y、Z三种金属,如果把这三种金属均投入到稀硫酸中,X、Y表面均无明显现象,Z表面有大量气泡产生。若将X、Y这两种金属放在氧气中加热,X表面无明显现象,Y表面发黑。则这三种金属活动性顺序为 ( )A、X>Y>Z B、Z>Y>X
C、Y>X>Z D、Z>X>YB再想想能不能设计一个鉴定“真黄金”与“假黄金”的方法?探究活动二金属与某些化合物溶液的反应实验步骤:
1.把一根用砂纸打磨过的铝丝浸入硫酸铜溶液中,一会取出,观察。
2.把一洁净铜丝浸入硝酸银溶液中,一会取出,观察。
3.把另一根洁净铜丝浸入硫酸铝溶液中,一会取出,观察。
实验现象填于下面表格中铝丝浸入硫酸铜溶液中 铜丝浸入硝酸银溶液中 金属与金属化合物溶液铝丝上有红色物质生成,溶液颜色逐渐变淡
铜丝上有银白色
物质生成,溶液
由无色逐渐变为
淡蓝色
没有明显变化Cu+2AgNO3 = 2Ag+Cu(NO3)22Al+3CuCl2 = 3Cu+2AlCl3
铝、铜、银三种金属的活动性顺序是
讨论得出AlCuAg>>规律学习 通过无数的科学探究,科学家总结出一个 重要规律:金属活动性顺序
K Ca Na Mg Al Zn Fe Sn Pb(H)Cu Hg Ag Pt Au
金属活动性由强逐渐减弱
判断常见金属活泼性的方法(1)金属能否与酸反应及反应的剧烈程度(2)金属能否与金属化合物(盐)溶液反应
1、在金属活动性顺序里,金属的位置越靠前,它的活动性就越强。
2、在金属活动性顺序里,位于氢前面的金属能置换出盐酸,稀硫酸中的氢
3、在金属活动顺序里,位于前面的金属(钾、钙、钠除外) 能把位于后面的金属从它们化合物的溶液中置换出来。
金属活动性顺序的应用1.根据金属活动性顺序,下列能发生反应的是( )
A. Ag 和 H2SO4 溶液 B. Fe 和 CuSO4 溶液
C. Cu 和 AgCl D. Zn 和 NaCl 溶液
2.将X. Y. Z三种金属分别浸入稀硫酸中, Z溶解, X. Y
不溶解;将X浸入Y的化合物溶液中,在X的表面析出Y.
则 X. Y. Z三种金属的活动性由强到弱的顺序为( )
A. Z>Y>X B. Y>Z>X
C. Z>X>Y D. Y>X>Z
练 习 巩 固BC1、大多数金属能与氧气发生反应,但反应的难易和剧烈程度不同。
2、活泼金属都能和稀盐酸、稀硫酸反应,但反应的难易和剧烈程度不同。
3、排在前面的金属可以和排在后面金属化合物(盐)的溶液反应。
4、金属的活动性顺序
K Ca Na Mg Al Zn Fe Sn Pb(H)Cu Hg Ag Pt Au
金属活动性由强逐渐减弱
金属的化学性质
归 纳 小 结
在CuCl2和MgCl2的混合溶液中加入过量Zn粉,充分反应后过滤,留在滤纸上的物质是( )
A. Zn B. Cu
C. Cu和Zn D. Mg和Cu 拓 展 延 伸C祝大家开心快乐!!
同课章节目录
