中考二轮复习 专题3 基本实验和跨学科实践 课件(共57张PPT)
文档属性
| 名称 | 中考二轮复习 专题3 基本实验和跨学科实践 课件(共57张PPT) |

|
|
| 格式 | pptx | ||
| 文件大小 | 3.1MB | ||
| 资源类型 | 试卷 | ||
| 版本资源 | 通用版 | ||
| 科目 | 化学 | ||
| 更新时间 | 2025-02-14 00:00:00 | ||
图片预览











文档简介
(共57张PPT)
第二部分 题型训练
第二部分
专题三
专题三 基本实验和跨学科实践
CONTENTS
目录
题型解读
01
KAO DIAN DUI BIAO
02
ZHEN TI JIE DU
真题解读
基础练习
03
ZHI SHI GOU JIAN
04
HANG SHI JI CHU
备考演练
SU YANG TI SHENG
PART ONE
01
2025
题型解读
真题解读
题型解读
基础练习
备考演练
1. 题型分析
本题主要考查学生教材中的八大基本实验和跨学科实践相关知识。
2. 解题策略
①知识储备:能写出教材中气体制备的反应原理(制取氧气、二氧化碳、氢气);
②装置及作用:常见完整系统的装置:发生、净化、干燥、收集(性质实验)、尾气处理装置,明确装置的选取、作用,装置的链接顺序;
③答题规范:实验器材不能写错别字如:酒精灯、锥形瓶、集气瓶、长颈漏斗、试管等;实验现象观察和描述:熟悉氧气、二氧化碳检验的现象、物质在氧气中燃烧的现象;答案组织要条理清晰,结合原理解释现象或原因;
④答题技巧:注意题目中给出的所有信息,包括实验装置图、数据表格、文字说明等;
⑤回顾复习整理课本八大基础实验。
ZHEN TI JIE DU
PART TWO
02
2025
真题解读
真题解读
题型解读
基础练习
备考演练
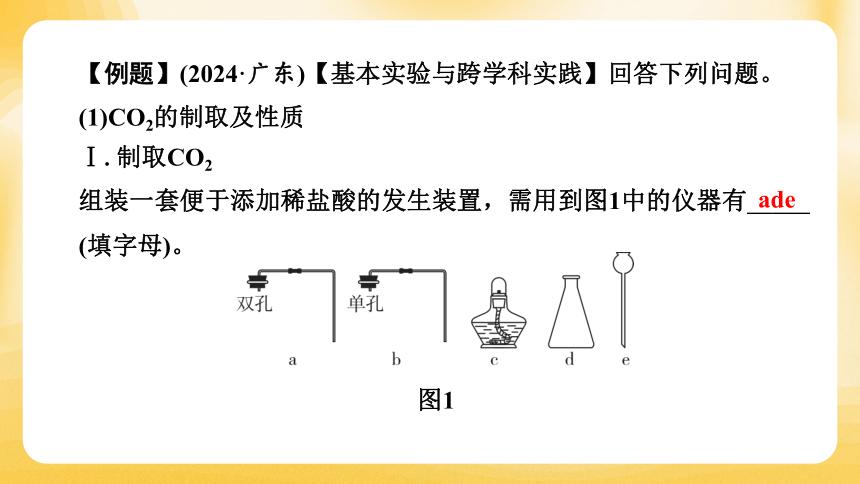
【例题】(2024·广东)【基本实验与跨学科实践】回答下列问题。
(1)CO2的制取及性质
Ⅰ.制取CO2
组装一套便于添加稀盐酸的发生装置,需用到图1中的仪器有 ade (填字母)。
图1
ade
【详解】Ⅰ.组装便于添加液体试剂的发生装置,应该选择长颈漏斗e,制取二氧化碳的反应物为固液常温型,可以选择锥形瓶d,长颈漏斗需要双孔橡胶塞,故选择a,所以需要的仪器有ade。
Ⅱ.性质实验
操作 现象 性质
X为澄清石灰水时,现象为 澄清石灰水变浑浊 CO2能与石灰水反应
X为 紫色石蕊溶液 时,现象为 溶液由紫色变红色 CO2能与水反应生成酸性物质
澄清石灰水变浑浊
紫色石蕊溶液
溶液由紫色
变红色
操作 现象 性质
低处的蜡烛先熄灭,高处的蜡烛后熄灭 CO2密度比空气大 ;
CO2不燃烧,也不支持燃烧
CO2密度比空气大
【详解】Ⅱ.若X为澄清石灰水,其与二氧化碳反应会生成水和碳酸钙沉淀,故现象是,澄清石灰水变浑浊。二氧化碳与水反应生成碳酸,碳酸呈酸性,可以用紫色石蕊溶液检验,碳酸能使紫色石蕊溶液变红色,故填:紫色石蕊溶液;溶液由紫色变红色。将二氧化碳倒入烧杯中,观察到低处的蜡烛先熄灭,高处的蜡烛后熄灭,说明了二氧化碳密度比空气大;二氧化碳不燃烧、不支持燃烧;
(2)低碳行动方案
同学们展示如图2所示的方案,并交流讨论、完善方案。
Ⅰ.完善方案中的内容(各补写一条):a. 减少一次性餐具的使用 ;b. 人工降雨 ;c. 乙醇 。
减少一次性餐具的使用
人工降雨
乙醇
【详解】Ⅰ.a中低碳生活,是指减少碳的排放,低能耗、低开支的生活方式有很多:如光盘行动、减纸减塑、衣物回收利用、减少一次性餐具的使用、低碳出行等。b中二氧化碳的物理利用,不产生新物质的用途,包括有:冷藏保鲜、人工降雨、灭火等。C中二氧化碳化学利用,产生新的物质的用途,包括有:转化成甲醇、乙醇等有机物。
Ⅱ.CO2物理利用 不能 (填“能”或“不能”)从总量上减少CO2。
【详解】Ⅱ.根据图中“CO2物理利用”,可以知道利用二氧化碳冷藏保鲜、人工降雨,仅是物理利用,不能从总量上减少CO2。
不能
Ⅲ.植树造林,利用绿色植物的 光合 作用吸收CO2。
【详解】Ⅲ.植树造林,绿色植物可以进行光合作用,二氧化碳和水在叶绿体中,在光照的条件下反应生成有机物,并释放氧气,故是利用植物的光合作用吸收二氧化碳。
光合
【点拨】本题涉及选择仪器组装一套便于添加稀盐酸制取CO2的发生装置;选择试剂设计实验方案验证CO2能与石灰水反应以及CO2能与水反应生成酸性物质;设计实验方案,依据“低处的蜡烛先熄灭,高处的蜡烛后熄灭”得出何种结论;举例补充完善低碳生活、CO2的物理利用和CO2的化学利用的实例;推断CO2的物理利用能否从总量减碳;植树造林减碳的原理等。要求考生掌握并会应用气体制备、性质实验相关知识解决问题,CO2的物理性质及化学性质会灵活运用。
JI CHU LIAN XI
PART THREE
03
2025
基础练习
真题解读
题型解读
基础练习
备考演练
1. (2023·广东)(1)实验室制取O2及性质检验
Ⅰ.如图中仪器a的名称是 锥形瓶 。
锥形瓶
Ⅱ.用高锰酸钾制取O2,应选择如图1中的发生装置 A (填字母),化学方程式为 2KMnO4 K2MnO4+MnO2+O2↑ 。
A
2KMnO4 K2MnO4+MnO2+O2↑
Ⅲ.收集一瓶O2并进行性质检验。
操作 现象 结论
硫燃烧时, c (填字母),生成刺激性气味的气体 a.产生大量白烟 b.生成黑色固体 c.发出蓝紫色火焰 O2具有氧化性
集气瓶中NaOH溶液的作用是 吸收二氧化硫,防止污染空气 c
吸收二氧化硫,防止污染空气
(2)制作氧自救呼吸器
查阅资料,超氧化钾(KO2)为黄色固体,可分别与CO2、H2O反应生成O2和白色固体,产氧效率高、适合作生氧剂。
图2
原理分析:4KO2+2CO2 2K2CO3+3O2,4KO2+2H2O 4X+3O2↑,则X的化学式为 KOH 。
动手实践:设计并制作氧自救呼吸器,如图2所示。使用一段时间后,观察到生氧剂由 黄色变为白色 (填颜色变化)时,则基本失效。
KOH
黄色变为白色
2. (2022·广东)具备基本化学实验技能是学习化学的基础和保证。在化学实验操作考试中,小明和小英分别抽取了Ⅰ、Ⅱ两组试题。可供选择的实验试剂有大理石、KClO3、MnO2、稀盐酸、NaOH溶液、H2O2溶液、酚酞溶液、石蕊溶液等,相关实验装置如图所示。
Ⅰ组:O2和CO2的实验室制取。
(1)仪器a的名称是 试管 。
(2)小明想用同一套装置分别制取O2和CO2,应选用发生装置是 B 和收集装置 C (填字母)。其中,制取O2的化学方程式为 2H2O2 2H2O+ 。
试管
B
C
2H2O+O2↑
2H2O2
Ⅱ组:溶液酸碱性的检验和酸、碱的化学性质。
(3)为了鉴别稀盐酸和NaOH溶液,小英要测定溶液的pH,正确的操作是 用洁净干燥的玻璃棒蘸取溶液,滴在pH试纸上,把变色的pH试纸与标准比色卡对照,即可得溶液的pH 。测得pH=1的溶液为 稀盐酸 。
用洁净干燥的玻璃棒蘸取溶液,滴在pH试纸上,把变色的pH
试纸与标准比色卡对照,即可得溶液的pH
稀盐酸
(4)稀盐酸和NaOH溶液反应无明显现象。为使该反应“可视化”,小英向NaOH溶液中滴加 酚酞 溶液,再逐滴加入稀盐酸至过量,观察到溶液由 红 色变为无色。
酚酞
红
3. (2021·广东)根据下图中的实验装置回答。
(1)仪器a的名称是 锥形瓶 。
(2)用装置A制取CO2,分液漏斗中盛装的试剂是 稀盐酸 ;用装置C收集CO2,气体应从 b 导管口(填“b”或“c”)通入。
锥形瓶
稀盐酸
b
(3)用装置B制取O2,检查装置气密性的操作是 将导气管伸入水中,用手捂住试管,导气管末端有气泡冒出,说明气密性好 ,试管中反应的化学方程式为 2KMnO4 K2MnO4+MnO2+ 。
将导气管伸入水
中,用手捂住试管,导气管末端有气泡冒出,说明气密性好
2KMnO4 K2MnO4+MnO2+O2↑
(4)某同学在学习氮肥时,查阅资料:
①氨气极易溶于水,其水溶液称为氨水;
②氨水在浓度大或受热时易分解放出氨气。
实验室用生石灰和浓氨水能快速制取氨气的原因是 生石灰和水反应生成氢氧化钙放热 ;制得的氨气 不能 (填“能”或“不能”)用装置D收集。
生石灰和水反
应生成氢氧化钙放热
不能
SU YANG TI SHENG
PART FOUR
04
2025
备考演练
真题解读
题型解读
基础练习
备考演练
4. 化学是一门以实验为基础的科学,化学小组的同学利用如图装置进行实验探究,结合装置回答下列问题。
(1)仪器a的名称为 试管 ,下列制取气体的反应可选用装置A的是 ③ (填序号)。
①二氧化锰与浓盐酸加热制取Cl2 ②大理石与稀盐酸制取CO2
试管
③
③加热高锰酸钾制取O2 ④锌粒与稀硫酸制取H2
(2)实验室用过氧化氢和二氧化锰制取氧气,反应的化学方程式是 2H2O2 2H2O+O2↑。可选用的收集装置是 C或 。
2H2O2 2H2O+O2↑
C或E
(3)硫化氢(H2S)气体有毒,密度比空气大,溶于水形成酸,能在空气中燃烧生成SO2和水。实验室用块状硫化亚铁(FeS)和稀硫酸发生复分解反应制取H2S,该反应的化学方程式是 FeS+H2SO4 FeSO4+H2S↑ ,应选用的发生装置是 B ,该实验需要对剩余的硫化氢气体进行尾气处理,下列方法正确的是 b (填字母)。
a.用稀硫酸吸收 b.用氢氧化钠溶液吸收 c.点燃
FeS+ H2SO4
FeSO4+H2S↑
B
b
(4)某同学将图中G装置产生的气体通入H中,若试剂X是新制澄清石灰水,H中一直未出现浑浊现象,其原因是 二氧化碳中含有氯化氢气体 ;若Ⅰ中干燥的紫色石蕊纸花没有变红,则X可能是下列选项 ad (填字母)。
a.浓硫酸 b.饱和NaHCO3溶液
二氧化碳中含有氯化
氢气体
ad
c.CaCl2溶液 d.NaOH浓溶液
5. (2024·福建) 请参加“氯化钠欢乐之旅”的实践活动。
任务一 参观盐场
(1)利用风吹和日晒使海水不断蒸发至有晶体析出,此过程溶液中NaCl的质量分数逐渐 增大 (填“增大”或“减小”)。
增大
任务二 提纯粗盐
(2)粗盐提纯的有关操作如图所示。
①正确的操作顺序是 B、C、A (填字母);
②操作A中,当加热到蒸发皿中出现 较多固体 时,停止加热;
③操作C中,玻璃棒的作用是 引流 。
B、C、A
较多固体
引流
任务三 应用食盐
(3)农业上常用质量分数为16%的NaCl溶液选种。若在实验室中配制该溶液,需要的玻璃仪器有烧杯、玻璃棒、胶头滴管和 量筒 。
(4)NaCl是一种重要的化工原料。从元素守恒的视角,以NaCl为基本原料,可能制取的物质有 NaOH(或Cl2) (写一种)。
量筒
NaOH(或Cl2)
6. (2024·山东滨州)化学是一门以实验为基础的学科。
Ⅰ.结合下图有关实验,回答问题。
(1)过滤操作中仪器a的名称是 铁架台 。
(2)水电解器的b玻璃管中产生的气体是 氧气(或O2) (填化学式)。
铁架台
氧气(或O2)
(3)从安全角度考虑,在点燃氢气前,一定要检验氢气的 纯度 。
(4)将铝片与铝合金互相刻划,可证明铝合金的硬度 大于 (填“大于”“小于”或“等于”)铝片的硬度。
纯度
大于
Ⅱ.空间站采用循环技术保证航天员的用水和呼吸循环系统(部分)如图所示。
(5)为模拟大气环境,工作舱内氧气的体积分数应为 21 %。
(6)疏松多孔的新型分子筛具有 吸附 性,用于除去水中的异味。
21
吸附
(7)萨巴蒂尔反应系统内部提供高温、高压和催化剂等条件,反应系统内发生反应的化学方程式为 CO2+4H2 CH4+ 。
CO2+4H2 CH4+2H2O
7. (2024·陕西中考)根据下面图示的三个实验回答问题。
(1)写出标有序号①的仪器名称: 水槽 。
(2)实验乙中,发生反应的化学方程式是 3Fe+2O2 Fe3O4 。
水槽
3Fe+2O2 Fe3O4
(3)实验甲中, 不能 (填“能”或“不能”)用细铁丝代替红磷测定空气中氧气的含量。
(4)实验丙中,纸花a用紫色石蕊溶液浸泡后干燥,纸花b用紫色石蕊溶液润湿,通入CO2气体后,纸花 b (填字母)变红。
不能
b
8. (2024·云南中考)化学是一门以实验为基础的学科。
(1)仪器a的名称为 铁架台 。
铁架台
(2)实验室用高锰酸钾制取氧气,发生反应的化学方程式为 2KMnO4 K2MnO4+MnO2+O2↑ 。用B装置收集氧气,体现了氧气的物理性质是 氧气不易溶于水 ;停止加热时,为防止倒吸,应先进行的操作是 把导管移出水面 (填“熄灭酒精灯”或“把导管移出水面”)。
(3)用上述收集的O2完成如图C所示的实验,观察到澄清石灰水 变浑浊 。
2KMnO4 K2MnO4+MnO2+O2↑
氧气不易溶于水
把导管移出水面
变
浑浊
(4)某同学为探究燃烧的条件设计了如图实验。已知白磷的着火点是40℃。
向装置甲中通入空气,甲中的热水压入到乙中,甲、乙中的白磷均燃烧。由液面降低后甲中白磷燃烧的事实,说明燃烧需要 与空气接触 ;由热水进入后乙中白磷燃烧的事实,说明燃烧需要 温度达到可燃物的着火点 。
与空气
接触
温度
达到可燃物的着火点
9. (2024·江苏盐城)我国向世界承诺:努力争取2060年前实现“碳中和”——CO2排放量和转化量相等,达到相对零排放,为人类社会可持续发展贡献中国力量。
Ⅰ.了解二氧化碳排放
(1)CO2排放量增加可能引发的后果有 ABCD (填字母,下同)。
A. 冰川融化,海平面上升
B. 极端天气频发
C. 土地沙漠化,造成农业减产
D. 影响自然生态系统,改变生物多样性
ABCD
(2)空气中的CO2主要来自于 AB 。
A. 动植物的呼吸作用
B. 化石燃料的燃烧
C. 植物的光合作用
AB
(3)实验室制备CO2。根据下列仪器装置,回答问题。
①写出标号仪器的名称:a. 试管 ,b. 集气瓶 ;
②制取CO2可在A~E中选用装置 BC ;装置F是在装置B基础上的改进,其优点是 可以控制反应发生与停止 。
试管
集气瓶
BC
可以控制反应发生与停止
分别注入等体积的水、澄清石灰水、2%NaOH溶液,盖上瓶盖,
Ⅱ.探究二氧化碳转化
(4)CO2的吸收是其转化的有效方法。现有三种试剂:水、澄清石灰水、2%NaOH溶液,你认为最佳的CO2吸收剂是 2%NaOH溶 ,设计实验方案证明你的结论: 用三只相同的塑料瓶收集二氧化碳,分别注入等体积的水、澄清石灰水、2%NaOH溶液,盖 上瓶盖,充分振荡,若注入2%氢氧化钠溶液的塑料瓶变瘪程度最大,说明2%氢氧化钠溶液吸收二氧化碳效 。
2%NaOH溶液
用三只相同的塑料瓶收集二氧化碳,
充分振荡,若注入2%氢氧化钠溶液的塑料瓶变瘪程度最大,说明2%
氢氧化钠溶液吸收二氧化碳效果最好
Ⅲ.研制低碳行动方案
(5)低碳行动涵盖国际合作、国家工程和个人行为三个层面。请从“个人行为”层面策应“低碳行动”,写出你的一个行动打算: 出行乘坐公交车(合理即可) 。
出行乘坐公交车(合理即可)
10. (7分)(2024·越秀区校级二模)实验室制取气体和检验气体性质的部分装置如图所示.请回答问题。
(1)写出仪器的名称:① 长颈漏斗 ;② 锥形瓶 。
长颈漏斗
锥形瓶
(2)乙炔(化学式C2H2)俗称电石气,实验室中常用电石(一种灰色块状固体,化学式CaC2)与水在常温下反应制取,该反应同时还有氢氧化钙生成。通常情况下,乙炔是一种无色、无味、难溶于水的气体,标准状况下,乙炔的密度是1.16g/L(空气的密度为1.293 g/L),能与浓硫酸反应生成乙炔基硫酸酯。
Ⅰ、写出电石与水反应的化学方程式 CaC2+2H2O Ca(OH)2+C2H2↑ ;
CaC2+2H2O Ca(OH)2
+C2H2↑
Ⅱ、实际操作中,常采用饱和食盐水代替水以降低化学反应速率.若要获得平稳的乙炔气流,上图中最适合作为发生装置的是 C ,收集装置是 F 。
C
F
(3)若把G装置中的浓硫酸换成水并盛满,用来收集难溶于水的气体时,气体应从 b (填“a”或“b”端通入)。
(4)实验室制取二氧化碳时,在下图装置中连接压强传感器,得到曲线图。曲线中bc段压强保持不变的原因是 液体被压入长颈漏斗,固液分离,反应停止,不再生成气体,保持内部压强不变 ,曲线中c点对应的操作是 打开弹簧夹 。
b
液体被压入长颈漏斗,
固液分离,反应停止,不再生成气体,保持内部压强不变
打开弹簧夹
11. (2024·福田区模拟)如图是实验室常见制取气体的发生装置及收集装置,请回答。
Ⅰ.气体的制备与性质
(1)仪器a的名称是 锥形瓶 。
(2)实验室用固体加热制取比较纯净的氧气,应选择的发生装置和收集装置的组合是 AC (填序号,从A~E中选),该反应的化学方程式是 2KMnO4 K2MnO4+MnO2+O2↑ 。
(3)小圳同学想设计实验验证CO2与水反应,他将足量新制的CO2分别通过F中①和②进行对照实验,由于新制的CO2含有水蒸气,为了保证实验的效果,试剂X应该是 浓硫酸 (填名称)。
锥形瓶
AC
2KMnO4 K2MnO4+MnO2+O2↑
浓硫酸
Ⅱ.气体制备在生活与航空的应用
(4)图1是一种常见的家用制氧机的工作原理简图,图2是小圳同学用实验室常见仪器组装出具有相似功能的仪器,其中,装置甲相当于制氧机中的 过滤仓 (填“过滤仓”或“反应仓”)。
过滤仓
(5)我国科学家进行如图3所示的氧循环研究,实现了空间站氧气的再生。其中反应Ⅰ需要在催化剂和加热的条件下才能发生,写出该反应的化学方程式 CO2+4H2 CH4+2H2O 。
CO2+4H2 CH4+2H2O
第二部分 题型训练
第二部分
专题三
专题三 基本实验和跨学科实践
CONTENTS
目录
题型解读
01
KAO DIAN DUI BIAO
02
ZHEN TI JIE DU
真题解读
基础练习
03
ZHI SHI GOU JIAN
04
HANG SHI JI CHU
备考演练
SU YANG TI SHENG
PART ONE
01
2025
题型解读
真题解读
题型解读
基础练习
备考演练
1. 题型分析
本题主要考查学生教材中的八大基本实验和跨学科实践相关知识。
2. 解题策略
①知识储备:能写出教材中气体制备的反应原理(制取氧气、二氧化碳、氢气);
②装置及作用:常见完整系统的装置:发生、净化、干燥、收集(性质实验)、尾气处理装置,明确装置的选取、作用,装置的链接顺序;
③答题规范:实验器材不能写错别字如:酒精灯、锥形瓶、集气瓶、长颈漏斗、试管等;实验现象观察和描述:熟悉氧气、二氧化碳检验的现象、物质在氧气中燃烧的现象;答案组织要条理清晰,结合原理解释现象或原因;
④答题技巧:注意题目中给出的所有信息,包括实验装置图、数据表格、文字说明等;
⑤回顾复习整理课本八大基础实验。
ZHEN TI JIE DU
PART TWO
02
2025
真题解读
真题解读
题型解读
基础练习
备考演练
【例题】(2024·广东)【基本实验与跨学科实践】回答下列问题。
(1)CO2的制取及性质
Ⅰ.制取CO2
组装一套便于添加稀盐酸的发生装置,需用到图1中的仪器有 ade (填字母)。
图1
ade
【详解】Ⅰ.组装便于添加液体试剂的发生装置,应该选择长颈漏斗e,制取二氧化碳的反应物为固液常温型,可以选择锥形瓶d,长颈漏斗需要双孔橡胶塞,故选择a,所以需要的仪器有ade。
Ⅱ.性质实验
操作 现象 性质
X为澄清石灰水时,现象为 澄清石灰水变浑浊 CO2能与石灰水反应
X为 紫色石蕊溶液 时,现象为 溶液由紫色变红色 CO2能与水反应生成酸性物质
澄清石灰水变浑浊
紫色石蕊溶液
溶液由紫色
变红色
操作 现象 性质
低处的蜡烛先熄灭,高处的蜡烛后熄灭 CO2密度比空气大 ;
CO2不燃烧,也不支持燃烧
CO2密度比空气大
【详解】Ⅱ.若X为澄清石灰水,其与二氧化碳反应会生成水和碳酸钙沉淀,故现象是,澄清石灰水变浑浊。二氧化碳与水反应生成碳酸,碳酸呈酸性,可以用紫色石蕊溶液检验,碳酸能使紫色石蕊溶液变红色,故填:紫色石蕊溶液;溶液由紫色变红色。将二氧化碳倒入烧杯中,观察到低处的蜡烛先熄灭,高处的蜡烛后熄灭,说明了二氧化碳密度比空气大;二氧化碳不燃烧、不支持燃烧;
(2)低碳行动方案
同学们展示如图2所示的方案,并交流讨论、完善方案。
Ⅰ.完善方案中的内容(各补写一条):a. 减少一次性餐具的使用 ;b. 人工降雨 ;c. 乙醇 。
减少一次性餐具的使用
人工降雨
乙醇
【详解】Ⅰ.a中低碳生活,是指减少碳的排放,低能耗、低开支的生活方式有很多:如光盘行动、减纸减塑、衣物回收利用、减少一次性餐具的使用、低碳出行等。b中二氧化碳的物理利用,不产生新物质的用途,包括有:冷藏保鲜、人工降雨、灭火等。C中二氧化碳化学利用,产生新的物质的用途,包括有:转化成甲醇、乙醇等有机物。
Ⅱ.CO2物理利用 不能 (填“能”或“不能”)从总量上减少CO2。
【详解】Ⅱ.根据图中“CO2物理利用”,可以知道利用二氧化碳冷藏保鲜、人工降雨,仅是物理利用,不能从总量上减少CO2。
不能
Ⅲ.植树造林,利用绿色植物的 光合 作用吸收CO2。
【详解】Ⅲ.植树造林,绿色植物可以进行光合作用,二氧化碳和水在叶绿体中,在光照的条件下反应生成有机物,并释放氧气,故是利用植物的光合作用吸收二氧化碳。
光合
【点拨】本题涉及选择仪器组装一套便于添加稀盐酸制取CO2的发生装置;选择试剂设计实验方案验证CO2能与石灰水反应以及CO2能与水反应生成酸性物质;设计实验方案,依据“低处的蜡烛先熄灭,高处的蜡烛后熄灭”得出何种结论;举例补充完善低碳生活、CO2的物理利用和CO2的化学利用的实例;推断CO2的物理利用能否从总量减碳;植树造林减碳的原理等。要求考生掌握并会应用气体制备、性质实验相关知识解决问题,CO2的物理性质及化学性质会灵活运用。
JI CHU LIAN XI
PART THREE
03
2025
基础练习
真题解读
题型解读
基础练习
备考演练
1. (2023·广东)(1)实验室制取O2及性质检验
Ⅰ.如图中仪器a的名称是 锥形瓶 。
锥形瓶
Ⅱ.用高锰酸钾制取O2,应选择如图1中的发生装置 A (填字母),化学方程式为 2KMnO4 K2MnO4+MnO2+O2↑ 。
A
2KMnO4 K2MnO4+MnO2+O2↑
Ⅲ.收集一瓶O2并进行性质检验。
操作 现象 结论
硫燃烧时, c (填字母),生成刺激性气味的气体 a.产生大量白烟 b.生成黑色固体 c.发出蓝紫色火焰 O2具有氧化性
集气瓶中NaOH溶液的作用是 吸收二氧化硫,防止污染空气 c
吸收二氧化硫,防止污染空气
(2)制作氧自救呼吸器
查阅资料,超氧化钾(KO2)为黄色固体,可分别与CO2、H2O反应生成O2和白色固体,产氧效率高、适合作生氧剂。
图2
原理分析:4KO2+2CO2 2K2CO3+3O2,4KO2+2H2O 4X+3O2↑,则X的化学式为 KOH 。
动手实践:设计并制作氧自救呼吸器,如图2所示。使用一段时间后,观察到生氧剂由 黄色变为白色 (填颜色变化)时,则基本失效。
KOH
黄色变为白色
2. (2022·广东)具备基本化学实验技能是学习化学的基础和保证。在化学实验操作考试中,小明和小英分别抽取了Ⅰ、Ⅱ两组试题。可供选择的实验试剂有大理石、KClO3、MnO2、稀盐酸、NaOH溶液、H2O2溶液、酚酞溶液、石蕊溶液等,相关实验装置如图所示。
Ⅰ组:O2和CO2的实验室制取。
(1)仪器a的名称是 试管 。
(2)小明想用同一套装置分别制取O2和CO2,应选用发生装置是 B 和收集装置 C (填字母)。其中,制取O2的化学方程式为 2H2O2 2H2O+ 。
试管
B
C
2H2O+O2↑
2H2O2
Ⅱ组:溶液酸碱性的检验和酸、碱的化学性质。
(3)为了鉴别稀盐酸和NaOH溶液,小英要测定溶液的pH,正确的操作是 用洁净干燥的玻璃棒蘸取溶液,滴在pH试纸上,把变色的pH试纸与标准比色卡对照,即可得溶液的pH 。测得pH=1的溶液为 稀盐酸 。
用洁净干燥的玻璃棒蘸取溶液,滴在pH试纸上,把变色的pH
试纸与标准比色卡对照,即可得溶液的pH
稀盐酸
(4)稀盐酸和NaOH溶液反应无明显现象。为使该反应“可视化”,小英向NaOH溶液中滴加 酚酞 溶液,再逐滴加入稀盐酸至过量,观察到溶液由 红 色变为无色。
酚酞
红
3. (2021·广东)根据下图中的实验装置回答。
(1)仪器a的名称是 锥形瓶 。
(2)用装置A制取CO2,分液漏斗中盛装的试剂是 稀盐酸 ;用装置C收集CO2,气体应从 b 导管口(填“b”或“c”)通入。
锥形瓶
稀盐酸
b
(3)用装置B制取O2,检查装置气密性的操作是 将导气管伸入水中,用手捂住试管,导气管末端有气泡冒出,说明气密性好 ,试管中反应的化学方程式为 2KMnO4 K2MnO4+MnO2+ 。
将导气管伸入水
中,用手捂住试管,导气管末端有气泡冒出,说明气密性好
2KMnO4 K2MnO4+MnO2+O2↑
(4)某同学在学习氮肥时,查阅资料:
①氨气极易溶于水,其水溶液称为氨水;
②氨水在浓度大或受热时易分解放出氨气。
实验室用生石灰和浓氨水能快速制取氨气的原因是 生石灰和水反应生成氢氧化钙放热 ;制得的氨气 不能 (填“能”或“不能”)用装置D收集。
生石灰和水反
应生成氢氧化钙放热
不能
SU YANG TI SHENG
PART FOUR
04
2025
备考演练
真题解读
题型解读
基础练习
备考演练
4. 化学是一门以实验为基础的科学,化学小组的同学利用如图装置进行实验探究,结合装置回答下列问题。
(1)仪器a的名称为 试管 ,下列制取气体的反应可选用装置A的是 ③ (填序号)。
①二氧化锰与浓盐酸加热制取Cl2 ②大理石与稀盐酸制取CO2
试管
③
③加热高锰酸钾制取O2 ④锌粒与稀硫酸制取H2
(2)实验室用过氧化氢和二氧化锰制取氧气,反应的化学方程式是 2H2O2 2H2O+O2↑。可选用的收集装置是 C或 。
2H2O2 2H2O+O2↑
C或E
(3)硫化氢(H2S)气体有毒,密度比空气大,溶于水形成酸,能在空气中燃烧生成SO2和水。实验室用块状硫化亚铁(FeS)和稀硫酸发生复分解反应制取H2S,该反应的化学方程式是 FeS+H2SO4 FeSO4+H2S↑ ,应选用的发生装置是 B ,该实验需要对剩余的硫化氢气体进行尾气处理,下列方法正确的是 b (填字母)。
a.用稀硫酸吸收 b.用氢氧化钠溶液吸收 c.点燃
FeS+ H2SO4
FeSO4+H2S↑
B
b
(4)某同学将图中G装置产生的气体通入H中,若试剂X是新制澄清石灰水,H中一直未出现浑浊现象,其原因是 二氧化碳中含有氯化氢气体 ;若Ⅰ中干燥的紫色石蕊纸花没有变红,则X可能是下列选项 ad (填字母)。
a.浓硫酸 b.饱和NaHCO3溶液
二氧化碳中含有氯化
氢气体
ad
c.CaCl2溶液 d.NaOH浓溶液
5. (2024·福建) 请参加“氯化钠欢乐之旅”的实践活动。
任务一 参观盐场
(1)利用风吹和日晒使海水不断蒸发至有晶体析出,此过程溶液中NaCl的质量分数逐渐 增大 (填“增大”或“减小”)。
增大
任务二 提纯粗盐
(2)粗盐提纯的有关操作如图所示。
①正确的操作顺序是 B、C、A (填字母);
②操作A中,当加热到蒸发皿中出现 较多固体 时,停止加热;
③操作C中,玻璃棒的作用是 引流 。
B、C、A
较多固体
引流
任务三 应用食盐
(3)农业上常用质量分数为16%的NaCl溶液选种。若在实验室中配制该溶液,需要的玻璃仪器有烧杯、玻璃棒、胶头滴管和 量筒 。
(4)NaCl是一种重要的化工原料。从元素守恒的视角,以NaCl为基本原料,可能制取的物质有 NaOH(或Cl2) (写一种)。
量筒
NaOH(或Cl2)
6. (2024·山东滨州)化学是一门以实验为基础的学科。
Ⅰ.结合下图有关实验,回答问题。
(1)过滤操作中仪器a的名称是 铁架台 。
(2)水电解器的b玻璃管中产生的气体是 氧气(或O2) (填化学式)。
铁架台
氧气(或O2)
(3)从安全角度考虑,在点燃氢气前,一定要检验氢气的 纯度 。
(4)将铝片与铝合金互相刻划,可证明铝合金的硬度 大于 (填“大于”“小于”或“等于”)铝片的硬度。
纯度
大于
Ⅱ.空间站采用循环技术保证航天员的用水和呼吸循环系统(部分)如图所示。
(5)为模拟大气环境,工作舱内氧气的体积分数应为 21 %。
(6)疏松多孔的新型分子筛具有 吸附 性,用于除去水中的异味。
21
吸附
(7)萨巴蒂尔反应系统内部提供高温、高压和催化剂等条件,反应系统内发生反应的化学方程式为 CO2+4H2 CH4+ 。
CO2+4H2 CH4+2H2O
7. (2024·陕西中考)根据下面图示的三个实验回答问题。
(1)写出标有序号①的仪器名称: 水槽 。
(2)实验乙中,发生反应的化学方程式是 3Fe+2O2 Fe3O4 。
水槽
3Fe+2O2 Fe3O4
(3)实验甲中, 不能 (填“能”或“不能”)用细铁丝代替红磷测定空气中氧气的含量。
(4)实验丙中,纸花a用紫色石蕊溶液浸泡后干燥,纸花b用紫色石蕊溶液润湿,通入CO2气体后,纸花 b (填字母)变红。
不能
b
8. (2024·云南中考)化学是一门以实验为基础的学科。
(1)仪器a的名称为 铁架台 。
铁架台
(2)实验室用高锰酸钾制取氧气,发生反应的化学方程式为 2KMnO4 K2MnO4+MnO2+O2↑ 。用B装置收集氧气,体现了氧气的物理性质是 氧气不易溶于水 ;停止加热时,为防止倒吸,应先进行的操作是 把导管移出水面 (填“熄灭酒精灯”或“把导管移出水面”)。
(3)用上述收集的O2完成如图C所示的实验,观察到澄清石灰水 变浑浊 。
2KMnO4 K2MnO4+MnO2+O2↑
氧气不易溶于水
把导管移出水面
变
浑浊
(4)某同学为探究燃烧的条件设计了如图实验。已知白磷的着火点是40℃。
向装置甲中通入空气,甲中的热水压入到乙中,甲、乙中的白磷均燃烧。由液面降低后甲中白磷燃烧的事实,说明燃烧需要 与空气接触 ;由热水进入后乙中白磷燃烧的事实,说明燃烧需要 温度达到可燃物的着火点 。
与空气
接触
温度
达到可燃物的着火点
9. (2024·江苏盐城)我国向世界承诺:努力争取2060年前实现“碳中和”——CO2排放量和转化量相等,达到相对零排放,为人类社会可持续发展贡献中国力量。
Ⅰ.了解二氧化碳排放
(1)CO2排放量增加可能引发的后果有 ABCD (填字母,下同)。
A. 冰川融化,海平面上升
B. 极端天气频发
C. 土地沙漠化,造成农业减产
D. 影响自然生态系统,改变生物多样性
ABCD
(2)空气中的CO2主要来自于 AB 。
A. 动植物的呼吸作用
B. 化石燃料的燃烧
C. 植物的光合作用
AB
(3)实验室制备CO2。根据下列仪器装置,回答问题。
①写出标号仪器的名称:a. 试管 ,b. 集气瓶 ;
②制取CO2可在A~E中选用装置 BC ;装置F是在装置B基础上的改进,其优点是 可以控制反应发生与停止 。
试管
集气瓶
BC
可以控制反应发生与停止
分别注入等体积的水、澄清石灰水、2%NaOH溶液,盖上瓶盖,
Ⅱ.探究二氧化碳转化
(4)CO2的吸收是其转化的有效方法。现有三种试剂:水、澄清石灰水、2%NaOH溶液,你认为最佳的CO2吸收剂是 2%NaOH溶 ,设计实验方案证明你的结论: 用三只相同的塑料瓶收集二氧化碳,分别注入等体积的水、澄清石灰水、2%NaOH溶液,盖 上瓶盖,充分振荡,若注入2%氢氧化钠溶液的塑料瓶变瘪程度最大,说明2%氢氧化钠溶液吸收二氧化碳效 。
2%NaOH溶液
用三只相同的塑料瓶收集二氧化碳,
充分振荡,若注入2%氢氧化钠溶液的塑料瓶变瘪程度最大,说明2%
氢氧化钠溶液吸收二氧化碳效果最好
Ⅲ.研制低碳行动方案
(5)低碳行动涵盖国际合作、国家工程和个人行为三个层面。请从“个人行为”层面策应“低碳行动”,写出你的一个行动打算: 出行乘坐公交车(合理即可) 。
出行乘坐公交车(合理即可)
10. (7分)(2024·越秀区校级二模)实验室制取气体和检验气体性质的部分装置如图所示.请回答问题。
(1)写出仪器的名称:① 长颈漏斗 ;② 锥形瓶 。
长颈漏斗
锥形瓶
(2)乙炔(化学式C2H2)俗称电石气,实验室中常用电石(一种灰色块状固体,化学式CaC2)与水在常温下反应制取,该反应同时还有氢氧化钙生成。通常情况下,乙炔是一种无色、无味、难溶于水的气体,标准状况下,乙炔的密度是1.16g/L(空气的密度为1.293 g/L),能与浓硫酸反应生成乙炔基硫酸酯。
Ⅰ、写出电石与水反应的化学方程式 CaC2+2H2O Ca(OH)2+C2H2↑ ;
CaC2+2H2O Ca(OH)2
+C2H2↑
Ⅱ、实际操作中,常采用饱和食盐水代替水以降低化学反应速率.若要获得平稳的乙炔气流,上图中最适合作为发生装置的是 C ,收集装置是 F 。
C
F
(3)若把G装置中的浓硫酸换成水并盛满,用来收集难溶于水的气体时,气体应从 b (填“a”或“b”端通入)。
(4)实验室制取二氧化碳时,在下图装置中连接压强传感器,得到曲线图。曲线中bc段压强保持不变的原因是 液体被压入长颈漏斗,固液分离,反应停止,不再生成气体,保持内部压强不变 ,曲线中c点对应的操作是 打开弹簧夹 。
b
液体被压入长颈漏斗,
固液分离,反应停止,不再生成气体,保持内部压强不变
打开弹簧夹
11. (2024·福田区模拟)如图是实验室常见制取气体的发生装置及收集装置,请回答。
Ⅰ.气体的制备与性质
(1)仪器a的名称是 锥形瓶 。
(2)实验室用固体加热制取比较纯净的氧气,应选择的发生装置和收集装置的组合是 AC (填序号,从A~E中选),该反应的化学方程式是 2KMnO4 K2MnO4+MnO2+O2↑ 。
(3)小圳同学想设计实验验证CO2与水反应,他将足量新制的CO2分别通过F中①和②进行对照实验,由于新制的CO2含有水蒸气,为了保证实验的效果,试剂X应该是 浓硫酸 (填名称)。
锥形瓶
AC
2KMnO4 K2MnO4+MnO2+O2↑
浓硫酸
Ⅱ.气体制备在生活与航空的应用
(4)图1是一种常见的家用制氧机的工作原理简图,图2是小圳同学用实验室常见仪器组装出具有相似功能的仪器,其中,装置甲相当于制氧机中的 过滤仓 (填“过滤仓”或“反应仓”)。
过滤仓
(5)我国科学家进行如图3所示的氧循环研究,实现了空间站氧气的再生。其中反应Ⅰ需要在催化剂和加热的条件下才能发生,写出该反应的化学方程式 CO2+4H2 CH4+2H2O 。
CO2+4H2 CH4+2H2O
同课章节目录
