2.2.2 离子反应 课件(共18张PPT)
文档属性
| 名称 | 2.2.2 离子反应 课件(共18张PPT) |

|
|
| 格式 | pptx | ||
| 文件大小 | 109.8MB | ||
| 资源类型 | 教案 | ||
| 版本资源 | 鲁科版(2019) | ||
| 科目 | 化学 | ||
| 更新时间 | 2025-02-13 00:00:00 | ||
图片预览





文档简介
(共18张PPT)
第二章 元素与物质世界
第二节 电解质的电离 离子反应
第二课时 离子反应
【知识回顾】
1.什么是电解质?
2.电解质在溶液中会发生怎样的变化?
电解质:在水溶液里或熔化状态下能够导电的化合物
物质溶于水或受热熔化时,离解成能够自由移动的离子的过程称为电离。
电离
【观察·思考】
观察稀硫酸与氢氧化钡反应,请大家
思考,其反应的实质是什么呢?
稀硫酸与氢氧化钡在水溶液中的反应
记录实验现象并分析产生现象的原因,填入下表。
实验现象 产生现象的原因
①溶液的红色逐渐变浅,直至消失;
②不断产生白色沉淀;
③指针不断偏向零,再滴加时,又不断偏大。
① H+和OH-发生了反应,溶液中OH-离子浓度逐渐减小,
②Ba2+与SO42-发生了反应,生成了BaSO4白色沉淀;
③溶液中离子浓度先减小,有离子参加了反应,硫酸过量后离子浓度又增加。
实验·探究
通过这个实验,你对稀硫酸与氢氧化钡溶液的反应有了哪些新的认识?这个反应的实质是什么?
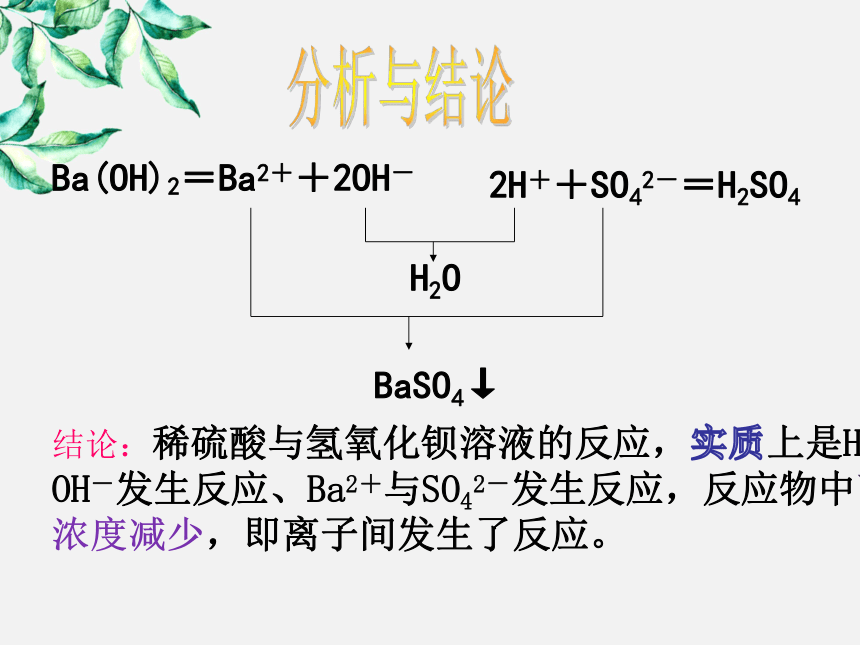
分析与结论
Ba(OH)2=Ba2++2OH-
2H++SO42-=H2SO4
H2O
BaSO4↓
结论:稀硫酸与氢氧化钡溶液的反应,实质上是H+与OH-发生反应、Ba2+与SO42-发生反应,反应物中离子浓度减少,即离子间发生了反应。
◎请从电解质电离的角度分析下列反应的实质,反应前后溶液中电解质所产生的离子种类和数量的变化。
【交流·研讨】
1.稀硫酸与NaOH溶液反应
反应前 反应后
稀硫酸离子种类 NaOH溶液离子种类 溶液离子种类
结论: OH-与H+结合生成H2O沉淀
H+、 SO42-
Na+ 、 OH-
Na+ 、 SO42-
反应前 反应后
CuSO4溶液离子种类 NaOH溶液离子种类 溶液离子种类
结论: Cu2+、 SO42-
Na+ 、 OH-
Na+ 、 SO42-
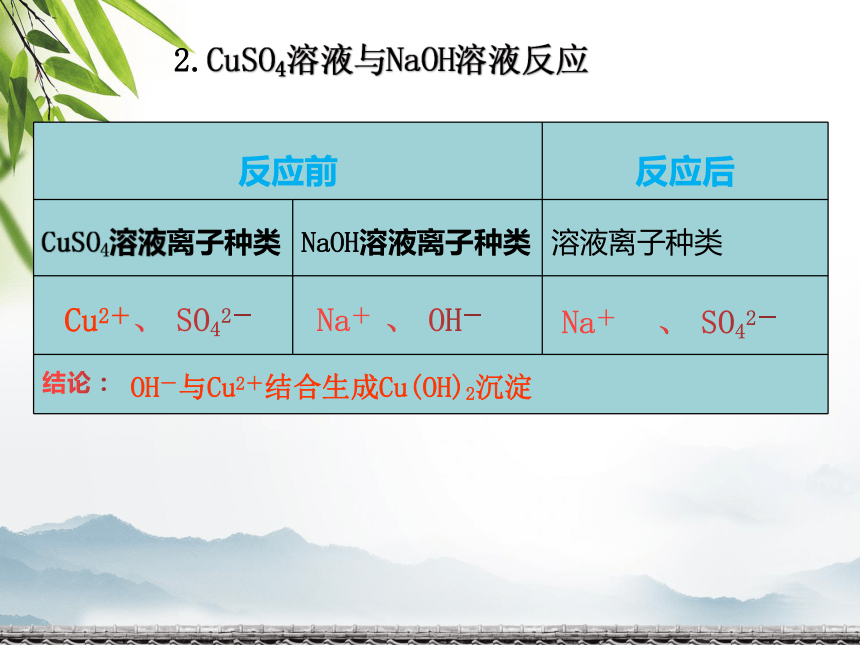
2.CuSO4溶液与NaOH溶液反应
OH-与Cu2+结合生成Cu(OH)2沉淀
3.盐酸与Na2CO3溶液的反应
这些反应有什么共同特点?
反应前 反应后
盐酸离子种类 Na2CO3溶液离子种类 溶液离子种类
结论: H+、 Cl-
Na+ 、 CO32-
Na+ 、 Cl-
H+与CO32-反应生成CO2和H2O
用相同的思路分析以下反应: NaCl溶液与AgNO3溶液反应;
KCl溶液与AgNO3溶液反应。
◆ 离子反应:有离子参加的化学反应。
1.电解质在水溶液中反应的实质
小结:电解质溶液之间的反应都是离子反应。
反应物中某些离子浓度减少的离子反应。
◆ 电解质在水溶液中反应的实质:
交流与探讨:
生成难溶物质(沉淀)或易挥发物质(气体)或难电离物质
离子反应发生的条件?
酸、碱和盐在溶液中互相交换成份的反应,实质上是一种离子反应
方法一:
⑴写出反应物在溶液中的的主要存在形式及微粒间的数量关系,写出电离方程式;
⑵确定发生化学反应的微粒、产物及其数量关系;
⑶写出离子方程式 并配平。
H2SO4 = 2H+ + SO42-
Ba(OH)2=Ba2+ + 2OH-
离子方程式的书写
以稀硫酸与Ba(OH)2溶液反应为例
2H+
SO42-
Ba2+
2OH-
2H2O
BaSO4
2H+ + SO42-+ Ba2+ + 2OH-= 2H2O + BaSO4
Na2CO3=2Na++CO32-
HCl=H++Cl-
1.稀盐酸与NaOH溶液反应
写出下列反应的离子方程式
NaOH=Na++OH-
HCl=H++Cl-
H++OH-=H2O
2.CuSO4溶液与NaOH溶液反应
NaOH=Na++OH-
CuSO4=Cu2++SO42-
2OH-+Cu2+=Cu(OH)2↓
3.Na2CO3溶液与稀盐酸反应
CO32-+2H+=CO2↑+H2O
注意:书写离子方程式时要遵守原子守恒和电荷守恒,要符合反应事实
⑴写出化学方程式
⑵改写成离子形式
⑶删除相同离子
⑷检查并写出离子方程式
离子方程式的书写
AgNO3+KCl=AgCl↓+KNO3
Ag+ + NO3 - + K++Cl-=
AgCl↓+ K+ + NO3 -
Ag+ +Cl-=AgCl↓
方法二:
以AgNO3溶液与KCl溶液反应为例
易溶于水且易电离的物质改写成离子符号(如强酸、强碱、可溶性盐);难溶于水的物质、挥发性物质和水仍用化学式
遵循原子守恒及其电荷守恒
离子方程式的含义
H++OH-=H2O
表示一类反应
强酸
强碱
生成H2O
Ba(OH)2+2HNO3=Ba(NO3)2+2H2O
2NaOH+H2SO4=Na2SO4↓+2H2O
课堂练习
1.下列两种物质混合后不能发生离子反应的是( )
A.硝酸溶液和碳酸钠溶液混合
B.氯化钠溶液和硝酸银溶液混合
C.硫酸钾溶液和氯化钡溶液混合
D.硝酸钾溶液和氯化钡溶液混合
D
2.下列离子反应不能发生的是( )
A.KHCO3+HCl===KCl+CO2↑+H2O
B.AgNO3+NaCl===AgCl↓+NaNO3
C.Na2CO3+Ca(OH)2===CaCO3↓+2NaOH
D.2HCl+Na2SO4===2NaCl+H2SO4
3.下列各组中两种物质在溶液中的反应,可用同一离子方程式表示的是 ( )
A. Cu(OH)2+HCl;Cu(OH)2+CH3COOH
B. Na2CO3+H2SO4;K2CO3+HCl
C. Na2CO3+NaOH;CaCCl2+NaOH
D. BaCl2+H2SO4;Ba(OH)2+H2SO4
D
B
4.在下列化学方程式中,不能用离子方程式Ba2++SO42-=BaSO4↓表示的是 ( )
A.BaCl2+K2SO4=BaSO4↓+2KCl
B.BaCO3+H2SO4 = BaSO4↓+CO2↑+H2O
C.Ba(NO3)2+ H2SO4= BaSO4↓+2HNO3
D.Ba(OH)2+ 2K2SO4 =BaSO4↓+2KOH
B
谢 谢!
第二章 元素与物质世界
第二节 电解质的电离 离子反应
第二课时 离子反应
【知识回顾】
1.什么是电解质?
2.电解质在溶液中会发生怎样的变化?
电解质:在水溶液里或熔化状态下能够导电的化合物
物质溶于水或受热熔化时,离解成能够自由移动的离子的过程称为电离。
电离
【观察·思考】
观察稀硫酸与氢氧化钡反应,请大家
思考,其反应的实质是什么呢?
稀硫酸与氢氧化钡在水溶液中的反应
记录实验现象并分析产生现象的原因,填入下表。
实验现象 产生现象的原因
①溶液的红色逐渐变浅,直至消失;
②不断产生白色沉淀;
③指针不断偏向零,再滴加时,又不断偏大。
① H+和OH-发生了反应,溶液中OH-离子浓度逐渐减小,
②Ba2+与SO42-发生了反应,生成了BaSO4白色沉淀;
③溶液中离子浓度先减小,有离子参加了反应,硫酸过量后离子浓度又增加。
实验·探究
通过这个实验,你对稀硫酸与氢氧化钡溶液的反应有了哪些新的认识?这个反应的实质是什么?
分析与结论
Ba(OH)2=Ba2++2OH-
2H++SO42-=H2SO4
H2O
BaSO4↓
结论:稀硫酸与氢氧化钡溶液的反应,实质上是H+与OH-发生反应、Ba2+与SO42-发生反应,反应物中离子浓度减少,即离子间发生了反应。
◎请从电解质电离的角度分析下列反应的实质,反应前后溶液中电解质所产生的离子种类和数量的变化。
【交流·研讨】
1.稀硫酸与NaOH溶液反应
反应前 反应后
稀硫酸离子种类 NaOH溶液离子种类 溶液离子种类
结论: OH-与H+结合生成H2O沉淀
H+、 SO42-
Na+ 、 OH-
Na+ 、 SO42-
反应前 反应后
CuSO4溶液离子种类 NaOH溶液离子种类 溶液离子种类
结论: Cu2+、 SO42-
Na+ 、 OH-
Na+ 、 SO42-
2.CuSO4溶液与NaOH溶液反应
OH-与Cu2+结合生成Cu(OH)2沉淀
3.盐酸与Na2CO3溶液的反应
这些反应有什么共同特点?
反应前 反应后
盐酸离子种类 Na2CO3溶液离子种类 溶液离子种类
结论: H+、 Cl-
Na+ 、 CO32-
Na+ 、 Cl-
H+与CO32-反应生成CO2和H2O
用相同的思路分析以下反应: NaCl溶液与AgNO3溶液反应;
KCl溶液与AgNO3溶液反应。
◆ 离子反应:有离子参加的化学反应。
1.电解质在水溶液中反应的实质
小结:电解质溶液之间的反应都是离子反应。
反应物中某些离子浓度减少的离子反应。
◆ 电解质在水溶液中反应的实质:
交流与探讨:
生成难溶物质(沉淀)或易挥发物质(气体)或难电离物质
离子反应发生的条件?
酸、碱和盐在溶液中互相交换成份的反应,实质上是一种离子反应
方法一:
⑴写出反应物在溶液中的的主要存在形式及微粒间的数量关系,写出电离方程式;
⑵确定发生化学反应的微粒、产物及其数量关系;
⑶写出离子方程式 并配平。
H2SO4 = 2H+ + SO42-
Ba(OH)2=Ba2+ + 2OH-
离子方程式的书写
以稀硫酸与Ba(OH)2溶液反应为例
2H+
SO42-
Ba2+
2OH-
2H2O
BaSO4
2H+ + SO42-+ Ba2+ + 2OH-= 2H2O + BaSO4
Na2CO3=2Na++CO32-
HCl=H++Cl-
1.稀盐酸与NaOH溶液反应
写出下列反应的离子方程式
NaOH=Na++OH-
HCl=H++Cl-
H++OH-=H2O
2.CuSO4溶液与NaOH溶液反应
NaOH=Na++OH-
CuSO4=Cu2++SO42-
2OH-+Cu2+=Cu(OH)2↓
3.Na2CO3溶液与稀盐酸反应
CO32-+2H+=CO2↑+H2O
注意:书写离子方程式时要遵守原子守恒和电荷守恒,要符合反应事实
⑴写出化学方程式
⑵改写成离子形式
⑶删除相同离子
⑷检查并写出离子方程式
离子方程式的书写
AgNO3+KCl=AgCl↓+KNO3
Ag+ + NO3 - + K++Cl-=
AgCl↓+ K+ + NO3 -
Ag+ +Cl-=AgCl↓
方法二:
以AgNO3溶液与KCl溶液反应为例
易溶于水且易电离的物质改写成离子符号(如强酸、强碱、可溶性盐);难溶于水的物质、挥发性物质和水仍用化学式
遵循原子守恒及其电荷守恒
离子方程式的含义
H++OH-=H2O
表示一类反应
强酸
强碱
生成H2O
Ba(OH)2+2HNO3=Ba(NO3)2+2H2O
2NaOH+H2SO4=Na2SO4↓+2H2O
课堂练习
1.下列两种物质混合后不能发生离子反应的是( )
A.硝酸溶液和碳酸钠溶液混合
B.氯化钠溶液和硝酸银溶液混合
C.硫酸钾溶液和氯化钡溶液混合
D.硝酸钾溶液和氯化钡溶液混合
D
2.下列离子反应不能发生的是( )
A.KHCO3+HCl===KCl+CO2↑+H2O
B.AgNO3+NaCl===AgCl↓+NaNO3
C.Na2CO3+Ca(OH)2===CaCO3↓+2NaOH
D.2HCl+Na2SO4===2NaCl+H2SO4
3.下列各组中两种物质在溶液中的反应,可用同一离子方程式表示的是 ( )
A. Cu(OH)2+HCl;Cu(OH)2+CH3COOH
B. Na2CO3+H2SO4;K2CO3+HCl
C. Na2CO3+NaOH;CaCCl2+NaOH
D. BaCl2+H2SO4;Ba(OH)2+H2SO4
D
B
4.在下列化学方程式中,不能用离子方程式Ba2++SO42-=BaSO4↓表示的是 ( )
A.BaCl2+K2SO4=BaSO4↓+2KCl
B.BaCO3+H2SO4 = BaSO4↓+CO2↑+H2O
C.Ba(NO3)2+ H2SO4= BaSO4↓+2HNO3
D.Ba(OH)2+ 2K2SO4 =BaSO4↓+2KOH
B
谢 谢!
