第十单元 课题1 常见的酸和碱 课件(共32张PPT)
文档属性
| 名称 | 第十单元 课题1 常见的酸和碱 课件(共32张PPT) |

|
|
| 格式 | pptx | ||
| 文件大小 | 42.2MB | ||
| 资源类型 | 教案 | ||
| 版本资源 | 人教版 | ||
| 科目 | 化学 | ||
| 更新时间 | 2025-02-14 00:00:00 | ||
图片预览









文档简介
(共32张PPT)
九年级化学教学课件
第十单元 酸和碱
课题1 常见的酸和碱
课堂小结
预习导学
情境导入
探究新知
评价反思
第1课时 酸碱指示剂 几种常见的酸
1.我知道的酸有盐酸、硫酸、醋酸 等;
我知道的碱有氢氧化钙、氨水 等。
3.下列试剂瓶应有 标志的是( )
A.氯化钠 B.蒸馏水 C.浓硫酸 D.葡萄糖
2.向紫色石蕊溶液中吹气,可使紫色石蕊溶液变___色。
预习导学
红
C
“酸”一词从有酸味的酒而来。最早,把比较珍贵的酒放在酒窖中保存,在微生物的作用下,产生了酸。
资料卡片
酸碱的由来
导入新课
“碱”一词在阿拉伯语中表示灰。人们将草木灰放到水中,利用灰汁洗浴、印染等。
资料卡片
酸碱的由来
认识几种常见的酸,
知道盐酸、硫酸的物理性质和用途
02
知道石蕊、酚酞等酸碱指示剂的变色规律
01
探究新知
学习目标
了解浓硫酸的腐蚀性,
知道稀释浓硫酸的方法
03
酸碱指示剂
01
将8支试管分成两组,每组的4支试管中分别加入白醋、苹果汁、石灰水和氢氧化钠溶液。向其中一组试管中加入紫色石蕊溶液,向另一组试管中加入无色酚酞溶液。观察现象。
实验探究
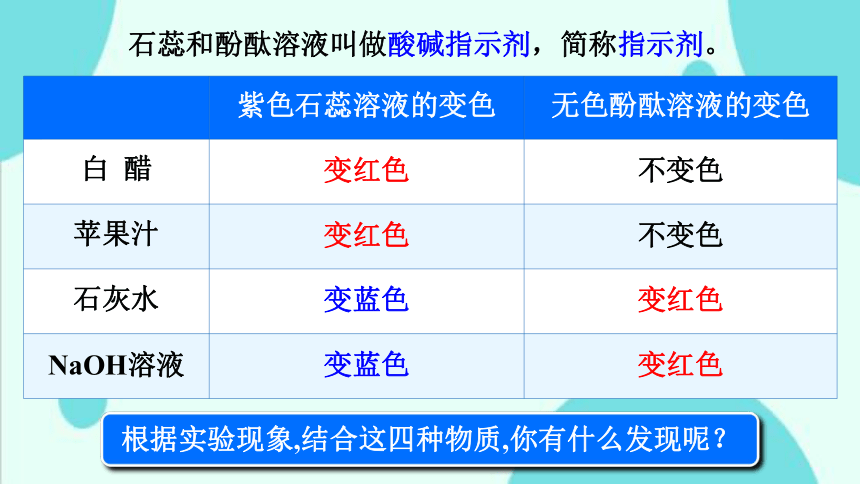
紫色石蕊溶液的变色 无色酚酞溶液的变色
白 醋 变红色 不变色
苹果汁 变红色 不变色
石灰水 变蓝色 变红色
NaOH溶液 变蓝色 变红色
石蕊和酚酞溶液叫做酸碱指示剂,简称指示剂。
根据实验现象,结合这四种物质,你有什么发现呢?
白醋、苹果汁、石灰水和氢氧化钠溶液等能使石蕊溶液、酚酞溶液显示不同的颜色。
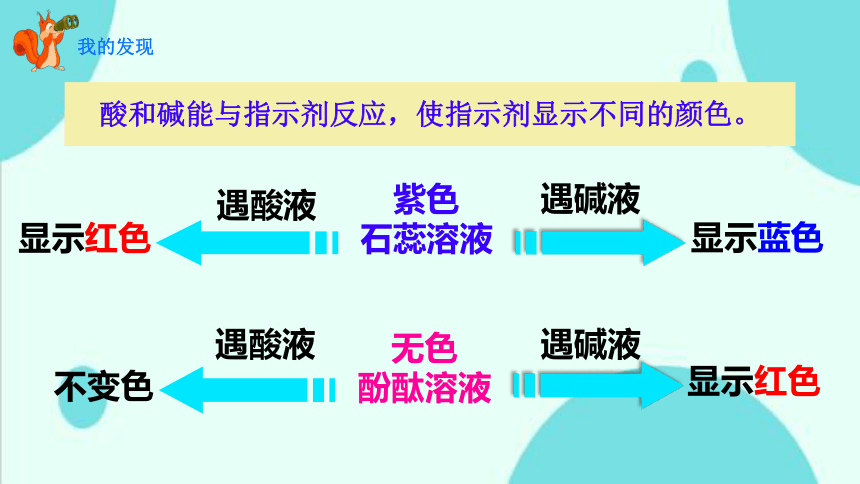
酸和碱能与指示剂反应,使指示剂显示不同的颜色。
遇酸液
遇碱液
显示红色
显示蓝色
紫色
石蕊溶液
遇酸液
遇碱液
显示红色
不变色
无色
酚酞溶液
我的发现
著名化学家波义耳在一次试验中不小心将盐酸溅到紫罗兰花瓣上,过一会儿他惊奇地发现,紫色的花瓣上出现了红点点。
波义耳对这一意外的发现做出了各种假设,经过多次试验验证,探究普遍规律,终于获得成功
生活中除了紫罗兰、紫甘蓝,还有哪些红色、
紫色的花瓣或果实也可以作指示剂呢?
你能设计一个方案试一试吗?
牵牛花
紫甘蓝(紫卷心菜)
美人蕉
紫萝卜
月季花
丝瓜花
拟代用 指示剂 酸性溶液中的 颜色变化 中性溶液 中的颜色 碱性溶液中的
颜色变化
牵牛花 红色 紫色 蓝色
月季花 浅红色 红色 黄色
美人焦 淡红色 红色 绿色
紫萝卜皮 红色 紫色 黄绿色
紫卷心菜 浅紫色 紫色 黄绿色
丝瓜花 黄色 黄绿色 黄色
酒精浸出液
思考:它们都可以用作酸碱指示剂吗?
几种常见的酸
02
浓盐酸
浓硫酸
水
观察浓硫酸和浓盐酸的颜色和状态;比较它们与同体积水的质量的大小;打开瓶塞,观察发生的现象;闻一闻是否有气味?
实验探究
浓盐酸 浓硫酸
颜色状态 无色液体 无色黏稠液体
打开瓶盖后的现象 有 白雾 出现 无现象
气 味 有刺激性气味 无气味
溶质的质量分数 36%-38% 98%
密 度 1.19g/mL 1.84g/mL
(难挥发)
浓盐酸和浓硫酸的部分物理性质
浓盐酸具有很强的挥发性,挥发出来的HCl气体与空气中的水蒸气结合,形成盐酸小液滴。
盐酸的用途
除铁锈
制造药品
人体胃液中含有盐酸,可帮助消化。
染料
硫酸的用途
精炼石油
火药
化肥
农药
浓硫酸具有吸水性,在实验室中常用它作干燥剂。
由于浓硫酸具有吸水性,常用作H2、O2和CO2的干燥剂。
用 途
盐 酸 HCl 重要化工产品。用于金属表面除锈、制造药物
(如盐酸麻黄素、氯化锌)等;人体胃液中有盐酸,可帮助消化。
硫 酸 H2SO4 重要化工原料。用于生产化肥、农药、火药、染料以及冶炼金属、精炼石油和金属除锈等。浓硫酸有吸水性,在实验室中常用它做干燥剂。
盐酸和硫酸的主要用途
如果不小心将浓硫酸和浓盐酸露置于空气中很长时间,你能从溶液组成上(溶质、溶剂、溶质的质量分数)分析它们发生了哪些变化?
质 量 溶质的
质量分数
溶质 溶剂 溶液 浓硫酸 不变 变大 变大 变小
浓盐酸 变小 不变 变小 变小
问题和讨论
在实验室和化工生产中常用的酸还有硝酸(HNO3)、醋酸(CH3COOH)等。另外,生活中常见的许多物质中也含有酸。
食醋中含有醋酸
柠檬、柑橘等水果中含有柠檬酸
车
用
铅
蓄
电
池
中
含
有
硫
酸
课堂活动
浓硫酸的腐蚀性
03
实 验 放置后的现象
“白水”写黑字 浓硫酸能夺取由碳、氢、氧等元素组成的化合物里的
“水” ( 氢、氧元素原子个数比为2:1 ),生成黑色的碳和水
木棍变黑 “水” 滴布穿 纸张、木材、棉布等物质都是由碳、氢、氧等元素组成的。
纸上显出
黑色字迹
蘸有浓硫酸的
部位变黑
滴有浓硫酸的部位
变黑甚至烧成洞
(脱水性)
化学性质
为什么会产生这些现象?你受到哪些启发?
腐蚀性
手的感觉 发热或发烫
分 析 浓硫酸溶于水放出大量的热
将浓硫酸沿烧杯壁缓慢地注入盛有水的烧杯里,用玻璃棒不断搅拌,并用手触碰烧杯外壁,有什么感觉?
实验探究
在稀释浓硫酸时,一定要把浓硫酸沿器壁慢慢注入水里,并不断搅拌。切不可将水直接倒入浓硫酸里。
注 意
浓硫酸
操作:酸入水、沿器壁、
缓缓倒、不断搅
浓硫酸
如果不慎将浓硫酸沾到皮肤或衣服上,应如何处理
如果将稀硫酸沾到皮肤或衣服上,是否也要进行这样的处理
应立即用大量水冲洗,然后涂上3%—5%的
碳酸氢钠(NaHCO3)溶液。
用大量的水冲洗。
讨论与交流
课堂小结
随堂训练
1.小李在学习酸碱指示剂与常见酸、碱溶液作用时,归纳成如图所示的关系。图中A、B、C、D是两圆相交的部分,分别表示指示剂与酸、碱溶液作用时所显示出的颜色,则其中表示不正确的是( )
A.红色 B.蓝色
C.紫色 D.无色
石蕊
酸
碱
酚酞
A
B
D
C
C
序号 实验目的 实验过程
① 稀释浓硫酸 取少量浓硫酸放入烧杯中,缓慢倒入水,并用玻璃棒搅拌
② 证明脱水性 取少量浓硫酸,滴在纸张或木片上
③ 证明吸水性 取少量浓硫酸,向其中加入水,变成稀硫酸
④ 除氧气中的水分 将混合气体通过盛有浓硫酸的洗气瓶,并用向上排空气法
2.下列有关浓硫酸的相关实验,其中合理的是( )
A. ②③ B. ①③ C. ②④ D. ①④
C
作 业
《学练优》第36,37页。
板书设计
01.酸碱指示剂
02.几种常见的酸
紫石蕊,遇酸红,遇碱蓝
浓盐酸和浓硫酸的物理性质
无酚酞,遇酸无,遇碱红
盐酸和硫酸的主要用途
03.浓硫酸的腐蚀性
浓硫酸的腐蚀性
稀释浓硫酸
酸入水、沿器壁、缓缓倒、不断搅
九年级化学教学课件
第十单元 酸和碱
课题1 常见的酸和碱
课堂小结
预习导学
情境导入
探究新知
评价反思
第1课时 酸碱指示剂 几种常见的酸
1.我知道的酸有盐酸、硫酸、醋酸 等;
我知道的碱有氢氧化钙、氨水 等。
3.下列试剂瓶应有 标志的是( )
A.氯化钠 B.蒸馏水 C.浓硫酸 D.葡萄糖
2.向紫色石蕊溶液中吹气,可使紫色石蕊溶液变___色。
预习导学
红
C
“酸”一词从有酸味的酒而来。最早,把比较珍贵的酒放在酒窖中保存,在微生物的作用下,产生了酸。
资料卡片
酸碱的由来
导入新课
“碱”一词在阿拉伯语中表示灰。人们将草木灰放到水中,利用灰汁洗浴、印染等。
资料卡片
酸碱的由来
认识几种常见的酸,
知道盐酸、硫酸的物理性质和用途
02
知道石蕊、酚酞等酸碱指示剂的变色规律
01
探究新知
学习目标
了解浓硫酸的腐蚀性,
知道稀释浓硫酸的方法
03
酸碱指示剂
01
将8支试管分成两组,每组的4支试管中分别加入白醋、苹果汁、石灰水和氢氧化钠溶液。向其中一组试管中加入紫色石蕊溶液,向另一组试管中加入无色酚酞溶液。观察现象。
实验探究
紫色石蕊溶液的变色 无色酚酞溶液的变色
白 醋 变红色 不变色
苹果汁 变红色 不变色
石灰水 变蓝色 变红色
NaOH溶液 变蓝色 变红色
石蕊和酚酞溶液叫做酸碱指示剂,简称指示剂。
根据实验现象,结合这四种物质,你有什么发现呢?
白醋、苹果汁、石灰水和氢氧化钠溶液等能使石蕊溶液、酚酞溶液显示不同的颜色。
酸和碱能与指示剂反应,使指示剂显示不同的颜色。
遇酸液
遇碱液
显示红色
显示蓝色
紫色
石蕊溶液
遇酸液
遇碱液
显示红色
不变色
无色
酚酞溶液
我的发现
著名化学家波义耳在一次试验中不小心将盐酸溅到紫罗兰花瓣上,过一会儿他惊奇地发现,紫色的花瓣上出现了红点点。
波义耳对这一意外的发现做出了各种假设,经过多次试验验证,探究普遍规律,终于获得成功
生活中除了紫罗兰、紫甘蓝,还有哪些红色、
紫色的花瓣或果实也可以作指示剂呢?
你能设计一个方案试一试吗?
牵牛花
紫甘蓝(紫卷心菜)
美人蕉
紫萝卜
月季花
丝瓜花
拟代用 指示剂 酸性溶液中的 颜色变化 中性溶液 中的颜色 碱性溶液中的
颜色变化
牵牛花 红色 紫色 蓝色
月季花 浅红色 红色 黄色
美人焦 淡红色 红色 绿色
紫萝卜皮 红色 紫色 黄绿色
紫卷心菜 浅紫色 紫色 黄绿色
丝瓜花 黄色 黄绿色 黄色
酒精浸出液
思考:它们都可以用作酸碱指示剂吗?
几种常见的酸
02
浓盐酸
浓硫酸
水
观察浓硫酸和浓盐酸的颜色和状态;比较它们与同体积水的质量的大小;打开瓶塞,观察发生的现象;闻一闻是否有气味?
实验探究
浓盐酸 浓硫酸
颜色状态 无色液体 无色黏稠液体
打开瓶盖后的现象 有 白雾 出现 无现象
气 味 有刺激性气味 无气味
溶质的质量分数 36%-38% 98%
密 度 1.19g/mL 1.84g/mL
(难挥发)
浓盐酸和浓硫酸的部分物理性质
浓盐酸具有很强的挥发性,挥发出来的HCl气体与空气中的水蒸气结合,形成盐酸小液滴。
盐酸的用途
除铁锈
制造药品
人体胃液中含有盐酸,可帮助消化。
染料
硫酸的用途
精炼石油
火药
化肥
农药
浓硫酸具有吸水性,在实验室中常用它作干燥剂。
由于浓硫酸具有吸水性,常用作H2、O2和CO2的干燥剂。
用 途
盐 酸 HCl 重要化工产品。用于金属表面除锈、制造药物
(如盐酸麻黄素、氯化锌)等;人体胃液中有盐酸,可帮助消化。
硫 酸 H2SO4 重要化工原料。用于生产化肥、农药、火药、染料以及冶炼金属、精炼石油和金属除锈等。浓硫酸有吸水性,在实验室中常用它做干燥剂。
盐酸和硫酸的主要用途
如果不小心将浓硫酸和浓盐酸露置于空气中很长时间,你能从溶液组成上(溶质、溶剂、溶质的质量分数)分析它们发生了哪些变化?
质 量 溶质的
质量分数
溶质 溶剂 溶液 浓硫酸 不变 变大 变大 变小
浓盐酸 变小 不变 变小 变小
问题和讨论
在实验室和化工生产中常用的酸还有硝酸(HNO3)、醋酸(CH3COOH)等。另外,生活中常见的许多物质中也含有酸。
食醋中含有醋酸
柠檬、柑橘等水果中含有柠檬酸
车
用
铅
蓄
电
池
中
含
有
硫
酸
课堂活动
浓硫酸的腐蚀性
03
实 验 放置后的现象
“白水”写黑字 浓硫酸能夺取由碳、氢、氧等元素组成的化合物里的
“水” ( 氢、氧元素原子个数比为2:1 ),生成黑色的碳和水
木棍变黑 “水” 滴布穿 纸张、木材、棉布等物质都是由碳、氢、氧等元素组成的。
纸上显出
黑色字迹
蘸有浓硫酸的
部位变黑
滴有浓硫酸的部位
变黑甚至烧成洞
(脱水性)
化学性质
为什么会产生这些现象?你受到哪些启发?
腐蚀性
手的感觉 发热或发烫
分 析 浓硫酸溶于水放出大量的热
将浓硫酸沿烧杯壁缓慢地注入盛有水的烧杯里,用玻璃棒不断搅拌,并用手触碰烧杯外壁,有什么感觉?
实验探究
在稀释浓硫酸时,一定要把浓硫酸沿器壁慢慢注入水里,并不断搅拌。切不可将水直接倒入浓硫酸里。
注 意
浓硫酸
操作:酸入水、沿器壁、
缓缓倒、不断搅
浓硫酸
如果不慎将浓硫酸沾到皮肤或衣服上,应如何处理
如果将稀硫酸沾到皮肤或衣服上,是否也要进行这样的处理
应立即用大量水冲洗,然后涂上3%—5%的
碳酸氢钠(NaHCO3)溶液。
用大量的水冲洗。
讨论与交流
课堂小结
随堂训练
1.小李在学习酸碱指示剂与常见酸、碱溶液作用时,归纳成如图所示的关系。图中A、B、C、D是两圆相交的部分,分别表示指示剂与酸、碱溶液作用时所显示出的颜色,则其中表示不正确的是( )
A.红色 B.蓝色
C.紫色 D.无色
石蕊
酸
碱
酚酞
A
B
D
C
C
序号 实验目的 实验过程
① 稀释浓硫酸 取少量浓硫酸放入烧杯中,缓慢倒入水,并用玻璃棒搅拌
② 证明脱水性 取少量浓硫酸,滴在纸张或木片上
③ 证明吸水性 取少量浓硫酸,向其中加入水,变成稀硫酸
④ 除氧气中的水分 将混合气体通过盛有浓硫酸的洗气瓶,并用向上排空气法
2.下列有关浓硫酸的相关实验,其中合理的是( )
A. ②③ B. ①③ C. ②④ D. ①④
C
作 业
《学练优》第36,37页。
板书设计
01.酸碱指示剂
02.几种常见的酸
紫石蕊,遇酸红,遇碱蓝
浓盐酸和浓硫酸的物理性质
无酚酞,遇酸无,遇碱红
盐酸和硫酸的主要用途
03.浓硫酸的腐蚀性
浓硫酸的腐蚀性
稀释浓硫酸
酸入水、沿器壁、缓缓倒、不断搅
同课章节目录
