10.2 第4课时 中和反应 课件(共22张PPT内嵌视频)
文档属性
| 名称 | 10.2 第4课时 中和反应 课件(共22张PPT内嵌视频) |

|
|
| 格式 | pptx | ||
| 文件大小 | 41.5MB | ||
| 资源类型 | 教案 | ||
| 版本资源 | 人教版 | ||
| 科目 | 化学 | ||
| 更新时间 | 2025-02-15 00:00:00 | ||
图片预览








文档简介
(共22张PPT)
人教版九年级下册
化学
第十单元 常见的酸、碱、盐
课题2 常见的酸和碱
第4课时 中和反应
学习目标
1.学会借助指示剂判断无明显现象反应的发生,通过实验理解酸和碱之间能发生中和反应,通过对物质构成的分析,初步形成盐的定义。
2.通过反应的微观分析,初步了解中和反应发生的实质并学会书写酸与碱发生中和反应的化学方程式。
3.了解中和反应在生产、生活中的应用,体会中和反应与人类生产、生活、人体健康的密切联系。
4.通过思考、讨论,设计实验方案证明无明显现象的中和反应的发生,体会其设计思路和方法。
5.通过实验活动,体会对获得的事实进行分析得出结论的科学方法。
6.在讨论和实验中,增强与同学合作、交流,发表自己的观点。
环节一 导入新课
环节二 实验探究 确定酸与碱能反应
问题
酸与碱之间能否反应?我们以稀盐酸和氢氧化钠为例。
实验
分析
实验操作 实验现象 结论
将稀盐酸逐滴滴入氢氧化钠溶液中,振荡,观察现象
无明显现象
?
氢氧化钠溶液与稀盐酸混合后无明显现象,要证明两者间发生了化学反应,一是可通过检验有新物质生成,二是可通过检测反应物消耗或消失证明。
实验
向烧杯中加入适量氢氧化钠溶液,滴加数滴无色酚酞溶液,搅拌,再用胶头滴管向烧杯中逐滴滴加稀盐酸,并用玻璃棒搅拌,观察现象。
现象
分析
结论
氢氧化钠溶液中滴入无色酚酞溶液后变红,滴加稀盐酸时,溶液最终变成无色。
酚酞遇碱性溶液变红,遇中性溶液和酸性溶液均不变色。氢氧化钠溶液显碱性,使酚酞变红,随着稀盐酸的加入,溶液最终变为无色,说明随着稀盐酸的加入,氢氧化钠不断被消耗,溶液恰好变成无色时,氢氧化钠与盐酸恰好完全反应。
氢氧化钠能与稀盐酸反应。
质疑
分析
溶液颜色的变化是否可能是由于滴加稀盐酸过程中使溶液稀释所造成的呢
溶液稀释时,溶液的酸性或碱性会减弱,但溶液的酸碱性不会改变,因此实验过程中,溶液颜色的变化不是由于稀释造成的。
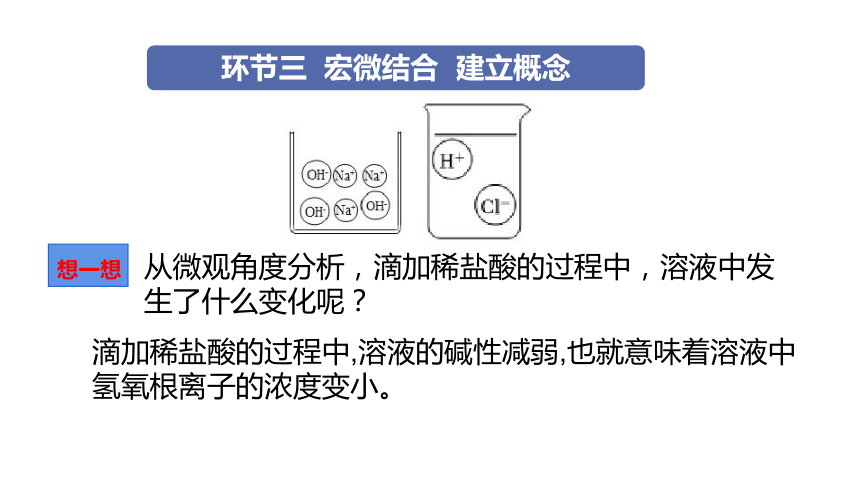
环节三 宏微结合 建立概念
想一想
从微观角度分析,滴加稀盐酸的过程中,溶液中发生了什么变化呢?
滴加稀盐酸的过程中,溶液的碱性减弱,也就意味着溶液中氢氧根离子的浓度变小。
资料
用pH计测得向氢氧化钠溶液中滴加稀盐酸时,溶液的pH变化如下图所示。
刚开始加入稀盐酸时,溶液不显酸性,仍然显碱性,说明刚开始时,加入的稀盐酸中的氢离子被氢氧化钠完全消耗,即该过程中,氢氧根离子与氢离子结合生成水分子,可表示为H++OH-==H2O。
想一想
这一过程中,氢氧根离子与哪种离子发生了反应呢
氢氧化钠与盐酸的反应,实质是氢氧化钠溶液中的氢氧根离子与盐酸中的氢离子结合生成水分子:
想一想
你能写出该反应的化学方程式吗?
HCl + NaOH ==== NaCl +H2O
事实上,除盐酸与氢氧化钠能反应外,其他的酸和碱之间也能发生反应,如
H2SO4 + 2NaOH ==== Na2SO4 + 2H2O、
2HCl + Ca(OH)2==== CaCl2 + 2H2O 等。
HCl + NaOH ==== NaCl + H2O
盐:由金属离子和酸根离子组成的化合物
酸
碱
盐
水
和
作用生成
和
的反应
中和反应
中和反应的实质是H++OH-==H2O
环节四 逻辑推理 辨析概念
想一想
1.中和反应的产物是盐和水,那么生成盐和水的反应一定是中和反应吗?
酸与金属氧化物反应(如Fe2O3+6HCl ==2FeCl3+3H2O等)、碱与非金属氧化物(如2NaOH+CO2==Na2CO3+H2O等)反应都生成盐和水,但反应物却有酸无碱或有碱无酸,都不属于中和反应。
2.中和反应一定没有明显的现象吗?
实验:取适量硫酸铜溶液于试管中,向其中滴加适量的氢氧化钠溶液,制得氢氧化铜沉淀,将上层清液倒出,向沉淀中滴加稀盐酸,振荡。
向硫酸铜溶液中滴入氢氧化钠溶液有蓝色沉淀生成,向蓝色沉淀中滴入稀盐酸,沉淀溶解得到蓝色溶液。
不是所有的中和反应都没有明显现象。
环节五 问题解决 运用概念
中和反应在生产、生活中有广泛的应用,如:
(1)医疗上服用含氢氧化铝的药物治疗胃酸过多症,请写出反应的化学方程式。
3HCl + Al(OH)3 ==== AlCl3 + 3H2O
(2)农业上常用熟石灰改良酸性土壤,若土壤中含有的酸为硫酸,请写出反应的化学方程式。
H2SO4+ Ca(OH)2 ==== CaSO4 + 2H2O
(3)工业上常用熟石灰处理含盐酸、硫酸、硝酸(HNO3)等的废水,写出熟石灰与硝酸反应的化学方程式。
2HNO3+ Ca(OH)2 ==== Ca(NO3)2 + 2H2O
(4)蜂或蚂蚁叮咬人的皮肤后,在皮肤内分泌出蚁酸(一种酸),会使叮咬处很快出现肿、痛或瘙痒等症状,涂抹一些肥皂水等碱性的物质可减轻症状。
课堂小结
(1)中和反应的概念。
(2)中和反应的实质。
(3)中和反应的应用。
1.小烧杯中盛有含石蕊的硝酸溶液,向其中逐滴加入氢氧化钠溶液至过量,烧杯中溶液颜色变化顺序是 ( )
A.红色—紫色—蓝色 B.紫色—红色—蓝色
C.蓝色—红色—紫色 D.紫色—蓝色—红色
A
课堂作业
2.向澄清石灰水中滴加稀盐酸,在滴加过程中,对溶液描述不正确的是( )
A.Ca2+数目基本不变 B.OH﹣数目减少
C.Cl﹣数目增多 D.溶液的pH逐渐增大
D
3.向NaOH溶液中加入盐酸,至恰好完全反应,反应的微观示意图如图所示,下列说法正确的是( )
A.该反应的实质是Na+和Cl﹣结合生成NaCl分子
B.酸与碱的反应会有水生成
C.反应前后数量没有变化的粒子是Na+、Cl﹣和H2O
D.该反应属于基本反应类型中的中和反应
B
4.图Ⅰ为稀盐酸与氢氧化钠溶液中和滴定实验,滴定过程中pH和温度变化情况如图Ⅱ、图Ⅲ,请判断下列说法中正确的是 ( )
A.仪器A中溶液的溶质是氢氧化钠
B.图Ⅲ中V的数值最接近16
C.图Ⅱ中b点所示溶液中的溶质是NaCl和NaOH
D.图Ⅱ中c→d所示溶液中NaCl的质量不断增加
C
谢 谢 观 看
人教版九年级下册
化学
第十单元 常见的酸、碱、盐
课题2 常见的酸和碱
第4课时 中和反应
学习目标
1.学会借助指示剂判断无明显现象反应的发生,通过实验理解酸和碱之间能发生中和反应,通过对物质构成的分析,初步形成盐的定义。
2.通过反应的微观分析,初步了解中和反应发生的实质并学会书写酸与碱发生中和反应的化学方程式。
3.了解中和反应在生产、生活中的应用,体会中和反应与人类生产、生活、人体健康的密切联系。
4.通过思考、讨论,设计实验方案证明无明显现象的中和反应的发生,体会其设计思路和方法。
5.通过实验活动,体会对获得的事实进行分析得出结论的科学方法。
6.在讨论和实验中,增强与同学合作、交流,发表自己的观点。
环节一 导入新课
环节二 实验探究 确定酸与碱能反应
问题
酸与碱之间能否反应?我们以稀盐酸和氢氧化钠为例。
实验
分析
实验操作 实验现象 结论
将稀盐酸逐滴滴入氢氧化钠溶液中,振荡,观察现象
无明显现象
?
氢氧化钠溶液与稀盐酸混合后无明显现象,要证明两者间发生了化学反应,一是可通过检验有新物质生成,二是可通过检测反应物消耗或消失证明。
实验
向烧杯中加入适量氢氧化钠溶液,滴加数滴无色酚酞溶液,搅拌,再用胶头滴管向烧杯中逐滴滴加稀盐酸,并用玻璃棒搅拌,观察现象。
现象
分析
结论
氢氧化钠溶液中滴入无色酚酞溶液后变红,滴加稀盐酸时,溶液最终变成无色。
酚酞遇碱性溶液变红,遇中性溶液和酸性溶液均不变色。氢氧化钠溶液显碱性,使酚酞变红,随着稀盐酸的加入,溶液最终变为无色,说明随着稀盐酸的加入,氢氧化钠不断被消耗,溶液恰好变成无色时,氢氧化钠与盐酸恰好完全反应。
氢氧化钠能与稀盐酸反应。
质疑
分析
溶液颜色的变化是否可能是由于滴加稀盐酸过程中使溶液稀释所造成的呢
溶液稀释时,溶液的酸性或碱性会减弱,但溶液的酸碱性不会改变,因此实验过程中,溶液颜色的变化不是由于稀释造成的。
环节三 宏微结合 建立概念
想一想
从微观角度分析,滴加稀盐酸的过程中,溶液中发生了什么变化呢?
滴加稀盐酸的过程中,溶液的碱性减弱,也就意味着溶液中氢氧根离子的浓度变小。
资料
用pH计测得向氢氧化钠溶液中滴加稀盐酸时,溶液的pH变化如下图所示。
刚开始加入稀盐酸时,溶液不显酸性,仍然显碱性,说明刚开始时,加入的稀盐酸中的氢离子被氢氧化钠完全消耗,即该过程中,氢氧根离子与氢离子结合生成水分子,可表示为H++OH-==H2O。
想一想
这一过程中,氢氧根离子与哪种离子发生了反应呢
氢氧化钠与盐酸的反应,实质是氢氧化钠溶液中的氢氧根离子与盐酸中的氢离子结合生成水分子:
想一想
你能写出该反应的化学方程式吗?
HCl + NaOH ==== NaCl +H2O
事实上,除盐酸与氢氧化钠能反应外,其他的酸和碱之间也能发生反应,如
H2SO4 + 2NaOH ==== Na2SO4 + 2H2O、
2HCl + Ca(OH)2==== CaCl2 + 2H2O 等。
HCl + NaOH ==== NaCl + H2O
盐:由金属离子和酸根离子组成的化合物
酸
碱
盐
水
和
作用生成
和
的反应
中和反应
中和反应的实质是H++OH-==H2O
环节四 逻辑推理 辨析概念
想一想
1.中和反应的产物是盐和水,那么生成盐和水的反应一定是中和反应吗?
酸与金属氧化物反应(如Fe2O3+6HCl ==2FeCl3+3H2O等)、碱与非金属氧化物(如2NaOH+CO2==Na2CO3+H2O等)反应都生成盐和水,但反应物却有酸无碱或有碱无酸,都不属于中和反应。
2.中和反应一定没有明显的现象吗?
实验:取适量硫酸铜溶液于试管中,向其中滴加适量的氢氧化钠溶液,制得氢氧化铜沉淀,将上层清液倒出,向沉淀中滴加稀盐酸,振荡。
向硫酸铜溶液中滴入氢氧化钠溶液有蓝色沉淀生成,向蓝色沉淀中滴入稀盐酸,沉淀溶解得到蓝色溶液。
不是所有的中和反应都没有明显现象。
环节五 问题解决 运用概念
中和反应在生产、生活中有广泛的应用,如:
(1)医疗上服用含氢氧化铝的药物治疗胃酸过多症,请写出反应的化学方程式。
3HCl + Al(OH)3 ==== AlCl3 + 3H2O
(2)农业上常用熟石灰改良酸性土壤,若土壤中含有的酸为硫酸,请写出反应的化学方程式。
H2SO4+ Ca(OH)2 ==== CaSO4 + 2H2O
(3)工业上常用熟石灰处理含盐酸、硫酸、硝酸(HNO3)等的废水,写出熟石灰与硝酸反应的化学方程式。
2HNO3+ Ca(OH)2 ==== Ca(NO3)2 + 2H2O
(4)蜂或蚂蚁叮咬人的皮肤后,在皮肤内分泌出蚁酸(一种酸),会使叮咬处很快出现肿、痛或瘙痒等症状,涂抹一些肥皂水等碱性的物质可减轻症状。
课堂小结
(1)中和反应的概念。
(2)中和反应的实质。
(3)中和反应的应用。
1.小烧杯中盛有含石蕊的硝酸溶液,向其中逐滴加入氢氧化钠溶液至过量,烧杯中溶液颜色变化顺序是 ( )
A.红色—紫色—蓝色 B.紫色—红色—蓝色
C.蓝色—红色—紫色 D.紫色—蓝色—红色
A
课堂作业
2.向澄清石灰水中滴加稀盐酸,在滴加过程中,对溶液描述不正确的是( )
A.Ca2+数目基本不变 B.OH﹣数目减少
C.Cl﹣数目增多 D.溶液的pH逐渐增大
D
3.向NaOH溶液中加入盐酸,至恰好完全反应,反应的微观示意图如图所示,下列说法正确的是( )
A.该反应的实质是Na+和Cl﹣结合生成NaCl分子
B.酸与碱的反应会有水生成
C.反应前后数量没有变化的粒子是Na+、Cl﹣和H2O
D.该反应属于基本反应类型中的中和反应
B
4.图Ⅰ为稀盐酸与氢氧化钠溶液中和滴定实验,滴定过程中pH和温度变化情况如图Ⅱ、图Ⅲ,请判断下列说法中正确的是 ( )
A.仪器A中溶液的溶质是氢氧化钠
B.图Ⅲ中V的数值最接近16
C.图Ⅱ中b点所示溶液中的溶质是NaCl和NaOH
D.图Ⅱ中c→d所示溶液中NaCl的质量不断增加
C
谢 谢 观 看
同课章节目录
