苏教版高中化学高三一轮复习电解池复习教学课件(共22张PPT)
文档属性
| 名称 | 苏教版高中化学高三一轮复习电解池复习教学课件(共22张PPT) |  | |
| 格式 | pptx | ||
| 文件大小 | 3.9MB | ||
| 资源类型 | 试卷 | ||
| 版本资源 | 苏教版(2019) | ||
| 科目 | 化学 | ||
| 更新时间 | 2025-02-16 17:33:18 | ||
图片预览





文档简介
(共22张PPT)
2022级高三化学一轮复习
第16讲 电解池工作原理及应用
(1)电极名称判断
(2)电极反应式的书写
(3)微粒的迁移方向
(4)定量计算
(5)电解液的物质变化
核心考点
年份 2024 2023 2022 2021 2020
题号 13题 18题(2)(5) 13题 17题(4) 5题D
13题
考查内容 (1)电极名称判断 (2)电极反应式的书写 (5)电解液的物质变化 (2)电极反应式的书写 (4)计算 (5)电解液的物质变化 (3)微粒的迁移方向 (5)电解液的物质变化 (3)微粒的迁移方向
(4)计算
(5)电解液的物质变化
研究高考命题特点,把握高考命题方向
试题来源 情景类型 情景来源 情景信息
24年河北 电化学装置设计 学术 Mg-CO2电池
24年湖南 电化学装置应用 学术 合成K4C6N16
24年湖北 电化学装置应用 学术 甘氨酸合成
24年东三省 电化学装置应用 学术 电化学装置制氢气
24年安徽 电化学装置设计 学术 基于超分子材料设计锌电池
24年甘肃 电化学装置设计 学术 固体电解质原电池
24年全国卷 电化学装置应用 学术 原电池控制血糖
24年全国卷 电化学装置设计 学术 MnO2-Zn可充电电池
24年山东卷 电化学装置设计 学术 电解制备H2、O2
24年浙江 电化学装置应用 教材 电化学防腐
24年江苏 电化学装置设计 教材 碱性锌锰干电池
学习目标
1.能分析、解释电解池的工作原理,构建认知模型。
2.掌握常见离子放电顺序,熟练书写电极反应式、总反应式并能进行相关计算,进行思维建模。
3.认识电解在实现物质转化和能量转化中的具体应用,通过模型应用来分析和解决实际问题。
1. 电解池认知模型
装置 外接电源
电极 名称
电子流向
微粒移向 阴阳相吸
电极反应 阳极(氧化反应)
阴极(还原反应)
放电顺序
一、电解池工作原理
回归教材 构建认知模型
CuCl2溶液
S2﹣ >I﹣ >Br﹣>Cl﹣>OH﹣>含氧酸根离子>F﹣
Ag+>Fe3+>Cu2+>H+(酸)>Pb2+>Sn2+>Fe2+>Zn2+
>Al3+>Mg2+>Na+>Ca2+>K+
阴极
阳极
溶液中的微粒得电子
惰性电极
活泼电极
溶液中的微粒失电子
活泼电极自身失电子
放电顺序
典例1.【人教版选修1教材119课后习题改编】锌–空气燃料电池可用作电动车动力电源,两电极材料分别为锌和石墨,电池的电解质溶液为KOH溶液,反应为2Zn+O2+4OH–+2H2O=2[Zn(OH)4]2-。当电池充电时,下列说法正确的是( )
A.电解质溶液中K+向阳极移动
B.电解质溶液中c(OH-) 逐渐减小
C.阴极反应为:[Zn(OH)4]2-+2e–=Zn+4OH–
D.电路中通过2mol电子,生成氧气22.4L(标准状况)
C
(人教2019版选择性必修一第四章第二节电解池课后习题)利用电解法可将含有Fe、Zn、Ag、Pt等杂质的粗铜提纯。下列叙述中正确的是
A.电解时以精铜作阳极
B.电解时阴极上发生的反应为Cu2++2e-=Cu
C.粗铜连接电源的负极,其电极反应为Cu2++2e-=Cu
D.电解后,电解槽底部会形成含有少量Ag、Pt等金属的阳极泥
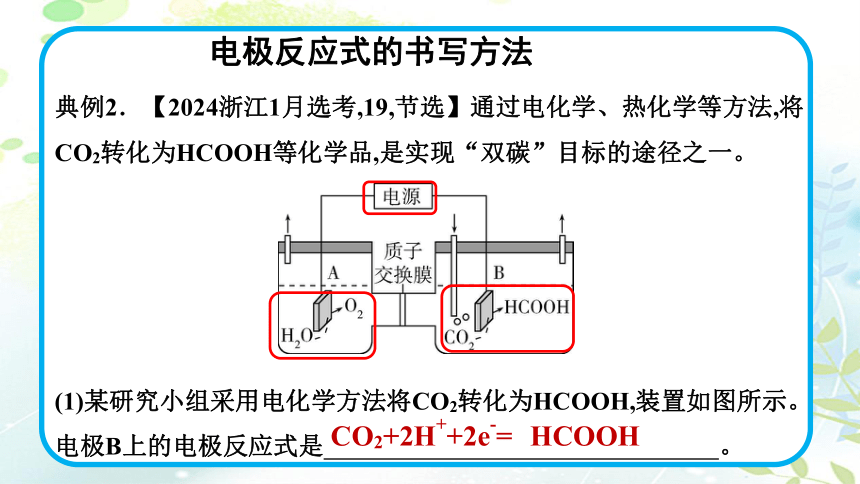
典例2.【2024浙江1月选考,19,节选】通过电化学、热化学等方法,将CO2转化为HCOOH等化学品,是实现“双碳”目标的途径之一。
(1)某研究小组采用电化学方法将CO2转化为HCOOH,装置如图所示。电极B上的电极反应式是 。
电极反应式的书写方法
CO2+2H++2e-=HCOOH
典例3.【2021·湖南 16节选】利用电解原理,将氨转化为高纯氢气,其装置如图所示。
(1)电解过程中OH-的移动方向为__________(填“从左往右”或“从右往左”)。
(2)阳极的电极反应式为_______________________________________。
从右往左
2NH3-6e-+6OH-===N2+6H2O
变式练1【人教版选修1教材109页资料卡片 改编】:制造尼龙-66的原料己二腈[NC(CH2)4CN]用量很大,用电合成法可以先利用丙烯为原料制备丙烯腈[CH2=CHCN],再用丙烯腈电合成己二腈,已知电合成己二腈的总反应如下:4CH2=CHCN+2H2O=2NC(CH2)4CN+O2,
写出电合成己二腈时的阴极反应式: 。
2CH2=CHCN+2H++2e-=NC(CH2)4CN
2CH2=CHCN+2H++2e-=NC(CH2)4CN
人教版选修一教材109页
与其他有机合成相比,电有机合成具有反应条件温和、反应试剂纯净和生产效率高等优点。
二、电解原理应用
1.电解饱和食盐水(氯碱工业)
①电极反应?总反应?
②进出口物质分析?
③离子交换膜的类型?作用?
回归教材 电解模型应用
2.电解精炼
粗铜
精铜
(含Zn、Fe、Ni、Ag、Au等杂质)
CuSO4溶液
当电路中通过电流时,
①在两电极上的电极反应式分别是什么?
②依据得失电子守恒,溶液中的铜离子浓度有何变化?
回归教材 电解模型应用
3.电镀
阳极反应:Cu-2e-==Cu2+(进入溶液)
阴极反应:Cu2++2e-==Cu(在镀件上沉积)
①根据左图分别写出两电极反应
②待镀金属制品 一般作 极?
③镀层金属 一般为作 极?
④若待镀制品为塑料制品呢?
回归教材 电解模型应用
3.电镀
回归教材 电解模型应用
苏教版选修一教材27页
4.电冶金
阴极环绕在阳极外面,两极之间用隔膜隔开。
在阴极区得到液态钠,在阳极区得到氯气。
隔膜选择 离子交换膜?
回归教材 电解模型应用
人教版选修一教材108页
典例4.【2023·浙江卷13 改编】 氯碱工业能耗大,通过如图改进的设计可大幅度降低能耗。下列说法不正确的是( )
A.电极A接电源正极,发生氧化反应
B.电极B的电极反应式为:
2H2O+2e-===H2↑+2OH-
C.应选用阳离子交换膜,在右室
获得浓度较高的NaOH溶液
D.电极A的电极电势比电极B的高
E. 改进设计中通过提高电极B上反应物的氧化性降低电解电压,减少能耗
B
链接高考 构建解题模型
B
典例5.【2022·广东卷10改编】以熔融盐为电解液,以含Cu、Mg和Si等的铝合金废料为阳极进行电解,实现Al的再生。该过程中( )
A.阴极发生的反应为Cu-2e-=Cu2+
B.阳极上Al被氧化
C.在电解槽底部产生含Mg的阳极泥
D.阳极和阴极的质量变化相等
链接高考 构建解题模型
典例6.【2024·黑吉辽卷 13 改编】“绿色零碳”氢能前景广阔。为解决传统电解水制“绿氢”阳极电势高、反应速率缓慢的问题,科技工作者设计耦合HCHO高效制H2的方法,装置如图所示。部分反应机理为:
下列说法错误的是( )
A. 阴极反应:2H2O+2e- =2 OH-+ H2↑
B. 电解时OH- 通过阴离子交换膜向b极方向移动
C. 阳极反应: 2HCHO-2e-+4OH-=2HCOO-+2H2O + H2↑
D. 当电路中通过2mol电子时,H2理论产量为22.4L(标况下)
E. 电解时阳极区溶液的pH减小
D
链接高考 构建解题模型
装置
电极
电极反应式
微粒移向、隔膜
定量计算
反应类型;电子流向;离子迁移等
写物质;明得失;配补项;查守恒
电荷守恒;隔膜-生产目标
电路中转移电子数相等
有无外接电源;放电或充电
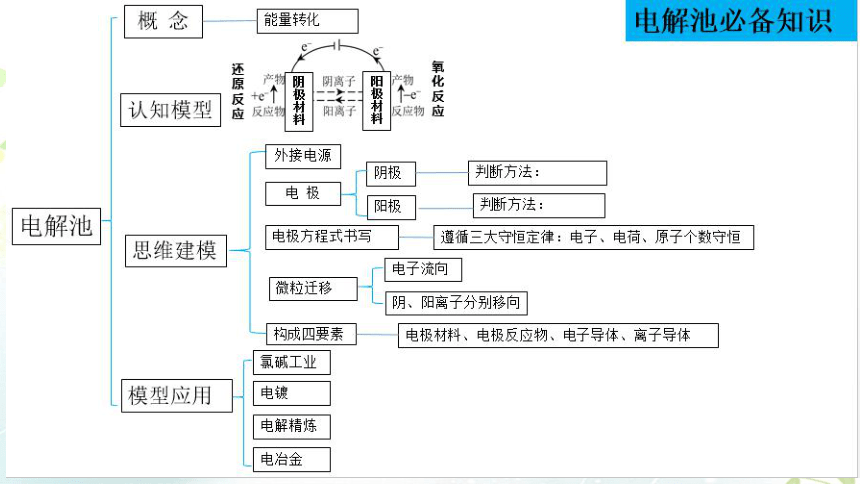
电解池
概 念
认知模型
思维建模
阳极
电 极
阴极
电极方程式书写
能量转化
微粒迁移
模型应用
判断方法:
判断方法:
遵循三大守恒定律:电子、电荷、原子个数守恒
阴、阳离子分别移向
电子流向
阳极材料
氧化
反应
还原
反应
阴极材料
外接电源
氯碱工业
电镀
电冶金
电解精炼
构成四要素
电极材料、电极反应物、电子导体、离子导体
电解池必备知识
2022级高三化学一轮复习
第16讲 电解池工作原理及应用
(1)电极名称判断
(2)电极反应式的书写
(3)微粒的迁移方向
(4)定量计算
(5)电解液的物质变化
核心考点
年份 2024 2023 2022 2021 2020
题号 13题 18题(2)(5) 13题 17题(4) 5题D
13题
考查内容 (1)电极名称判断 (2)电极反应式的书写 (5)电解液的物质变化 (2)电极反应式的书写 (4)计算 (5)电解液的物质变化 (3)微粒的迁移方向 (5)电解液的物质变化 (3)微粒的迁移方向
(4)计算
(5)电解液的物质变化
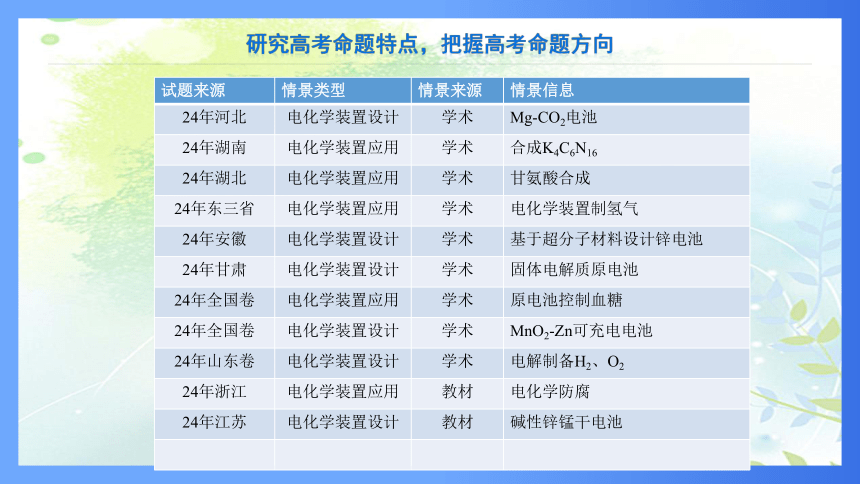
研究高考命题特点,把握高考命题方向
试题来源 情景类型 情景来源 情景信息
24年河北 电化学装置设计 学术 Mg-CO2电池
24年湖南 电化学装置应用 学术 合成K4C6N16
24年湖北 电化学装置应用 学术 甘氨酸合成
24年东三省 电化学装置应用 学术 电化学装置制氢气
24年安徽 电化学装置设计 学术 基于超分子材料设计锌电池
24年甘肃 电化学装置设计 学术 固体电解质原电池
24年全国卷 电化学装置应用 学术 原电池控制血糖
24年全国卷 电化学装置设计 学术 MnO2-Zn可充电电池
24年山东卷 电化学装置设计 学术 电解制备H2、O2
24年浙江 电化学装置应用 教材 电化学防腐
24年江苏 电化学装置设计 教材 碱性锌锰干电池
学习目标
1.能分析、解释电解池的工作原理,构建认知模型。
2.掌握常见离子放电顺序,熟练书写电极反应式、总反应式并能进行相关计算,进行思维建模。
3.认识电解在实现物质转化和能量转化中的具体应用,通过模型应用来分析和解决实际问题。
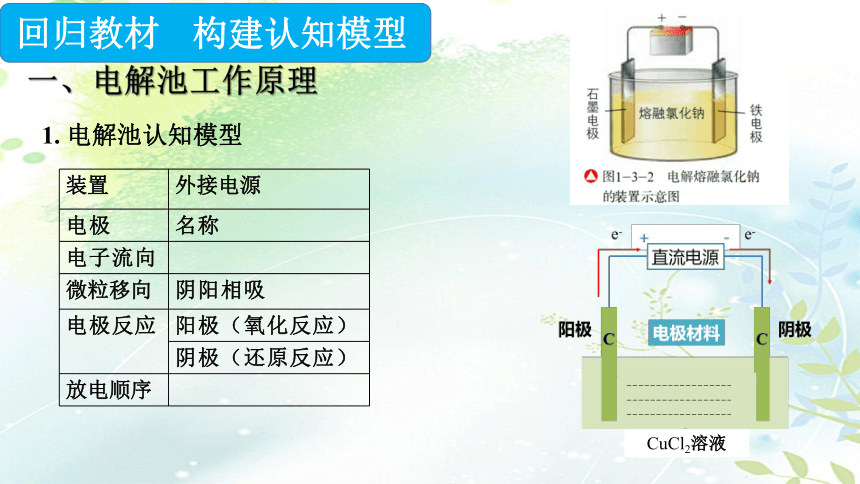
1. 电解池认知模型
装置 外接电源
电极 名称
电子流向
微粒移向 阴阳相吸
电极反应 阳极(氧化反应)
阴极(还原反应)
放电顺序
一、电解池工作原理
回归教材 构建认知模型
CuCl2溶液
S2﹣ >I﹣ >Br﹣>Cl﹣>OH﹣>含氧酸根离子>F﹣
Ag+>Fe3+>Cu2+>H+(酸)>Pb2+>Sn2+>Fe2+>Zn2+
>Al3+>Mg2+>Na+>Ca2+>K+
阴极
阳极
溶液中的微粒得电子
惰性电极
活泼电极
溶液中的微粒失电子
活泼电极自身失电子
放电顺序
典例1.【人教版选修1教材119课后习题改编】锌–空气燃料电池可用作电动车动力电源,两电极材料分别为锌和石墨,电池的电解质溶液为KOH溶液,反应为2Zn+O2+4OH–+2H2O=2[Zn(OH)4]2-。当电池充电时,下列说法正确的是( )
A.电解质溶液中K+向阳极移动
B.电解质溶液中c(OH-) 逐渐减小
C.阴极反应为:[Zn(OH)4]2-+2e–=Zn+4OH–
D.电路中通过2mol电子,生成氧气22.4L(标准状况)
C
(人教2019版选择性必修一第四章第二节电解池课后习题)利用电解法可将含有Fe、Zn、Ag、Pt等杂质的粗铜提纯。下列叙述中正确的是
A.电解时以精铜作阳极
B.电解时阴极上发生的反应为Cu2++2e-=Cu
C.粗铜连接电源的负极,其电极反应为Cu2++2e-=Cu
D.电解后,电解槽底部会形成含有少量Ag、Pt等金属的阳极泥
典例2.【2024浙江1月选考,19,节选】通过电化学、热化学等方法,将CO2转化为HCOOH等化学品,是实现“双碳”目标的途径之一。
(1)某研究小组采用电化学方法将CO2转化为HCOOH,装置如图所示。电极B上的电极反应式是 。
电极反应式的书写方法
CO2+2H++2e-=HCOOH
典例3.【2021·湖南 16节选】利用电解原理,将氨转化为高纯氢气,其装置如图所示。
(1)电解过程中OH-的移动方向为__________(填“从左往右”或“从右往左”)。
(2)阳极的电极反应式为_______________________________________。
从右往左
2NH3-6e-+6OH-===N2+6H2O
变式练1【人教版选修1教材109页资料卡片 改编】:制造尼龙-66的原料己二腈[NC(CH2)4CN]用量很大,用电合成法可以先利用丙烯为原料制备丙烯腈[CH2=CHCN],再用丙烯腈电合成己二腈,已知电合成己二腈的总反应如下:4CH2=CHCN+2H2O=2NC(CH2)4CN+O2,
写出电合成己二腈时的阴极反应式: 。
2CH2=CHCN+2H++2e-=NC(CH2)4CN
2CH2=CHCN+2H++2e-=NC(CH2)4CN
人教版选修一教材109页
与其他有机合成相比,电有机合成具有反应条件温和、反应试剂纯净和生产效率高等优点。
二、电解原理应用
1.电解饱和食盐水(氯碱工业)
①电极反应?总反应?
②进出口物质分析?
③离子交换膜的类型?作用?
回归教材 电解模型应用
2.电解精炼
粗铜
精铜
(含Zn、Fe、Ni、Ag、Au等杂质)
CuSO4溶液
当电路中通过电流时,
①在两电极上的电极反应式分别是什么?
②依据得失电子守恒,溶液中的铜离子浓度有何变化?
回归教材 电解模型应用
3.电镀
阳极反应:Cu-2e-==Cu2+(进入溶液)
阴极反应:Cu2++2e-==Cu(在镀件上沉积)
①根据左图分别写出两电极反应
②待镀金属制品 一般作 极?
③镀层金属 一般为作 极?
④若待镀制品为塑料制品呢?
回归教材 电解模型应用
3.电镀
回归教材 电解模型应用
苏教版选修一教材27页
4.电冶金
阴极环绕在阳极外面,两极之间用隔膜隔开。
在阴极区得到液态钠,在阳极区得到氯气。
隔膜选择 离子交换膜?
回归教材 电解模型应用
人教版选修一教材108页
典例4.【2023·浙江卷13 改编】 氯碱工业能耗大,通过如图改进的设计可大幅度降低能耗。下列说法不正确的是( )
A.电极A接电源正极,发生氧化反应
B.电极B的电极反应式为:
2H2O+2e-===H2↑+2OH-
C.应选用阳离子交换膜,在右室
获得浓度较高的NaOH溶液
D.电极A的电极电势比电极B的高
E. 改进设计中通过提高电极B上反应物的氧化性降低电解电压,减少能耗
B
链接高考 构建解题模型
B
典例5.【2022·广东卷10改编】以熔融盐为电解液,以含Cu、Mg和Si等的铝合金废料为阳极进行电解,实现Al的再生。该过程中( )
A.阴极发生的反应为Cu-2e-=Cu2+
B.阳极上Al被氧化
C.在电解槽底部产生含Mg的阳极泥
D.阳极和阴极的质量变化相等
链接高考 构建解题模型
典例6.【2024·黑吉辽卷 13 改编】“绿色零碳”氢能前景广阔。为解决传统电解水制“绿氢”阳极电势高、反应速率缓慢的问题,科技工作者设计耦合HCHO高效制H2的方法,装置如图所示。部分反应机理为:
下列说法错误的是( )
A. 阴极反应:2H2O+2e- =2 OH-+ H2↑
B. 电解时OH- 通过阴离子交换膜向b极方向移动
C. 阳极反应: 2HCHO-2e-+4OH-=2HCOO-+2H2O + H2↑
D. 当电路中通过2mol电子时,H2理论产量为22.4L(标况下)
E. 电解时阳极区溶液的pH减小
D
链接高考 构建解题模型
装置
电极
电极反应式
微粒移向、隔膜
定量计算
反应类型;电子流向;离子迁移等
写物质;明得失;配补项;查守恒
电荷守恒;隔膜-生产目标
电路中转移电子数相等
有无外接电源;放电或充电
电解池
概 念
认知模型
思维建模
阳极
电 极
阴极
电极方程式书写
能量转化
微粒迁移
模型应用
判断方法:
判断方法:
遵循三大守恒定律:电子、电荷、原子个数守恒
阴、阳离子分别移向
电子流向
阳极材料
氧化
反应
还原
反应
阴极材料
外接电源
氯碱工业
电镀
电冶金
电解精炼
构成四要素
电极材料、电极反应物、电子导体、离子导体
电解池必备知识
同课章节目录
