2025年九年级中考化学一轮专题复习 工艺流程(共27张PPT)
文档属性
| 名称 | 2025年九年级中考化学一轮专题复习 工艺流程(共27张PPT) |

|
|
| 格式 | pptx | ||
| 文件大小 | 1.7MB | ||
| 资源类型 | 教案 | ||
| 版本资源 | 通用版 | ||
| 科目 | 化学 | ||
| 更新时间 | 2025-02-17 00:00:00 | ||
图片预览





文档简介
(共27张PPT)
工艺流程
类型 1 框图流程
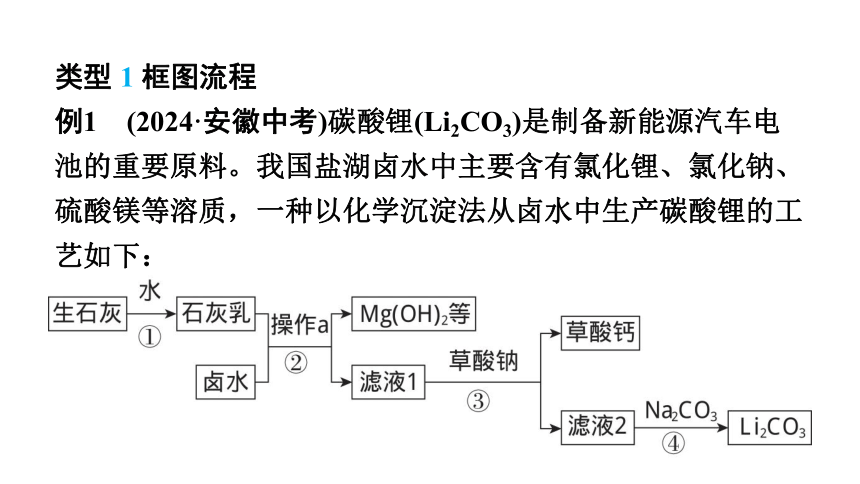
例1 (2024·安徽中考)碳酸锂(Li2CO3)是制备新能源汽车电池的重要原料。我国盐湖卤水中主要含有氯化锂、氯化钠、硫酸镁等溶质,一种以化学沉淀法从卤水中生产碳酸锂的工艺如下:
回答下列问题:
(1)步骤①发生反应的化学方程式为
。
(2)步骤②操作a的名称是 。
(3)步骤③中加入草酸钠,其中草酸根(C2)的化合价是-2价,则草酸钠的化学式为 。
(4)滤液2中含有LiCl,步骤④中生成Li2CO3的反应类型是
。
(5)该工艺中用到的氧化物有 (写1种即可)。
CaO(或H2O)
复分解反应
Na2C2O4
过滤
CaO+H2O===Ca(OH)2
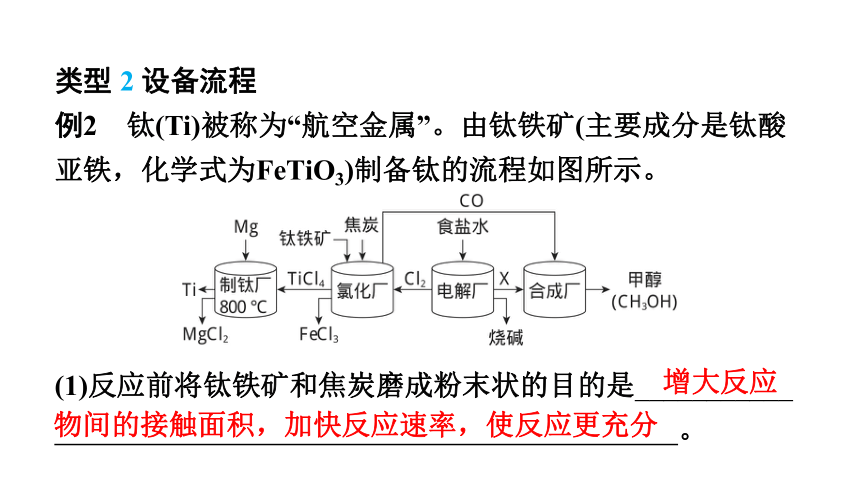
(1)反应前将钛铁矿和焦炭磨成粉末状的目的是___________
。
物间的接触面积,加快反应速率,使反应更充分
类型 2 设备流程
例2 钛(Ti)被称为“航空金属”。由钛铁矿(主要成分是钛酸亚铁,化学式为FeTiO3)制备钛的流程如图所示。
增大反应
(2)制钛厂中发生反应的化学方程式为
,该反应属于____________
(填基本反应类型);通过以上反应说明Mg与Ti的金属活动性强弱关系为Mg Ti(填“<”“>”或“=”)。
(3)电解厂中电解食盐水除生成烧碱和Cl2外,还生成气体X,则X的化学式为 。
(4)该流程将制钛厂、氯化厂、电解厂和合成厂组成产业链的优点是 (写出1点即可)。
TiCl4+2Mg2MgCl2+Ti
提高资源利用率,减少污染(合理即可)
H2
>
置换反应
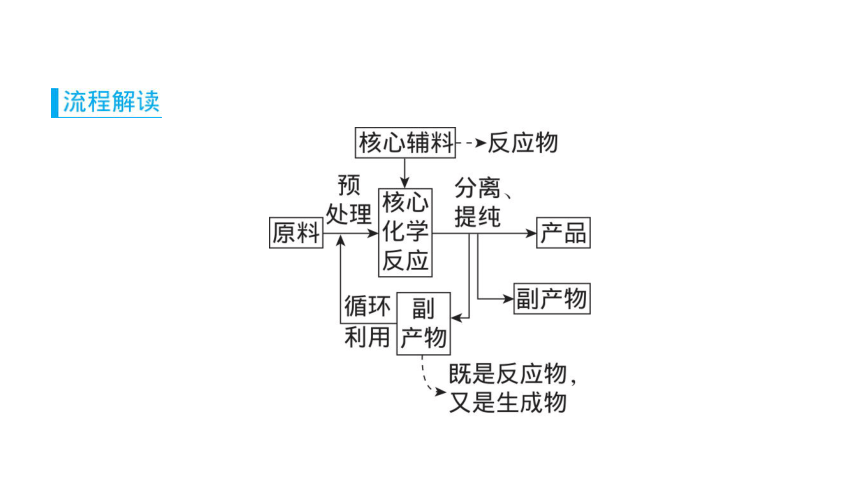
(1)原料预处理的方法及目的
①粉碎(研磨):增大反应物间的接触面积,加快反应速率,使反应更充分。
②灼烧(煅烧、焙烧):使固体在高温下氧化、分解;除去可燃性杂质等。
③酸浸:溶解金属、金属氧化物、难溶性碱或碳酸盐等。
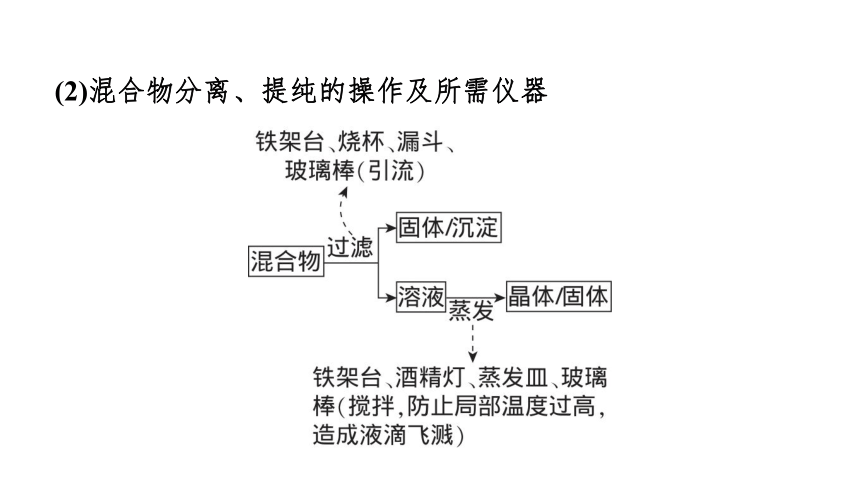
(2)混合物分离、提纯的操作及所需仪器
(3)陌生化学方程式的书写
根据箭头方向,箭头进去的是反应物,出去的是生成物。
(4)流程的作用及评价
①成本角度:原料价格低、易得;耗能少等。
②节约与环保角度:废物再利用;无污染或污染小等。
(1)步骤①发生反应的化学方程式是
。
针对训练
1.(2023·安徽中考)活性氧化铜用于印刷电路板制造,由普通氧化铜制备活性氧化铜的工艺流程如下。回答下列问题:
CuO+2HCl===CuCl2+H2O
(2)下列说法正确的是 (填字母序号)。
A.过滤时用玻璃棒在漏斗中不断搅拌
B.步骤②溶液中的水参加了反应
C.Cu2(OH)2CO3易溶于水
D.Na2CO3的俗名是纯碱
(3)步骤②Na2CO3溶液加入时有气泡产生,原因是_________
。
(4)步骤③发生反应的反应类型是 。
分解反应
与CuCl2溶液中过量的盐酸反应生成CO2(合理即可)
Na2CO3
BD
(1)二氧化硅属于 (填“单质”或“化合物”)。
2.(2024·武汉中考)硫酸钡是白色固体,医疗上常用作透视肠胃的内服剂。以毒重石(主要成分是碳酸钡,还含少量氧化铁和二氧化硅)为原料生产硫酸钡的工艺流程如图所示。
化合物
(2)上述流程中涉及过滤,实验室进行该操作时用到的玻璃仪器有 。
(3)“除铁”时发生反应的化学方程式为___________________
(写出1个即可)。
(4)可溶性钡盐和碳酸钡均有毒,而硫酸钡无毒,说明硫酸钡具有的性质是 。
难溶于水,且不和盐酸反应
Fe(OH)3↓+3NaCl(或NaOH+HCl===NaCl+H2O)
3NaOH+FeCl3===
烧杯、漏斗和玻璃棒
(5)为变废为宝,将“滤液”转化为氯化钠溶液的方法是
____________________________________________________
(简述试剂、用量及操作)。
过滤(合理即可)
向滤液中加入适量氯化钡和稀盐酸的混合液,充分反应后
3.(2024·合肥瑶海区一模)硫化氢(H2S)气体有剧毒,且易燃、易爆,不能直接排放。我国回收硫化氢气体的方法主要是生产硫酸(H2SO4)。其主要生产流程如下:
(1)H2S中硫元素的化合价为 。
(2)在高温条件下,转化器中发生反应的化学方程式为
,该反应属于 (填基
本反应类型)。
(3)冷凝器上方的浓硫酸(浓度小)以雾状喷出,其目的是
。
(4)实验室稀释浓硫酸的操作是_________________________
。
2SO2+O22SO3
水中,并用玻璃棒不断搅拌
将浓硫酸沿器壁慢慢注入
增大反应物间的接触面积,使其充分反应
化合反应
-2
(1)写出生成气体A的化学方程式:
。
4.某金属废料中含有铜、铁、金等金属单质,为回收铜和金并得到氧化铁,专业人员设计了如图所示的工艺流程。
Fe+H2SO4===FeSO4+H2↑
(2)固体A在空气中灼烧后再与稀硫酸进行反应,固体A在空气中灼烧的目的是 。
(3)实验室进行操作2后,得到的滤液B仍浑浊的原因可能是
____________________________________________________ (写出1点即可)。
(4)流程中加入的物质X为 。
(5)该工艺流程的价值是 。
废物再利用,节约资源(合理即可)
铁
液面高于滤纸边缘(或承接滤液的烧杯不干净,合理即可)
使铜和氧气在加热条件下反应生成氧化铜
5. (2024·成都中考)皮蛋是成渝等地人们喜爱的食品,制作流程如图。
资料:①草木灰(含K2CO3)中常含有砂石和未燃尽的秸秆等固体。
②碱可与蛋白质作用,使其凝固。
(1)选料:“过筛”的目的是_____________________________
。
(2)调浆:调浆过程发生复分解反应的化学方程式为
____________________________________________________
(写出1个即可),料浆浸出液中一定含有的阴离子有 (填离子符号)。
OH-和Cl-
===CaCO3↓+2KOH]
Na2CO3+Ca(OH)2===CaCO3↓+2NaOH[或K2CO3+Ca(OH)2
粒较大的固体
除去砂石和未燃尽的秸秆等颗
(3)裹泥:裹泥时,皮肤不慎接触料浆,处理方法为_______
。
(4)封存:需要“密封”的主要原因是减少水分蒸发和_______
。
空气中CO2与皮蛋表面的碱反应,避免皮蛋制作失败
减少
量清水冲洗,再涂上质量分数为1%的硼酸溶液
用大
6.(2024·巴中中考改编)海洋是一个巨大的资源宝库。广泛应用于火箭、导弹和飞机制造业的金属镁,就是利用从海水中提取的镁盐制取的。如图是模拟从海水中制取镁的简易流程。
(1)步骤①得到的母液是氯化钠的 (填“饱和”或“不饱和”)溶液。
(2)蒸发过程中,玻璃棒的作用是_______________________
。
(3)步骤②中加入氢氧化钠溶液需过量的目的是___________
。
(4)写出步骤③发生反应的化学方程式:
。
Mg(OH)2+2HCl===MgCl2+2H2O
全转化为Mg(OH)2沉淀
将MgCl2完
过高,造成液滴飞溅
搅拌,防止因局部温度
饱和
已知:NH3极易溶于水,形成的水溶液显碱性。
(1)沉淀池中先通入NH3再通入CO2,你认为原因是________
。
易溶于水形成碱性溶液,更有利于吸收CO2
7.某工厂利用氨气、二氧化碳和硫酸钙悬浊液制备硫酸铵的部分工艺流程如图所示。
NH3极
(2)煅烧炉中发生的主要反应的化学方程式为
。
(3)该流程中可循环利用的物质是 。
(4)写出硫酸铵在农业生产中的一种用途: 。
CaCO3CaO+CO2↑
作氮肥(合理即可)
CO2
(1)X常用作食品干燥剂,其化学式为 。
8.(2024·济宁中考)某化学兴趣小组模拟工厂苛化法制备烧碱的流程如下。
CaO
(2)写出反应池中发生反应的化学方程式:
。
(3)实验室中将滤液A盛装在 (填仪器名称)中完成操作2。
(4)滤液B可加入反应池中循环利用,目的是______________
。
少污染
降低成本,减
蒸发皿
Ca(OH)2+Na2CO3===CaCO3↓+2NaOH
工艺流程
类型 1 框图流程
例1 (2024·安徽中考)碳酸锂(Li2CO3)是制备新能源汽车电池的重要原料。我国盐湖卤水中主要含有氯化锂、氯化钠、硫酸镁等溶质,一种以化学沉淀法从卤水中生产碳酸锂的工艺如下:
回答下列问题:
(1)步骤①发生反应的化学方程式为
。
(2)步骤②操作a的名称是 。
(3)步骤③中加入草酸钠,其中草酸根(C2)的化合价是-2价,则草酸钠的化学式为 。
(4)滤液2中含有LiCl,步骤④中生成Li2CO3的反应类型是
。
(5)该工艺中用到的氧化物有 (写1种即可)。
CaO(或H2O)
复分解反应
Na2C2O4
过滤
CaO+H2O===Ca(OH)2
(1)反应前将钛铁矿和焦炭磨成粉末状的目的是___________
。
物间的接触面积,加快反应速率,使反应更充分
类型 2 设备流程
例2 钛(Ti)被称为“航空金属”。由钛铁矿(主要成分是钛酸亚铁,化学式为FeTiO3)制备钛的流程如图所示。
增大反应
(2)制钛厂中发生反应的化学方程式为
,该反应属于____________
(填基本反应类型);通过以上反应说明Mg与Ti的金属活动性强弱关系为Mg Ti(填“<”“>”或“=”)。
(3)电解厂中电解食盐水除生成烧碱和Cl2外,还生成气体X,则X的化学式为 。
(4)该流程将制钛厂、氯化厂、电解厂和合成厂组成产业链的优点是 (写出1点即可)。
TiCl4+2Mg2MgCl2+Ti
提高资源利用率,减少污染(合理即可)
H2
>
置换反应
(1)原料预处理的方法及目的
①粉碎(研磨):增大反应物间的接触面积,加快反应速率,使反应更充分。
②灼烧(煅烧、焙烧):使固体在高温下氧化、分解;除去可燃性杂质等。
③酸浸:溶解金属、金属氧化物、难溶性碱或碳酸盐等。
(2)混合物分离、提纯的操作及所需仪器
(3)陌生化学方程式的书写
根据箭头方向,箭头进去的是反应物,出去的是生成物。
(4)流程的作用及评价
①成本角度:原料价格低、易得;耗能少等。
②节约与环保角度:废物再利用;无污染或污染小等。
(1)步骤①发生反应的化学方程式是
。
针对训练
1.(2023·安徽中考)活性氧化铜用于印刷电路板制造,由普通氧化铜制备活性氧化铜的工艺流程如下。回答下列问题:
CuO+2HCl===CuCl2+H2O
(2)下列说法正确的是 (填字母序号)。
A.过滤时用玻璃棒在漏斗中不断搅拌
B.步骤②溶液中的水参加了反应
C.Cu2(OH)2CO3易溶于水
D.Na2CO3的俗名是纯碱
(3)步骤②Na2CO3溶液加入时有气泡产生,原因是_________
。
(4)步骤③发生反应的反应类型是 。
分解反应
与CuCl2溶液中过量的盐酸反应生成CO2(合理即可)
Na2CO3
BD
(1)二氧化硅属于 (填“单质”或“化合物”)。
2.(2024·武汉中考)硫酸钡是白色固体,医疗上常用作透视肠胃的内服剂。以毒重石(主要成分是碳酸钡,还含少量氧化铁和二氧化硅)为原料生产硫酸钡的工艺流程如图所示。
化合物
(2)上述流程中涉及过滤,实验室进行该操作时用到的玻璃仪器有 。
(3)“除铁”时发生反应的化学方程式为___________________
(写出1个即可)。
(4)可溶性钡盐和碳酸钡均有毒,而硫酸钡无毒,说明硫酸钡具有的性质是 。
难溶于水,且不和盐酸反应
Fe(OH)3↓+3NaCl(或NaOH+HCl===NaCl+H2O)
3NaOH+FeCl3===
烧杯、漏斗和玻璃棒
(5)为变废为宝,将“滤液”转化为氯化钠溶液的方法是
____________________________________________________
(简述试剂、用量及操作)。
过滤(合理即可)
向滤液中加入适量氯化钡和稀盐酸的混合液,充分反应后
3.(2024·合肥瑶海区一模)硫化氢(H2S)气体有剧毒,且易燃、易爆,不能直接排放。我国回收硫化氢气体的方法主要是生产硫酸(H2SO4)。其主要生产流程如下:
(1)H2S中硫元素的化合价为 。
(2)在高温条件下,转化器中发生反应的化学方程式为
,该反应属于 (填基
本反应类型)。
(3)冷凝器上方的浓硫酸(浓度小)以雾状喷出,其目的是
。
(4)实验室稀释浓硫酸的操作是_________________________
。
2SO2+O22SO3
水中,并用玻璃棒不断搅拌
将浓硫酸沿器壁慢慢注入
增大反应物间的接触面积,使其充分反应
化合反应
-2
(1)写出生成气体A的化学方程式:
。
4.某金属废料中含有铜、铁、金等金属单质,为回收铜和金并得到氧化铁,专业人员设计了如图所示的工艺流程。
Fe+H2SO4===FeSO4+H2↑
(2)固体A在空气中灼烧后再与稀硫酸进行反应,固体A在空气中灼烧的目的是 。
(3)实验室进行操作2后,得到的滤液B仍浑浊的原因可能是
____________________________________________________ (写出1点即可)。
(4)流程中加入的物质X为 。
(5)该工艺流程的价值是 。
废物再利用,节约资源(合理即可)
铁
液面高于滤纸边缘(或承接滤液的烧杯不干净,合理即可)
使铜和氧气在加热条件下反应生成氧化铜
5. (2024·成都中考)皮蛋是成渝等地人们喜爱的食品,制作流程如图。
资料:①草木灰(含K2CO3)中常含有砂石和未燃尽的秸秆等固体。
②碱可与蛋白质作用,使其凝固。
(1)选料:“过筛”的目的是_____________________________
。
(2)调浆:调浆过程发生复分解反应的化学方程式为
____________________________________________________
(写出1个即可),料浆浸出液中一定含有的阴离子有 (填离子符号)。
OH-和Cl-
===CaCO3↓+2KOH]
Na2CO3+Ca(OH)2===CaCO3↓+2NaOH[或K2CO3+Ca(OH)2
粒较大的固体
除去砂石和未燃尽的秸秆等颗
(3)裹泥:裹泥时,皮肤不慎接触料浆,处理方法为_______
。
(4)封存:需要“密封”的主要原因是减少水分蒸发和_______
。
空气中CO2与皮蛋表面的碱反应,避免皮蛋制作失败
减少
量清水冲洗,再涂上质量分数为1%的硼酸溶液
用大
6.(2024·巴中中考改编)海洋是一个巨大的资源宝库。广泛应用于火箭、导弹和飞机制造业的金属镁,就是利用从海水中提取的镁盐制取的。如图是模拟从海水中制取镁的简易流程。
(1)步骤①得到的母液是氯化钠的 (填“饱和”或“不饱和”)溶液。
(2)蒸发过程中,玻璃棒的作用是_______________________
。
(3)步骤②中加入氢氧化钠溶液需过量的目的是___________
。
(4)写出步骤③发生反应的化学方程式:
。
Mg(OH)2+2HCl===MgCl2+2H2O
全转化为Mg(OH)2沉淀
将MgCl2完
过高,造成液滴飞溅
搅拌,防止因局部温度
饱和
已知:NH3极易溶于水,形成的水溶液显碱性。
(1)沉淀池中先通入NH3再通入CO2,你认为原因是________
。
易溶于水形成碱性溶液,更有利于吸收CO2
7.某工厂利用氨气、二氧化碳和硫酸钙悬浊液制备硫酸铵的部分工艺流程如图所示。
NH3极
(2)煅烧炉中发生的主要反应的化学方程式为
。
(3)该流程中可循环利用的物质是 。
(4)写出硫酸铵在农业生产中的一种用途: 。
CaCO3CaO+CO2↑
作氮肥(合理即可)
CO2
(1)X常用作食品干燥剂,其化学式为 。
8.(2024·济宁中考)某化学兴趣小组模拟工厂苛化法制备烧碱的流程如下。
CaO
(2)写出反应池中发生反应的化学方程式:
。
(3)实验室中将滤液A盛装在 (填仪器名称)中完成操作2。
(4)滤液B可加入反应池中循环利用,目的是______________
。
少污染
降低成本,减
蒸发皿
Ca(OH)2+Na2CO3===CaCO3↓+2NaOH
同课章节目录
