广东省汕头市蓝田中学2023-2024 学年九年级下学期化学开学摸底考试(含答案)
文档属性
| 名称 | 广东省汕头市蓝田中学2023-2024 学年九年级下学期化学开学摸底考试(含答案) |

|
|
| 格式 | docx | ||
| 文件大小 | 1010.7KB | ||
| 资源类型 | 教案 | ||
| 版本资源 | 通用版 | ||
| 科目 | 化学 | ||
| 更新时间 | 2025-02-20 00:00:00 | ||
图片预览




文档简介
广东省汕头市蓝田中学2023-2024 学年九年级下学期
化学开学摸底考试
一、选择题:本大题共15小题,每小题3分,共45分。在每小题列出的四个选项中,只有一项是符合题目要求的。
1.化学,是关于物质变化的学问。下列变化中,发生了化学变化的是( )
A.水结成冰 B.燃气燃烧
C.纸剪窗花 D.干冰升华
2.下列有关物质的用途、性质等信息对应不正确的是( )
A.液氢用作火箭升空的燃料——可燃性——化学性质
B.石墨用作电刷——导电性——物理性质
C.活性炭用于净化空气——吸附性——化学性质
D.氮气用作食品保护气——常温时稳定——化学性质
3.下列物质的用途主要取决于其化学性质的是( )
A.用铜制导线 B.用氧气进行医疗急救
C.用氦气充探空气球 D.用生铁铸造铁锅
4.分类是化学学习和研究的重要方法之一,下列分类正确的是( )
A.污染空气气体有:一氧化碳、二氧化硫、二氧化氮
B.纯净物:洁净的空气、高锰酸钾分解后剩余物、冰水混合物
C.可在酒精灯上加热的仪器:试管、烧杯、量筒
D.物理性质包括:溶解性、挥发性、可燃性
5.研发多种用于石油化工生产的催化剂,为我国炼油催化剂制造技术奠定基础的科学家是( )
A.拉瓦锡 B.闵恩泽 C.张青莲 D.道尔顿
6.关注实验安全,规范实验操作。下列做法中,不符合实验操作规范的是( )
A.点燃氢气等可燃性的气体之前,一定要检验其纯度
B.取液后的胶头滴管,应保持橡胶胶帽在上,不要平放
C.给试管里的液体加热,将试管口对着自己,便于观察现象
D.不能用燃着的酒精灯去点燃另一个酒精灯,也不能用嘴吹灭
7.“生命可贵,安全第一”。从安全角度出发,下列做法不合理的是( )
A.加油站、加气站要严禁烟火,但可以拨打电话
B.建筑物内起火,不要急于开窗
C.厨房油锅起火,立即用锅盖盖灭
D.天然气泄漏时,应立即关闭阀门并开窗通风
8.天宫课堂中,航天员王亚平展示了“锆金属熔化与凝固”实验。如下图是锆元素在元素周期表中的信息及原子结构示意图。下列说法不正确的是( )
A.锆原子的中子数为40
B.锆元素的相对原子质量为91.22
C.锆原子在化学变化中容易失去两个电子
D.锆元素位于元素周期表的第五周期
9.近年来一些手机厂商纷纷发布自己的可折叠手机。化学物质吡唑啉是生产折叠手机用到的柔性屏幕的重要物质,其化学式为C3H6N2,下列有关吡唑啉C3H6N2的说法正确的是( )
A.吡唑啉属于有机高分子化合物
B.吡唑啉是由3个碳原子、6个氢原子和2个氮原子构成的
C.吡唑啉中碳元素质量分数最大
D.吡唑啉的化学式量为70g
10.“宏观辨识与微观探析”是化学学科核心素养之一。对下列事实的解释错误的是( )
A.氧气能被液化储存于钢瓶中——分子之间有间隔且间隔能改变
B.众人拾柴火焰高——可燃物越多,着火点越低,越易燃烧
C.化学反应前后各物质的质量总和不变——化学反应前后原子的种类、数目、质量均不改变
D.铁丝在空气中不燃烧,在氧气中剧烈燃烧——单位体积内氧分子数目决定反应的剧烈程度
11.下表中概念间不符合图所示的从属关系的是( )
选项 X Y Z
A 非金属单质 单质 纯净物
B 氧化反应 化合反应 化学反应
C 饱和溶液 溶液 混合物
D 氧化物 无机化合物 化合物
A.A B.B C.C D.D
12.“光解制氢”可实现水的高效分解,其反应示意图如图,下列说法正确的是( )
A.该反应的反应物分子不可分
B.反应前后原子种类不发生改变
C.a、b的组成元素相同,化学性质相同
D.在化学变化中,原子可以再分
13.下列实验方案和对应的化学方程式,均完全正确的是 ( )
选项 实验目的 实验方案 化学方程式
比较与金属活动性强弱 在溶液中放入铁片,观察现象
检验气体 把气体通入溶液中,观察现象
除去溶液中少量的 滴加适量的溶液,过滤
除去中少量的 高温煅烧至固体质量不再减少
A. B. C. D.
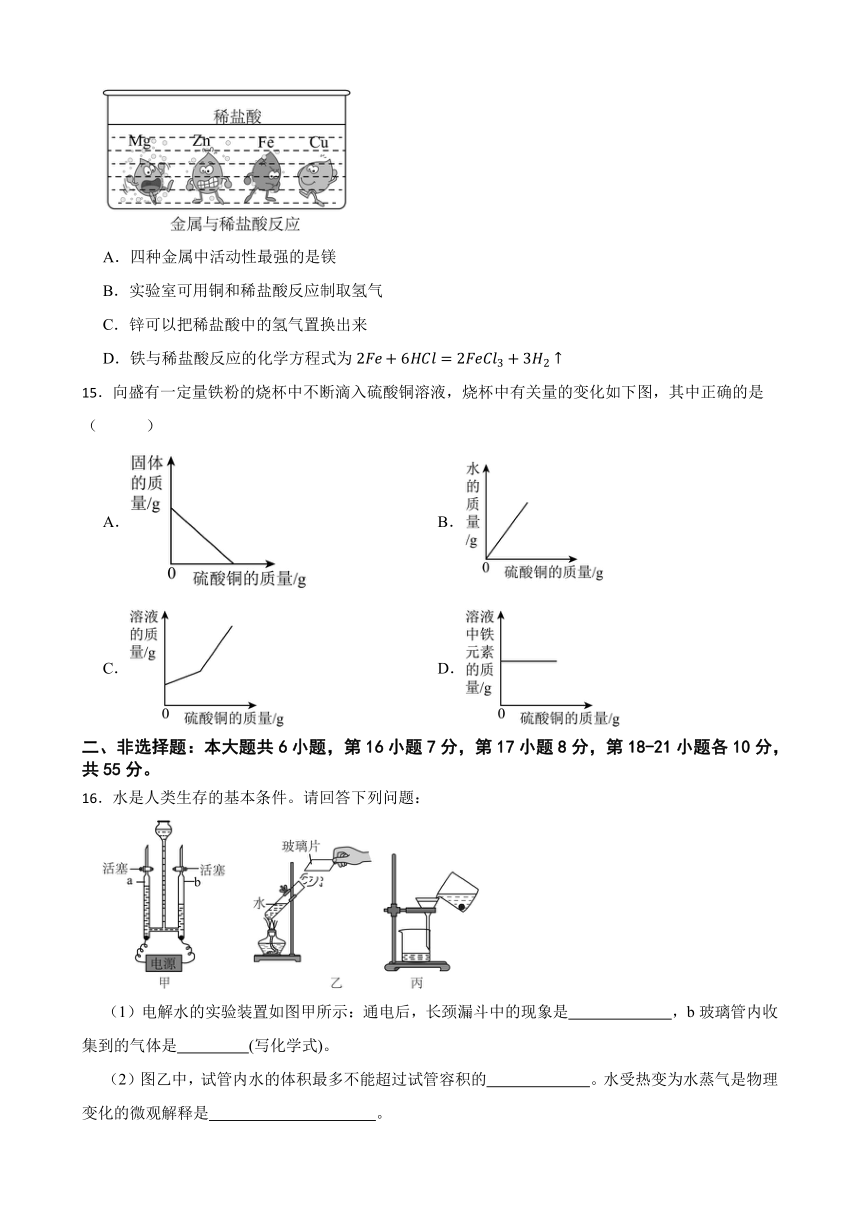
14.常见金属与稀盐酸反应的示意图如图所示,下列说法正确的是( )
A.四种金属中活动性最强的是镁
B.实验室可用铜和稀盐酸反应制取氢气
C.锌可以把稀盐酸中的氢气置换出来
D.铁与稀盐酸反应的化学方程式为
15.向盛有一定量铁粉的烧杯中不断滴入硫酸铜溶液,烧杯中有关量的变化如下图,其中正确的是( )
A. B.
C. D.
二、非选择题:本大题共6小题,第16小题7分,第17小题8分,第18-21小题各10分,共55分。
16.水是人类生存的基本条件。请回答下列问题:
(1)电解水的实验装置如图甲所示:通电后,长颈漏斗中的现象是 ,b玻璃管内收集到的气体是 (写化学式)。
(2)图乙中,试管内水的体积最多不能超过试管容积的 。水受热变为水蒸气是物理变化的微观解释是 。
(3)图丙中缺少的一种玻璃仪器是 ,它的作用是 。生活中常用的对自来水进行消毒并可以降低水的硬度的方法是 。
17.北京冬奥,科技助梦,化学在其中扮演着重要角色。从化学视角回答下列问题:
(1)国产氢氧燃料电池豪华中巴在冬奥会投入使用。氢气在氧气中燃烧反应的化学方程式为 ,氢气作燃料能实现“零排放”的原因是 。
(2)“冰丝带”速滑馆采用单层双向正交马鞍形索网屋面,将用钢量降到传统屋面的1/4,大幅减少了冶炼钢铁产生的碳排放。
①“冰丝带”速滑馆所用钢属于 材料,与纯铁比较具有 等优点;
②工业炼铁的原理是CO在高温下还原赤铁矿,其化学方程式为 。
(3)冬奥会纪念钞是我国第一枚拥有完全自主知识产权的聚丙烯塑料钞。聚丙烯化学式可表示为(C3H6)n ,它属于 材料,其中碳、氢元素的质量比为 。
(4)冬奥会礼仪服“瑞雪祥云”采用了高科技石墨烯发热材料,在-30 ℃也能御寒。石墨烯是单层石墨片,下列有关石墨烯的说法正确的是________(填序号)。
A.属于化合物 B.与金刚石的硬度相近
C.导热性能好 D.室温下能够稳定存在
18.通过这段时间的学习,你已经掌握了实验室制取气体的一些知识,请你结合如图装置图回答问题:(友情提示:所选装置均填序号)
(1)写出指定仪器名称:① ,② 。
(2)实验室制取和收集CO2气体时应选用 两装置相连接,检验集气瓶中CO2是否收集满的方法是: 。
(3)实验室用KMnO4制取O2时,用排水法收集O2完毕后,停止实验时的操作顺序是 。
(4)已知氨气(NH3)是一种无色、有刺激性气味的气体,密度比空气小,极易溶于水.实验室常用加热氯化铵和熟石灰的固体混合物来制取氨气.其发生装置是 ,收集装置是 。
19.“新冠”疫情牵动人心。我校安全复课措施之一是餐桌放置“pp”隔离板。“近云”学习小组的同学对“pp”板的组成进行了探究,实验装置如下图。
查阅资料:
①碱石灰为NaOH和CaO固体的混合物;
②“pp”板可能含有C、H、O中的两种或三种元素。
③Na2CO3溶液能与BaCl2溶液反应产生白色沉淀。
(1)装置B中浓硫酸的作用 。
(2)写出装置E中反应的方程式 。
(3)要确定“pp”板的元素组成,取2.1g“pp”板样品在装置C中完全反应,还需测定反应前后另外两个装置质量的增加量,这两个装置是 (填装置序号)。
(4)装置F的作用是 。
(5)充分反应后,还要继续通一段时间的氧气,目的是 。
(6)该实验需保证吸收试剂稍过量,为判断E中NaOH溶液是否过量,实验结束后进行了以下探究,对实验后E中溶液的溶质作出猜想:猜想①:NaOH;猜想②:Na2CO3;猜想③: 。
甲同学取少量液体进行实验:
实验操作 现象 结论
加入足量BaCl2溶液 猜想③正确
滴加少量酚酞溶液
结论:实验时E中NaOH溶液一定过量。
(7)若试验中测得生成的二氧化碳质量为6.6g,生成的水的质量为2.7g,则该“pp”板中含有的元素种类为 。
20.氢能的开发是当前研究的热点。
(1)电解水制氢需消耗电能。煤炭、风能均可发电,其中属于绿色能源的是 。
(2)图-1是某种太阳能热循环制备氢气的原理。
①写出生成H2的化学方程式 。
②该制氢方法的优点是 。
(3)图-2为一种天然气(主要成分为CH4)为原料,制备高纯H2的流程。
①天然气是 (“可再生”或“不可再生”)能源。“反应器”中,高温催化分解天然气可生成C和H2,该反应的化学方程式为 。
②流程中可回收利用的物质是 (填化学式)。
③反应过程中,催化剂表面若堆积较多的炭黑,则会形成“积炭”而降低反应速率,其本质原因是 ;为消除“积炭”,可在高温下,将“积炭”的催化剂置于CO2气流中,即可消除积炭。该反应的化学方程式为 ;此外,还可以在高温下将“积炭”的催化剂置于 (填化学式)气流中。
④不同催化剂的相关参数如下表,分析可知,最合适的催化剂为 (填序号)
催化剂序号 最佳反应温度/℃ 最佳反应温度下的使用寿命/h 积炭量/mg
a 500 90 250
b 600 80 585
c 760 2 19
21.纳米铁(单质铁)在环保领域应用广泛,以菱铁矿(主要成分为FeCO3,杂质不溶于水且不与其他物质发生反应)为原料,制备纳米铁的反应为H2+FeCO3Fe+H2O+CO2.加热一段时间后,某学习小组对剩余固体的成分进行探究。(已知装置气密性良好。装置内药品均足量)
【提出问题】剩余固体的成分是什么?
【作出猜想】
(1)猜想一:Fe和杂质;猜想二:FeCO3和杂质;猜想三:________。
【实验探究】该学习小组利用如图所示装置,对m1g的剩余固体的成分进行探究,请回答下列问题。
(2)打开K1通N2一段时间,关闭K1.点燃E处的酒精灯。向盛有m1g剩余固体的锥形瓶中加入足量的稀硫酸,锥形瓶中有气泡产生且溶液变为浅绿色。小芳同学判断猜想一正确,小刚同学认为小芳同学的判断不合理,理由是________(用化学方程式表示)。
(3)实验过程中,E处玻璃管内出现了明显的现象,该现象为:________。
(4)充分反应后,熄灭酒精灯,继续通N2一段时间至装置冷却到室温。实验结束后测得:装置A中固体减少了m2g,装置C、D的总质量共增加了m3g,装置F内固体增加了m4g。经分析得知猜想三正确。请选择合适的数据,计算剩余固体中单质铁的质量分数为________(填表达式)。
(5)关于该实验的说法正确的是___________。
A. 实验时先通N2一段时间再点燃酒精灯是为了排尽空气,防止加热时发生爆炸。
B. 若加入的稀硫酸不足,则测得铁的质量分数偏小
C. 若没有D装置,则测得铁的质量分数偏小
D. 若氧化铜的量不足,不影响测得的铁的质量分数
E. 若熄灭酒精灯后没有通一段时间的N2,则测得铁的质量分数偏大
答案解析部分
1.B
A. 水结成冰的过程中,只是水的状态发生改变,没有新物质生成,属于物理变化,故不符合题意;
B. 燃气燃烧过程中,有新物质生成,属于化学变化,故符合题意;
C. 纸剪窗花过程中,只是物质的形状发生改变,没有新物质生成,属于物理变化,故不符合题意;
D. 干冰升华过程中,只是物质的状态发生改变,没有新物质生成,属于物理变化,故不符合题意。
故答案为:B。
化学变化的特征是有新物质生成。
2.C
3.B
4.A
5.B
6.C
A、氢气等可燃性的气体与空气混合容易形成爆炸性混合物,故点燃氢气等可燃性的气体之前一定要检验其纯度,该说法正确,不符合题意;
B、取液后的胶头滴管应保持橡胶胶帽在上,不要平放防止液体流入胶头内腐蚀胶头,该说法正确,不符合题意;
C、加热试管中的液体时,试管口不对着自己或他人,以免液体喷出伤人,该说法错误,符合题意;
D、不能用燃着的酒精灯去点燃另一个酒精灯,也不能用嘴吹灭,避免引发火灾,该说法正确,不符合题意。
故答案为:C.
A、根据可燃性的气体燃烧前均需检查气体的纯度,否则混合气体燃烧会产生爆炸事件来解答;
B、根据滴管使用后应保持橡胶胶帽在上,不要平放防止液体流入胶头内腐蚀胶头来解答;
C、根据加热试管中的液体时,试管口不对着自己或他人,以免液体喷出伤人来解答;
D、根据酒精灯使用不能用燃着的酒精灯去点燃另一个酒精灯,也不能用嘴吹灭,避免引发火灾来解答。
7.A
A、加油站、加气站的空气中含有大量的可燃性颗粒,混有一定量的空气,遇到明火(或电火花),容易发生爆炸,故加油站、加气站要严禁烟火,也不能拨打电话,A选项做法错误,符合题意;
B、建筑物内起火,如果迅速打开门窗,会加速空气流通,增加氧气的含量,会使火燃烧的更旺,所以不要急于打开窗户,B选项做法正确,不符合题意;
C、厨房油锅起火,立即用锅盖盖灭,可隔绝氧气,达到灭火的目的,C选项做法正确,不符合题意;
D、天然气具有可燃性,混有一定量的空气,遇到明火(或电火花),容易发生爆炸,故天然气泄漏时,应立即关闭阀门并开窗通风,不能打开排气扇等,D选项做法正确,不符合题意;
故选:A。
根据灭火的原理和方法,以及灭火的安全知识进行分析判断。
8.A
A、锆原子序数=质子数=40,相对原子质量为91.22,则锆原子的中子数为91-40=51,符合题意;
B、由元素周期表中的一格可知,锆的相对原子质量为91.22,不符合题意;
C、锆原子最外层电子数为2<4,在化学变化中容易失去两个电子,不符合题意;
D、锆原子的核外电子层数为5,则锆元素位于元素周期表的第五周期,不符合题意;
故答案为:A。
根据元素周期表中的小格信息,左上角的数字表示原子序数,汉字下方的数字表示相对原子质量,在原子中,原子序数=质子数,相对原子质量≈质子数+中子数,元素周期数与原子核外电子层数相等,最外层电子数小于4的易失电子分析。
9.C
A、吡唑啉的化学式量为:(12×3)+(1×6)+(14×2)=70,有机高分子化合物的相对分子质量高达几万到几十万,甚至几百万或更高,故吡唑啉不属于有机高分子化合物,该选项说法不符合题意;
B、吡唑啉由分子构成,每个吡唑啉分子是由3个碳原子、6个氢原子和2个氮原子构成的,该选项说法不符合题意;
C、吡唑啉中碳原子相对原子质量和最大,因此碳元素质量分数最大,该选项说法符合题意;
D、吡唑啉的化学式量为:(12×3)+(1×6)+(14×2)=70,单位是“1”,不是“g”该选项说法不符合题意。
故答案为:C。
A、 吡唑啉是含有碳元素的化合物,故属于有机物,相等分子质为:3×12+6+2×14=70,故不属于有机高分子化合物;
B、根据 吡唑啉的化学式可知,该物质有 吡唑啉分子构成,而每个 吡唑啉分子由 由3个碳原子、6个氢原子和2个氮原子构成的 ;
C、根据 吡唑啉中碳氢氮元素的质量比,即可判断碳元素质量分数最大;
D、根据相对分子质量的单位为1分析。
10.B
11.B
A. 纯净物分为单质和化合物,单质又分为金属单质和非金属单质,符合图所示的从属关系,故不符合题意;
B. 氧化反应是指物质与氧气的反应,化合反应是由两种或两种以上物质生成另一种物质的反应,两者属于交叉关系,不符合图所示的从属关系,故符合题意;
C. 溶液是均一、稳定的混合物,溶液分为饱和溶液和不饱和溶液,符合图所示的从属关系,故不符合题意;
D. 氧化物是指由两种元素组成且其中一种元素是氧元素的化合物,无机化合物通常指不含碳元素的化合物,包括碳的氧化物、碳酸盐、氢化物等,符合图所示的从属关系,故不符合题意。
故答案为:B。
A、根据纯净物分为单质和化合物,单质又分为金属单质和非金属单质,分析。
B、根据氧化反应、化合反应的概念分析。
C、根据溶液是均一、稳定的混合物,溶液分为饱和溶液和不饱和溶液,符合图所示的从属关系,故不符合题意;
D、根据氧化物、无机化合物的概念分析。
12.B
A、该反应中,反应物的分子可分成原子,原子再重新组成,不符合题意;
B、化学反应前后原子种类不发生改变,符合题意;
C、a为水、b为过氧化氢,二者组成元素相同,但分子构成不同,所以化学性质不同,不符合题意;
D、在化学变化中,原子不可分,只是重新组合,不符合题意。
故答案为:B。
A、根据化学变化中分子可分成原子分析;
B、根据化学反应中原子种类不变分析;
C、根据由分子构成的物质,其分子保持物质化学性质,不同种分子化学性质不同分析;
D、根据化学反应中原子不可再分分析。
13.D
A、在AgNO3溶液中加入铁片,铁片可与AgNO3反应生成硝酸亚铁和银,则说明Fe的金属活动性比Ag强,因此,该反应的化学方程式为:,故A不符合题意;
B、将气体通入NaOH溶液中,氢氧化钠可与二氧化碳反应生成碳酸钠和水,观察不到明显的现象,故B不符合题意;
C、在含有氯化钡的氯化钾中加入适量的硫酸钾,硫酸钾可与氯化钡反应生成硫酸钡沉淀和氯化钾,因此,该反应的化学方程式为:,故C不符合题意;
D、碳酸钙在高温条件下可生成氧化钙和二氧化碳,故D符合题意;
故答案为:D。
A、根据金属活动性顺序进行分析解答;
B、根据检验二氧化碳的方法进行分析解答;
C、根据除杂所满足的条件进行分析解答;
D、根据除杂多满足的条件进行分析解答。
14.A
15.B
16.(1)液面升高;H2
(2)三分之一;没有产生新的分子
(3)玻璃棒;引流;煮沸
(1)电解水时,正极产生氧气,负极产生氢气,氧气与氢气的体积比约为1∶2。由于产生了气体,长颈漏斗中的现象是液面升高;b玻璃管内产生的气体较多,说明该气体是氢气(H2)。
(2)加热水时,试管内水的体积最多不能超过试管容积的三分之一;微观上物理变化是没有新分子生成的变化,化学变化是有新分子生成的变化。水受热变为水蒸气是物理变化的微观解释是:没有产生新的分子。
(3)过滤时,应遵循“一贴二低三靠”的规则,需使用玻璃棒引流,图丙中缺少的一种玻璃仪器是玻璃棒,它的作用是引流;硬水是含有较多可溶性钙、镁化合物的水,这些钙、镁化合物在高温条件下会转化为碳酸钙沉淀、氢氧化镁沉淀,因此生活中常用的对自来水进行消毒并可以降低水的硬度的方法是煮沸。
(1)根据电解水产生气体,正氧负氢分析;
(2)根据加热试管内液体不能超过管容积的三分之一,物理变化时分子种类不变分析;
(3)根据过滤所需仪器,煮沸可降低水的硬度分析。
(1)电解水时,正极产生氧气,负极产生氢气,氧气与氢气的体积比约为1∶2。由于产生了气体,长颈漏斗中的现象是液面升高;
b玻璃管内产生的气体较多,说明该气体是氢气(H2)。
(2)加热水时,试管内水的体积最多不能超过试管容积的三分之一;
微观上物理变化是没有新分子生成的变化,化学变化是有新分子生成的变化。水受热变为水蒸气是物理变化的微观解释是:没有产生新的分子。
(3)过滤时,应遵循“一贴二低三靠”的规则,需使用玻璃棒引流,图丙中缺少的一种玻璃仪器是玻璃棒,它的作用是引流;
硬水是含有较多可溶性钙、镁化合物的水,这些钙、镁化合物在高温条件下会转化为碳酸钙沉淀、氢氧化镁沉淀,因此生活中常用的对自来水进行消毒并可以降低水的硬度的方法是煮沸。
17.(1);氢气无毒,且燃烧产物是水,不污染空气
(2)金属;强度和硬度更高,抗腐蚀性能更好;
(3)合成;6:1
(4)C;D
18.(1)长颈漏斗;水槽
(2)BC;用燃着的木条放在集气瓶口,若木条熄灭,则说明已经集满,反之,则没满
(3)先将导管从水槽中移出,再熄灭酒精灯
(4)A;D
(1) 仪器①名称为长颈漏斗, ②为水槽。
(2) 实验室利用大理石与稀盐酸反应制取二氧化碳,二氧化碳能溶于水,密度比空气大,制取和收集CO2气体时应选用BC装置连接, 验满方法是将燃着木条放在集气瓶口,木条熄灭,则证明已满。
(3)实验室用KMnO4制取O2时,用排水法收集O2完毕后,停止实验时为防止产生倒吸,需先将导管从水槽中移出,再熄灭酒精灯。
(4) 实验室常用加热氯化铵和熟石灰的固体混合物来制取氨气 ,需选择固体加热型发生装置,即A,氨气密度比空气小,极易溶于水,要选择向下排空气法收集,即D。
(1)根据常用仪器名称分析;
(2)根据二氧化碳的制取原理及密度和溶解性选择发生装置和收集装置,二氧化碳利用燃着木条放瓶口进行验满分析;
(3)根据高锰酸钾制氧气排水法收集实验结束后要防止发生倒吸分析;
(4)根据反应物状态及反应条件选择发生装置,由气体密度和溶解性选择收集装置分析。
19.(1)干燥气体
(2)
(3)DE
(4)防止空气中水蒸气和二氧化碳进入E中,影响实验结果
(5)使生成气体被完全吸收
(6);产生白色沉淀;溶液变红
(7)C、H
20.(1)风能
(2);节约能源(合理即可)
(3)不可再生;;CH4;催化剂表面的积碳积聚变多,覆盖在催化剂表面,隔开了甲烷和催化剂,减小了接触面积,导致反应速率降低;;H2O;a
21.(1) Fe、FeCO3和杂质
(2)
(3) 黑色固体逐渐变为红色
(4)
(5) AB
化学开学摸底考试
一、选择题:本大题共15小题,每小题3分,共45分。在每小题列出的四个选项中,只有一项是符合题目要求的。
1.化学,是关于物质变化的学问。下列变化中,发生了化学变化的是( )
A.水结成冰 B.燃气燃烧
C.纸剪窗花 D.干冰升华
2.下列有关物质的用途、性质等信息对应不正确的是( )
A.液氢用作火箭升空的燃料——可燃性——化学性质
B.石墨用作电刷——导电性——物理性质
C.活性炭用于净化空气——吸附性——化学性质
D.氮气用作食品保护气——常温时稳定——化学性质
3.下列物质的用途主要取决于其化学性质的是( )
A.用铜制导线 B.用氧气进行医疗急救
C.用氦气充探空气球 D.用生铁铸造铁锅
4.分类是化学学习和研究的重要方法之一,下列分类正确的是( )
A.污染空气气体有:一氧化碳、二氧化硫、二氧化氮
B.纯净物:洁净的空气、高锰酸钾分解后剩余物、冰水混合物
C.可在酒精灯上加热的仪器:试管、烧杯、量筒
D.物理性质包括:溶解性、挥发性、可燃性
5.研发多种用于石油化工生产的催化剂,为我国炼油催化剂制造技术奠定基础的科学家是( )
A.拉瓦锡 B.闵恩泽 C.张青莲 D.道尔顿
6.关注实验安全,规范实验操作。下列做法中,不符合实验操作规范的是( )
A.点燃氢气等可燃性的气体之前,一定要检验其纯度
B.取液后的胶头滴管,应保持橡胶胶帽在上,不要平放
C.给试管里的液体加热,将试管口对着自己,便于观察现象
D.不能用燃着的酒精灯去点燃另一个酒精灯,也不能用嘴吹灭
7.“生命可贵,安全第一”。从安全角度出发,下列做法不合理的是( )
A.加油站、加气站要严禁烟火,但可以拨打电话
B.建筑物内起火,不要急于开窗
C.厨房油锅起火,立即用锅盖盖灭
D.天然气泄漏时,应立即关闭阀门并开窗通风
8.天宫课堂中,航天员王亚平展示了“锆金属熔化与凝固”实验。如下图是锆元素在元素周期表中的信息及原子结构示意图。下列说法不正确的是( )
A.锆原子的中子数为40
B.锆元素的相对原子质量为91.22
C.锆原子在化学变化中容易失去两个电子
D.锆元素位于元素周期表的第五周期
9.近年来一些手机厂商纷纷发布自己的可折叠手机。化学物质吡唑啉是生产折叠手机用到的柔性屏幕的重要物质,其化学式为C3H6N2,下列有关吡唑啉C3H6N2的说法正确的是( )
A.吡唑啉属于有机高分子化合物
B.吡唑啉是由3个碳原子、6个氢原子和2个氮原子构成的
C.吡唑啉中碳元素质量分数最大
D.吡唑啉的化学式量为70g
10.“宏观辨识与微观探析”是化学学科核心素养之一。对下列事实的解释错误的是( )
A.氧气能被液化储存于钢瓶中——分子之间有间隔且间隔能改变
B.众人拾柴火焰高——可燃物越多,着火点越低,越易燃烧
C.化学反应前后各物质的质量总和不变——化学反应前后原子的种类、数目、质量均不改变
D.铁丝在空气中不燃烧,在氧气中剧烈燃烧——单位体积内氧分子数目决定反应的剧烈程度
11.下表中概念间不符合图所示的从属关系的是( )
选项 X Y Z
A 非金属单质 单质 纯净物
B 氧化反应 化合反应 化学反应
C 饱和溶液 溶液 混合物
D 氧化物 无机化合物 化合物
A.A B.B C.C D.D
12.“光解制氢”可实现水的高效分解,其反应示意图如图,下列说法正确的是( )
A.该反应的反应物分子不可分
B.反应前后原子种类不发生改变
C.a、b的组成元素相同,化学性质相同
D.在化学变化中,原子可以再分
13.下列实验方案和对应的化学方程式,均完全正确的是 ( )
选项 实验目的 实验方案 化学方程式
比较与金属活动性强弱 在溶液中放入铁片,观察现象
检验气体 把气体通入溶液中,观察现象
除去溶液中少量的 滴加适量的溶液,过滤
除去中少量的 高温煅烧至固体质量不再减少
A. B. C. D.
14.常见金属与稀盐酸反应的示意图如图所示,下列说法正确的是( )
A.四种金属中活动性最强的是镁
B.实验室可用铜和稀盐酸反应制取氢气
C.锌可以把稀盐酸中的氢气置换出来
D.铁与稀盐酸反应的化学方程式为
15.向盛有一定量铁粉的烧杯中不断滴入硫酸铜溶液,烧杯中有关量的变化如下图,其中正确的是( )
A. B.
C. D.
二、非选择题:本大题共6小题,第16小题7分,第17小题8分,第18-21小题各10分,共55分。
16.水是人类生存的基本条件。请回答下列问题:
(1)电解水的实验装置如图甲所示:通电后,长颈漏斗中的现象是 ,b玻璃管内收集到的气体是 (写化学式)。
(2)图乙中,试管内水的体积最多不能超过试管容积的 。水受热变为水蒸气是物理变化的微观解释是 。
(3)图丙中缺少的一种玻璃仪器是 ,它的作用是 。生活中常用的对自来水进行消毒并可以降低水的硬度的方法是 。
17.北京冬奥,科技助梦,化学在其中扮演着重要角色。从化学视角回答下列问题:
(1)国产氢氧燃料电池豪华中巴在冬奥会投入使用。氢气在氧气中燃烧反应的化学方程式为 ,氢气作燃料能实现“零排放”的原因是 。
(2)“冰丝带”速滑馆采用单层双向正交马鞍形索网屋面,将用钢量降到传统屋面的1/4,大幅减少了冶炼钢铁产生的碳排放。
①“冰丝带”速滑馆所用钢属于 材料,与纯铁比较具有 等优点;
②工业炼铁的原理是CO在高温下还原赤铁矿,其化学方程式为 。
(3)冬奥会纪念钞是我国第一枚拥有完全自主知识产权的聚丙烯塑料钞。聚丙烯化学式可表示为(C3H6)n ,它属于 材料,其中碳、氢元素的质量比为 。
(4)冬奥会礼仪服“瑞雪祥云”采用了高科技石墨烯发热材料,在-30 ℃也能御寒。石墨烯是单层石墨片,下列有关石墨烯的说法正确的是________(填序号)。
A.属于化合物 B.与金刚石的硬度相近
C.导热性能好 D.室温下能够稳定存在
18.通过这段时间的学习,你已经掌握了实验室制取气体的一些知识,请你结合如图装置图回答问题:(友情提示:所选装置均填序号)
(1)写出指定仪器名称:① ,② 。
(2)实验室制取和收集CO2气体时应选用 两装置相连接,检验集气瓶中CO2是否收集满的方法是: 。
(3)实验室用KMnO4制取O2时,用排水法收集O2完毕后,停止实验时的操作顺序是 。
(4)已知氨气(NH3)是一种无色、有刺激性气味的气体,密度比空气小,极易溶于水.实验室常用加热氯化铵和熟石灰的固体混合物来制取氨气.其发生装置是 ,收集装置是 。
19.“新冠”疫情牵动人心。我校安全复课措施之一是餐桌放置“pp”隔离板。“近云”学习小组的同学对“pp”板的组成进行了探究,实验装置如下图。
查阅资料:
①碱石灰为NaOH和CaO固体的混合物;
②“pp”板可能含有C、H、O中的两种或三种元素。
③Na2CO3溶液能与BaCl2溶液反应产生白色沉淀。
(1)装置B中浓硫酸的作用 。
(2)写出装置E中反应的方程式 。
(3)要确定“pp”板的元素组成,取2.1g“pp”板样品在装置C中完全反应,还需测定反应前后另外两个装置质量的增加量,这两个装置是 (填装置序号)。
(4)装置F的作用是 。
(5)充分反应后,还要继续通一段时间的氧气,目的是 。
(6)该实验需保证吸收试剂稍过量,为判断E中NaOH溶液是否过量,实验结束后进行了以下探究,对实验后E中溶液的溶质作出猜想:猜想①:NaOH;猜想②:Na2CO3;猜想③: 。
甲同学取少量液体进行实验:
实验操作 现象 结论
加入足量BaCl2溶液 猜想③正确
滴加少量酚酞溶液
结论:实验时E中NaOH溶液一定过量。
(7)若试验中测得生成的二氧化碳质量为6.6g,生成的水的质量为2.7g,则该“pp”板中含有的元素种类为 。
20.氢能的开发是当前研究的热点。
(1)电解水制氢需消耗电能。煤炭、风能均可发电,其中属于绿色能源的是 。
(2)图-1是某种太阳能热循环制备氢气的原理。
①写出生成H2的化学方程式 。
②该制氢方法的优点是 。
(3)图-2为一种天然气(主要成分为CH4)为原料,制备高纯H2的流程。
①天然气是 (“可再生”或“不可再生”)能源。“反应器”中,高温催化分解天然气可生成C和H2,该反应的化学方程式为 。
②流程中可回收利用的物质是 (填化学式)。
③反应过程中,催化剂表面若堆积较多的炭黑,则会形成“积炭”而降低反应速率,其本质原因是 ;为消除“积炭”,可在高温下,将“积炭”的催化剂置于CO2气流中,即可消除积炭。该反应的化学方程式为 ;此外,还可以在高温下将“积炭”的催化剂置于 (填化学式)气流中。
④不同催化剂的相关参数如下表,分析可知,最合适的催化剂为 (填序号)
催化剂序号 最佳反应温度/℃ 最佳反应温度下的使用寿命/h 积炭量/mg
a 500 90 250
b 600 80 585
c 760 2 19
21.纳米铁(单质铁)在环保领域应用广泛,以菱铁矿(主要成分为FeCO3,杂质不溶于水且不与其他物质发生反应)为原料,制备纳米铁的反应为H2+FeCO3Fe+H2O+CO2.加热一段时间后,某学习小组对剩余固体的成分进行探究。(已知装置气密性良好。装置内药品均足量)
【提出问题】剩余固体的成分是什么?
【作出猜想】
(1)猜想一:Fe和杂质;猜想二:FeCO3和杂质;猜想三:________。
【实验探究】该学习小组利用如图所示装置,对m1g的剩余固体的成分进行探究,请回答下列问题。
(2)打开K1通N2一段时间,关闭K1.点燃E处的酒精灯。向盛有m1g剩余固体的锥形瓶中加入足量的稀硫酸,锥形瓶中有气泡产生且溶液变为浅绿色。小芳同学判断猜想一正确,小刚同学认为小芳同学的判断不合理,理由是________(用化学方程式表示)。
(3)实验过程中,E处玻璃管内出现了明显的现象,该现象为:________。
(4)充分反应后,熄灭酒精灯,继续通N2一段时间至装置冷却到室温。实验结束后测得:装置A中固体减少了m2g,装置C、D的总质量共增加了m3g,装置F内固体增加了m4g。经分析得知猜想三正确。请选择合适的数据,计算剩余固体中单质铁的质量分数为________(填表达式)。
(5)关于该实验的说法正确的是___________。
A. 实验时先通N2一段时间再点燃酒精灯是为了排尽空气,防止加热时发生爆炸。
B. 若加入的稀硫酸不足,则测得铁的质量分数偏小
C. 若没有D装置,则测得铁的质量分数偏小
D. 若氧化铜的量不足,不影响测得的铁的质量分数
E. 若熄灭酒精灯后没有通一段时间的N2,则测得铁的质量分数偏大
答案解析部分
1.B
A. 水结成冰的过程中,只是水的状态发生改变,没有新物质生成,属于物理变化,故不符合题意;
B. 燃气燃烧过程中,有新物质生成,属于化学变化,故符合题意;
C. 纸剪窗花过程中,只是物质的形状发生改变,没有新物质生成,属于物理变化,故不符合题意;
D. 干冰升华过程中,只是物质的状态发生改变,没有新物质生成,属于物理变化,故不符合题意。
故答案为:B。
化学变化的特征是有新物质生成。
2.C
3.B
4.A
5.B
6.C
A、氢气等可燃性的气体与空气混合容易形成爆炸性混合物,故点燃氢气等可燃性的气体之前一定要检验其纯度,该说法正确,不符合题意;
B、取液后的胶头滴管应保持橡胶胶帽在上,不要平放防止液体流入胶头内腐蚀胶头,该说法正确,不符合题意;
C、加热试管中的液体时,试管口不对着自己或他人,以免液体喷出伤人,该说法错误,符合题意;
D、不能用燃着的酒精灯去点燃另一个酒精灯,也不能用嘴吹灭,避免引发火灾,该说法正确,不符合题意。
故答案为:C.
A、根据可燃性的气体燃烧前均需检查气体的纯度,否则混合气体燃烧会产生爆炸事件来解答;
B、根据滴管使用后应保持橡胶胶帽在上,不要平放防止液体流入胶头内腐蚀胶头来解答;
C、根据加热试管中的液体时,试管口不对着自己或他人,以免液体喷出伤人来解答;
D、根据酒精灯使用不能用燃着的酒精灯去点燃另一个酒精灯,也不能用嘴吹灭,避免引发火灾来解答。
7.A
A、加油站、加气站的空气中含有大量的可燃性颗粒,混有一定量的空气,遇到明火(或电火花),容易发生爆炸,故加油站、加气站要严禁烟火,也不能拨打电话,A选项做法错误,符合题意;
B、建筑物内起火,如果迅速打开门窗,会加速空气流通,增加氧气的含量,会使火燃烧的更旺,所以不要急于打开窗户,B选项做法正确,不符合题意;
C、厨房油锅起火,立即用锅盖盖灭,可隔绝氧气,达到灭火的目的,C选项做法正确,不符合题意;
D、天然气具有可燃性,混有一定量的空气,遇到明火(或电火花),容易发生爆炸,故天然气泄漏时,应立即关闭阀门并开窗通风,不能打开排气扇等,D选项做法正确,不符合题意;
故选:A。
根据灭火的原理和方法,以及灭火的安全知识进行分析判断。
8.A
A、锆原子序数=质子数=40,相对原子质量为91.22,则锆原子的中子数为91-40=51,符合题意;
B、由元素周期表中的一格可知,锆的相对原子质量为91.22,不符合题意;
C、锆原子最外层电子数为2<4,在化学变化中容易失去两个电子,不符合题意;
D、锆原子的核外电子层数为5,则锆元素位于元素周期表的第五周期,不符合题意;
故答案为:A。
根据元素周期表中的小格信息,左上角的数字表示原子序数,汉字下方的数字表示相对原子质量,在原子中,原子序数=质子数,相对原子质量≈质子数+中子数,元素周期数与原子核外电子层数相等,最外层电子数小于4的易失电子分析。
9.C
A、吡唑啉的化学式量为:(12×3)+(1×6)+(14×2)=70,有机高分子化合物的相对分子质量高达几万到几十万,甚至几百万或更高,故吡唑啉不属于有机高分子化合物,该选项说法不符合题意;
B、吡唑啉由分子构成,每个吡唑啉分子是由3个碳原子、6个氢原子和2个氮原子构成的,该选项说法不符合题意;
C、吡唑啉中碳原子相对原子质量和最大,因此碳元素质量分数最大,该选项说法符合题意;
D、吡唑啉的化学式量为:(12×3)+(1×6)+(14×2)=70,单位是“1”,不是“g”该选项说法不符合题意。
故答案为:C。
A、 吡唑啉是含有碳元素的化合物,故属于有机物,相等分子质为:3×12+6+2×14=70,故不属于有机高分子化合物;
B、根据 吡唑啉的化学式可知,该物质有 吡唑啉分子构成,而每个 吡唑啉分子由 由3个碳原子、6个氢原子和2个氮原子构成的 ;
C、根据 吡唑啉中碳氢氮元素的质量比,即可判断碳元素质量分数最大;
D、根据相对分子质量的单位为1分析。
10.B
11.B
A. 纯净物分为单质和化合物,单质又分为金属单质和非金属单质,符合图所示的从属关系,故不符合题意;
B. 氧化反应是指物质与氧气的反应,化合反应是由两种或两种以上物质生成另一种物质的反应,两者属于交叉关系,不符合图所示的从属关系,故符合题意;
C. 溶液是均一、稳定的混合物,溶液分为饱和溶液和不饱和溶液,符合图所示的从属关系,故不符合题意;
D. 氧化物是指由两种元素组成且其中一种元素是氧元素的化合物,无机化合物通常指不含碳元素的化合物,包括碳的氧化物、碳酸盐、氢化物等,符合图所示的从属关系,故不符合题意。
故答案为:B。
A、根据纯净物分为单质和化合物,单质又分为金属单质和非金属单质,分析。
B、根据氧化反应、化合反应的概念分析。
C、根据溶液是均一、稳定的混合物,溶液分为饱和溶液和不饱和溶液,符合图所示的从属关系,故不符合题意;
D、根据氧化物、无机化合物的概念分析。
12.B
A、该反应中,反应物的分子可分成原子,原子再重新组成,不符合题意;
B、化学反应前后原子种类不发生改变,符合题意;
C、a为水、b为过氧化氢,二者组成元素相同,但分子构成不同,所以化学性质不同,不符合题意;
D、在化学变化中,原子不可分,只是重新组合,不符合题意。
故答案为:B。
A、根据化学变化中分子可分成原子分析;
B、根据化学反应中原子种类不变分析;
C、根据由分子构成的物质,其分子保持物质化学性质,不同种分子化学性质不同分析;
D、根据化学反应中原子不可再分分析。
13.D
A、在AgNO3溶液中加入铁片,铁片可与AgNO3反应生成硝酸亚铁和银,则说明Fe的金属活动性比Ag强,因此,该反应的化学方程式为:,故A不符合题意;
B、将气体通入NaOH溶液中,氢氧化钠可与二氧化碳反应生成碳酸钠和水,观察不到明显的现象,故B不符合题意;
C、在含有氯化钡的氯化钾中加入适量的硫酸钾,硫酸钾可与氯化钡反应生成硫酸钡沉淀和氯化钾,因此,该反应的化学方程式为:,故C不符合题意;
D、碳酸钙在高温条件下可生成氧化钙和二氧化碳,故D符合题意;
故答案为:D。
A、根据金属活动性顺序进行分析解答;
B、根据检验二氧化碳的方法进行分析解答;
C、根据除杂所满足的条件进行分析解答;
D、根据除杂多满足的条件进行分析解答。
14.A
15.B
16.(1)液面升高;H2
(2)三分之一;没有产生新的分子
(3)玻璃棒;引流;煮沸
(1)电解水时,正极产生氧气,负极产生氢气,氧气与氢气的体积比约为1∶2。由于产生了气体,长颈漏斗中的现象是液面升高;b玻璃管内产生的气体较多,说明该气体是氢气(H2)。
(2)加热水时,试管内水的体积最多不能超过试管容积的三分之一;微观上物理变化是没有新分子生成的变化,化学变化是有新分子生成的变化。水受热变为水蒸气是物理变化的微观解释是:没有产生新的分子。
(3)过滤时,应遵循“一贴二低三靠”的规则,需使用玻璃棒引流,图丙中缺少的一种玻璃仪器是玻璃棒,它的作用是引流;硬水是含有较多可溶性钙、镁化合物的水,这些钙、镁化合物在高温条件下会转化为碳酸钙沉淀、氢氧化镁沉淀,因此生活中常用的对自来水进行消毒并可以降低水的硬度的方法是煮沸。
(1)根据电解水产生气体,正氧负氢分析;
(2)根据加热试管内液体不能超过管容积的三分之一,物理变化时分子种类不变分析;
(3)根据过滤所需仪器,煮沸可降低水的硬度分析。
(1)电解水时,正极产生氧气,负极产生氢气,氧气与氢气的体积比约为1∶2。由于产生了气体,长颈漏斗中的现象是液面升高;
b玻璃管内产生的气体较多,说明该气体是氢气(H2)。
(2)加热水时,试管内水的体积最多不能超过试管容积的三分之一;
微观上物理变化是没有新分子生成的变化,化学变化是有新分子生成的变化。水受热变为水蒸气是物理变化的微观解释是:没有产生新的分子。
(3)过滤时,应遵循“一贴二低三靠”的规则,需使用玻璃棒引流,图丙中缺少的一种玻璃仪器是玻璃棒,它的作用是引流;
硬水是含有较多可溶性钙、镁化合物的水,这些钙、镁化合物在高温条件下会转化为碳酸钙沉淀、氢氧化镁沉淀,因此生活中常用的对自来水进行消毒并可以降低水的硬度的方法是煮沸。
17.(1);氢气无毒,且燃烧产物是水,不污染空气
(2)金属;强度和硬度更高,抗腐蚀性能更好;
(3)合成;6:1
(4)C;D
18.(1)长颈漏斗;水槽
(2)BC;用燃着的木条放在集气瓶口,若木条熄灭,则说明已经集满,反之,则没满
(3)先将导管从水槽中移出,再熄灭酒精灯
(4)A;D
(1) 仪器①名称为长颈漏斗, ②为水槽。
(2) 实验室利用大理石与稀盐酸反应制取二氧化碳,二氧化碳能溶于水,密度比空气大,制取和收集CO2气体时应选用BC装置连接, 验满方法是将燃着木条放在集气瓶口,木条熄灭,则证明已满。
(3)实验室用KMnO4制取O2时,用排水法收集O2完毕后,停止实验时为防止产生倒吸,需先将导管从水槽中移出,再熄灭酒精灯。
(4) 实验室常用加热氯化铵和熟石灰的固体混合物来制取氨气 ,需选择固体加热型发生装置,即A,氨气密度比空气小,极易溶于水,要选择向下排空气法收集,即D。
(1)根据常用仪器名称分析;
(2)根据二氧化碳的制取原理及密度和溶解性选择发生装置和收集装置,二氧化碳利用燃着木条放瓶口进行验满分析;
(3)根据高锰酸钾制氧气排水法收集实验结束后要防止发生倒吸分析;
(4)根据反应物状态及反应条件选择发生装置,由气体密度和溶解性选择收集装置分析。
19.(1)干燥气体
(2)
(3)DE
(4)防止空气中水蒸气和二氧化碳进入E中,影响实验结果
(5)使生成气体被完全吸收
(6);产生白色沉淀;溶液变红
(7)C、H
20.(1)风能
(2);节约能源(合理即可)
(3)不可再生;;CH4;催化剂表面的积碳积聚变多,覆盖在催化剂表面,隔开了甲烷和催化剂,减小了接触面积,导致反应速率降低;;H2O;a
21.(1) Fe、FeCO3和杂质
(2)
(3) 黑色固体逐渐变为红色
(4)
(5) AB
同课章节目录
