10.2.3常见的碱、碱的化学性质 教学设计--人教版(2024)化学九年级下
文档属性
| 名称 | 10.2.3常见的碱、碱的化学性质 教学设计--人教版(2024)化学九年级下 |  | |
| 格式 | docx | ||
| 文件大小 | 765.4KB | ||
| 资源类型 | 试卷 | ||
| 版本资源 | 人教版 | ||
| 科目 | 化学 | ||
| 更新时间 | 2025-02-23 23:03:02 | ||
图片预览


文档简介
中小学教育资源及组卷应用平台
10.2.3常见的碱、碱的化学性质 教学设计
课题 10.2.3常见的碱、碱的化学性质 授课教师 化学 课型 公开课
教 材 分 析 在本课题中,学生通过实验探究氢氧化钠和氢氧化钙的性质,进而认识碱类物质的主要性质和用途。教材内容从这两种常见碱的具体实例入手,引导学生通过观察和实验,理解碱的溶解性、与非金属氧化物反应等基本性质。学生在实验中能够直观地看到这些反应,并用化学方程式进行表达,这有助于强化对化学变化的理解。此外,教材还强调碱的腐蚀性及其使用时的安全注意事项,增强学生的安全意识和责任感,确保在实验和实际应用中采取适当的安全措施。通过对比、分类和概括的方法,学生逐步建立起物质分类的认识,从而形成基于物质类别研究物质及其变化的视角,不仅帮助学生更好地理解和记忆碱的性质,还能培养其独立思考和解决实际问题的能力。
学 情 分 析 大多数学生已经具备了一定的化学基础知识,对元素和简单化合物有所了解,但对碱类物质的具体性质和应用了解较少。他们对通过实验探索化学反应的过程具有一定的兴趣,这为本课题的实验教学提供了良好的基础。然而,学生在理解和表达化学反应方程式上可能存在困难,这需要教师在课堂上加以引导和强化。学生对化学用语和符号的掌握程度不一,因此需要通过逐步引导和反复练习来增强他们的化学语言表达能力。此外,部分学生可能对实验安全不够重视,因此在教学中要特别强调实验安全的重要性。在这个年龄段,学生的抽象思维能力正逐渐发展,通过比较、分类和概括的学习方法,他们可以更好地理解物质的分类及其性质。这为后续更复杂的化学学习奠定了基础。因此,教师需要利用学生的好奇心和探索欲,设计有趣且富有挑战性的实验活动,以激发他们的学习动机,并逐步引导他们形成系统的化学知识体系。
核 心 素 养 目 标 1.化学观念:学生通过实验了解碱的基本性质,逐步形成对碱类物质的系统认识,这帮助他们 建立起物质分类和化学反应本质的科学观念。。 2.科学思维:在实验过程中,学生需要观察、记录及分析实验现象,并通过化学方程式表达化学反应。这培养了他们的逻辑思维和分析能力,帮助他们用科学的方式思考和解释化学现象。 3.科学探究与实践:学生通过动手实验,加深对化学知识的理解,并学习使用科学方法解决问 题。这一过程培养了他们的实验技能和动手能力,激发了他们的探索精神和创新思维。 4.科学态度与责任:强调实验安全和化学物质的安全使用,增强了学生的安全意识和责任感。学生在实验中不仅要严谨对待每个步骤,还要对自己的学习和实验行为负责。。
教 学 重 难 点 重点: 常见碱的主要性质。 2.难点: 氢氧化钠和氢氧化钙的特性。
教学 方法 讲授法、实验教学、多媒体教学法,学生采用自主学习、合作探究的方法。
教学 环节 教学活动 设计意图
一、 探究活动1 【展示]生活中含有“碱”性物品的物质——变蛋、肥皂等 “碱”最早表示灰。人们将草木灰放到水中,利用得到的碱性灰汁洗浴、印染等。那些尝起来涩涩的,摸起来滑滑的中都含有碱性物质。 【展示]实验室中常见的碱:氢氧化钠、氢氧化钙、氢氧化钾 这些碱有哪些性质和用途呢 本节课我们一起探究吧! 激发学生探究学习的兴趣。
二、 探究活动2 任务一: 【总结】氢氧化钠是白色固体,氢氧化钠俗称火碱、烧碱或苛性钠。 【学生活动】阅读教材P71,了解氢氧化钠的特性。 【视频展示】鸡翅泡在氢氧化钠溶液中会怎样 梳理了旧知,并及时联系生活,在学生理解知识的层面促进知识向运用层面转化。
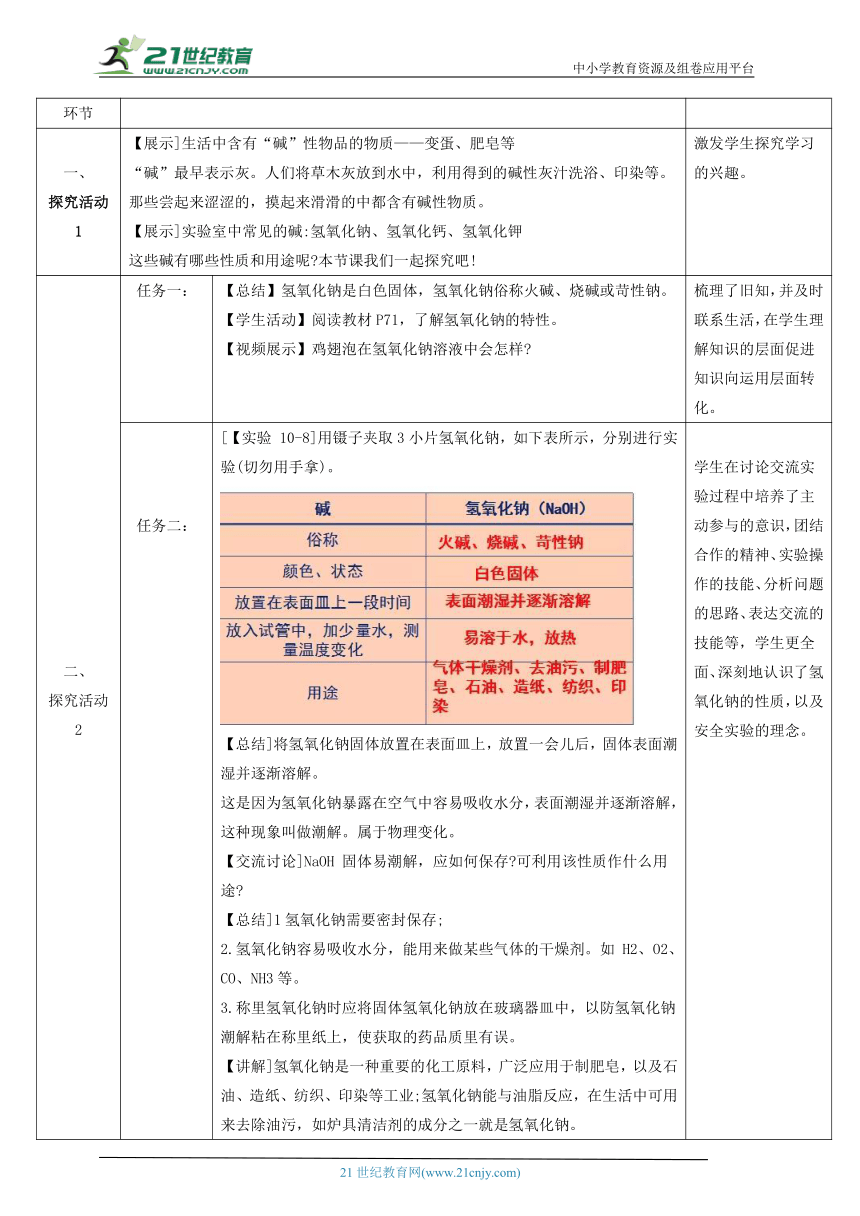
任务二: [【实验 10-8]用镊子夹取3小片氢氧化钠,如下表所示,分别进行实验(切勿用手拿)。 【总结]将氢氧化钠固体放置在表面皿上,放置一会儿后,固体表面潮湿并逐渐溶解。 这是因为氢氧化钠暴露在空气中容易吸收水分,表面潮湿并逐渐溶解,这种现象叫做潮解。属于物理变化。 【交流讨论]NaOH 固体易潮解,应如何保存 可利用该性质作什么用途 【总结]1氢氧化钠需要密封保存; 2.氢氧化钠容易吸收水分,能用来做某些气体的干燥剂。如 H2、O2、CO、NH3等。 3.称里氢氧化钠时应将固体氢氧化钠放在玻璃器皿中,以防氢氧化钠潮解粘在称里纸上,使获取的药品质里有误。 【讲解]氢氧化钠是一种重要的化工原料,广泛应用于制肥皂,以及石油、造纸、纺织、印染等工业;氢氧化钠能与油脂反应,在生活中可用来去除油污,如炉具清洁剂的成分之一就是氢氧化钠。 【回顾总结】去油污的几种原理:氢氧化钠能与油脂反应,可去除油污(化学变化);洗涤剂能与油污发生乳化作用(物理变化);汽油能溶解油污(物理变化)。 学生在讨论交流实验过程中培养了主动参与的意识,团结合作的精神、实验操作的技能、分析问题的思路、表达交流的技能等,学生更全面、深刻地认识了氢氧化钠的性质,以及安全实验的理念。
任务三: 氢氧化钙 【学生活动】阅读教材P72,说一说氢氧化钙的俗称及特性。 【总结】澄清石灰水的溶质就是氢氧化钙,氢氧化钙是白色粉末状固体,俗称熟石灰、消石灰,也具有腐蚀性,使用时要注意安全。 【实验10-9]取一小药匙氢氧化钙,观察它的颜色和状态,然后放入小烧杯中,加入30mL水,用玻璃棒搅拌,观察氢氧化钙在水中的溶解情况。 【总结]20℃时,Ca(OH)2的溶解度为0.17g,且溶解度随温度的升高而降低,故氢氧化钙微溶于水。氢氧化钙微溶于水,水溶液俗称石灰水。当石灰水中存在较多未溶解的熟石灰,叫石灰乳、石灰浆。 【讲解]氢氧化钙在生产和生活中具有广泛的用途。例如:建筑上用熟石灰与沙子混合来砌砖;在树木上涂刷含有硫黄粉等的石灰浆,可保护树木,防止冻伤,并防止害虫产卵;农业上可用石灰乳与硫酸铜溶液等配制成具有杀菌作用的波尔多液,作为农药使用;熟石灰还可用来改良酸性土壤;等等。 培养归纳总结能力和语言表达能力。理解知识在生产和日常生活中的应用。
任务四: 1.【学生实验】在白色点滴板上分别滴有氢氧化钠和氢氧化钙溶液,然后再分别滴加紫色的石蕊溶液和无色的酚酞溶液,观察并记录现象。 2.碱能与部分非金属氧化物反应:碱+非金属氧化物→盐+水 碱在水中都能解离出OH-和金属离子,这就是碱具有相似的化学性质的原因。 [思考]利用碱的化学性质解释下列事实: ①熟石灰与沙子混合砌砖;熟石灰跟空气中的二氧化碳发生反应,逐渐转变成坚硬的碳酸钙,从而把砖和沙子牢牢地粘在一起。 ②氢氧化钠必须密封保存。 固体氢氧化钠曝露在空气中易吸水潮解,潮解后的氢氧化钠会与空气中的二氧化碳反应而变质,因此必须密封保存。 【学生活动]交流讨论:分析实验室用氢氧化钠溶液吸收二氧化碳而用澄清石灰水检验二氧化碳的原因。 [总结] 原因1:20℃时,NaOH的溶解度是111g,Ca(OH)2的溶解度为0.17g。所以 NaOH的溶解度大,吸收的里多。 原因 2:NaOH与 CO2反应无明显现象,Ca(OH)2与CO2反应现象明显,易于观察。
三、小结作业 课后习题 直观形象,突出本节课重点知识,形成完整的知识体系,学练结合。
四、板书设计 一、几种常见的碱 1.氢氧化钠:烧碱、火碱、苛性钠 (1)强腐蚀性 (2)易潮解:干燥剂 (3)用途 2.氢氧化钙:熟石灰、消石灰 (1)微溶于水 (2)用途 (3)制取:CaO+H2O=Ca(OH)2 二、碱的化学性质 (1)碱能使紫色石蕊试液变成蓝色,使无色酚酞试液变红色; (2)碱能与某些非金属反应生成金属化合物和水。
五、教学反思 亮点:通过实验引导学生主动探索,结合理论与实际应用,帮助学生理解化学知识的实际价值,并通过引导总结化学性质的共性,培养学生的分析和总结能力。 不足:部分实验因资源限制未能充分展开,对不同学习能力学生的关注和指导可能不够全面。 教学建议:加强实验设备和材料准备以优化实验设计,根据学生不同学提供个性化指导,增加师生互动和讨论环节以促进深入理解和思考。
21世纪教育网 www.21cnjy.com 精品试卷·第 2 页 (共 2 页)
21世纪教育网(www.21cnjy.com)
10.2.3常见的碱、碱的化学性质 教学设计
课题 10.2.3常见的碱、碱的化学性质 授课教师 化学 课型 公开课
教 材 分 析 在本课题中,学生通过实验探究氢氧化钠和氢氧化钙的性质,进而认识碱类物质的主要性质和用途。教材内容从这两种常见碱的具体实例入手,引导学生通过观察和实验,理解碱的溶解性、与非金属氧化物反应等基本性质。学生在实验中能够直观地看到这些反应,并用化学方程式进行表达,这有助于强化对化学变化的理解。此外,教材还强调碱的腐蚀性及其使用时的安全注意事项,增强学生的安全意识和责任感,确保在实验和实际应用中采取适当的安全措施。通过对比、分类和概括的方法,学生逐步建立起物质分类的认识,从而形成基于物质类别研究物质及其变化的视角,不仅帮助学生更好地理解和记忆碱的性质,还能培养其独立思考和解决实际问题的能力。
学 情 分 析 大多数学生已经具备了一定的化学基础知识,对元素和简单化合物有所了解,但对碱类物质的具体性质和应用了解较少。他们对通过实验探索化学反应的过程具有一定的兴趣,这为本课题的实验教学提供了良好的基础。然而,学生在理解和表达化学反应方程式上可能存在困难,这需要教师在课堂上加以引导和强化。学生对化学用语和符号的掌握程度不一,因此需要通过逐步引导和反复练习来增强他们的化学语言表达能力。此外,部分学生可能对实验安全不够重视,因此在教学中要特别强调实验安全的重要性。在这个年龄段,学生的抽象思维能力正逐渐发展,通过比较、分类和概括的学习方法,他们可以更好地理解物质的分类及其性质。这为后续更复杂的化学学习奠定了基础。因此,教师需要利用学生的好奇心和探索欲,设计有趣且富有挑战性的实验活动,以激发他们的学习动机,并逐步引导他们形成系统的化学知识体系。
核 心 素 养 目 标 1.化学观念:学生通过实验了解碱的基本性质,逐步形成对碱类物质的系统认识,这帮助他们 建立起物质分类和化学反应本质的科学观念。。 2.科学思维:在实验过程中,学生需要观察、记录及分析实验现象,并通过化学方程式表达化学反应。这培养了他们的逻辑思维和分析能力,帮助他们用科学的方式思考和解释化学现象。 3.科学探究与实践:学生通过动手实验,加深对化学知识的理解,并学习使用科学方法解决问 题。这一过程培养了他们的实验技能和动手能力,激发了他们的探索精神和创新思维。 4.科学态度与责任:强调实验安全和化学物质的安全使用,增强了学生的安全意识和责任感。学生在实验中不仅要严谨对待每个步骤,还要对自己的学习和实验行为负责。。
教 学 重 难 点 重点: 常见碱的主要性质。 2.难点: 氢氧化钠和氢氧化钙的特性。
教学 方法 讲授法、实验教学、多媒体教学法,学生采用自主学习、合作探究的方法。
教学 环节 教学活动 设计意图
一、 探究活动1 【展示]生活中含有“碱”性物品的物质——变蛋、肥皂等 “碱”最早表示灰。人们将草木灰放到水中,利用得到的碱性灰汁洗浴、印染等。那些尝起来涩涩的,摸起来滑滑的中都含有碱性物质。 【展示]实验室中常见的碱:氢氧化钠、氢氧化钙、氢氧化钾 这些碱有哪些性质和用途呢 本节课我们一起探究吧! 激发学生探究学习的兴趣。
二、 探究活动2 任务一: 【总结】氢氧化钠是白色固体,氢氧化钠俗称火碱、烧碱或苛性钠。 【学生活动】阅读教材P71,了解氢氧化钠的特性。 【视频展示】鸡翅泡在氢氧化钠溶液中会怎样 梳理了旧知,并及时联系生活,在学生理解知识的层面促进知识向运用层面转化。
任务二: [【实验 10-8]用镊子夹取3小片氢氧化钠,如下表所示,分别进行实验(切勿用手拿)。 【总结]将氢氧化钠固体放置在表面皿上,放置一会儿后,固体表面潮湿并逐渐溶解。 这是因为氢氧化钠暴露在空气中容易吸收水分,表面潮湿并逐渐溶解,这种现象叫做潮解。属于物理变化。 【交流讨论]NaOH 固体易潮解,应如何保存 可利用该性质作什么用途 【总结]1氢氧化钠需要密封保存; 2.氢氧化钠容易吸收水分,能用来做某些气体的干燥剂。如 H2、O2、CO、NH3等。 3.称里氢氧化钠时应将固体氢氧化钠放在玻璃器皿中,以防氢氧化钠潮解粘在称里纸上,使获取的药品质里有误。 【讲解]氢氧化钠是一种重要的化工原料,广泛应用于制肥皂,以及石油、造纸、纺织、印染等工业;氢氧化钠能与油脂反应,在生活中可用来去除油污,如炉具清洁剂的成分之一就是氢氧化钠。 【回顾总结】去油污的几种原理:氢氧化钠能与油脂反应,可去除油污(化学变化);洗涤剂能与油污发生乳化作用(物理变化);汽油能溶解油污(物理变化)。 学生在讨论交流实验过程中培养了主动参与的意识,团结合作的精神、实验操作的技能、分析问题的思路、表达交流的技能等,学生更全面、深刻地认识了氢氧化钠的性质,以及安全实验的理念。
任务三: 氢氧化钙 【学生活动】阅读教材P72,说一说氢氧化钙的俗称及特性。 【总结】澄清石灰水的溶质就是氢氧化钙,氢氧化钙是白色粉末状固体,俗称熟石灰、消石灰,也具有腐蚀性,使用时要注意安全。 【实验10-9]取一小药匙氢氧化钙,观察它的颜色和状态,然后放入小烧杯中,加入30mL水,用玻璃棒搅拌,观察氢氧化钙在水中的溶解情况。 【总结]20℃时,Ca(OH)2的溶解度为0.17g,且溶解度随温度的升高而降低,故氢氧化钙微溶于水。氢氧化钙微溶于水,水溶液俗称石灰水。当石灰水中存在较多未溶解的熟石灰,叫石灰乳、石灰浆。 【讲解]氢氧化钙在生产和生活中具有广泛的用途。例如:建筑上用熟石灰与沙子混合来砌砖;在树木上涂刷含有硫黄粉等的石灰浆,可保护树木,防止冻伤,并防止害虫产卵;农业上可用石灰乳与硫酸铜溶液等配制成具有杀菌作用的波尔多液,作为农药使用;熟石灰还可用来改良酸性土壤;等等。 培养归纳总结能力和语言表达能力。理解知识在生产和日常生活中的应用。
任务四: 1.【学生实验】在白色点滴板上分别滴有氢氧化钠和氢氧化钙溶液,然后再分别滴加紫色的石蕊溶液和无色的酚酞溶液,观察并记录现象。 2.碱能与部分非金属氧化物反应:碱+非金属氧化物→盐+水 碱在水中都能解离出OH-和金属离子,这就是碱具有相似的化学性质的原因。 [思考]利用碱的化学性质解释下列事实: ①熟石灰与沙子混合砌砖;熟石灰跟空气中的二氧化碳发生反应,逐渐转变成坚硬的碳酸钙,从而把砖和沙子牢牢地粘在一起。 ②氢氧化钠必须密封保存。 固体氢氧化钠曝露在空气中易吸水潮解,潮解后的氢氧化钠会与空气中的二氧化碳反应而变质,因此必须密封保存。 【学生活动]交流讨论:分析实验室用氢氧化钠溶液吸收二氧化碳而用澄清石灰水检验二氧化碳的原因。 [总结] 原因1:20℃时,NaOH的溶解度是111g,Ca(OH)2的溶解度为0.17g。所以 NaOH的溶解度大,吸收的里多。 原因 2:NaOH与 CO2反应无明显现象,Ca(OH)2与CO2反应现象明显,易于观察。
三、小结作业 课后习题 直观形象,突出本节课重点知识,形成完整的知识体系,学练结合。
四、板书设计 一、几种常见的碱 1.氢氧化钠:烧碱、火碱、苛性钠 (1)强腐蚀性 (2)易潮解:干燥剂 (3)用途 2.氢氧化钙:熟石灰、消石灰 (1)微溶于水 (2)用途 (3)制取:CaO+H2O=Ca(OH)2 二、碱的化学性质 (1)碱能使紫色石蕊试液变成蓝色,使无色酚酞试液变红色; (2)碱能与某些非金属反应生成金属化合物和水。
五、教学反思 亮点:通过实验引导学生主动探索,结合理论与实际应用,帮助学生理解化学知识的实际价值,并通过引导总结化学性质的共性,培养学生的分析和总结能力。 不足:部分实验因资源限制未能充分展开,对不同学习能力学生的关注和指导可能不够全面。 教学建议:加强实验设备和材料准备以优化实验设计,根据学生不同学提供个性化指导,增加师生互动和讨论环节以促进深入理解和思考。
21世纪教育网 www.21cnjy.com 精品试卷·第 2 页 (共 2 页)
21世纪教育网(www.21cnjy.com)
同课章节目录
