破难点3 归因解释、过程评价 课件(共37张PPT) 2025届高考化学二轮复习
文档属性
| 名称 | 破难点3 归因解释、过程评价 课件(共37张PPT) 2025届高考化学二轮复习 |

|
|
| 格式 | pptx | ||
| 文件大小 | 1.0MB | ||
| 资源类型 | 教案 | ||
| 版本资源 | 通用版 | ||
| 科目 | 化学 | ||
| 更新时间 | 2025-02-22 00:00:00 | ||
图片预览









文档简介
(共37张PPT)
主题2
无机物转化与应用
破难点3 归因解释、过程评价
内容索引
检测反馈
难点精讲
名卷优选
名 卷 优 选
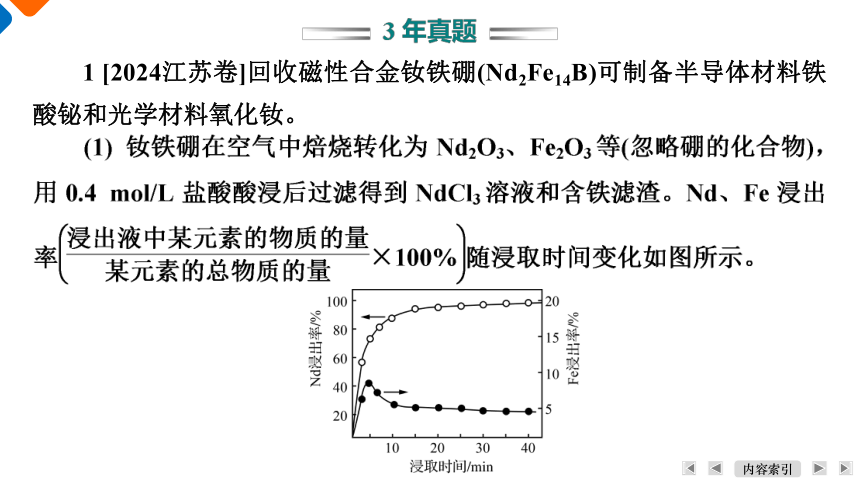
1 [2024江苏卷]回收磁性合金钕铁硼(Nd2Fe14B)可制备半导体材料铁酸铋和光学材料氧化钕。
浸出初期,起始c(H+)较大,Fe2O3与H+反应生成Fe3+;约5 min后,c(H+)较小,Fe3+水解程度增大,生成Fe(OH)3沉淀进入滤渣
<
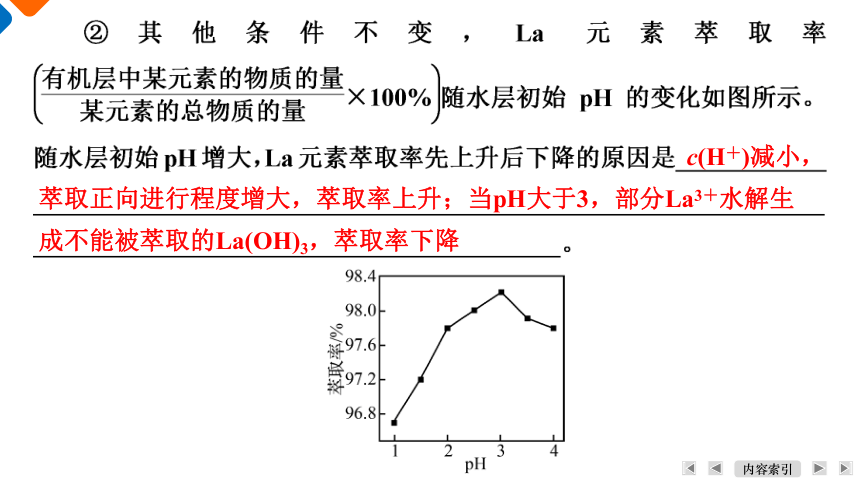
c(H+)减小,萃取正向进行程度增大,萃取率上升;当pH大于3,部分La3+水解生成不能被萃取的La(OH)3,萃取率下降
(2) [2024常州期末]聚合氯化铝(PAC)水解过程中会产生聚合稳定态物质[AlO4Al12(OH)24(H2O)12]7+(简称Al13)。Al13对水中胶体和颗粒物具有高度电中和桥联作用,是净水过程中的重要物质。
①Al3+在水解过程中会产生[Al(OH)]2+、[Al(OH)2]+等产物。写出 Al3+水解产生[Al(OH)]2+的离子方程式:___________________________ ________。
②使用Al3+净水时应控制pH在6.80~8.02之间,否则净水效果不佳。在强酸性和强碱性环境时净水效果差的原因是___________________ ______________________________________________________________________________________。
H+
强酸性环境,抑制Al3+的水解,主要以Al3+形式存在;强碱性环境,Al元素主要以[Al(OH)4]-形式存在
[温度的影响]
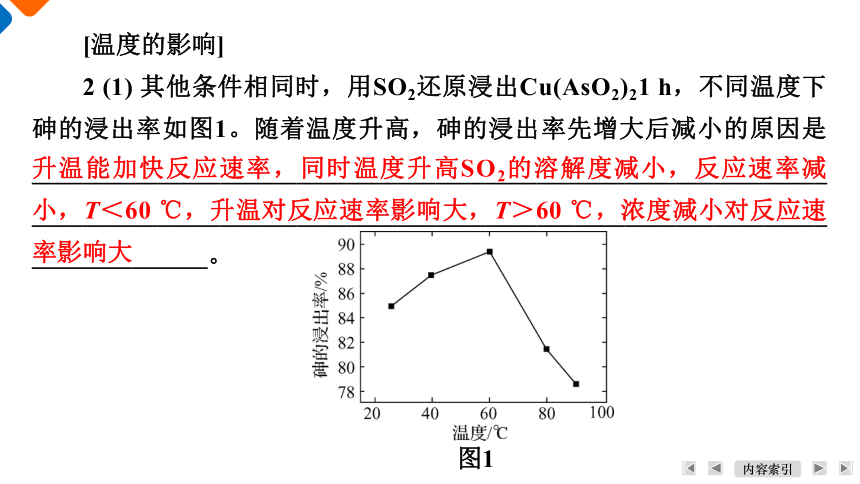
2 (1) 其他条件相同时,用SO2还原浸出Cu(AsO2)21 h,不同温度下砷的浸出率如图1。随着温度升高,砷的浸出率先增大后减小的原因是____________________________________________________________________________________________________________________________________________。
图1
升温能加快反应速率,同时温度升高SO2的溶解度减小,反应速率减小,T<60 ℃,升温对反应速率影响大,T>60 ℃,浓度减小对反应速率影响大
(2) “转化”后所得LiHCO3溶液中含有
的Ca2+需要加入Li3PO4除去。除钙步骤中其
他条件不变,反应相同时间,温度对除钙率
和Li2CO3产率的影响如图2。
①随着温度升高,最终Li2CO3的产率逐
渐减小的原因是________________________________________________ ______________。
②当温度高于50 ℃时,除钙率下降的原因可能是________________ _______________________。
图2
温度过高LiHCO3分解产生Li2CO3沉淀,与Ca3(PO4)2
一同被过滤
(3) [2024南京、盐城期末]V2O5-WO3/TiO2催化剂可以催化NH3脱除烟气中的NO。
反应:4NO(g)+4NH3(g)+O2(g)===4N2(g)+6H2O(g) ΔH=
-1 632.4 kJ/mol。
将模拟烟气以一定流速通过装有V2O5-WO3/TiO2催化剂的反应管,反应相同时间,测得NO的转化率随温度的变化如图3所示。
图3
①反应温度高于350 ℃,NO转化率下降的原因可能是____________ __________________________________________________。
②若烟气中含有SO2,则会导致催化剂失活,原因可能是_________ ________________________________________________________________________________________________________________________________________________________________________________________________________________________________________________________________________。
催化剂活性
下降,反应速率减小;NH3与O2发生反应生成NO
SO2会被(V2O5)催化氧化为SO3,SO3与NH3作用生成NH4HSO4或(NH4)2SO4,覆盖(沉积)在催化剂的表面,大大减小了催化剂和反应物的接触面积[或SO2与NH3作用生成NH4HSO3或(NH4)2SO3,最终被氧化为NH4HSO4或(NH4)2SO4,覆盖(沉积)在催化剂的表面,大大减小了催化剂和反应物的接触面积]
[物质性质与反应的影响]
3 (1) [2024常州期末]实验室以废旧磷酸铁锂(LiFePO4)电极粉末为原料回收Li2CO3,其实验过程如图1。
图1
图2
以盐酸-次氯酸钠体系选择性浸出锂。将2 g磷酸铁锂加入三颈烧瓶中(装置见图2),滴液漏斗a装有0.6 mol/L 盐酸、b中装有0.8 mol/L NaClO溶液。控制25 ℃,依次将两种溶液加入三颈烧瓶,充分反应30 min后,过滤。
已知:常温时,Ka1(H3PO4)=7.5×10-3,Ka2(H3PO4)=6.2×10-8,Ka3(H3PO4)=2.2×10-13,Ksp(FePO4)=1.3×10-22。
①浸出后过滤,所得滤渣的主要成分为FePO4。写出LiFePO4转化为FePO4的离子方程式:___________________________________________ _______________。
②控制原料n(LiFePO4)∶n(HCl)∶n(NaClO)=1∶1.3∶0.6,锂的浸出率为95.59%。若提高盐酸用量,可使锂浸出率达99%以上,但同时可能存在的缺陷有_________________________________________________ ________________________________________________________________________________________。
2LiFePO4+ClO-+2H+===2FePO4+2Li++
Cl-+H2O
过量的盐酸溶解FePO4,Fe元素也随Li元素一起浸出,导致产品纯度下降;产生Cl2,污染环境;后阶段消耗更多的Na2CO3,增加试剂成本
(2) [2024无锡期末]使用ZnMnO3脱硫剂脱除CH4或H2中的H2S。ZnMnO3脱硫和再生的过程如图3所示(部分产物已省略),在脱硫过程中脱硫剂表面形成羟基,有利于H2S的脱除。
图3
①脱除H2S(步骤Ⅰ、Ⅱ、Ⅲ,需350 ℃)的化学方程式为__________ __________________________________________。
②中间体MnSO4对脱硫剂的再生起关键作用,原因是____________ _____________________________________________________________________________________________________。
③天然气中少量的水蒸气加快了H2S的脱除,原因是____________ ________________________________________________。
2H2S+3O2
MnSO4高温
(850 ℃)分解产生SO2等气体,生成多孔MnO2和ZnO(或生成多孔ZnMnO3),增加了脱硫剂的比表面积
水分子吸附
在脱硫剂表面,增加了羟基,有利于H2S的脱除
【解析】 (1) ①在酸性条件下,LiFePO4中的Fe(Ⅱ)被ClO-(自身被还原为Cl-)氧化为FePO4中的Fe(Ⅲ),根据得失电子守恒、电荷守恒以及原子守恒可写出反应的离子方程式。②由于盐酸的酸性强于磷酸,故过量的盐酸能溶解FePO4,从而使得Fe元素也随Li元素一起浸出,导致产品纯度下降;同时过量的盐酸与NaClO反应产生Cl2,污染环境;后阶段中加入的Na2CO3也能与盐酸反应,使得Na2CO3消耗增多,从而增加了试剂成本。(2) ③已知:脱硫剂表面形成羟基,有利于H2S的脱除,故水分子吸附在脱硫剂表面,可增加羟基数目,有利于H2S的脱除。
难 点 精 讲
难点1 化工生产适宜条件选择的一般原则
条件 原则
从化学反应速率分析 既不能过大,又不能过小
从化学平衡移动分析 既要注意外界条件对速率和平衡影响的一致性,又要注意二者影响的矛盾性
从原料的利用率分析 增加易得廉价原料,提高难得高价原料的利用率,从而降低生产成本
从实际生产能力分析 如设备承受高温、高压能力等
从催化剂的使用活性分析 注意催化剂的活性对温度的限制
难点2 温度控制
1 控制温度的目的
提高反应速率、提高产率和转化率、减少副反应、提高产品纯度;加热可增大反应速率或促进反应的某个方向(一般是有利于生成物生成的方向)反应程度更大。
2 在一定范围内控制温度的目的
(1) 若温度过低,则反应速率(或溶解速率)较小。
(2) 若温度过高,某些物质会分解(如H2O2、NH4HCO3、氨水、浓硝酸)或挥发(如浓硝酸、浓盐酸)或被氧化(如Na2SO3)或促进水解(如AlCl3)。
3 冰水浴冷却的目的
(1) 使某物质液化、降低产物的溶解度。
(2) 减少其他副反应,提高产品纯度。
难点3 其他原因分析
1 浓度
(1) 根据需要选择适宜的浓度或投料比,不仅可控制一定的反应速率,还可使反应更有利于目标产物的生成。
(2) 反应物过量,能保证反应的完全发生或提高其他物质的转化率,但对后续操作也会产生影响。
2 压强:改变反应速率,使平衡向需要的方向移动。
3 催化剂:选择合适的催化剂,能增大反应速率。
4 使用保护气:(1) 隔绝空气(主要是隔绝O2、H2O)。
(2) 抑制弱离子的水解(如HCl氛围)。
5 其他归因列举。
目的或原因 思考方向
沉淀(晶体)洗涤的目的 若滤渣是所需的物质,洗涤的目的是除去晶体表面的可溶性杂质,得到更纯净的沉淀物
若滤液是所需的物质,洗涤的目的是洗涤过滤所得到的滤渣,把有用的物质(如目标产物)尽可能洗出来
沉淀(晶体)用冰水洗涤的目的 既能洗去晶体表面的杂质离子,又能减少晶体在洗涤过程中的溶解损耗
目的或原因 思考方向
沉淀(晶体)用有机溶剂(酒精、丙酮等)洗涤的目的 既能洗去晶体表面的杂质离子,又能减少晶体在洗涤过程中的溶解损耗,此外又利用有机溶剂的挥发性,除去固体表面的有机溶剂,产品易干燥
控制溶液pH的目的 防止××离子水解;防止××离子沉淀;确保××离子沉淀完全;防止××溶解等
目的或原因 思考方向
温度不高于×× ℃的原因 温度过高,××物质分解(如H2O2、浓硝酸、NH4HCO3);××物质挥发(如浓硝酸、浓盐酸);××物质被氧化(如Na2SO3);促进××物质水解(如AlCl3)
蒸发、反应时的气体氛围 抑制××离子的水解(如加热蒸发AlCl3溶液时,需在HCl气流中进行;加热MgCl2·6H2O得MgCl2时,也需在HCl气流中进行)
检 测 反 馈
2
1
3
1 [2024南京调研]NaClO溶液处理含氨氮废水(pH为6.0~7.0)。室温下,分别取200 mL预处理后的废水,将初始pH调节至不同值,加入等量NaClO溶液,30分钟后检测剩余氨氮浓度。不同初始pH对NaClO氧化脱除氨氮效果的影响如图1所示,不同初始pH对应反应结束后的pH如图2所示。
图1
图2
2
1
3
(1) NaClO将废水中NH3氧化为无污染气体,反应的化学方程式为_______________________________________,实验中NaClO溶液的实际投入量大于理论计算量,其原因是______________________________。
(2) 处理后的废水pH在6.0~9.0之间才能排放。NaClO溶液处理含氨氮废水初始pH设置为7.0而不是2.0的原因是_________________________ ________________________。
2NH3+3NaClO===N2↑+3H2O+3NaCl
NaClO(或HClO)不稳定,易分解
pH为7.0时氨氮去除率高且
调节pH所需的酸更少
2
1
3
【解析】 (1) 由题意先写出NH3+NaClO——N2+NaCl,再根据得失电子守恒写出2NH3+3NaClO——N2+3NaCl,最后根据原子守恒配平。由于反应肯定是控制在一定时间内,反应物不能反应完全,为使NH3在一定时间内尽可能被氧化去除,故应增大NaClO的实际投入量;另外次氯酸盐或次氯酸易分解,也是增大其投入量的原因之一。(2) 由图1知,当pH=7.0时氨氮去除率更高,由图2知,当pH=7.0或2.0时,反应后的废水都符合排放标准,但调节初始pH=2.0所需的酸更多。
2
1
3
(1) 从反应后的混合物中获得较高产率的NaFeY·3H2O粗品的实验操作是__________________________________,过滤,水洗,干燥。检验NaFeY·3H2O是否洗净的试剂是________________________。
冷却至室温,加入乙醇
AgNO3溶液和稀硝酸
2
1
3
(2) 保持其他条件不变,乙二胺四乙酸铁钠的产率随反应液pH的变化如图所示。pH过低或过高产品产率均减小的主要原因是____________ ________________________________________________________________________________________________________。
pH过低,H4Y电离出的Y4-浓度小(或pH过低,H4Y在水中溶出量小),pH过高,Fe3+转为Fe(OH)3,溶液中Fe3+浓度减小
2
3
1
3 [2024宿迁调研]燃煤烟气中含有大量SO2和NO。某实验室模拟“软锰矿浆同步脱硫脱硝技术”并制备MnSO4·H2O,部分流程如下:
已知:①软锰矿(主要成分为MnO2,另含有少量Fe2O3、CaO、SiO2等杂质);
②Ksp(MnF2)=1.6×10-3;Ksp(CaF2)=8.0×10-11;
2
3
【解析】 (2) 除气时,一定量的O3可将NO转化为NO2,而NO2易与水反应,NO难溶于水,这样会提高NO的脱除率。
1
(1) ①“浸锰”过程,SO2发生的主要化学方程式为______________ ______________。
②滤渣Ⅰ的主要成分为__________________(填化学式)。
(2) “除气”过程,烟气中混入一定量O3可提高NO脱除率,其可能的原因是_______________________________________________________ ______。
MnO2+SO2
===MnSO4
SiO2、CaSO4
O3可将NO氧化为在水中溶解性好的NO2;NO2氧化性强于
NO
谢谢观看
Thank you for watching
主题2
无机物转化与应用
破难点3 归因解释、过程评价
内容索引
检测反馈
难点精讲
名卷优选
名 卷 优 选
1 [2024江苏卷]回收磁性合金钕铁硼(Nd2Fe14B)可制备半导体材料铁酸铋和光学材料氧化钕。
浸出初期,起始c(H+)较大,Fe2O3与H+反应生成Fe3+;约5 min后,c(H+)较小,Fe3+水解程度增大,生成Fe(OH)3沉淀进入滤渣
<
c(H+)减小,萃取正向进行程度增大,萃取率上升;当pH大于3,部分La3+水解生成不能被萃取的La(OH)3,萃取率下降
(2) [2024常州期末]聚合氯化铝(PAC)水解过程中会产生聚合稳定态物质[AlO4Al12(OH)24(H2O)12]7+(简称Al13)。Al13对水中胶体和颗粒物具有高度电中和桥联作用,是净水过程中的重要物质。
①Al3+在水解过程中会产生[Al(OH)]2+、[Al(OH)2]+等产物。写出 Al3+水解产生[Al(OH)]2+的离子方程式:___________________________ ________。
②使用Al3+净水时应控制pH在6.80~8.02之间,否则净水效果不佳。在强酸性和强碱性环境时净水效果差的原因是___________________ ______________________________________________________________________________________。
H+
强酸性环境,抑制Al3+的水解,主要以Al3+形式存在;强碱性环境,Al元素主要以[Al(OH)4]-形式存在
[温度的影响]
2 (1) 其他条件相同时,用SO2还原浸出Cu(AsO2)21 h,不同温度下砷的浸出率如图1。随着温度升高,砷的浸出率先增大后减小的原因是____________________________________________________________________________________________________________________________________________。
图1
升温能加快反应速率,同时温度升高SO2的溶解度减小,反应速率减小,T<60 ℃,升温对反应速率影响大,T>60 ℃,浓度减小对反应速率影响大
(2) “转化”后所得LiHCO3溶液中含有
的Ca2+需要加入Li3PO4除去。除钙步骤中其
他条件不变,反应相同时间,温度对除钙率
和Li2CO3产率的影响如图2。
①随着温度升高,最终Li2CO3的产率逐
渐减小的原因是________________________________________________ ______________。
②当温度高于50 ℃时,除钙率下降的原因可能是________________ _______________________。
图2
温度过高LiHCO3分解产生Li2CO3沉淀,与Ca3(PO4)2
一同被过滤
(3) [2024南京、盐城期末]V2O5-WO3/TiO2催化剂可以催化NH3脱除烟气中的NO。
反应:4NO(g)+4NH3(g)+O2(g)===4N2(g)+6H2O(g) ΔH=
-1 632.4 kJ/mol。
将模拟烟气以一定流速通过装有V2O5-WO3/TiO2催化剂的反应管,反应相同时间,测得NO的转化率随温度的变化如图3所示。
图3
①反应温度高于350 ℃,NO转化率下降的原因可能是____________ __________________________________________________。
②若烟气中含有SO2,则会导致催化剂失活,原因可能是_________ ________________________________________________________________________________________________________________________________________________________________________________________________________________________________________________________________________。
催化剂活性
下降,反应速率减小;NH3与O2发生反应生成NO
SO2会被(V2O5)催化氧化为SO3,SO3与NH3作用生成NH4HSO4或(NH4)2SO4,覆盖(沉积)在催化剂的表面,大大减小了催化剂和反应物的接触面积[或SO2与NH3作用生成NH4HSO3或(NH4)2SO3,最终被氧化为NH4HSO4或(NH4)2SO4,覆盖(沉积)在催化剂的表面,大大减小了催化剂和反应物的接触面积]
[物质性质与反应的影响]
3 (1) [2024常州期末]实验室以废旧磷酸铁锂(LiFePO4)电极粉末为原料回收Li2CO3,其实验过程如图1。
图1
图2
以盐酸-次氯酸钠体系选择性浸出锂。将2 g磷酸铁锂加入三颈烧瓶中(装置见图2),滴液漏斗a装有0.6 mol/L 盐酸、b中装有0.8 mol/L NaClO溶液。控制25 ℃,依次将两种溶液加入三颈烧瓶,充分反应30 min后,过滤。
已知:常温时,Ka1(H3PO4)=7.5×10-3,Ka2(H3PO4)=6.2×10-8,Ka3(H3PO4)=2.2×10-13,Ksp(FePO4)=1.3×10-22。
①浸出后过滤,所得滤渣的主要成分为FePO4。写出LiFePO4转化为FePO4的离子方程式:___________________________________________ _______________。
②控制原料n(LiFePO4)∶n(HCl)∶n(NaClO)=1∶1.3∶0.6,锂的浸出率为95.59%。若提高盐酸用量,可使锂浸出率达99%以上,但同时可能存在的缺陷有_________________________________________________ ________________________________________________________________________________________。
2LiFePO4+ClO-+2H+===2FePO4+2Li++
Cl-+H2O
过量的盐酸溶解FePO4,Fe元素也随Li元素一起浸出,导致产品纯度下降;产生Cl2,污染环境;后阶段消耗更多的Na2CO3,增加试剂成本
(2) [2024无锡期末]使用ZnMnO3脱硫剂脱除CH4或H2中的H2S。ZnMnO3脱硫和再生的过程如图3所示(部分产物已省略),在脱硫过程中脱硫剂表面形成羟基,有利于H2S的脱除。
图3
①脱除H2S(步骤Ⅰ、Ⅱ、Ⅲ,需350 ℃)的化学方程式为__________ __________________________________________。
②中间体MnSO4对脱硫剂的再生起关键作用,原因是____________ _____________________________________________________________________________________________________。
③天然气中少量的水蒸气加快了H2S的脱除,原因是____________ ________________________________________________。
2H2S+3O2
MnSO4高温
(850 ℃)分解产生SO2等气体,生成多孔MnO2和ZnO(或生成多孔ZnMnO3),增加了脱硫剂的比表面积
水分子吸附
在脱硫剂表面,增加了羟基,有利于H2S的脱除
【解析】 (1) ①在酸性条件下,LiFePO4中的Fe(Ⅱ)被ClO-(自身被还原为Cl-)氧化为FePO4中的Fe(Ⅲ),根据得失电子守恒、电荷守恒以及原子守恒可写出反应的离子方程式。②由于盐酸的酸性强于磷酸,故过量的盐酸能溶解FePO4,从而使得Fe元素也随Li元素一起浸出,导致产品纯度下降;同时过量的盐酸与NaClO反应产生Cl2,污染环境;后阶段中加入的Na2CO3也能与盐酸反应,使得Na2CO3消耗增多,从而增加了试剂成本。(2) ③已知:脱硫剂表面形成羟基,有利于H2S的脱除,故水分子吸附在脱硫剂表面,可增加羟基数目,有利于H2S的脱除。
难 点 精 讲
难点1 化工生产适宜条件选择的一般原则
条件 原则
从化学反应速率分析 既不能过大,又不能过小
从化学平衡移动分析 既要注意外界条件对速率和平衡影响的一致性,又要注意二者影响的矛盾性
从原料的利用率分析 增加易得廉价原料,提高难得高价原料的利用率,从而降低生产成本
从实际生产能力分析 如设备承受高温、高压能力等
从催化剂的使用活性分析 注意催化剂的活性对温度的限制
难点2 温度控制
1 控制温度的目的
提高反应速率、提高产率和转化率、减少副反应、提高产品纯度;加热可增大反应速率或促进反应的某个方向(一般是有利于生成物生成的方向)反应程度更大。
2 在一定范围内控制温度的目的
(1) 若温度过低,则反应速率(或溶解速率)较小。
(2) 若温度过高,某些物质会分解(如H2O2、NH4HCO3、氨水、浓硝酸)或挥发(如浓硝酸、浓盐酸)或被氧化(如Na2SO3)或促进水解(如AlCl3)。
3 冰水浴冷却的目的
(1) 使某物质液化、降低产物的溶解度。
(2) 减少其他副反应,提高产品纯度。
难点3 其他原因分析
1 浓度
(1) 根据需要选择适宜的浓度或投料比,不仅可控制一定的反应速率,还可使反应更有利于目标产物的生成。
(2) 反应物过量,能保证反应的完全发生或提高其他物质的转化率,但对后续操作也会产生影响。
2 压强:改变反应速率,使平衡向需要的方向移动。
3 催化剂:选择合适的催化剂,能增大反应速率。
4 使用保护气:(1) 隔绝空气(主要是隔绝O2、H2O)。
(2) 抑制弱离子的水解(如HCl氛围)。
5 其他归因列举。
目的或原因 思考方向
沉淀(晶体)洗涤的目的 若滤渣是所需的物质,洗涤的目的是除去晶体表面的可溶性杂质,得到更纯净的沉淀物
若滤液是所需的物质,洗涤的目的是洗涤过滤所得到的滤渣,把有用的物质(如目标产物)尽可能洗出来
沉淀(晶体)用冰水洗涤的目的 既能洗去晶体表面的杂质离子,又能减少晶体在洗涤过程中的溶解损耗
目的或原因 思考方向
沉淀(晶体)用有机溶剂(酒精、丙酮等)洗涤的目的 既能洗去晶体表面的杂质离子,又能减少晶体在洗涤过程中的溶解损耗,此外又利用有机溶剂的挥发性,除去固体表面的有机溶剂,产品易干燥
控制溶液pH的目的 防止××离子水解;防止××离子沉淀;确保××离子沉淀完全;防止××溶解等
目的或原因 思考方向
温度不高于×× ℃的原因 温度过高,××物质分解(如H2O2、浓硝酸、NH4HCO3);××物质挥发(如浓硝酸、浓盐酸);××物质被氧化(如Na2SO3);促进××物质水解(如AlCl3)
蒸发、反应时的气体氛围 抑制××离子的水解(如加热蒸发AlCl3溶液时,需在HCl气流中进行;加热MgCl2·6H2O得MgCl2时,也需在HCl气流中进行)
检 测 反 馈
2
1
3
1 [2024南京调研]NaClO溶液处理含氨氮废水(pH为6.0~7.0)。室温下,分别取200 mL预处理后的废水,将初始pH调节至不同值,加入等量NaClO溶液,30分钟后检测剩余氨氮浓度。不同初始pH对NaClO氧化脱除氨氮效果的影响如图1所示,不同初始pH对应反应结束后的pH如图2所示。
图1
图2
2
1
3
(1) NaClO将废水中NH3氧化为无污染气体,反应的化学方程式为_______________________________________,实验中NaClO溶液的实际投入量大于理论计算量,其原因是______________________________。
(2) 处理后的废水pH在6.0~9.0之间才能排放。NaClO溶液处理含氨氮废水初始pH设置为7.0而不是2.0的原因是_________________________ ________________________。
2NH3+3NaClO===N2↑+3H2O+3NaCl
NaClO(或HClO)不稳定,易分解
pH为7.0时氨氮去除率高且
调节pH所需的酸更少
2
1
3
【解析】 (1) 由题意先写出NH3+NaClO——N2+NaCl,再根据得失电子守恒写出2NH3+3NaClO——N2+3NaCl,最后根据原子守恒配平。由于反应肯定是控制在一定时间内,反应物不能反应完全,为使NH3在一定时间内尽可能被氧化去除,故应增大NaClO的实际投入量;另外次氯酸盐或次氯酸易分解,也是增大其投入量的原因之一。(2) 由图1知,当pH=7.0时氨氮去除率更高,由图2知,当pH=7.0或2.0时,反应后的废水都符合排放标准,但调节初始pH=2.0所需的酸更多。
2
1
3
(1) 从反应后的混合物中获得较高产率的NaFeY·3H2O粗品的实验操作是__________________________________,过滤,水洗,干燥。检验NaFeY·3H2O是否洗净的试剂是________________________。
冷却至室温,加入乙醇
AgNO3溶液和稀硝酸
2
1
3
(2) 保持其他条件不变,乙二胺四乙酸铁钠的产率随反应液pH的变化如图所示。pH过低或过高产品产率均减小的主要原因是____________ ________________________________________________________________________________________________________。
pH过低,H4Y电离出的Y4-浓度小(或pH过低,H4Y在水中溶出量小),pH过高,Fe3+转为Fe(OH)3,溶液中Fe3+浓度减小
2
3
1
3 [2024宿迁调研]燃煤烟气中含有大量SO2和NO。某实验室模拟“软锰矿浆同步脱硫脱硝技术”并制备MnSO4·H2O,部分流程如下:
已知:①软锰矿(主要成分为MnO2,另含有少量Fe2O3、CaO、SiO2等杂质);
②Ksp(MnF2)=1.6×10-3;Ksp(CaF2)=8.0×10-11;
2
3
【解析】 (2) 除气时,一定量的O3可将NO转化为NO2,而NO2易与水反应,NO难溶于水,这样会提高NO的脱除率。
1
(1) ①“浸锰”过程,SO2发生的主要化学方程式为______________ ______________。
②滤渣Ⅰ的主要成分为__________________(填化学式)。
(2) “除气”过程,烟气中混入一定量O3可提高NO脱除率,其可能的原因是_______________________________________________________ ______。
MnO2+SO2
===MnSO4
SiO2、CaSO4
O3可将NO氧化为在水中溶解性好的NO2;NO2氧化性强于
NO
谢谢观看
Thank you for watching
同课章节目录
