破难点1 陌生情境下方程式的书写 课件 (共23张PPT)2025届高考化学二轮复习
文档属性
| 名称 | 破难点1 陌生情境下方程式的书写 课件 (共23张PPT)2025届高考化学二轮复习 |

|
|
| 格式 | pptx | ||
| 文件大小 | 1.6MB | ||
| 资源类型 | 教案 | ||
| 版本资源 | 通用版 | ||
| 科目 | 化学 | ||
| 更新时间 | 2025-02-22 00:00:00 | ||
图片预览





文档简介
(共23张PPT)
主题2
无机物转化与应用
破难点1 陌生情境下方程式的书写
内容索引
难点精讲
检测反馈
难 点 精 讲
难点1 常见氧化剂、还原剂及其产物的预测与判断
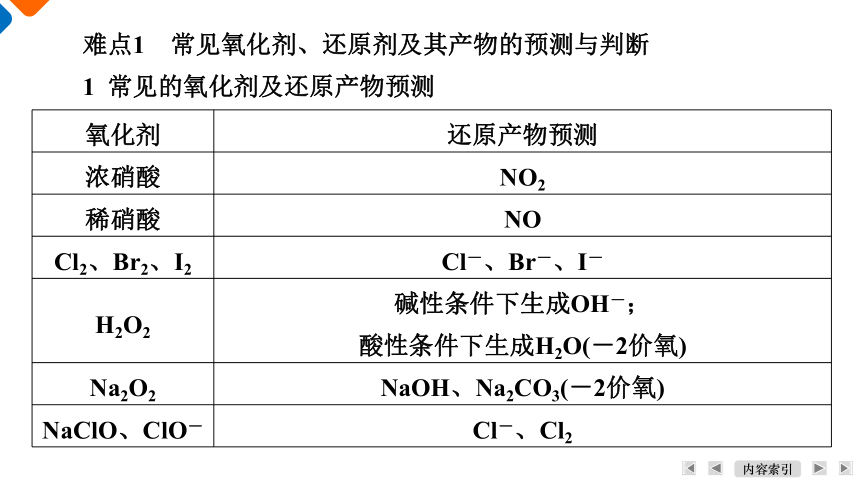
1 常见的氧化剂及还原产物预测
氧化剂 还原产物预测
浓硝酸 NO2
稀硝酸 NO
Cl2、Br2、I2 Cl-、Br-、I-
H2O2 碱性条件下生成OH-;
酸性条件下生成H2O(-2价氧)
Na2O2 NaOH、Na2CO3(-2价氧)
NaClO、ClO- Cl-、Cl2
氧化剂 还原产物预测
NaClO3 Cl2、ClO2、Cl-
KMnO4 酸性条件下生成Mn2+
K2Cr2O7(酸性) 酸性条件下生成Cr3+
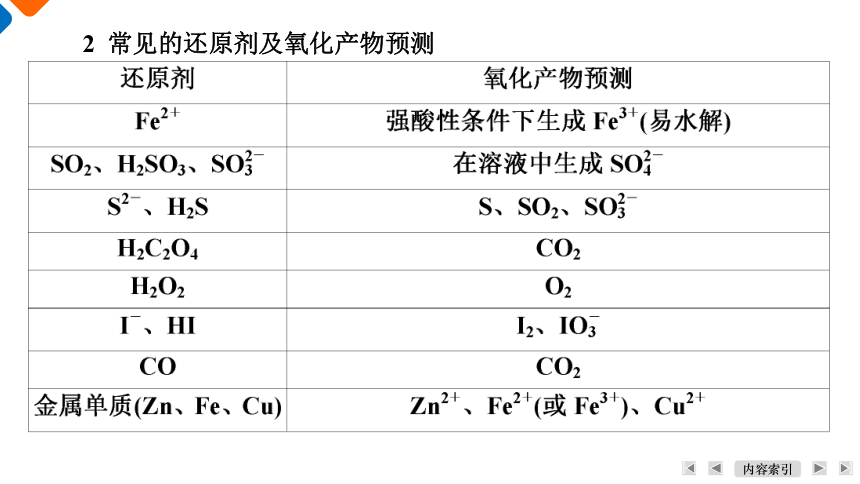
2 常见的还原剂及氧化产物预测
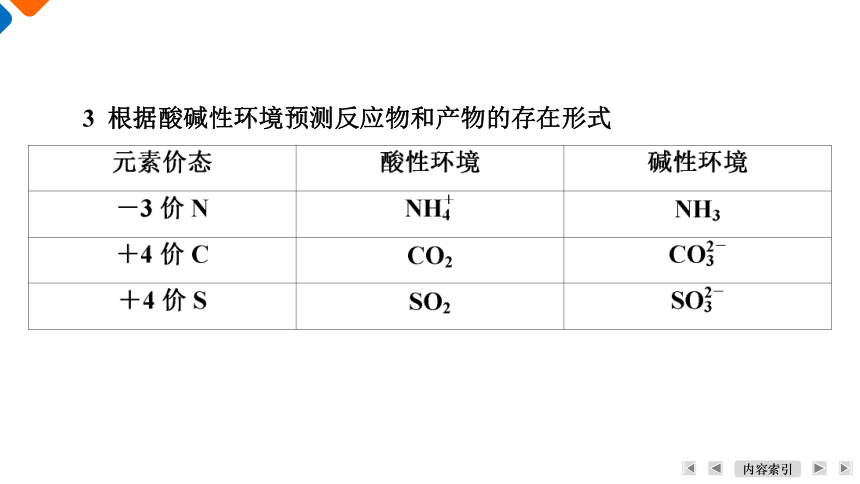
3 根据酸碱性环境预测反应物和产物的存在形式
4 歧化反应与归中反应
(1) 卤素单质“碱性歧化,酸性归中”。
难点2 陌生氧化还原反应化学(或离子)方程式的书写
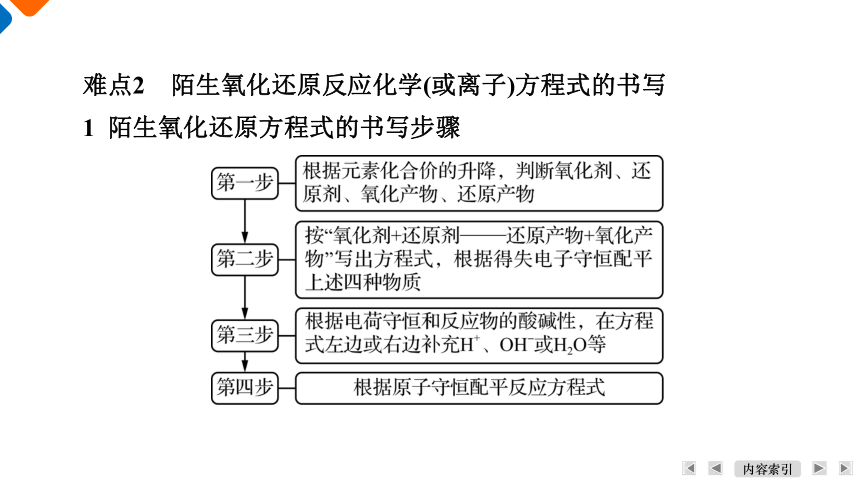
1 陌生氧化还原方程式的书写步骤
2 陌生氧化还原方程式的常考题型
(1) 陈述信息型
碱性条件下,KClO饱和溶液与Fe(NO3)3饱和溶液反应可制备K2FeO4,写出该反应的离子方程式:______________________________ _______________________。
(2) 流程图型
[2024连云港、淮安一模]以含钼(Mo)废催化剂(含MoS2,以及Al2O3、Fe2O3、CuO等)为原料制备MoO3,其过程表示如下:
【解析】 碱性条件下足量的空气能把-2价硫氧化为+6价硫酸盐,可以与工业脱硫对应。
焙烧时,将废催化剂和足量NaOH固体置于焙烧炉中,通入足量空气加热至750 ℃充分反应。焙烧过程中MoS2转化为Na2MoO4的化学方程式为_________________________________________________________。
(3) 反应机理图型
在酸性和催化剂的作用下,黄铁矿(主要成分为FeS2)可发生如图所示的转化。
4Fe(NO)2++
O2+4H+===4Fe3++4NO+2H2O
检 测 反 馈
2
4
1
3
1 (1) [2025扬州开学考试]Li2CO3和Co3O4混合后,在空气中高温加热可以制备锂电池的正极材料LiCoO2,写出反应的化学方程式:_______________________________________________。
2
4
1
3
(3) [2025南京开学考试]氧化亚铜(Cu2O)主要用于制造杀虫剂、分析试剂和红色玻璃等。Cu2O在酸性溶液中歧化为二价铜离子和铜单质。以黄铜矿(主要成分为CuFeS2,含有杂质SiO2)为原料制取Cu2O的一种工艺流程如图所示。写出“浸泡”时CuFeS2发生反应的离子方程式:______________________________________。
CuFeS2+4Fe3+===5Fe2++Cu2++2S
2
4
1
3
图1
2
4
1
3
(2) 活性自由基HO·可有效除去废水中的苯酚等有机污染物。H2O2在Fe3O4表面产生HO·除去废水中的苯酚的原理如图2所示。酸性条件下产生HO·的反应(1分子H2O2产生1个HO·)的离子方程式为________________ _____________________________。HO·除去苯酚反应的化学方程式为_____________________________________________。
图2
H++H2O2+
Fe2+===H2O+Fe3++HO·
4HO·+C6H5OH+H2O===3CH3COOH
2
4
3
1
3 (1) [2024盐城、南京期末]V2O5的回收。回收V2O5的过程可表示如下:
酸浸过程中,V2O5转化成VO2+,该反应的离子方程式为______________________________________________。
(2) [2024泰州期末] 实验室制备氧钒(Ⅳ)碱式碳酸铵晶体,过程如下:
①“还原”步骤中生成N2,反应的化学方程式为________________ _________________________________。
2V2O5+N2H4+
8HCl===N2↑+4VOCl2+6H2O
2
4
3
1
②V2O5可溶于强酸强碱。常温下,不同pH、不同钒元素浓度时,+5价V存在形态如图所示。
将0.01 mol V2O5溶解在200 mL烧碱溶液中,剩余溶液的c(OH-)=0.01 mol/L,反应的离子方程式为______________________________。
2
4
3
1
2
4
3
1
(2) [2023苏州调研]氢气是一种理想的绿色清洁能源,氢气的制取是氢能源利用领域的研究热点。用氧缺位铁酸铜(CuFe2O4-x)作催化剂,利用太阳能热化学循环分解H2O可制H2。氧缺位铁酸铜通过两步反应分解水制氢。已知第二步反应为2CuFe2O4===2CuFe2O4-x+xO2↑,则第一步反应的化学方程式为_________________________________________。
+4OH-
CuFe2O4-x+xH2O===CuFe2O4+xH2↑
2
4
3
1
(3) [2023盐城调研]向SrCl2溶液中加入适量NH4HCO3溶液,微热、过滤、洗涤得到高纯度SrCO3。写出沉淀过程中发生反应的化学方程式:_________________________________________________________。
rCl2+2NH4HCO3===SrCO3↓+2NH4Cl+CO2↑+H2O
谢谢观看
Thank you for watching
主题2
无机物转化与应用
破难点1 陌生情境下方程式的书写
内容索引
难点精讲
检测反馈
难 点 精 讲
难点1 常见氧化剂、还原剂及其产物的预测与判断
1 常见的氧化剂及还原产物预测
氧化剂 还原产物预测
浓硝酸 NO2
稀硝酸 NO
Cl2、Br2、I2 Cl-、Br-、I-
H2O2 碱性条件下生成OH-;
酸性条件下生成H2O(-2价氧)
Na2O2 NaOH、Na2CO3(-2价氧)
NaClO、ClO- Cl-、Cl2
氧化剂 还原产物预测
NaClO3 Cl2、ClO2、Cl-
KMnO4 酸性条件下生成Mn2+
K2Cr2O7(酸性) 酸性条件下生成Cr3+
2 常见的还原剂及氧化产物预测
3 根据酸碱性环境预测反应物和产物的存在形式
4 歧化反应与归中反应
(1) 卤素单质“碱性歧化,酸性归中”。
难点2 陌生氧化还原反应化学(或离子)方程式的书写
1 陌生氧化还原方程式的书写步骤
2 陌生氧化还原方程式的常考题型
(1) 陈述信息型
碱性条件下,KClO饱和溶液与Fe(NO3)3饱和溶液反应可制备K2FeO4,写出该反应的离子方程式:______________________________ _______________________。
(2) 流程图型
[2024连云港、淮安一模]以含钼(Mo)废催化剂(含MoS2,以及Al2O3、Fe2O3、CuO等)为原料制备MoO3,其过程表示如下:
【解析】 碱性条件下足量的空气能把-2价硫氧化为+6价硫酸盐,可以与工业脱硫对应。
焙烧时,将废催化剂和足量NaOH固体置于焙烧炉中,通入足量空气加热至750 ℃充分反应。焙烧过程中MoS2转化为Na2MoO4的化学方程式为_________________________________________________________。
(3) 反应机理图型
在酸性和催化剂的作用下,黄铁矿(主要成分为FeS2)可发生如图所示的转化。
4Fe(NO)2++
O2+4H+===4Fe3++4NO+2H2O
检 测 反 馈
2
4
1
3
1 (1) [2025扬州开学考试]Li2CO3和Co3O4混合后,在空气中高温加热可以制备锂电池的正极材料LiCoO2,写出反应的化学方程式:_______________________________________________。
2
4
1
3
(3) [2025南京开学考试]氧化亚铜(Cu2O)主要用于制造杀虫剂、分析试剂和红色玻璃等。Cu2O在酸性溶液中歧化为二价铜离子和铜单质。以黄铜矿(主要成分为CuFeS2,含有杂质SiO2)为原料制取Cu2O的一种工艺流程如图所示。写出“浸泡”时CuFeS2发生反应的离子方程式:______________________________________。
CuFeS2+4Fe3+===5Fe2++Cu2++2S
2
4
1
3
图1
2
4
1
3
(2) 活性自由基HO·可有效除去废水中的苯酚等有机污染物。H2O2在Fe3O4表面产生HO·除去废水中的苯酚的原理如图2所示。酸性条件下产生HO·的反应(1分子H2O2产生1个HO·)的离子方程式为________________ _____________________________。HO·除去苯酚反应的化学方程式为_____________________________________________。
图2
H++H2O2+
Fe2+===H2O+Fe3++HO·
4HO·+C6H5OH+H2O===3CH3COOH
2
4
3
1
3 (1) [2024盐城、南京期末]V2O5的回收。回收V2O5的过程可表示如下:
酸浸过程中,V2O5转化成VO2+,该反应的离子方程式为______________________________________________。
(2) [2024泰州期末] 实验室制备氧钒(Ⅳ)碱式碳酸铵晶体,过程如下:
①“还原”步骤中生成N2,反应的化学方程式为________________ _________________________________。
2V2O5+N2H4+
8HCl===N2↑+4VOCl2+6H2O
2
4
3
1
②V2O5可溶于强酸强碱。常温下,不同pH、不同钒元素浓度时,+5价V存在形态如图所示。
将0.01 mol V2O5溶解在200 mL烧碱溶液中,剩余溶液的c(OH-)=0.01 mol/L,反应的离子方程式为______________________________。
2
4
3
1
2
4
3
1
(2) [2023苏州调研]氢气是一种理想的绿色清洁能源,氢气的制取是氢能源利用领域的研究热点。用氧缺位铁酸铜(CuFe2O4-x)作催化剂,利用太阳能热化学循环分解H2O可制H2。氧缺位铁酸铜通过两步反应分解水制氢。已知第二步反应为2CuFe2O4===2CuFe2O4-x+xO2↑,则第一步反应的化学方程式为_________________________________________。
+4OH-
CuFe2O4-x+xH2O===CuFe2O4+xH2↑
2
4
3
1
(3) [2023盐城调研]向SrCl2溶液中加入适量NH4HCO3溶液,微热、过滤、洗涤得到高纯度SrCO3。写出沉淀过程中发生反应的化学方程式:_________________________________________________________。
rCl2+2NH4HCO3===SrCO3↓+2NH4Cl+CO2↑+H2O
谢谢观看
Thank you for watching
同课章节目录
