微主题2 物质的性质、用途与转化 课件 (共73张PPT) 2025届高考化学二轮复习
文档属性
| 名称 | 微主题2 物质的性质、用途与转化 课件 (共73张PPT) 2025届高考化学二轮复习 |

|
|
| 格式 | pptx | ||
| 文件大小 | 4.1MB | ||
| 资源类型 | 教案 | ||
| 版本资源 | 通用版 | ||
| 科目 | 化学 | ||
| 更新时间 | 2025-02-22 00:00:00 | ||
图片预览










文档简介
(共73张PPT)
主题2
无机物转化与应用
微主题2 物质的性质、用途与转化
内容索引
核心串讲
体系建构
名卷优选
基础回归
检测反馈
基 础 回 归
1 判断下列物质的性质和用途是否有对应关系,若无对应关系,需简要说明理由。
(1) FeCl3溶液具有酸性,可用于制作铜质印刷线路板。
__________________________________________________________________________________________________。
(2) 酒精能使蛋白质变性,可用于医用消毒。______________。
(3) 葡萄糖能与银氨溶液发生银镜反应,可用于检验糖尿病。______________。
无对应关系。Fe3+具有氧化性,能与Cu反应,所以FeCl3溶液可用于制作铜质印刷电路板,与其酸性无关
有对应关系
有对应关系
2 判断下列物质在指定条件下的转化是否正确,错误的请改正。
×
将NO改为NO2
√
√
3 指出下列物质转化的条件。
(1) MgCl2·6H2O―→MgCl2
____________________。
(2) Fe―→Fe3O4
________________________________。
(3) NaOH―→NaHCO3
___________________________________。
HCl氛围,加热
氧气、点燃(或水蒸气、高温)
向NaOH溶液中通入过量CO2
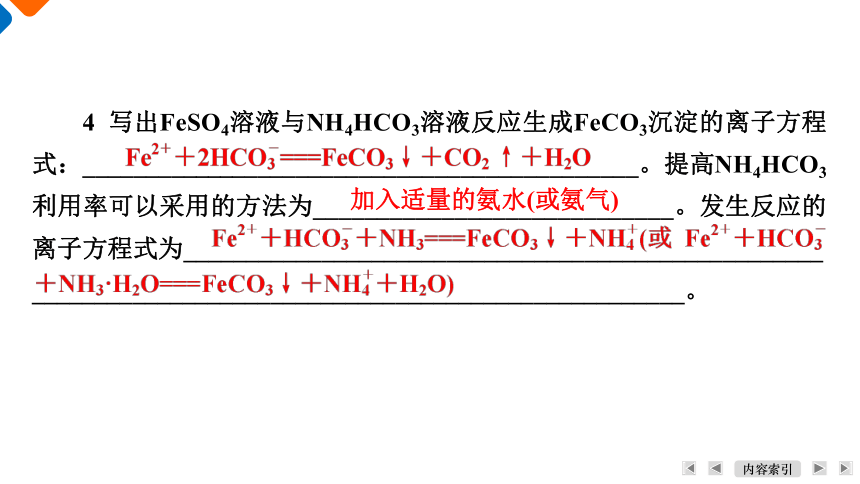
4 写出FeSO4溶液与NH4HCO3溶液反应生成FeCO3沉淀的离子方程式:____________________________________________。提高NH4HCO3利用率可以采用的方法为____________________________。发生反应的离子方程式为___________________________________________________ ____________________________________________________。
加入适量的氨水(或氨气)
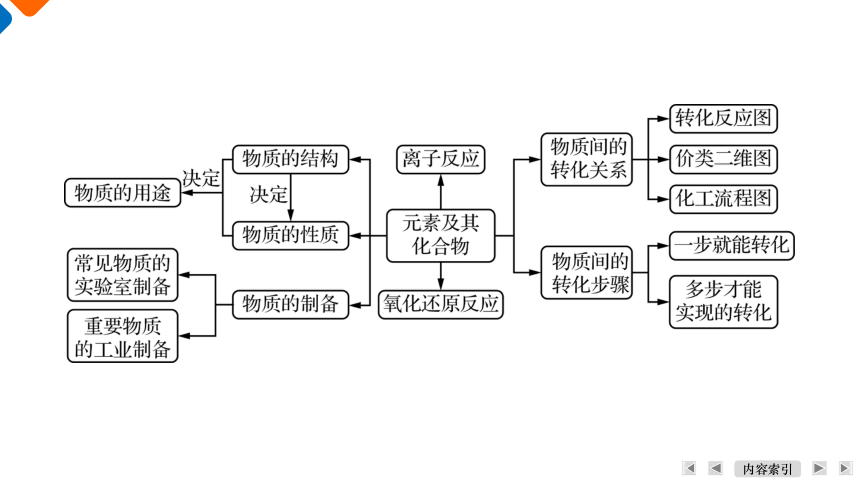
体 系 建 构
名 卷 优 选
1 [2023江苏卷]下列物质的结构与性质或物质的性质与用途具有对应关系的是( )
A. H2具有还原性,可作为氢氧燃料电池的燃料
B. 氨极易溶于水,液氨可用作制冷剂
C. H2O分子之间形成氢键,H2O(g)的热稳定性比H2S(g)的高
D. N2H4中的N原子与H+形成配位键,N2H4具有还原性
A
【解析】 液氨可用作制冷剂,主要原因是液氨汽化吸热,和氨极易溶于水无关,B错误;H2O(g)的热稳定性比H2S(g)高,主要原因是H—O的键能高于H—S,和H2O分子之间形成氢键无关,C错误;N2H4具有还原性在于N本身可以失电子,N2H4中无配位键,D错误。
2 [2022江苏卷]下列物质的性质与用途具有对应关系的是( )
A. 石墨能导电,可用作润滑剂
B. 单晶硅熔点高,可用作半导体材料
C. 青铜的熔点比纯铜低、硬度大,古代用青铜铸剑
D. 含铅化合物颜色丰富,可用作电极材料
【解析】 石墨是混合型晶体,质软,可用作润滑剂,A错误;单晶硅可用作半导体材料,与空穴可传递电子有关,与熔点高无关,B错误;青铜是铜合金,熔点比纯铜低、硬度大,易于锻造,古代用青铜铸剑,C正确;含铅化合物可在正极得到电子发生还原反应,所以可用作电极材料,与含铅化合物颜色丰富无关,D错误。
C
3 [2021江苏卷]下列有关物质的性质与用途不具有对应关系的是( )
A. 铁粉能与O2反应,可用作食品保存的吸氧剂
B. 纳米Fe3O4能与酸反应,可用作铁磁性材料
C. FeCl3具有氧化性,可用于腐蚀印刷电路板上的Cu
D. 聚合硫酸铁能水解并形成胶体,可用于净水
【解析】 因为铁粉能与O2反应,所以可用作食品保存的吸氧剂,A正确;纳米Fe3O4具有磁性,可用作铁磁性材料,B错误;FeCl3溶液与Cu反应生成FeCl2和CuCl2,主要利用其氧化性,C正确;聚合硫酸铁能水解并形成胶体,具有吸附性,可用于净水,D正确。
B
考向2 氧化还原反应 离子反应
4 写出下列相关反应的化学(或离子)方程式。
(1) [2024江苏卷]①向NdCl3溶液中加入(NH4)2CO3溶液,Nd3+可转化为Nd(OH)CO3沉淀。该反应的离子方程式为______________________ _____________________________。
②在AgCl沉淀中埋入铁圈并压实,加入足量0.5 mol/L盐酸后静置,充分反应得到Ag。铁将AgCl转化为单质Ag的化学方程式为______________________________。
Fe+2AgCl===FeCl2+2Ag
②将一定物质的量浓度的NO、O2、NH3(其余为N2)气体匀速通过装有V2O5-WO3/TiO2催化剂的反应器,测得NO的转化率随温度的变化如图所示。反应温度高于380 ℃,NO的转化率下降,除因为进入反应器的
NO被还原的量减少外,还有______________________________________ (用化学方程式表示)。
2CeO2+H2O2+6H+===2Ce3++O2↑+4H2O
【解析】 (2) ②根据题意可知,NO的转化率下降是由反应导致,由于主反应的速率减小,故只能是发生副反应生成NO,此环境中氨气、氮气均可与氧气反应生成NO,但氨气与氧气反应更容易,故得出结论。
5 氧化还原反应中的相关计算。
(1) [2024江苏卷]利用铁及其氧化物循环制氢,原理如图所示。反应器Ⅰ中化合价发生改变的元素有________________;含CO和H2各1 mol
的混合气体通过该方法制氢,理论上可获得_______mol H2。
(2) [2023江苏卷改编]金属硫化物(MxSy)催化反应:CH4(g)+2H2S(g) ===CS2 (g)+4H2 (g),该反应中每消耗1 mol H2S,转移电子的数目约为__________________。
C、H、Fe
4×6.02×1023
3×6.02×1023
考向3 常见无机物间的转化
6 [2024江苏卷]在给定条件下,下列制备过程涉及的物质转化均可实现的是( )
A
【解析】 电解氯化钠溶液可以得到H2和Cl2,H2在Cl2中安静的燃烧,生成HCl,A正确;氢氧化镁和盐酸反应可以得到氯化镁溶液,但是电解氯化镁溶液得不到Mg,电解熔融MgCl2才能得到Mg,B错误;纯碱工业是在饱和食盐水中依次通入NH3和CO2,先得到NaHCO3,然后NaHCO3受热分解为Na2CO3,C错误;工业制备硫酸,首先是黄铁矿和氧气反应生成SO2,其次是SO2催化氧化为SO3,最后是SO3和H2O反应生成H2SO4,SO2和水反应生成H2SO3,D错误。
7 [2023江苏卷]氮及其化合物的转化具有重要应用。下列说法不正确的是( )
【解析】 NO不能与H2O反应生成HNO3,B错误。
B
8 [2022江苏卷]氮及其化合物的转化具有重要应用。下列说法不正确的是( )
A. 自然固氮、人工固氮都是将N2转化为NH3
B. 侯氏制碱法以H2O、NH3、CO2、NaCl为原料制备NaHCO3和NH4Cl
C. 工业上通过NH3催化氧化等反应过程生产HNO3
D. 多种形态的氮及其化合物间的转化形成了自然界的“氮循环”
A
考向1 物质的性质与用途对应关系
1 [2024南京二模]下列物质结构与性质或性质与用途不具有对应关系的是( )
A. MgCl2易溶于水,可用于制作豆腐的凝固剂
B. MgO是碱性氧化物,可用于吸收燃煤烟气中的SO2
C. NaCl晶体中离子间存在较强的离子键,NaCl晶体的硬度较大
A
【解析】 N2与O2均为分子晶体,一般来说,相对分子质量越高,熔、沸点越高,与化学键无关,A错误;H2O2与H2O分子间可以形成氢键,是其能与水以任意比互溶的重要原因,B错误;O3氧化性大于O2,可用于饮用水的杀菌消毒,D错误。
2 [2024南京学情调研]下列物质结构与性质或物质性质与用途具有对应关系的是( )
A. N2分子中含共价三键,N2的沸点比O2的低
B. H2O2分子之间形成氢键,可与水以任意比例互溶
C. O2具有氧化性,可作为燃料电池的氧化剂
D. O3的溶解度比O2大,可用于饮用水消毒杀菌
C
【解析】 Fe与O2反应放热,故可作暖贴,A正确;Fe2O3为红棕色粉末,故可作红色颜料,B错误;FeCl3溶液氧化Cu时,FeCl3表现氧化性,C错误;FeS中+2价铁具有还原性,可以与六价铬[Cr(Ⅵ)]发生氧化还原反应,从而除去六价铬[Cr(Ⅵ)],D错误。
3 [2024苏州期初]下列有关铁及其化合物的性质与用途具有对应关系的是( )
A. 铁粉遇空气放热,可用于制作暖贴
B. Fe2O3能与酸反应,可用于制作红色颜料
C. FeCl3溶液显酸性,可用于腐蚀印刷电路板上的铜
D. FeS难溶于水,可用于去除废水中微量六价铬[Cr(Ⅵ)]
A
考向2 氧化还原反应 离子反应
4 [2024南通、泰州等六市一调改编]下列化学反应表示不正确的是( )
A. FeS2与足量稀盐酸反应:FeS2+4H+=== Fe2++2H2S↑
【解析】 离子方程式的电荷不守恒,A错误。
A
5 写出下列相关反应的化学(或离子)方程式。
(1) [2024南通、泰州等八市三调]Cu2Te与NaOH、NaClO3反应生成Cu2O、Na2TeO3、NaCl的离子方程式为____________________________ ________________________。
(2) [2024南京二模]①NaClO2的制备。一种制备NaClO2的过程可表示如下:
“反应2”的化学方程式为____________________________________ ________________________。
2ClO2+H2O2+2NaOH===2NaClO2
+O2+2H2O
NH2COONH4+
3NiO===3Ni+N2↑+3H2O+CO2↑
6 氧化还原反应中的相关计算。
8
4×6.02×1023
考向3 常见无机物间的转化
7 [2024苏锡常镇二调]在指定条件下,下列工业制备流程中涉及的物质转化关系不正确的是( )
B
8 [2024苏州期末]硫及其化合物的转化形态丰富。下列说法正确的是( )
D
【解析】 SO2过量,应该生成NH4HSO3,A错误;FeS2不能一步转化为SO3,B错误;O原子不守恒,电荷也不守恒,C错误。
核 心 串 讲
核心1 物质之间的转化关系
1 价类二维图
(5) 钠、镁、铝及其化合物
(6) 铁、铜及其化合物
2 常见物质间转化关系
(1) 连续氧化反应(注:不一定是制备路线)
(2) 三角转化关系
名称 原理(主要的离子或化学方程式) 说明
所加除杂试剂一般要过量,且易除去。
Na2CO3和 BaCl2加入顺序:________________________;
过滤放在加盐酸前还是加盐酸后:__________________
3 重要的化工生产
(1) 以海水为资源的化工生产
先加BaCl2后加Na2CO3
过滤放在加盐酸前
名称 原理(主要的离子或化学方程式) 说明
②氯碱工业 氯碱工业的化学方程式为_____________________________________________________
阳离子交换膜的作用是_______________________________________________________________________________________;
能否使用阴离子交换膜?________
防止氢气和氯气混合反应,防止OH-迁移到左极室与氯气反应,让Na+迁移到右极室产生NaOH
不能
先通氨气后通二氧化碳
名称 原理(主要的离子或化学方程式) 说明
④电解熔融的氯化钠制钠 ____________________________
_______为阳极,_____为阴极;电解的是__________________
石墨
铁
熔融的NaCl
Cl2+2Br-===2Cl-+Br2
挥发性
4I-+4H++O2===2I2+2H2O
坩埚
升华
(2) 以空气为资源的化工生产
名称 原理(主要的离子或化学方程式) 说明
①合成氨 _________________________ 从空气中获得氮气的方法:________________________________________
②工业制硝酸 主要反应有_____________________ _________、____________________、_______________________________
液化空气后升高温度,首先分离得到氮气
+6H2O
2NO+O2===2NO2
3NO2+H2O===NO+2HNO3
(3) 以矿石为资源的化工生产
名称 原理(主要的化学方程式) 说明
①工业制硫酸 沸腾炉:__________________ _____________、 接触室:__________________ ______、 吸收塔:__________________
三步反应都是________(填“放热”或“吸热”)反应;为了充分利用能源,进入接触室的气体要净化、预热;用_________________吸收SO3,得到发烟硫酸,再稀释成不同浓度的工业产品
2Fe2O3+8SO2
2SO3
SO3+H2O===H2SO4
放热
98.3%的浓硫酸
Al2O3+2NaOH+3H2O===2Na[Al(OH)4]
Na[Al(OH)4]+CO2===Al(OH)3↓+NaHCO3
CO
核心2 离子方程式书写
1 审清题意“三注意”
(1) 反应环境:如介质的酸碱性。
(2) 试剂滴加顺序,不同的滴加顺序,过程中先后可能会发生不同的反应。
(3) 反应过程中反应物之间量的关系,不同的比例关系可能会发生不同的反应。如:
2 ★与量有关的离子方程式书写方法——“少定多变”法
(1) “少定”就是把相对量较少的物质定为“1 mol”,若少量物质有两种或两种以上离子参加反应,则参加反应的离子的物质的量之比与原物质组成比相符。
(2) “多变”就是过量的反应物离子的化学计量数根据反应实际需求量来确定,不受化学式中的比例制约。如:向Ca(HCO3)2溶液中加入过量NaOH溶液,离子方程式的书写方法如下:
检 测 反 馈
2
4
1
3
【解析】 甲烷在高温下分解得到炭黑,与甲烷的热值(J/kg)大小无关,B错误。
1 [2024无锡期末]下列物质的性质与其应用不具有对应关系的是( )
A. 锂的容量密度(mAh/g)高:用作电池负极材料
B. 甲烷的热值(J/kg)高:用于工业制备炭黑
C. 葡萄糖具有还原性:用于玻璃等材料表面化学覆银
D. 氢气在高温下具有还原性:用于工业绿色化炼铁
5
B
2
4
1
3
2 [2023南通如皋适应性考试]铁的单质及许多化合物均具有重要用途。K2FeO4可用作净水剂,K2FeO4在水中不稳定,会生成Fe(OH)3胶体,碱性条件下KClO的氧化性比K2FeO4的大。下列有关铁及其化合物的相关转化,在指定条件下能实现的是( )
5
D
2
4
1
3
【解析】 在高温下,铁与水蒸气反应生成Fe3O4,A错误;K2FeO4在水中反应,铁元素的化合价降低,则水中应是氧元素的化合价升高,不应该是氢元素的化合价降低,B错误;Fe2O3与水不反应,C错误。
5
2
4
3
1
3 [2024苏州期末改编]含锂物质在能源方面有重要应用。锂在氧气中燃烧与Mg相似,其燃烧热为299 kJ/mol。锂与氮气反应得到的Li3N可用作储氢材料。锂-空气电池是一种二次电池,放电时主要产物为Li2O2,充电时阴极产物易形成固态枝晶,导致电池短路。目前应用广泛的是锂离子电池,例如,磷酸铁锂电池充电时,锂离子由LiFePO4电极迁移至石墨电极形成LiCx,LiFePO4的前体FePO4可由NH4H2PO4、FeSO4、H2O2在pH=2的条件下反应制得。下列化学反应表示正确的是( )
5
A
2
4
3
【解析】 Fe和H2O(g)反应生成Fe3O4和H2,B错误;电池充电时,阳极为失电子的一极,C错误;溶液的pH=2,溶液呈酸性,故离子方程式中不能出现OH-,D错误。
1
5
2
4
3
1
4 [2023南京、盐城期末]无水FeCl3常用作芳烃氯代反应的催化剂。以废铁屑(主要成分为Fe,还有少量Fe2O3、C和SiO2)制取无水FeCl3的流程如图所示。下列说法正确的是 ( )
A. “过滤”所得滤液中大量存在的离子有:Fe3+、Fe2+、H+、Cl-
B. “氧化”时可使用新制氯水作氧化剂
C. 将“氧化”后的溶液蒸干可获得FeCl3·6H2O
D. “脱水”时加入SOCl2能抑制FeCl3的水解,原因是SOCl2与水反应生成H2SO4和HCl
5
B
2
4
3
【解析】 废铁屑的主要成分为Fe,Fe和Fe3+反应生成Fe2+,“过滤”所得滤液中大量存在的离子有Fe2+、H+、Cl-,A错误;Cl2具有氧化性,且不引入新杂质,“氧化”时可使用新制氯水作氧化剂,B正确;Fe3+水解生成氢氧化铁,且蒸干会导致固体失H2O,不能将“氧化”后的溶液蒸干来获得FeCl3·6H2O,C错误;SOCl2与水反应生成SO2和HCl,D错误。
1
5
2
3
1
5 (1) [2024连云港期末]将CoCl2·2H2O和活性炭(催化剂)加入三颈瓶中,然后再依次通过滴液漏斗缓慢滴加NH4Cl和浓氨水混合溶液、H2O2溶液,控制温度不超过60 ℃充分反应,冷却后过滤。三颈瓶中制得
[Co(NH3)6]3+的离子方程式为_____________________________________
______________________________________________________________________________________。
5
4
2
3
【解析】 (2) 在该过程中,N元素由0价降低为-3价,故每生成1 mol NH3,转移3 mol电子。
1
5
4
(2) [2024无锡期末]以稀有金属为催化剂(镧、钌和锆)合成氨的机理如图所示。由N2和H2合成1 mol氨气,转移电子的物质的量为__________。
3 mol
谢谢观看
Thank you for watching
主题2
无机物转化与应用
微主题2 物质的性质、用途与转化
内容索引
核心串讲
体系建构
名卷优选
基础回归
检测反馈
基 础 回 归
1 判断下列物质的性质和用途是否有对应关系,若无对应关系,需简要说明理由。
(1) FeCl3溶液具有酸性,可用于制作铜质印刷线路板。
__________________________________________________________________________________________________。
(2) 酒精能使蛋白质变性,可用于医用消毒。______________。
(3) 葡萄糖能与银氨溶液发生银镜反应,可用于检验糖尿病。______________。
无对应关系。Fe3+具有氧化性,能与Cu反应,所以FeCl3溶液可用于制作铜质印刷电路板,与其酸性无关
有对应关系
有对应关系
2 判断下列物质在指定条件下的转化是否正确,错误的请改正。
×
将NO改为NO2
√
√
3 指出下列物质转化的条件。
(1) MgCl2·6H2O―→MgCl2
____________________。
(2) Fe―→Fe3O4
________________________________。
(3) NaOH―→NaHCO3
___________________________________。
HCl氛围,加热
氧气、点燃(或水蒸气、高温)
向NaOH溶液中通入过量CO2
4 写出FeSO4溶液与NH4HCO3溶液反应生成FeCO3沉淀的离子方程式:____________________________________________。提高NH4HCO3利用率可以采用的方法为____________________________。发生反应的离子方程式为___________________________________________________ ____________________________________________________。
加入适量的氨水(或氨气)
体 系 建 构
名 卷 优 选
1 [2023江苏卷]下列物质的结构与性质或物质的性质与用途具有对应关系的是( )
A. H2具有还原性,可作为氢氧燃料电池的燃料
B. 氨极易溶于水,液氨可用作制冷剂
C. H2O分子之间形成氢键,H2O(g)的热稳定性比H2S(g)的高
D. N2H4中的N原子与H+形成配位键,N2H4具有还原性
A
【解析】 液氨可用作制冷剂,主要原因是液氨汽化吸热,和氨极易溶于水无关,B错误;H2O(g)的热稳定性比H2S(g)高,主要原因是H—O的键能高于H—S,和H2O分子之间形成氢键无关,C错误;N2H4具有还原性在于N本身可以失电子,N2H4中无配位键,D错误。
2 [2022江苏卷]下列物质的性质与用途具有对应关系的是( )
A. 石墨能导电,可用作润滑剂
B. 单晶硅熔点高,可用作半导体材料
C. 青铜的熔点比纯铜低、硬度大,古代用青铜铸剑
D. 含铅化合物颜色丰富,可用作电极材料
【解析】 石墨是混合型晶体,质软,可用作润滑剂,A错误;单晶硅可用作半导体材料,与空穴可传递电子有关,与熔点高无关,B错误;青铜是铜合金,熔点比纯铜低、硬度大,易于锻造,古代用青铜铸剑,C正确;含铅化合物可在正极得到电子发生还原反应,所以可用作电极材料,与含铅化合物颜色丰富无关,D错误。
C
3 [2021江苏卷]下列有关物质的性质与用途不具有对应关系的是( )
A. 铁粉能与O2反应,可用作食品保存的吸氧剂
B. 纳米Fe3O4能与酸反应,可用作铁磁性材料
C. FeCl3具有氧化性,可用于腐蚀印刷电路板上的Cu
D. 聚合硫酸铁能水解并形成胶体,可用于净水
【解析】 因为铁粉能与O2反应,所以可用作食品保存的吸氧剂,A正确;纳米Fe3O4具有磁性,可用作铁磁性材料,B错误;FeCl3溶液与Cu反应生成FeCl2和CuCl2,主要利用其氧化性,C正确;聚合硫酸铁能水解并形成胶体,具有吸附性,可用于净水,D正确。
B
考向2 氧化还原反应 离子反应
4 写出下列相关反应的化学(或离子)方程式。
(1) [2024江苏卷]①向NdCl3溶液中加入(NH4)2CO3溶液,Nd3+可转化为Nd(OH)CO3沉淀。该反应的离子方程式为______________________ _____________________________。
②在AgCl沉淀中埋入铁圈并压实,加入足量0.5 mol/L盐酸后静置,充分反应得到Ag。铁将AgCl转化为单质Ag的化学方程式为______________________________。
Fe+2AgCl===FeCl2+2Ag
②将一定物质的量浓度的NO、O2、NH3(其余为N2)气体匀速通过装有V2O5-WO3/TiO2催化剂的反应器,测得NO的转化率随温度的变化如图所示。反应温度高于380 ℃,NO的转化率下降,除因为进入反应器的
NO被还原的量减少外,还有______________________________________ (用化学方程式表示)。
2CeO2+H2O2+6H+===2Ce3++O2↑+4H2O
【解析】 (2) ②根据题意可知,NO的转化率下降是由反应导致,由于主反应的速率减小,故只能是发生副反应生成NO,此环境中氨气、氮气均可与氧气反应生成NO,但氨气与氧气反应更容易,故得出结论。
5 氧化还原反应中的相关计算。
(1) [2024江苏卷]利用铁及其氧化物循环制氢,原理如图所示。反应器Ⅰ中化合价发生改变的元素有________________;含CO和H2各1 mol
的混合气体通过该方法制氢,理论上可获得_______mol H2。
(2) [2023江苏卷改编]金属硫化物(MxSy)催化反应:CH4(g)+2H2S(g) ===CS2 (g)+4H2 (g),该反应中每消耗1 mol H2S,转移电子的数目约为__________________。
C、H、Fe
4×6.02×1023
3×6.02×1023
考向3 常见无机物间的转化
6 [2024江苏卷]在给定条件下,下列制备过程涉及的物质转化均可实现的是( )
A
【解析】 电解氯化钠溶液可以得到H2和Cl2,H2在Cl2中安静的燃烧,生成HCl,A正确;氢氧化镁和盐酸反应可以得到氯化镁溶液,但是电解氯化镁溶液得不到Mg,电解熔融MgCl2才能得到Mg,B错误;纯碱工业是在饱和食盐水中依次通入NH3和CO2,先得到NaHCO3,然后NaHCO3受热分解为Na2CO3,C错误;工业制备硫酸,首先是黄铁矿和氧气反应生成SO2,其次是SO2催化氧化为SO3,最后是SO3和H2O反应生成H2SO4,SO2和水反应生成H2SO3,D错误。
7 [2023江苏卷]氮及其化合物的转化具有重要应用。下列说法不正确的是( )
【解析】 NO不能与H2O反应生成HNO3,B错误。
B
8 [2022江苏卷]氮及其化合物的转化具有重要应用。下列说法不正确的是( )
A. 自然固氮、人工固氮都是将N2转化为NH3
B. 侯氏制碱法以H2O、NH3、CO2、NaCl为原料制备NaHCO3和NH4Cl
C. 工业上通过NH3催化氧化等反应过程生产HNO3
D. 多种形态的氮及其化合物间的转化形成了自然界的“氮循环”
A
考向1 物质的性质与用途对应关系
1 [2024南京二模]下列物质结构与性质或性质与用途不具有对应关系的是( )
A. MgCl2易溶于水,可用于制作豆腐的凝固剂
B. MgO是碱性氧化物,可用于吸收燃煤烟气中的SO2
C. NaCl晶体中离子间存在较强的离子键,NaCl晶体的硬度较大
A
【解析】 N2与O2均为分子晶体,一般来说,相对分子质量越高,熔、沸点越高,与化学键无关,A错误;H2O2与H2O分子间可以形成氢键,是其能与水以任意比互溶的重要原因,B错误;O3氧化性大于O2,可用于饮用水的杀菌消毒,D错误。
2 [2024南京学情调研]下列物质结构与性质或物质性质与用途具有对应关系的是( )
A. N2分子中含共价三键,N2的沸点比O2的低
B. H2O2分子之间形成氢键,可与水以任意比例互溶
C. O2具有氧化性,可作为燃料电池的氧化剂
D. O3的溶解度比O2大,可用于饮用水消毒杀菌
C
【解析】 Fe与O2反应放热,故可作暖贴,A正确;Fe2O3为红棕色粉末,故可作红色颜料,B错误;FeCl3溶液氧化Cu时,FeCl3表现氧化性,C错误;FeS中+2价铁具有还原性,可以与六价铬[Cr(Ⅵ)]发生氧化还原反应,从而除去六价铬[Cr(Ⅵ)],D错误。
3 [2024苏州期初]下列有关铁及其化合物的性质与用途具有对应关系的是( )
A. 铁粉遇空气放热,可用于制作暖贴
B. Fe2O3能与酸反应,可用于制作红色颜料
C. FeCl3溶液显酸性,可用于腐蚀印刷电路板上的铜
D. FeS难溶于水,可用于去除废水中微量六价铬[Cr(Ⅵ)]
A
考向2 氧化还原反应 离子反应
4 [2024南通、泰州等六市一调改编]下列化学反应表示不正确的是( )
A. FeS2与足量稀盐酸反应:FeS2+4H+=== Fe2++2H2S↑
【解析】 离子方程式的电荷不守恒,A错误。
A
5 写出下列相关反应的化学(或离子)方程式。
(1) [2024南通、泰州等八市三调]Cu2Te与NaOH、NaClO3反应生成Cu2O、Na2TeO3、NaCl的离子方程式为____________________________ ________________________。
(2) [2024南京二模]①NaClO2的制备。一种制备NaClO2的过程可表示如下:
“反应2”的化学方程式为____________________________________ ________________________。
2ClO2+H2O2+2NaOH===2NaClO2
+O2+2H2O
NH2COONH4+
3NiO===3Ni+N2↑+3H2O+CO2↑
6 氧化还原反应中的相关计算。
8
4×6.02×1023
考向3 常见无机物间的转化
7 [2024苏锡常镇二调]在指定条件下,下列工业制备流程中涉及的物质转化关系不正确的是( )
B
8 [2024苏州期末]硫及其化合物的转化形态丰富。下列说法正确的是( )
D
【解析】 SO2过量,应该生成NH4HSO3,A错误;FeS2不能一步转化为SO3,B错误;O原子不守恒,电荷也不守恒,C错误。
核 心 串 讲
核心1 物质之间的转化关系
1 价类二维图
(5) 钠、镁、铝及其化合物
(6) 铁、铜及其化合物
2 常见物质间转化关系
(1) 连续氧化反应(注:不一定是制备路线)
(2) 三角转化关系
名称 原理(主要的离子或化学方程式) 说明
所加除杂试剂一般要过量,且易除去。
Na2CO3和 BaCl2加入顺序:________________________;
过滤放在加盐酸前还是加盐酸后:__________________
3 重要的化工生产
(1) 以海水为资源的化工生产
先加BaCl2后加Na2CO3
过滤放在加盐酸前
名称 原理(主要的离子或化学方程式) 说明
②氯碱工业 氯碱工业的化学方程式为_____________________________________________________
阳离子交换膜的作用是_______________________________________________________________________________________;
能否使用阴离子交换膜?________
防止氢气和氯气混合反应,防止OH-迁移到左极室与氯气反应,让Na+迁移到右极室产生NaOH
不能
先通氨气后通二氧化碳
名称 原理(主要的离子或化学方程式) 说明
④电解熔融的氯化钠制钠 ____________________________
_______为阳极,_____为阴极;电解的是__________________
石墨
铁
熔融的NaCl
Cl2+2Br-===2Cl-+Br2
挥发性
4I-+4H++O2===2I2+2H2O
坩埚
升华
(2) 以空气为资源的化工生产
名称 原理(主要的离子或化学方程式) 说明
①合成氨 _________________________ 从空气中获得氮气的方法:________________________________________
②工业制硝酸 主要反应有_____________________ _________、____________________、_______________________________
液化空气后升高温度,首先分离得到氮气
+6H2O
2NO+O2===2NO2
3NO2+H2O===NO+2HNO3
(3) 以矿石为资源的化工生产
名称 原理(主要的化学方程式) 说明
①工业制硫酸 沸腾炉:__________________ _____________、 接触室:__________________ ______、 吸收塔:__________________
三步反应都是________(填“放热”或“吸热”)反应;为了充分利用能源,进入接触室的气体要净化、预热;用_________________吸收SO3,得到发烟硫酸,再稀释成不同浓度的工业产品
2Fe2O3+8SO2
2SO3
SO3+H2O===H2SO4
放热
98.3%的浓硫酸
Al2O3+2NaOH+3H2O===2Na[Al(OH)4]
Na[Al(OH)4]+CO2===Al(OH)3↓+NaHCO3
CO
核心2 离子方程式书写
1 审清题意“三注意”
(1) 反应环境:如介质的酸碱性。
(2) 试剂滴加顺序,不同的滴加顺序,过程中先后可能会发生不同的反应。
(3) 反应过程中反应物之间量的关系,不同的比例关系可能会发生不同的反应。如:
2 ★与量有关的离子方程式书写方法——“少定多变”法
(1) “少定”就是把相对量较少的物质定为“1 mol”,若少量物质有两种或两种以上离子参加反应,则参加反应的离子的物质的量之比与原物质组成比相符。
(2) “多变”就是过量的反应物离子的化学计量数根据反应实际需求量来确定,不受化学式中的比例制约。如:向Ca(HCO3)2溶液中加入过量NaOH溶液,离子方程式的书写方法如下:
检 测 反 馈
2
4
1
3
【解析】 甲烷在高温下分解得到炭黑,与甲烷的热值(J/kg)大小无关,B错误。
1 [2024无锡期末]下列物质的性质与其应用不具有对应关系的是( )
A. 锂的容量密度(mAh/g)高:用作电池负极材料
B. 甲烷的热值(J/kg)高:用于工业制备炭黑
C. 葡萄糖具有还原性:用于玻璃等材料表面化学覆银
D. 氢气在高温下具有还原性:用于工业绿色化炼铁
5
B
2
4
1
3
2 [2023南通如皋适应性考试]铁的单质及许多化合物均具有重要用途。K2FeO4可用作净水剂,K2FeO4在水中不稳定,会生成Fe(OH)3胶体,碱性条件下KClO的氧化性比K2FeO4的大。下列有关铁及其化合物的相关转化,在指定条件下能实现的是( )
5
D
2
4
1
3
【解析】 在高温下,铁与水蒸气反应生成Fe3O4,A错误;K2FeO4在水中反应,铁元素的化合价降低,则水中应是氧元素的化合价升高,不应该是氢元素的化合价降低,B错误;Fe2O3与水不反应,C错误。
5
2
4
3
1
3 [2024苏州期末改编]含锂物质在能源方面有重要应用。锂在氧气中燃烧与Mg相似,其燃烧热为299 kJ/mol。锂与氮气反应得到的Li3N可用作储氢材料。锂-空气电池是一种二次电池,放电时主要产物为Li2O2,充电时阴极产物易形成固态枝晶,导致电池短路。目前应用广泛的是锂离子电池,例如,磷酸铁锂电池充电时,锂离子由LiFePO4电极迁移至石墨电极形成LiCx,LiFePO4的前体FePO4可由NH4H2PO4、FeSO4、H2O2在pH=2的条件下反应制得。下列化学反应表示正确的是( )
5
A
2
4
3
【解析】 Fe和H2O(g)反应生成Fe3O4和H2,B错误;电池充电时,阳极为失电子的一极,C错误;溶液的pH=2,溶液呈酸性,故离子方程式中不能出现OH-,D错误。
1
5
2
4
3
1
4 [2023南京、盐城期末]无水FeCl3常用作芳烃氯代反应的催化剂。以废铁屑(主要成分为Fe,还有少量Fe2O3、C和SiO2)制取无水FeCl3的流程如图所示。下列说法正确的是 ( )
A. “过滤”所得滤液中大量存在的离子有:Fe3+、Fe2+、H+、Cl-
B. “氧化”时可使用新制氯水作氧化剂
C. 将“氧化”后的溶液蒸干可获得FeCl3·6H2O
D. “脱水”时加入SOCl2能抑制FeCl3的水解,原因是SOCl2与水反应生成H2SO4和HCl
5
B
2
4
3
【解析】 废铁屑的主要成分为Fe,Fe和Fe3+反应生成Fe2+,“过滤”所得滤液中大量存在的离子有Fe2+、H+、Cl-,A错误;Cl2具有氧化性,且不引入新杂质,“氧化”时可使用新制氯水作氧化剂,B正确;Fe3+水解生成氢氧化铁,且蒸干会导致固体失H2O,不能将“氧化”后的溶液蒸干来获得FeCl3·6H2O,C错误;SOCl2与水反应生成SO2和HCl,D错误。
1
5
2
3
1
5 (1) [2024连云港期末]将CoCl2·2H2O和活性炭(催化剂)加入三颈瓶中,然后再依次通过滴液漏斗缓慢滴加NH4Cl和浓氨水混合溶液、H2O2溶液,控制温度不超过60 ℃充分反应,冷却后过滤。三颈瓶中制得
[Co(NH3)6]3+的离子方程式为_____________________________________
______________________________________________________________________________________。
5
4
2
3
【解析】 (2) 在该过程中,N元素由0价降低为-3价,故每生成1 mol NH3,转移3 mol电子。
1
5
4
(2) [2024无锡期末]以稀有金属为催化剂(镧、钌和锆)合成氨的机理如图所示。由N2和H2合成1 mol氨气,转移电子的物质的量为__________。
3 mol
谢谢观看
Thank you for watching
同课章节目录
