微主题4 反应热 电化学 课件(共75张PPT) 2025届高考化学二轮复习
文档属性
| 名称 | 微主题4 反应热 电化学 课件(共75张PPT) 2025届高考化学二轮复习 |

|
|
| 格式 | pptx | ||
| 文件大小 | 3.5MB | ||
| 资源类型 | 教案 | ||
| 版本资源 | 通用版 | ||
| 科目 | 化学 | ||
| 更新时间 | 2025-02-22 00:00:00 | ||
图片预览









文档简介
(共75张PPT)
主题3
反应原理与规律
微主题4 反应热 电化学
内容索引
核心串讲
体系建构
名卷优选
基础回归
检测反馈
基 础 回 归
1 SiHCl3(g)+H2(g)===Si(s)+3HCl(g) ΔH
从反应前后总能量变化角度:ΔH=____________________________ _______________________________;从键能的角度(E表示键能):ΔH=_____________________________________________________________。
2 CO2(g)+3H2(g)===CH3OH(g)+H2O(g)能在一定条件下自发进行的原因是________________。
Si(s)和HCl(g)的总能量-
SiHCl3(g)和H2(g)的总能量
3E(Si—Cl)+E(Si—H)+E(H—H)-2E(Si—Si) -3E(H—Cl)
反应ΔH<0
3 已知:①2NO2(g)+H2O(l)===HNO3(aq)+HNO2(aq) ΔH1= -116.1 kJ/mol
②3HNO2(aq)===HNO3(aq)+2NO(g)+H2O(l) ΔH2=+75.9 kJ/mol
反应3NO2(g)+H2O(l)===2HNO3(aq)+NO(g)的ΔH=____________ kJ/mol。
-136.2
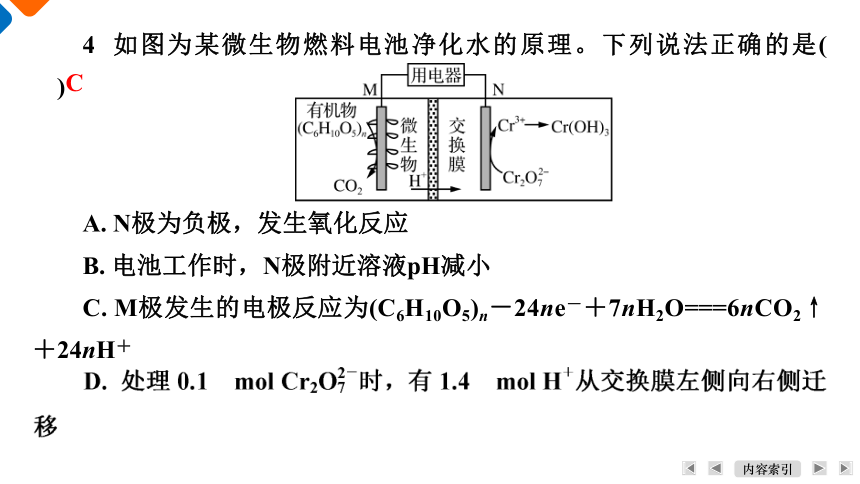
4 如图为某微生物燃料电池净化水的原理。下列说法正确的是( )
A. N极为负极,发生氧化反应
B. 电池工作时,N极附近溶液pH减小
C. M极发生的电极反应为(C6H10O5)n-24ne-+7nH2O===6nCO2↑+24nH+
C
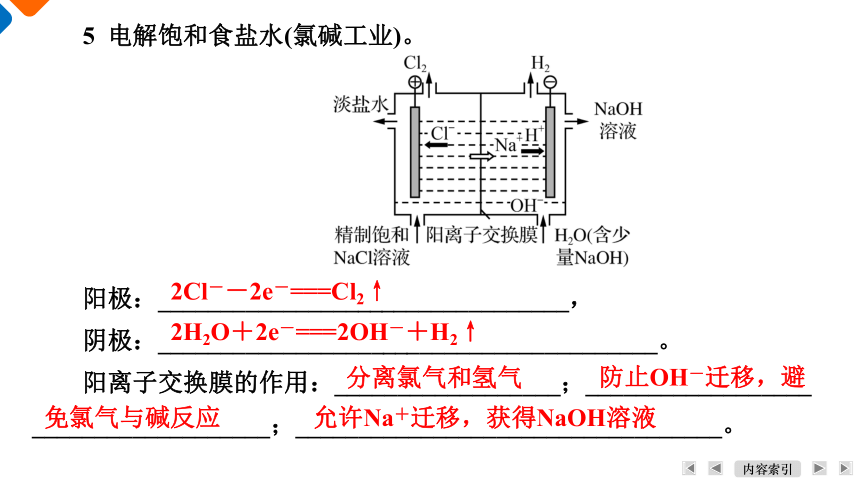
5 电解饱和食盐水(氯碱工业)。
阳极:_________________________________,
阴极:________________________________________。
阳离子交换膜的作用:__________________;__________________ ___________________;__________________________________。
2Cl--2e-===Cl2↑
2H2O+2e-===2OH-+H2↑
分离氯气和氢气
防止OH-迁移,避
免氯气与碱反应
允许Na+迁移,获得NaOH溶液
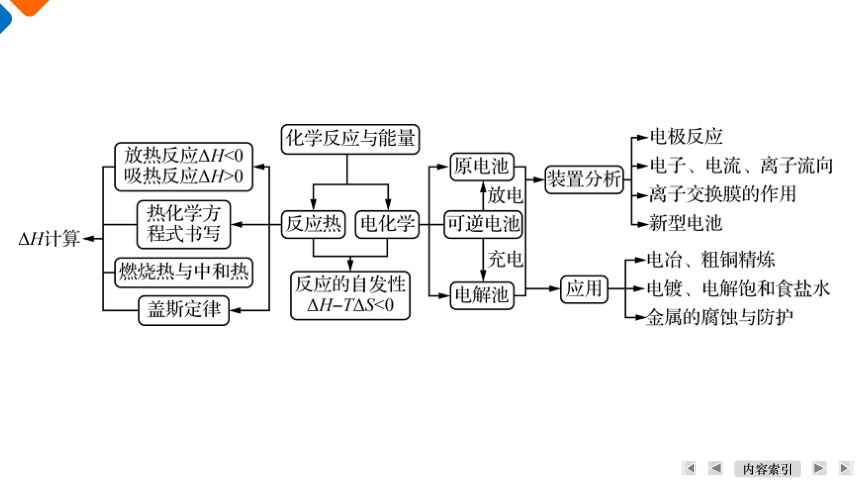
体 系 建 构
名 卷 优 选
考向1 化学反应与能量小综合
1 下列说法正确的是_____(填序号)。
①[2023江苏卷改编]金属硫化物(MxSy)催化反应CH4(g)+2H2S(g) ===CS2(g)+4H2(g),该反应的ΔS<0
③
⑤[2024江苏卷改编]SO2与O2反应生成SO3,催化剂V2O5能减小该反应的焓变
⑥[2023江苏卷改编]H2O(g)与足量C(s)反应生成1 mol H2 (g)和1 mol CO(g)吸收131.3 kJ的热量。则有C(s)+H2O(g)===H2 (g)+CO(g) ΔH=-131.3 kJ/mol
⑦[2022江苏卷改编]甲烷具有较大的燃烧热(890.3 kJ/mol),则甲烷的燃烧:CH4(g)+2O2(g)===CO2(g)+2H2O(g) ΔH=-890.3 kJ/mol
考向2 盖斯定律的应用
2 [2023江苏卷改编] 二氧化碳加氢制甲烷过程中的主要反应如下:
反应Ⅰ:CO2(g)+4H2 (g)===CH4 (g)+2H2O(g)
ΔH=-164.7 kJ/mol
反应Ⅱ:CO2(g)+H2 (g)===CO(g)+H2O (g)
ΔH=+41.2 kJ/mol
问题1:
反应Ⅲ:2CO2(g)+2H2(g)===2CO(g)+2H2O(g)
ΔH=______________kJ/mol
+82.4
反应Ⅳ:2CO(g)+2H2O(g)===2CO2(g)+2H2(g)
ΔH=___________kJ/mol
反应Ⅴ:2CO(g)+2H2(g)===CO2(g)+CH4(g)
ΔH=___________kJ/mol
问题2:
根据反应Ⅰ、Ⅱ与反应Ⅴ的关系,找准反应物和生成物,注意计量数;把反应Ⅴ没有出现的物质计量数对应约掉。反应Ⅴ=___________ ___________或反应Ⅰ+反应Ⅳ。ΔH计算同化学方程式。
-82.4
-247.1
反应Ⅰ-反
应Ⅱ×2
3 [2021江苏卷]CH4与CO2重整的主要反应的热化学方程式如下:
反应Ⅰ:CH4(g)+CO2(g)===2CO(g)+2H2(g) ΔH=+246.5 kJ/mol
反应Ⅱ:H2(g)+CO2(g)===CO(g)+H2O(g)
ΔH=+41.2 kJ/mol
反应Ⅲ:2CO(g)===CO2(g)+C(s)
ΔH=-172.5 kJ/mol
在CH4与CO2重整体系中通入适量H2O(g),可减少C(s)的生成,反应3CH4(g)+CO2(g)+2H2O(g)===4CO(g)+8H2(g)的ΔH=_____________。
+657.1 kJ/mol
【解析】 依据盖斯定律可知,Ⅰ×3-Ⅱ×2即得到反应:3CH4(g)+CO2(g)+2H2O(g)===4CO(g)+8H2(g) ΔH=+657.1 kJ/mol。
考向3 原电池的工作原理及应用
4 [2024江苏卷] 碱性锌锰电池的总反应为Zn+2MnO2+H2O=== ZnO+2MnOOH,电池构造示意图如图所示。下列有关说法正确的是( )
A. 电池工作时,MnO2发生氧化反应
B. 电池工作时,OH-通过隔膜向正极移动
C. 环境温度过低,不利于电池放电
D. 反应中每生成1 mol MnOOH,转移电子数
为2×6.02×1023
C
【解析】 电池工作时,MnO2为正极,得到电子,发生还原反应,A错误;电池工作时,OH-通过隔膜向负极移动,B错误;环境温度过低,化学反应速率下降,不利于电池放电,C正确;由电极反应式MnO2+e-+H2O===MnOOH+OH-可知,反应中每生成1 mol MnOOH,转移电子数为6.02×1023,D错误。
【解析】 不直接接触的转化应该考虑形成原电池,该题中存在铁和银两个电极,有盐酸作为电解质,故可以形成Fe-Ag原电池,正极AgCl得到电子生成Ag,电极反应式为AgCl+e-===Ag+Cl-。
5 [2024江苏卷]在AgCl沉淀中埋入铁圈并压实,加入足量0.5 mol/L盐酸后静置,充分反应得到Ag。不与铁圈直接接触的AgCl也能转化为Ag的原因是___________________________________________________ _______________________________________________________。
铁还原AgCl为Ag,形成Fe-Ag原电池,不与铁圈直接接触的AgCl在正极Ag表面得到电子被还原为Ag
【解析】 ①阳极失去电子,电解水时,在阳极得到氧气,错误;②可逆电池放电时,反应物在正极得到电子,题给电极反应式为负极反应式,错误。
考向4 电解池的工作原理及应用
6 下列说法不正确的是__________(填序号)。
①[2023江苏卷改编]电解水制氢的阳极反应:2H2O-2e-===H2↑+2OH-
①②
7 [2023江苏卷]空气中CO2含量的控制和CO2资源利用具有重要意义。催化电解吸收CO2的KOH溶液可将CO2转化为有机物。在相同条件下,恒定通过电解池的电量,电解得到的部分还原产物的法拉第效率(FE%)随电解电压的变化如图所示。
其中,QX=nF,n表示电解生成还原产物X所转移电子的物质的量,F表示法拉第常数。
(1) 当电解电压为U1 V时,电解过程中含碳还原产物的FE%为0,阴极主要还原产物为________(填化学式)。
H2
8 [2022江苏卷]氢气是一种清洁能源,绿色环保制氢技术研究具有重要意义。“CuCl-H2O热电循环制氢”经过溶解、电解、热水解和热分解4个步骤,其过程如图所示。
考向1 化学反应与能量小综合
1 下列说法正确的是________(填序号)。
③④
2 [2024盐城、南京期末] 氨的饱和食盐水捕获CO2是CO2利用的方法之一,反应原理如下:NaCl(aq)+NH3(g)+CO2(g)+H2O(l)=== NaHCO3(s)+NH4Cl(aq)。该反应常温下能自发进行的原因是__________ _________。
反应ΔH
<0
考向2 盖斯定律的应用
3 (1) [2024苏州期初]CO2催化加氢制CH4是CO2的有机资源转化途径之一。
反应Ⅰ:CO2(g)+4H2(g)===CH4(g)+2H2O(g)
ΔH1=-164.7 kJ/mol
反应Ⅱ:CO2(g)+H2(g)===CO(g)+H2O(g)
ΔH2=+41.2 kJ/mol
反应Ⅲ:2CO(g)+2H2(g)===CO2(g)+CH4(g)
ΔH=__________kJ/mol
-247.1
(2) [2024南京学情调研]“碳达峰、碳中和”是我国社会发展重大战略之一。CH4与CO2经催化重整可制得CO和H2,相关反应如下:
主反应:
CH4(g)+CO2(g)===2CO(g)+2H2(g) ΔH
副反应:
Ⅰ. H2(g)+CO2(g)===H2O(g)+CO(g) ΔH1
Ⅱ. 2CO(g)===CO2(g)+C(s) ΔH2
Ⅲ. CH4(g)===C(s)+2H2(g) ΔH3
Ⅳ. CO(g)+H2(g)===C(s)+H2O(g) ΔH4
其中,副反应Ⅱ、Ⅲ、Ⅳ形成的积碳易导致催化剂活性降低。
主反应的ΔH=______________________________。
ΔH3-ΔH2或ΔH1+ΔH3-ΔH4
【解析】 (1) 依据盖斯定律,反应Ⅰ—反应Ⅱ×2得ΔH=(-164.7-41.2×2)kJ/mol=-247.1 kJ/mol。
考向3 原电池的工作原理及应用
4 [2024苏州期初]氨硼烷-H2O2燃料电
池装置如图所示,该电池在常温下即可工作,
总反应为NH3·BH3+3H2O2===NH4BO2+
4H2O。下列说法不正确的是( )
B
【解析】 NH3·BH3中N原子上的H原子能与H2O中O原子形成氢键,H2O中的H原子能与NH3·BH3中的N原子形成氢键,两者作用力增大,故NH3·BH3易溶于水,A正确;a电极为负极,应失去电子,B错误;b电极的电极反应式为H2O2+2e-+2H+===2H2O,1 mol H2O2参与反应时转移2 mol e-,C正确;H2SO4为强电解质,可以增强溶液的导电性,D正确。
【解析】 用“铁粉还原法”处理废水中的Cr(Ⅵ)时,加入Cu2+后,Fe将Cu2+还原生成Cu,Fe、Cu可构成原电池,随着Cu2+浓度由0升高至15 mg/L,废水中形成很多微小的原电池,加快了Fe2+的生成速率,使Cr(Ⅵ)的去除率增大。
5 [2024南京二模]为探究铜离子浓度对Cr(Ⅵ)去除率的影响,向 1 000 mL某浓度酸性废水中加入2.0 g铁粉,随着Cu2+浓度由0升高至15 mg/L,测得废水中Cr(Ⅵ)的去除率增大,其可能原因为______________ _____________________________________________________________。
铁粉置换出铜形成Fe-Cu原电池,增大了c(Fe2+),Cr(Ⅵ)去除率增大
考向4 电解池的工作原理及应用
6 [2024南京学情调研]锂-硫电池因成本低、比能量高被寄予厚望。一种锂-硫电池的结构如图所示,硫电极采用柔性聚丙烯-石墨烯-硫复合材料。工作时,在硫电极发生反应:
D
7 (1) [2024南通、泰州等八市三模]钴酸锂电池
放电时示意图如图所示。放电时,Li+从LixC6中脱
嵌。请写出放电至完全时Li1-xCoO2电极的电极反
应式:_____________________________________。
Li1-xCoO2+xe-+xLi+===LiCoO2
(3) [2024无锡期终调研]FeCO3晶体细微多孔,能集纳和释放Li+,可作为Li+电池的负极材料。以金属锂片作为阳极,将FeCO3和活化剂混合压制成阴极,以LiPF6/(EC+DMC)为电解液进行充、放电测试。放电时,FeCO3电极的电极反应式为________________。
Li-e-===Li+
8 [2024苏州期初]电催化还原法是CO2的有
机资源化的研究热点。控制其他条件相同,将
一定量的CO2通入盛有酸性溶液的电催化装置
中,CO2可转化为有机物,阴极所得产物及其
物质的量与电压的关系如图。
(1) 电解电压为U1 V时,电解时转移电子的
物质的量为___________。
(2) 电解电压为U2 V时,阴极由CO2生成甲醇的电极反应式为_____________________________________。
(3) 在实际生产中发现当pH过低时,有机物产率降低,可能的原因是_____________________________________________________________ _________________________________________。
2.8 mol
CO2+6e-+6H+===CH3OH+H2O
pH过低,c(H+)增大,H+在阴极表面得电子生成H2增多,CO2被还原为有机物的比例减小,有机物产率降低
【解析】 (1) 电解电压为U1 V时,生成物为0.2 mol C2H5OH和0.2 mol H2,CO2转化为C2H5OH,C元素的化合价由+4降为-2,生成1 mol C2H5OH时转移12 mol e-,H+生成H2,H元素的化合价由+1降为0,生成1 mol H2时,转移2 mol e-,一共转移的电子的物质的量=0.2 mol×12+0.2 mol×2=2.8 mol。(2) CO2转化为CH3OH,C元素的化合价由+4降为-2,变化6,1 mol CO2得到 6 mol e-生成1 mol CH3OH,由电荷守恒知,需要补6 mol H+,由H、O守恒知,生成1 mol H2O。(3) 酸性较强时,阴极处主要为H+得电子生成H2,CO2得电子生成有机物的比例减小,生成有机物的产率降低。
核 心 串 讲
核心1 反应热 热化学方程式
1 焓变ΔH的计算
ΔH与反应前后物质的能量 放热反应
吸热反应
ΔH=______________________________
ΔH与键能 ΔH=______________________________
生成物总能量-反应物总能量
反应物总键能-生成物总键能
ΔH与活化能 ΔH=正反应活化能-逆反应活化能
ΔH与盖斯定律
ΔH=________________
ΔH1+ΔH2+ΔH3
说明 1 mol常见物质中含有的σ键的物质的量。
晶体硅:Si—Si_______________ SiO2:Si—O_______________
石墨:C—C__________________ 金刚石:C—C______________
白磷(P4 ):P—P________________
2 mol
4 mol
1.5 mol
2 mol
6 mol
则ΔH1______ΔH2。
S(s)+O2(g)===SO2(g) ΔH3
S(g)+O2(g)===SO2(g) ΔH4
则ΔH3______ΔH4。
2H2(g)+O2(g)===2H2O(g) ΔH5
2H2(g)+O2(g)===2H2O(l) ΔH6
则ΔH5______ΔH6。
<
>
>
3 根据盖斯定律计算ΔH的步骤和方法
核心2 原电池原理与应用
1 原电池工作原理——以Cu-Zn原电池为例
2 燃料电池电极反应式的书写(以CH3OH燃料电池为例,体会不同介质对电极反应的影响)
CH3OH-6e-+H2O===CO2↑+6H+
O2+4e-+4H+===2H2O
O2+4e-+2H2O===4OH-
CH3OH-6e-+3O2-===CO2↑+2H2O
O2+4e-===2O2-
3 锂离子电池充、放电分析
正极材料:LiMO2(M:Co、Ni、Mn等)、LiM2O4(M:Co、Ni、Mn等)、LiMPO4(M:Fe等)
负极材料:石墨(能吸附锂原子)
LixCn-xe-===xLi++nC
Li1-xMO2+xLi++xe-===LiMO2
4★ 新型化学电源电极反应式的书写
核心3 电解原理与应用
1 电解池模型——以惰性电极电解CuCl2溶液为例
2★ 电解池电极反应式的书写
(1) 提取“信息”书写电极反应式
2Al-6e-+3H2O===Al2O3+6H+
2H++2e-===H2↑
2H2O+2e-===H2↑+2OH-
2H2O+2e-===H2↑+2OH-
将一定浓度的磷酸二氢铵(NH4H2PO4)、氯化锂混合液作为电解液,以铁棒作阳极,石墨作阴极,电解析出LiFePO4沉淀 阳极 ________________________________________________
阴极 _________________________________
2H2O+2e-===H2↑+2OH-
阳极 __________________________________
阴极 __________________________________
2I--2e-===I2
2H2O+2e-===H2↑+2OH-
②可用氨水作为吸收液吸收工业废气中的SO2,当吸收液失去吸收能力时,可通过电解法使吸收液再生而循环利用(电极均为石墨电极),并生成化工原料硫酸。其工作示意图如下:
阳极 (主反应) ______________________________
阴极 ______________________________
2H2O+2e-===H2↑+2OH-
3 电解原理的应用
(1) 电解饱和食盐水(氯碱工业)
阳极反应式:__________________________________
阴极反应式:____________________________________________
总化学方程式:_______________________________________
2Cl--2e-===Cl2↑
2H2O+2e-===H2↑+2OH-
(2) 电解精炼铜
电极材料:粗铜作________;纯铜作________。
电解质溶液:______________________。
阳极反应式:Zn-2e-===Zn2+、Fe-2e-===Fe2+、
Ni-2e-===Ni2+、Cu-2e-===Cu2+
阴极反应式:______________________
阳极泥的形成:在电解过程中,活动性位于铜之后的银、金等杂质,难以在阳极失去电子变成阳离子而溶解,它们以金属单质的形式沉积在电解槽底部,形成阳极泥。
阳极
阴极
含Cu2+的盐溶液
Cu2++2e-===Cu
(3) 电镀
如图为金属表面镀银的工作示意图。
镀件作阴极,镀层金属银作_______。电解质溶液是____________。
阳极反应式:______________________;
阴极反应式:______________________。
特点:阳极溶解,阴极沉积,电镀液的浓度________(填“变大”“变小”或“不变”)。
阳极
AgNO3溶液
Ag-e-===Ag+
Ag++e-===Ag
不变
4 金属的电化学防护
牺牲阳极法(原电池原理):被保护金属作________,比被保护的金属活泼的金属作________。
外加电流法(电解原理):被保护的金属作________,惰性电极作________。
正极
负极
阴极
阳极
核心4 离子交换膜
1 离子交换膜的作用
(1) 可平衡左、右两侧电荷,得到稳定电
流
(2)能将两极区隔离,阻止两极区产生的
物质接触,防止发生化学反应
阳离子交换膜只允许Na+通过,阻止阴离子(Cl-)和气体(Cl2)通过。这样既防止了两极产生的H2和Cl2混合爆炸,又避免了Cl2和阴极产生的NaOH反应生成NaClO而影响烧碱的质量。
(3) 制备某些特定产品
用NaOH溶液吸收烟气中的SO2,将所得的Na2SO3溶液进行电解,可循环再生NaOH,同时得到H2SO4,其原理如图所示。
2 多膜电解池中电极反应式的书写及分析
双膜三室电解技术处理吸收液(用NaOH溶液吸收烟气中的SO2)
Na2SO3
检 测 反 馈
2
4
1
3
①②
2
4
1
3
2 (1) [2023南通海安期末] 热化学硫碘循环分解水是一种高效、无污染的制氢方法。其反应过程如下:
反应Ⅰ:SO2(g)+2H2O(l)+I2(g)===H2SO4(l)+2HI(g)
ΔH1=+35.9 kJ/mol
反应Ⅱ:2H2SO4(l)===2SO2(g)+O2(g)+2H2O(l)
ΔH2
反应Ⅲ:2HI(g)===H2(g)+I2(g) ΔH3=+14.9 kJ/mol
已知:2H2(g)+O2(g)===2H2O(l) ΔH=-571.6 kJ/mol。
则反应Ⅱ的ΔH2=____________kJ/mol。
+470
2
4
1
3
【解析】 (1) 由盖斯定律可知,ΔH2=-ΔH-ΔH1×2-ΔH3×2= +470 kJ/mol。(2) 由盖斯定律知,ΔH=ΔH1+ΔH2=+233.5 kJ/mol。
(2) [2024苏锡常镇一调]采用热分解法脱除沼气中的H2S过程中涉及的主要反应如下:
反应Ⅰ:2H2S(g)===2H2(g)+S2(g)
ΔH1=+169.8 kJ/mol
反应Ⅱ:CH4(g)+S2(g)===CS2(g)+2H2(g)
ΔH2=+63.7 kJ/mol
反应Ⅲ:2H2S(g)+CH4(g)===CS2(g)+4H2(g) ΔH=_____________ kJ/mol
+233.5
2
4
3
1
3 [2024南京、盐城一模]一种以钒基氧化物
(V6O13)为正极材料的水系锌离子电池的工作原理
如图所示。通过使用孔径大小合适且分布均匀的
新型离子交换膜,可提高离子传输通量的均匀性,
从而保持电池的稳定性。下列说法正确的是( )
A. 放电过程中,Zn2+向Zn极一侧移动
B. 放电过程中,电子由Zn极经电解质溶液向V6O13极移动
C. 充电时,V6O13极与外接直流电源正极相连
D.充电时,阳极发生的电极反应可能为V6O13+xZn2++2xe-=== ZnxV6O13
C
2
4
3
【解析】 原电池工作时,阳离子移向正极,钒基氧化物(V6O13)为正极,Zn为负极,故放电过程中,Zn2+透过阳离子交换膜向V6O13极一侧移动,A错误;电子只在外电路中移动,不能经过电解质溶液,B错误;充电时,原电池的正极(V6O13极)与外接电源的正极相连,C正确;充电时,阳极失去电子,发生氧化反应,D错误。
1
2
4
3
1
4 [2023常州期末]近年来,生物电催化技术运用微生物电解池实现了CO2的甲烷化,其工作原理如图所示。
(1) 阴极反应式为_______________________________________。
(2) 如果处理有机物[(CH2O)n]产生标准状况下112 m3的CH4,则理论上导线中通过的电子的物质的量为________________。
CO2+8H++8e-===CH4+2H2O
4×104 mol
2
4
3
1
谢谢观看
Thank you for watching
主题3
反应原理与规律
微主题4 反应热 电化学
内容索引
核心串讲
体系建构
名卷优选
基础回归
检测反馈
基 础 回 归
1 SiHCl3(g)+H2(g)===Si(s)+3HCl(g) ΔH
从反应前后总能量变化角度:ΔH=____________________________ _______________________________;从键能的角度(E表示键能):ΔH=_____________________________________________________________。
2 CO2(g)+3H2(g)===CH3OH(g)+H2O(g)能在一定条件下自发进行的原因是________________。
Si(s)和HCl(g)的总能量-
SiHCl3(g)和H2(g)的总能量
3E(Si—Cl)+E(Si—H)+E(H—H)-2E(Si—Si) -3E(H—Cl)
反应ΔH<0
3 已知:①2NO2(g)+H2O(l)===HNO3(aq)+HNO2(aq) ΔH1= -116.1 kJ/mol
②3HNO2(aq)===HNO3(aq)+2NO(g)+H2O(l) ΔH2=+75.9 kJ/mol
反应3NO2(g)+H2O(l)===2HNO3(aq)+NO(g)的ΔH=____________ kJ/mol。
-136.2
4 如图为某微生物燃料电池净化水的原理。下列说法正确的是( )
A. N极为负极,发生氧化反应
B. 电池工作时,N极附近溶液pH减小
C. M极发生的电极反应为(C6H10O5)n-24ne-+7nH2O===6nCO2↑+24nH+
C
5 电解饱和食盐水(氯碱工业)。
阳极:_________________________________,
阴极:________________________________________。
阳离子交换膜的作用:__________________;__________________ ___________________;__________________________________。
2Cl--2e-===Cl2↑
2H2O+2e-===2OH-+H2↑
分离氯气和氢气
防止OH-迁移,避
免氯气与碱反应
允许Na+迁移,获得NaOH溶液
体 系 建 构
名 卷 优 选
考向1 化学反应与能量小综合
1 下列说法正确的是_____(填序号)。
①[2023江苏卷改编]金属硫化物(MxSy)催化反应CH4(g)+2H2S(g) ===CS2(g)+4H2(g),该反应的ΔS<0
③
⑤[2024江苏卷改编]SO2与O2反应生成SO3,催化剂V2O5能减小该反应的焓变
⑥[2023江苏卷改编]H2O(g)与足量C(s)反应生成1 mol H2 (g)和1 mol CO(g)吸收131.3 kJ的热量。则有C(s)+H2O(g)===H2 (g)+CO(g) ΔH=-131.3 kJ/mol
⑦[2022江苏卷改编]甲烷具有较大的燃烧热(890.3 kJ/mol),则甲烷的燃烧:CH4(g)+2O2(g)===CO2(g)+2H2O(g) ΔH=-890.3 kJ/mol
考向2 盖斯定律的应用
2 [2023江苏卷改编] 二氧化碳加氢制甲烷过程中的主要反应如下:
反应Ⅰ:CO2(g)+4H2 (g)===CH4 (g)+2H2O(g)
ΔH=-164.7 kJ/mol
反应Ⅱ:CO2(g)+H2 (g)===CO(g)+H2O (g)
ΔH=+41.2 kJ/mol
问题1:
反应Ⅲ:2CO2(g)+2H2(g)===2CO(g)+2H2O(g)
ΔH=______________kJ/mol
+82.4
反应Ⅳ:2CO(g)+2H2O(g)===2CO2(g)+2H2(g)
ΔH=___________kJ/mol
反应Ⅴ:2CO(g)+2H2(g)===CO2(g)+CH4(g)
ΔH=___________kJ/mol
问题2:
根据反应Ⅰ、Ⅱ与反应Ⅴ的关系,找准反应物和生成物,注意计量数;把反应Ⅴ没有出现的物质计量数对应约掉。反应Ⅴ=___________ ___________或反应Ⅰ+反应Ⅳ。ΔH计算同化学方程式。
-82.4
-247.1
反应Ⅰ-反
应Ⅱ×2
3 [2021江苏卷]CH4与CO2重整的主要反应的热化学方程式如下:
反应Ⅰ:CH4(g)+CO2(g)===2CO(g)+2H2(g) ΔH=+246.5 kJ/mol
反应Ⅱ:H2(g)+CO2(g)===CO(g)+H2O(g)
ΔH=+41.2 kJ/mol
反应Ⅲ:2CO(g)===CO2(g)+C(s)
ΔH=-172.5 kJ/mol
在CH4与CO2重整体系中通入适量H2O(g),可减少C(s)的生成,反应3CH4(g)+CO2(g)+2H2O(g)===4CO(g)+8H2(g)的ΔH=_____________。
+657.1 kJ/mol
【解析】 依据盖斯定律可知,Ⅰ×3-Ⅱ×2即得到反应:3CH4(g)+CO2(g)+2H2O(g)===4CO(g)+8H2(g) ΔH=+657.1 kJ/mol。
考向3 原电池的工作原理及应用
4 [2024江苏卷] 碱性锌锰电池的总反应为Zn+2MnO2+H2O=== ZnO+2MnOOH,电池构造示意图如图所示。下列有关说法正确的是( )
A. 电池工作时,MnO2发生氧化反应
B. 电池工作时,OH-通过隔膜向正极移动
C. 环境温度过低,不利于电池放电
D. 反应中每生成1 mol MnOOH,转移电子数
为2×6.02×1023
C
【解析】 电池工作时,MnO2为正极,得到电子,发生还原反应,A错误;电池工作时,OH-通过隔膜向负极移动,B错误;环境温度过低,化学反应速率下降,不利于电池放电,C正确;由电极反应式MnO2+e-+H2O===MnOOH+OH-可知,反应中每生成1 mol MnOOH,转移电子数为6.02×1023,D错误。
【解析】 不直接接触的转化应该考虑形成原电池,该题中存在铁和银两个电极,有盐酸作为电解质,故可以形成Fe-Ag原电池,正极AgCl得到电子生成Ag,电极反应式为AgCl+e-===Ag+Cl-。
5 [2024江苏卷]在AgCl沉淀中埋入铁圈并压实,加入足量0.5 mol/L盐酸后静置,充分反应得到Ag。不与铁圈直接接触的AgCl也能转化为Ag的原因是___________________________________________________ _______________________________________________________。
铁还原AgCl为Ag,形成Fe-Ag原电池,不与铁圈直接接触的AgCl在正极Ag表面得到电子被还原为Ag
【解析】 ①阳极失去电子,电解水时,在阳极得到氧气,错误;②可逆电池放电时,反应物在正极得到电子,题给电极反应式为负极反应式,错误。
考向4 电解池的工作原理及应用
6 下列说法不正确的是__________(填序号)。
①[2023江苏卷改编]电解水制氢的阳极反应:2H2O-2e-===H2↑+2OH-
①②
7 [2023江苏卷]空气中CO2含量的控制和CO2资源利用具有重要意义。催化电解吸收CO2的KOH溶液可将CO2转化为有机物。在相同条件下,恒定通过电解池的电量,电解得到的部分还原产物的法拉第效率(FE%)随电解电压的变化如图所示。
其中,QX=nF,n表示电解生成还原产物X所转移电子的物质的量,F表示法拉第常数。
(1) 当电解电压为U1 V时,电解过程中含碳还原产物的FE%为0,阴极主要还原产物为________(填化学式)。
H2
8 [2022江苏卷]氢气是一种清洁能源,绿色环保制氢技术研究具有重要意义。“CuCl-H2O热电循环制氢”经过溶解、电解、热水解和热分解4个步骤,其过程如图所示。
考向1 化学反应与能量小综合
1 下列说法正确的是________(填序号)。
③④
2 [2024盐城、南京期末] 氨的饱和食盐水捕获CO2是CO2利用的方法之一,反应原理如下:NaCl(aq)+NH3(g)+CO2(g)+H2O(l)=== NaHCO3(s)+NH4Cl(aq)。该反应常温下能自发进行的原因是__________ _________。
反应ΔH
<0
考向2 盖斯定律的应用
3 (1) [2024苏州期初]CO2催化加氢制CH4是CO2的有机资源转化途径之一。
反应Ⅰ:CO2(g)+4H2(g)===CH4(g)+2H2O(g)
ΔH1=-164.7 kJ/mol
反应Ⅱ:CO2(g)+H2(g)===CO(g)+H2O(g)
ΔH2=+41.2 kJ/mol
反应Ⅲ:2CO(g)+2H2(g)===CO2(g)+CH4(g)
ΔH=__________kJ/mol
-247.1
(2) [2024南京学情调研]“碳达峰、碳中和”是我国社会发展重大战略之一。CH4与CO2经催化重整可制得CO和H2,相关反应如下:
主反应:
CH4(g)+CO2(g)===2CO(g)+2H2(g) ΔH
副反应:
Ⅰ. H2(g)+CO2(g)===H2O(g)+CO(g) ΔH1
Ⅱ. 2CO(g)===CO2(g)+C(s) ΔH2
Ⅲ. CH4(g)===C(s)+2H2(g) ΔH3
Ⅳ. CO(g)+H2(g)===C(s)+H2O(g) ΔH4
其中,副反应Ⅱ、Ⅲ、Ⅳ形成的积碳易导致催化剂活性降低。
主反应的ΔH=______________________________。
ΔH3-ΔH2或ΔH1+ΔH3-ΔH4
【解析】 (1) 依据盖斯定律,反应Ⅰ—反应Ⅱ×2得ΔH=(-164.7-41.2×2)kJ/mol=-247.1 kJ/mol。
考向3 原电池的工作原理及应用
4 [2024苏州期初]氨硼烷-H2O2燃料电
池装置如图所示,该电池在常温下即可工作,
总反应为NH3·BH3+3H2O2===NH4BO2+
4H2O。下列说法不正确的是( )
B
【解析】 NH3·BH3中N原子上的H原子能与H2O中O原子形成氢键,H2O中的H原子能与NH3·BH3中的N原子形成氢键,两者作用力增大,故NH3·BH3易溶于水,A正确;a电极为负极,应失去电子,B错误;b电极的电极反应式为H2O2+2e-+2H+===2H2O,1 mol H2O2参与反应时转移2 mol e-,C正确;H2SO4为强电解质,可以增强溶液的导电性,D正确。
【解析】 用“铁粉还原法”处理废水中的Cr(Ⅵ)时,加入Cu2+后,Fe将Cu2+还原生成Cu,Fe、Cu可构成原电池,随着Cu2+浓度由0升高至15 mg/L,废水中形成很多微小的原电池,加快了Fe2+的生成速率,使Cr(Ⅵ)的去除率增大。
5 [2024南京二模]为探究铜离子浓度对Cr(Ⅵ)去除率的影响,向 1 000 mL某浓度酸性废水中加入2.0 g铁粉,随着Cu2+浓度由0升高至15 mg/L,测得废水中Cr(Ⅵ)的去除率增大,其可能原因为______________ _____________________________________________________________。
铁粉置换出铜形成Fe-Cu原电池,增大了c(Fe2+),Cr(Ⅵ)去除率增大
考向4 电解池的工作原理及应用
6 [2024南京学情调研]锂-硫电池因成本低、比能量高被寄予厚望。一种锂-硫电池的结构如图所示,硫电极采用柔性聚丙烯-石墨烯-硫复合材料。工作时,在硫电极发生反应:
D
7 (1) [2024南通、泰州等八市三模]钴酸锂电池
放电时示意图如图所示。放电时,Li+从LixC6中脱
嵌。请写出放电至完全时Li1-xCoO2电极的电极反
应式:_____________________________________。
Li1-xCoO2+xe-+xLi+===LiCoO2
(3) [2024无锡期终调研]FeCO3晶体细微多孔,能集纳和释放Li+,可作为Li+电池的负极材料。以金属锂片作为阳极,将FeCO3和活化剂混合压制成阴极,以LiPF6/(EC+DMC)为电解液进行充、放电测试。放电时,FeCO3电极的电极反应式为________________。
Li-e-===Li+
8 [2024苏州期初]电催化还原法是CO2的有
机资源化的研究热点。控制其他条件相同,将
一定量的CO2通入盛有酸性溶液的电催化装置
中,CO2可转化为有机物,阴极所得产物及其
物质的量与电压的关系如图。
(1) 电解电压为U1 V时,电解时转移电子的
物质的量为___________。
(2) 电解电压为U2 V时,阴极由CO2生成甲醇的电极反应式为_____________________________________。
(3) 在实际生产中发现当pH过低时,有机物产率降低,可能的原因是_____________________________________________________________ _________________________________________。
2.8 mol
CO2+6e-+6H+===CH3OH+H2O
pH过低,c(H+)增大,H+在阴极表面得电子生成H2增多,CO2被还原为有机物的比例减小,有机物产率降低
【解析】 (1) 电解电压为U1 V时,生成物为0.2 mol C2H5OH和0.2 mol H2,CO2转化为C2H5OH,C元素的化合价由+4降为-2,生成1 mol C2H5OH时转移12 mol e-,H+生成H2,H元素的化合价由+1降为0,生成1 mol H2时,转移2 mol e-,一共转移的电子的物质的量=0.2 mol×12+0.2 mol×2=2.8 mol。(2) CO2转化为CH3OH,C元素的化合价由+4降为-2,变化6,1 mol CO2得到 6 mol e-生成1 mol CH3OH,由电荷守恒知,需要补6 mol H+,由H、O守恒知,生成1 mol H2O。(3) 酸性较强时,阴极处主要为H+得电子生成H2,CO2得电子生成有机物的比例减小,生成有机物的产率降低。
核 心 串 讲
核心1 反应热 热化学方程式
1 焓变ΔH的计算
ΔH与反应前后物质的能量 放热反应
吸热反应
ΔH=______________________________
ΔH与键能 ΔH=______________________________
生成物总能量-反应物总能量
反应物总键能-生成物总键能
ΔH与活化能 ΔH=正反应活化能-逆反应活化能
ΔH与盖斯定律
ΔH=________________
ΔH1+ΔH2+ΔH3
说明 1 mol常见物质中含有的σ键的物质的量。
晶体硅:Si—Si_______________ SiO2:Si—O_______________
石墨:C—C__________________ 金刚石:C—C______________
白磷(P4 ):P—P________________
2 mol
4 mol
1.5 mol
2 mol
6 mol
则ΔH1______ΔH2。
S(s)+O2(g)===SO2(g) ΔH3
S(g)+O2(g)===SO2(g) ΔH4
则ΔH3______ΔH4。
2H2(g)+O2(g)===2H2O(g) ΔH5
2H2(g)+O2(g)===2H2O(l) ΔH6
则ΔH5______ΔH6。
<
>
>
3 根据盖斯定律计算ΔH的步骤和方法
核心2 原电池原理与应用
1 原电池工作原理——以Cu-Zn原电池为例
2 燃料电池电极反应式的书写(以CH3OH燃料电池为例,体会不同介质对电极反应的影响)
CH3OH-6e-+H2O===CO2↑+6H+
O2+4e-+4H+===2H2O
O2+4e-+2H2O===4OH-
CH3OH-6e-+3O2-===CO2↑+2H2O
O2+4e-===2O2-
3 锂离子电池充、放电分析
正极材料:LiMO2(M:Co、Ni、Mn等)、LiM2O4(M:Co、Ni、Mn等)、LiMPO4(M:Fe等)
负极材料:石墨(能吸附锂原子)
LixCn-xe-===xLi++nC
Li1-xMO2+xLi++xe-===LiMO2
4★ 新型化学电源电极反应式的书写
核心3 电解原理与应用
1 电解池模型——以惰性电极电解CuCl2溶液为例
2★ 电解池电极反应式的书写
(1) 提取“信息”书写电极反应式
2Al-6e-+3H2O===Al2O3+6H+
2H++2e-===H2↑
2H2O+2e-===H2↑+2OH-
2H2O+2e-===H2↑+2OH-
将一定浓度的磷酸二氢铵(NH4H2PO4)、氯化锂混合液作为电解液,以铁棒作阳极,石墨作阴极,电解析出LiFePO4沉淀 阳极 ________________________________________________
阴极 _________________________________
2H2O+2e-===H2↑+2OH-
阳极 __________________________________
阴极 __________________________________
2I--2e-===I2
2H2O+2e-===H2↑+2OH-
②可用氨水作为吸收液吸收工业废气中的SO2,当吸收液失去吸收能力时,可通过电解法使吸收液再生而循环利用(电极均为石墨电极),并生成化工原料硫酸。其工作示意图如下:
阳极 (主反应) ______________________________
阴极 ______________________________
2H2O+2e-===H2↑+2OH-
3 电解原理的应用
(1) 电解饱和食盐水(氯碱工业)
阳极反应式:__________________________________
阴极反应式:____________________________________________
总化学方程式:_______________________________________
2Cl--2e-===Cl2↑
2H2O+2e-===H2↑+2OH-
(2) 电解精炼铜
电极材料:粗铜作________;纯铜作________。
电解质溶液:______________________。
阳极反应式:Zn-2e-===Zn2+、Fe-2e-===Fe2+、
Ni-2e-===Ni2+、Cu-2e-===Cu2+
阴极反应式:______________________
阳极泥的形成:在电解过程中,活动性位于铜之后的银、金等杂质,难以在阳极失去电子变成阳离子而溶解,它们以金属单质的形式沉积在电解槽底部,形成阳极泥。
阳极
阴极
含Cu2+的盐溶液
Cu2++2e-===Cu
(3) 电镀
如图为金属表面镀银的工作示意图。
镀件作阴极,镀层金属银作_______。电解质溶液是____________。
阳极反应式:______________________;
阴极反应式:______________________。
特点:阳极溶解,阴极沉积,电镀液的浓度________(填“变大”“变小”或“不变”)。
阳极
AgNO3溶液
Ag-e-===Ag+
Ag++e-===Ag
不变
4 金属的电化学防护
牺牲阳极法(原电池原理):被保护金属作________,比被保护的金属活泼的金属作________。
外加电流法(电解原理):被保护的金属作________,惰性电极作________。
正极
负极
阴极
阳极
核心4 离子交换膜
1 离子交换膜的作用
(1) 可平衡左、右两侧电荷,得到稳定电
流
(2)能将两极区隔离,阻止两极区产生的
物质接触,防止发生化学反应
阳离子交换膜只允许Na+通过,阻止阴离子(Cl-)和气体(Cl2)通过。这样既防止了两极产生的H2和Cl2混合爆炸,又避免了Cl2和阴极产生的NaOH反应生成NaClO而影响烧碱的质量。
(3) 制备某些特定产品
用NaOH溶液吸收烟气中的SO2,将所得的Na2SO3溶液进行电解,可循环再生NaOH,同时得到H2SO4,其原理如图所示。
2 多膜电解池中电极反应式的书写及分析
双膜三室电解技术处理吸收液(用NaOH溶液吸收烟气中的SO2)
Na2SO3
检 测 反 馈
2
4
1
3
①②
2
4
1
3
2 (1) [2023南通海安期末] 热化学硫碘循环分解水是一种高效、无污染的制氢方法。其反应过程如下:
反应Ⅰ:SO2(g)+2H2O(l)+I2(g)===H2SO4(l)+2HI(g)
ΔH1=+35.9 kJ/mol
反应Ⅱ:2H2SO4(l)===2SO2(g)+O2(g)+2H2O(l)
ΔH2
反应Ⅲ:2HI(g)===H2(g)+I2(g) ΔH3=+14.9 kJ/mol
已知:2H2(g)+O2(g)===2H2O(l) ΔH=-571.6 kJ/mol。
则反应Ⅱ的ΔH2=____________kJ/mol。
+470
2
4
1
3
【解析】 (1) 由盖斯定律可知,ΔH2=-ΔH-ΔH1×2-ΔH3×2= +470 kJ/mol。(2) 由盖斯定律知,ΔH=ΔH1+ΔH2=+233.5 kJ/mol。
(2) [2024苏锡常镇一调]采用热分解法脱除沼气中的H2S过程中涉及的主要反应如下:
反应Ⅰ:2H2S(g)===2H2(g)+S2(g)
ΔH1=+169.8 kJ/mol
反应Ⅱ:CH4(g)+S2(g)===CS2(g)+2H2(g)
ΔH2=+63.7 kJ/mol
反应Ⅲ:2H2S(g)+CH4(g)===CS2(g)+4H2(g) ΔH=_____________ kJ/mol
+233.5
2
4
3
1
3 [2024南京、盐城一模]一种以钒基氧化物
(V6O13)为正极材料的水系锌离子电池的工作原理
如图所示。通过使用孔径大小合适且分布均匀的
新型离子交换膜,可提高离子传输通量的均匀性,
从而保持电池的稳定性。下列说法正确的是( )
A. 放电过程中,Zn2+向Zn极一侧移动
B. 放电过程中,电子由Zn极经电解质溶液向V6O13极移动
C. 充电时,V6O13极与外接直流电源正极相连
D.充电时,阳极发生的电极反应可能为V6O13+xZn2++2xe-=== ZnxV6O13
C
2
4
3
【解析】 原电池工作时,阳离子移向正极,钒基氧化物(V6O13)为正极,Zn为负极,故放电过程中,Zn2+透过阳离子交换膜向V6O13极一侧移动,A错误;电子只在外电路中移动,不能经过电解质溶液,B错误;充电时,原电池的正极(V6O13极)与外接电源的正极相连,C正确;充电时,阳极失去电子,发生氧化反应,D错误。
1
2
4
3
1
4 [2023常州期末]近年来,生物电催化技术运用微生物电解池实现了CO2的甲烷化,其工作原理如图所示。
(1) 阴极反应式为_______________________________________。
(2) 如果处理有机物[(CH2O)n]产生标准状况下112 m3的CH4,则理论上导线中通过的电子的物质的量为________________。
CO2+8H++8e-===CH4+2H2O
4×104 mol
2
4
3
1
谢谢观看
Thank you for watching
同课章节目录
