微主题5 化学反应速率与化学平衡 课件 (共106张PPT) 2025届高考化学二轮复习
文档属性
| 名称 | 微主题5 化学反应速率与化学平衡 课件 (共106张PPT) 2025届高考化学二轮复习 |

|
|
| 格式 | pptx | ||
| 文件大小 | 4.6MB | ||
| 资源类型 | 教案 | ||
| 版本资源 | 通用版 | ||
| 科目 | 化学 | ||
| 更新时间 | 2025-02-22 00:00:00 | ||
图片预览








文档简介
(共106张PPT)
主题3
反应原理与规律
微主题5 化学反应速率与化学平衡
内容索引
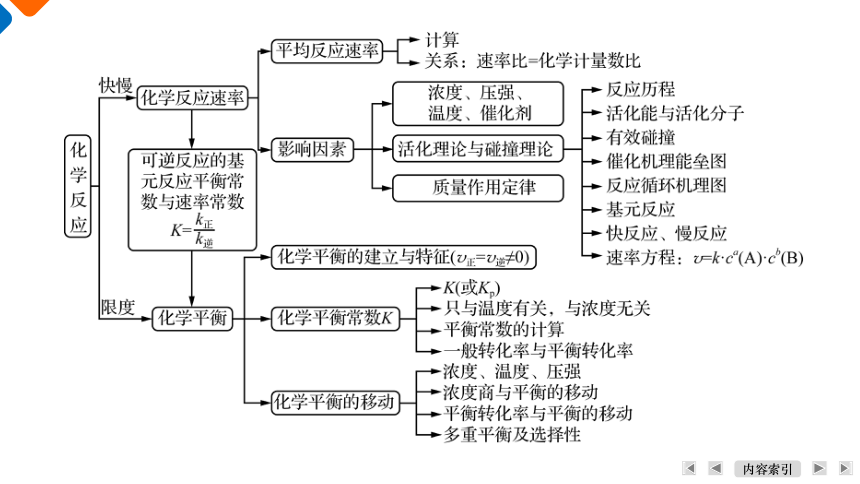
核心串讲
体系建构
名卷优选
基础回归
检测反馈
基 础 回 归
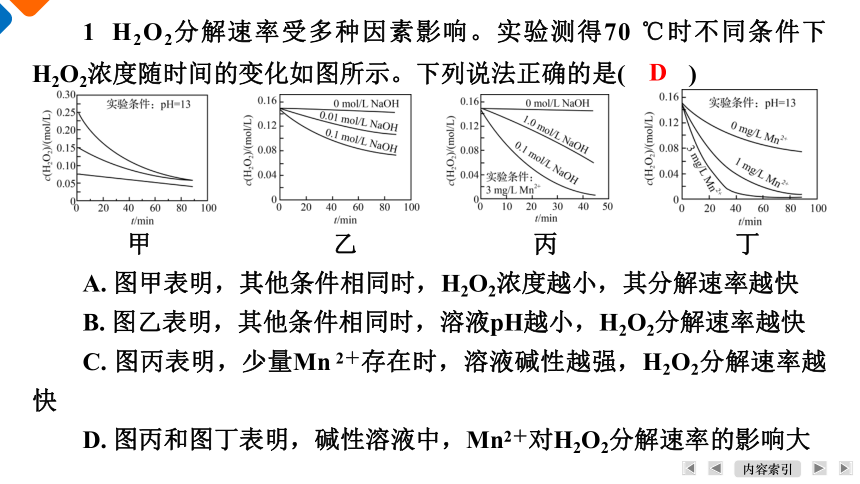
1 H2O2分解速率受多种因素影响。实验测得70 ℃时不同条件下H2O2浓度随时间的变化如图所示。下列说法正确的是( )
A. 图甲表明,其他条件相同时,H2O2浓度越小,其分解速率越快
B. 图乙表明,其他条件相同时,溶液pH越小,H2O2分解速率越快
C. 图丙表明,少量Mn 2+存在时,溶液碱性越强,H2O2分解速率越快
D. 图丙和图丁表明,碱性溶液中,Mn2+对H2O2分解速率的影响大
甲
乙
丙
丁
D
【解析】 图甲表明,其他条件相同时,H2O2浓度越大,其分解速率越快,A错误;图乙表明,其他条件相同时,氢氧化钠的浓度越大,即溶液的pH越大,H2O2分解速率越快,B错误;图丙表明,少量Mn2+存在时,在0.1 mol/L氢氧化钠溶液作用下,H2O2分解速率最快,C错误;图丙和图丁表明,碱性溶液中,Mn2+对H2O2分解速率的影响大,D正确。
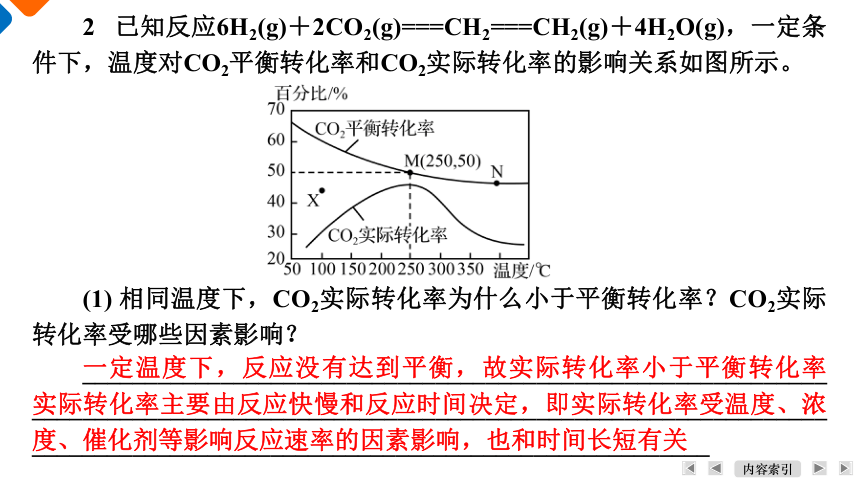
2 已知反应6H2(g)+2CO2(g)===CH2===CH2(g)+4H2O(g),一定条件下,温度对CO2平衡转化率和CO2实际转化率的影响关系如图所示。
(1) 相同温度下,CO2实际转化率为什么小于平衡转化率?CO2实际转化率受哪些因素影响?
________________________________________________________________________________________________________________________________________________________________________________
一定温度下,反应没有达到平衡,故实际转化率小于平衡转化率 实际转化率主要由反应快慢和反应时间决定,即实际转化率受温度、浓度、催化剂等影响反应速率的因素影响,也和时间长短有关
(2) 250 ℃时,CO2实际转化率达到最高,反应______(填“已”或“未”)达到平衡。
(3) CO2实际转化率随温度升高先升高后降低的原因是____________ ____________________________________________________________________________________________________________________。
(4) 反应为________(填“吸热”或“放热”)反应。
(5) M、N点反应的K:KM______(填“>”“<”或“=”)KN;100 ℃时,使该反应CO2转化率达到X点可以采用的方法有________________ _________________________________________________________(任写一种)。
未
前期转化率增大是因为温度升高和催化剂活性增强共同作用使反应速率增大;后期由于催化剂失活导致反应速率下降,使CO2转化率降低
放热
>
延长反应时间或适当增大H2的量或缩小容器容积或使用催化效率更高的催化剂
体 系 建 构
名 卷 优 选
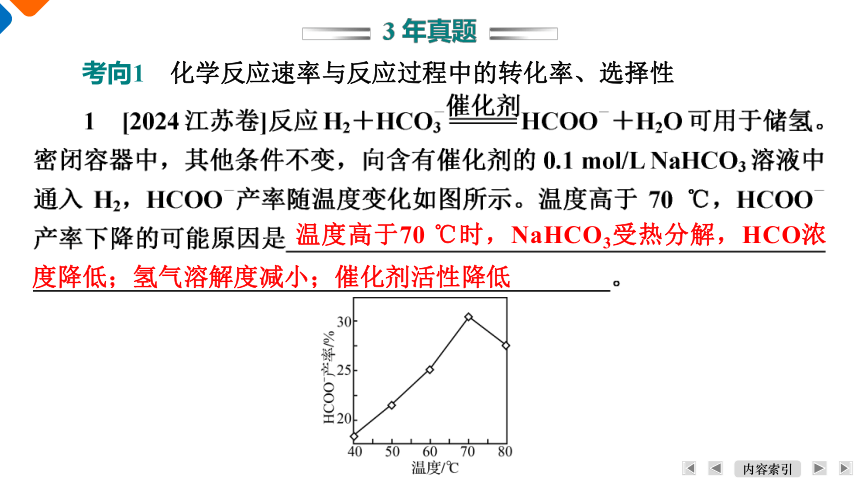
考向1 化学反应速率与反应过程中的转化率、选择性
温度高于70 ℃时,NaHCO3受热分解,HCO浓度降低;氢气溶解度减小;催化剂活性降低
【解析】 影响产品产率下降的因素有反应速率、副反应等。影响反应速率的因素有温度、浓度、催化剂等。
2 [2023江苏卷]V2O5-WO3/TiO2催化剂能催化NH3
脱除烟气中NO,反应为4NH3(g)+O2(g)+4NO(g)===
4N2(g)+6H2O(g) ΔH=-1 632.4 kJ/mol。
(1) 催化剂的应用。将一定物质的量浓度的NO、
O2、NH3(其余为N2)气体匀速通过装有V2O5-WO3/TiO2
催化剂的反应器,测得NO的转化率随温度的变化如图所示。反应温度在320~360 ℃内,NO转化率随温度变化不明显的原因是_______________ _____________________________________________________________________________________________________________;反应温度高于380 ℃,NO转化率下降,除因为进入反应器的NO被还原的量减少外,还有
_________________________________ (用化学方程式表示)。
在该温度范围内,催化剂的活性变化不大,消耗NO的反应速率与生成NO的反应速率随温度升高而增大,对NO转化率的影响相互抵消
(2) 废催化剂的回收。回收 V2O5-WO3/TiO2废催化剂并制备NH4VO3的过程可表示如图:
酸浸时,加料完成后,以一定速率搅拌反应。提高钒元素浸出率的方法还有______________________________。
提高反应温度,延长浸出时间
【解析】 (1) 将气体匀速通过装有催化剂的反应器,应该从反应速率角度思考问题。开始随温度升高催化剂活性增强,反应速率加快;反应一段时间,催化剂的活性基本不再变化,但温度继续升高,主反应速率仍然增大,此时NO转化率变化不明显,故应考虑生成的NO和消耗的NO量基本相等,反应的逆反应或副反应均可以生成NO,所以得出消耗NO的反应速率与生成NO的反应速率随温度升高而增大,对NO转化率的影响相互抵消。根据题意得出发生副反应使NO量增大,NH3和N2均可以与O2反应生成NO,但NH3与O2更容易反应,注意反应条件。(2) 提高浸出率的方法一般是指实际条件下(非平衡状态),此题是有限定条件的,限定了反应物和搅拌,故可通过升高温度加快反应速率提高浸取率,同时还要特别注意时间因素,即延长浸取时间可以增大反应的量,提高浸出率。
温度升高反应速率增
大,温度升高催化剂的活性增强
考向2 多重平衡体系分析
5 [2022江苏卷]乙醇-水催化重整可获得H2。其主要反应如下:
C2H5OH(g)+3H2O(g)===2CO2(g)+6H2(g)
ΔH=+173.3 kJ/mol
CO2(g)+H2(g)===CO(g)+H2O(g)
ΔH=+41.2 kJ/mol
在1.0×105 Pa、n始(C2H5OH)∶n始(H2O)=
1∶3时,若仅考虑上述反应,平衡时CO2和CO
的选择性及H2的产率随温度的变化如图所示。
B
【解析】 根据选择性定义,结合图像易知①③是CO或CO2平衡的选择性,②代表H2的平衡产率。300 ℃前,随温度升高,H2的产率增大,说明主要以反应①为主,含碳主要产物是CO2,所以①代表CO2的选择性,300 ℃后,氢气的产率降低,说明主要以反应②为主,消耗的氢气增大更多,氢气的产率减小,生成CO增多明显,所以③代表CO的选择性。由分析可知,A错误;根据分析,升高温度,平衡时CO的选择性增大,B正确;两种物质参加反应,增大一种物质的浓度,会降低该物质的平衡转化率,C错误;温度一定选用高效催化剂不能改变平衡,即不能改变平衡时H2产率,D错误。
6 [2020江苏卷改编]CH4与CO2重整生成H2和CO的过程中主要发生下列反应:
CH4(g)+CO2(g)===2H2(g)+2CO(g)
ΔH=+247.1 kJ/mol
H2(g)+CO2(g)===H2O(g)+CO(g)
ΔH=+41.2 kJ/mol
在恒压、反应物起始物质的量比n(CH4)∶
n(CO2)=1∶1条件下,CH4和CO2的平衡转化率
随温度变化的曲线如图所示。
下列有关说法正确的是( )
A.升高温度、增大压强均有利于提高CH4的平衡转化率
B.曲线A表示CH4的平衡转化率随温度的变化
C.相同条件下,改用高效催化剂能使曲线A和曲线B相重叠
D.恒压、800 K、n(CH4)∶n(CO2)=1∶1条件下,反应至CH4转化率达到X点的值,改变除温度外的特定条件继续反应,CH4转化率能达到Y点的值
D
【解析】 甲烷和二氧化碳反应是吸热反应,升高温度,平衡向吸热反应方向(即正向)移动,甲烷转化率增大,甲烷和二氧化碳反应是体积增大的反应,增大压强,平衡逆向移动,甲烷转化率减小,A错误;加入的CH4与CO2的物质的量相等,CO2消耗量大于CH4,因此CO2的平衡转化率大于CH4,曲线B表示CH4的平衡转化率随温度的变化,B错误;使用高效催化剂,只能提高反应速率,但不能改变平衡转化率,C错误;800 K时,甲烷的转化率为X点的值,可以通过增大二氧化碳的量继续反应,甲烷的转化率能达到Y点的值,D正确。
考向3 化学平衡和反应速率叠加
7 [2024江苏卷]二氧化碳加氢制甲醇的过程中的主要反应(忽略其他副反应)如下:
①CO2(g)+H2(g)===CO(g)+H2O(g) ΔH1=+41.2 kJ/mol
②CO(g)+2H2(g)===CH3OH(g) ΔH2
225 ℃、8×106 Pa下,将一定比例CO2、H2混合气匀速通过装有催化剂的绝热反应管。装置及L1、L2、L3…位点处(相邻位点距离相同)的气体温度、CO和CH3OH的体积分数如图所示。
(容器内与外界没有热量交换)
下列说法正确的是( )
A. L4处与L5处反应①的平衡常数K相等
B.反应②的焓变ΔH2>0
C. L6处的H2O的体积分数大于L5处
D.混合气从起始到通过L1处,CO的生成速率小于CH3OH的生成速率
C
【解析】 L4处与L5处的温度不同,故反应①的平衡常数K不相等,A错误;反应初始温度是225 ℃,由图可知,绝热装置中气体温度高于225 ℃,说明反应过程中有热量放出,已知反应①是吸热反应,故反应②为放热反应,ΔH2<0,B错误;由图可知,L6处的CH3OH的体积分数大于L5处,但CO体积分数没有明显变化,说明L5~L6反应①②均正向进行,n(H2O)增大,n总(气体)减小,故L6处的 H2O的体积分数大于L5处,C正确;由图可知,L1处CO 的体积分数大于 CH3OH,说明n(CO)>n(CH3OH),则CO的生成速率大于CH3OH的生成速率,D错误。
8 [2023江苏卷]二氧化碳加氢制甲烷过程
中的主要反应如下:
CO2(g)+4H2(g)===CH4(g)+2H2O(g)
ΔH=-164.7 kJ/mol
CO2(g)+H2(g)===CO(g)+H2O(g)
ΔH=+41.2 kJ/mol
下列说法正确的是( )
D
【解析】 根据盖斯定律,上式-下式×2即该反应,焓变应为 -247.1 kJ/mol,A错误;随温度升高,生成甲烷的反应正向进行程度减小,生成CO的反应正向进行程度增大,故CH4的平衡选择性随温度升高而减小,B错误;由于甲烷平衡选择性随温度升高而减小,适宜较低温度,结合CO2实际转化率分析,生成甲烷的适宜温度为350~400 ℃,C错误;450 ℃时,改变投料比或改变压强,平衡转化率可超过原平衡点而达到X点的值,D正确。
①含铁滤渣的主要成分为____________
(填化学式)。
②浸出初期Fe浸出率先上升后下降的原
因是__________________________________ ______________________________________
______________________________________。
考向4 化学反应速率与化学平衡综合
9 [2024江苏卷]回收磁性合金钕铁硼(Nd2Fe14B)可制备半导体材料铁酸铋和光学材料氧化钕。
Fe2O3
浸出初期,c(H+)较大,铁的浸出率较大,约5 min后,溶液酸性减弱,Fe3+水解生成Fe(OH)3进入滤渣
10 [2023江苏卷]合成尿素[CO(NH2)2]是利用CO2的途径之一。尿素合成主要通过下列反应实现:
反应Ⅰ:2NH3(g)+CO2(g)===NH2COONH4(l)
反应Ⅱ:NH2COONH4(l)===CO(NH2)2(l)+H2O(l)
(1) 密闭体系中反应Ⅰ的平衡常数K与温度的关系如图,反应Ⅰ的ΔH______(填“=”“>”或“<”)0。
<
(2) 反应体系中除发生反应Ⅰ、反应Ⅱ外,还发生尿素水解、尿素缩合生成缩二脲[(NH2CO)2NH]和尿素转化为氰酸铵(NH4OCN)等副反应。尿素生产中实际投入NH3和CO2的物质的量之比为n(NH3)∶n(CO2)=4∶1,其实际投料比值远大于理论值的原因是_______________________ ________________________________________。
抑制尿素水解,抑制尿
素缩合生成缩二脲,提高CO2的转化率
【解析】 (1) 由图可知,随着温度的升高,反应Ⅰ的lgK减小,即K随着温度的升高而减小,说明反应Ⅰ是放热反应,ΔH<0。(2) 尿素水解的化学方程式为CO(NH2)2+H2O===CO2↑+2NH3↑,尿素缩合生成缩二脲的化学方程式为2CO(NH2)2===(NH2CO)2NH+NH3↑,尿素转化为氰酸铵(NH4OCN)的化学方程式为CO(NH2)2===NH4OCN,前2个副反应中均生成NH3,尿素生产中实际投入的n(NH3)∶n(CO2)=4∶1,实际投料比值远大于理论值的原因是抑制尿素水解,抑制尿素缩合生成缩二脲,提高CO(NH2)2的产率,氨气与二氧化碳的投料比越大,二氧化碳的转化率越高。
11 [2021江苏卷]甲烷是重要的资源,通过下列过程可实现由甲烷到氢气的转化。
(1) 500 ℃时,CH4与H2O重整主要发生下列反应:
CH4(g)+H2O(g)===CO(g)+3H2(g)
CO(g)+H2O(g)===H2(g)+CO2(g)
已知:CaO(s)+CO2(g)===CaCO3(s) ΔH=-178.8 kJ/mol。
向重整反应体系中加入适量多孔CaO,其优点是________________ ________________________。
吸收CO2,提高
H2的产率,提供热量
(2) CH4与CO2重整的主要反应如下:
反应Ⅰ:CH4(g)+CO2(g)===2CO(g)+2H2(g)
ΔH1=+246.5 kJ/mol
反应Ⅱ:H2(g)+CO2(g)===CO(g)+H2O(g)
ΔH2=+41.2 kJ/mol
反应Ⅲ:2CO(g)===CO2(g)+C(s)
ΔH3=-172.5 kJ/mol
反应Ⅰ和反应Ⅱ的ΔH>0,高温下反应的平衡常数大(反应正向进行程度大),CO2的消耗量多,反应Ⅲ的ΔH<0,高温下反应的平衡常数小(反应正向进行程度小),CO2的生成量少
考向1 化学反应速率与反应过程中的转化率、选择性
1 (1) [2024苏州学业质量调研]尿素在结晶过程中主要副反应是尿素发生脱氨反应。其反应历程如下:
反应1:CO(NH2)2(l)===HNCO(g)+NH3(g)(快反应)
反应2:HNCO(g)+CO(NH2)2(l)===(H2NCO)2NH(l)(慢反应)
在尿素结晶过程中,反应1可视为处于平衡状态。实验表明,在合成尿素的体系中,NH3的浓度越高,缩二脲生成速率越慢,其原因是________________________________________________________________________________________________。
反应1处于平衡状态,NH3浓度越高,则HNCO浓度越低,反应2速率减慢,故生成缩二脲速率越慢
(2) [2024南通、泰州等八市三模] 将废旧锂离子电池(外壳为铁,电芯含铝)置于不同浓度的Na2S和NaCl溶液中使电池充分放电是电池回收工艺的首要步骤。电池在不同溶液中放电的残余电压随时间的变化如图1所示。对浸泡液中沉淀物热处理后,得到XRD示意图谱如图2所示。
图1
图2
①电池在5% Na2S溶液中比在5%NaCl溶液中放电速率更大,其原因是___________________________________________________________ ________________________________。
②与Na2S溶液相比,NaCl溶液的溶质质量分数由5%增大至10%时,电池残余电压降低速率更快。依据图2 XRD图谱,分析其主要原因:___________________________________________________________ _____________。
等质量分数的Na2S溶液中离子浓度更大、离子所带电荷更多; S2-、HS-还原性比Cl-强
NaCl质量分数由5%增大为10%时,对电池外壳和电芯的腐蚀速率加快
【解析】 (2) ①废旧锂离子电池的外壳为铁,电芯含铝,分别置于不同浓度的Na2S和NaCl溶液中使电池充分放电,由图1知,同种电解质溶液的物质的量浓度越大,电池放电速率快,说明电池放电快慢与离子浓度大小有关,与NaCl溶液相比,相同质量分数的Na2S溶液的离子浓度更大,离子所带电荷数更多,电池放电速率快;由图2知,放电过程中,Na2S溶液中有S生成,也会加快铁、铝放电,故电池放电速率更快的原因还应包括:S2-、HS-的还原性比Cl-的强。②图2所示的XRD(X射线衍射)图谱中,显示含有Fe2O3、Al2O3,而废旧锂离子电池的外壳为铁,电芯含铝,故猜测NaCl溶质质量分数由5%增大为10%时,电池残余电压降低速率更快的主要原因是电池外壳和电芯发生腐蚀速率加快。
2 [2024南京调研]“碳达峰、碳中和”是我国社会发展重大战略之一。CH4与CO2经催化重整可制得CO和H2,相关反应如下:
主反应:CH4(g)+CO2(g)===2CO(g)+2H2(g) ΔH
副反应:
Ⅰ. H2(g)+CO2(g)===H2O(g)+CO(g) ΔH1
Ⅱ. 2CO(g)===CO2(g)+C(s) ΔH2
Ⅲ. CH4(g)===C(s)+2H2(g) ΔH3
Ⅳ. CO(g)+H2(g)===C(s)+H2O(g) ΔH4
其中,副反应Ⅱ、Ⅲ、Ⅳ形成的积碳易导致催化剂活性降低。
图1
①CH4的转化率在800 ℃时远大于400
℃时的原因是_________________________ _____________________________________。
②400~600 ℃时,R值的变化情况为
______________________。
③1 000 ℃时R值为__________(写出计算过程)。
升高温度,化学反应速率加快;催化剂活性增强;发生副反应Ⅲ
R随温度升高而减小
1.8
(2) CH4在Pt-Ni合金或Sn-Ni合金催化下脱氢反应历程与相对能量关系如图2所示(*表示吸附在催化剂表面的物质)。从化学反应速率角度分析,脱氢反应选择的催化剂为________________(填“Pt-Ni 合金”或“Sn-Ni合金”),理由是______________________________________ ________________________________________。
图2
Pt-Ni合金
Pt-Ni合金作催化剂时,反应历程中基元反应的活化能都较小,化学反应速率更快
【解析】 (1) ①首先要明确该实验测得数据时的反应均未达到平衡状态,故CH4的转化率在800 ℃时远大于400 ℃时的原因是800 ℃时CH4的平均反应速率更大,具体原因可能是800 ℃时温度高,促进活化分子有效碰撞、催化剂活性增强、发生副反应Ⅲ。②由图1可知,温度低于600 ℃时,随温度升高,CH4的转化率增幅比CO2的大,故此温度范围内R值减小。(2) 化学反应的决速步骤是基元反应活化能最高的一步。由图2知,Pt-Ni合金作催化剂时,基元反应活化能普遍偏低,反应速率较快。
考向2 多重平衡体系分析
3 [2024盐城考前模拟]CO2催化加氢合成
CH3OH能实现碳的循环利用。一定压强下,1
mol CO2与3 mol H2在密闭容器中发生的主要
反应如下:
反应Ⅰ:CO2(g)+3H2(g)===CH3OH(g)+
H2O(g) ΔH1
反应Ⅱ:CO2(g)+H2(g)===CO(g)+H2O(g) ΔH2
下列说法不正确的是( )
A.该测定实验体系未达到化学平衡状态
B.相同条件下,压缩容器容积能提高CO2转化率的实验值
C.相同温度下,CH3OH选择性的实验值大于平衡值,说明反应Ⅰ的速率大于反应Ⅱ
D.260~280 ℃,CO2转化率平衡值随温度升高而增大,说明随温度升高反应Ⅰ平衡正向移动的程度大于反应Ⅱ平衡逆向移动的程度
D
【解析】 平衡值与实验值不重合,显然该测定实验体系未达到化学平衡状态,A正确;相同条件下,压缩容器容积能加快CO2的反应速率,CO2转化率的实验值增大,B正确;相同温度下,不考虑其他副反应,反应时间足够长,CH3OH选择性的实验值应等于平衡值,但CH3OH选择性的实验值大于平衡值,说明反应Ⅰ的速率大于反应Ⅱ,C正确;260~280 ℃内,CH3OH的平衡选择性降低,说明反应Ⅰ的进行程度减小,反应Ⅱ的进行程度增大,故CO2转化率平衡值随温度升高而增大,说明随温度升高反应Ⅱ平衡正向移动的程度大于反应Ⅰ平衡逆向移动的程度,D错误。
4 [2024盐城考前模拟]二氧化碳加氢制甲烷过程中的主要反应如下:
下列说法正确的是( )
D
【解析】 依据盖斯定律,反应Ⅰ-2×反应Ⅱ可得目标热化学方程式,ΔH=(-164.7-2×41.2)kJ/mol=-247.1 kJ/mol,A错误;300 ℃以前,CO的体积分数为0,即只发生反应Ⅰ,CO2和H2按物质的量之比为1∶1投料,平衡时CH4的体积分数小于CO2,故曲线①表示平衡时CO2的体积分数随温度的变化,曲线②表示平衡时CH4的体积分数随温度的变化,B错误;其他条件不变,使用高效催化剂不能提高平衡时甲烷的产率,C错误;温度在200~300 ℃时,只发生反应Ⅰ,设CO2、H2的物质的量均为1 mol,平衡时CO2转化了x mol,列三段式:
考向3 化学平衡和反应速率叠加
5 [2024南通、泰州等八市三模] CH3OH是一种液体燃料。利用CO2和H2合成CH3OH的主要反应为
反应Ⅰ:CO2(g)+3H2(g)===CH3OH
(g)+H2O(g) ΔH1=-58 kJ/mol
反应Ⅱ:CO2(g)+H2(g)===CO(g)
+H2O(g) ΔH2=+41 kJ/mol
在密闭容器中,1.01×105 Pa,n起始(CO2)∶n起始(H2)=1∶2 时,CO2平衡转化率、在催化剂作用下反应t min所测得的CO2实际转化率及CH3OH的选择性随温度的变化如图所示。
B
【解析】 由图可知,0~t min内,CH3OH的选择性:240 ℃> 280 ℃,CO2的实际转化率:240 ℃>280 ℃,故反应Ⅰ的速率:240 ℃>280 ℃,A正确;根据化学方程式知,CO2平衡转化率与H2O的平衡产率变化趋势基本一致,故从220~280 ℃,H2O的平衡产率先减小后缓慢增大,B错误;由图可知,280 ℃时CO2平衡转化率为40%,若在此基础上增大压强,则反应Ⅰ的平衡会正向移动,反应Ⅱ受反应Ⅰ影响会逆向移动,反应Ⅰ消耗CO2,反应Ⅱ产生CO2,两个反应进行的程度未知,故CO2的转化率有可能大于40%,C正确;反应Ⅰ是放热反应,高温不利于反应Ⅰ正向进行,CH3OH的产率低,虽然低温下反应正向进行程度大,但是反应速率慢,故需研发低温下CO2转化率高和CH3OH选择性高的催化剂,D正确。
6 [2024南京二模]利用管状透氧膜反应器实现乙醇-水重整制氢,具有无需额外热源、氧气可协助消除积碳等优点。其主要反应如下:
反应Ⅰ:C2H5OH(g)+H2O(g)===2CO(g)+4H2(g) ΔH1=+256 kJ/mol
反应Ⅱ:2C2H5OH(g)+3O2(g)===4CO2(g)+6H2(g) ΔH2=-1 107 kJ/mol
反应Ⅲ:CO(g)+H2O(g)===CO2(g)+H2(g) ΔH3=-41 kJ/mol
反应Ⅳ:2H2(g)+O2(g)===2H2O(g) ΔH4
B
考向4 化学反应速率与化学平衡综合
7 [2024苏锡常镇二调]丙烷脱氢制丙烯是较为理想的丙烯生产渠道。
(1) 丙烷直接催化脱氢
在Pd-C2N催化剂作用下,丙烷直接脱氢制丙烯反应历程中的相对能量变化如图1所示(*表示催化剂表面吸附位点,如*C3H8表示吸附在催化剂表面的C3H8)。
图1
①丙烷直接催化脱氢制丙烯反应C3H8(g)===C3H6(g)+H2(g)的ΔH=___________kJ/mol。
②该反应历程共分五步,其中速率控制步骤为第______________步。
③研究表明,实际生产中除使用Pd-C2N催化剂外,还需控制反应温度在480 ℃。选择温度为480 ℃的原因是_________________________ ____________________________________。
+123.21
四(或4)
该温度下催化剂的活性较
高,反应速率较快,丙烯的产率较高
图2
①随着反应的进行,4 h前A组分原料气中C3H8转化率和C3H6选择性均有所提升,且在反应床出口检测到CO。研究表明,CO2氧化丙烷脱氢经历了以下两个反应:
8 [2024盐城考前模拟]氢能是应用前景广阔的新能源。
(2) 释氢。MgH2可通过热分解和水解两种方法制得H2。相较于热分解,从物质转化和能量利用的角度分析,MgH2水解释氢方法的优点有_____________________________________________________________。
提高N2在合成气中的比例,增大N2在催化剂表面的吸附活化总量,加快反应速率;有利于提高H2的转化率,同时提高储氢率
等量的MgH2水解比热分解产生的氢气多,同时不需要消耗大量热能
(3) 储氢物质NH3的运用。NH3常用于烟气(主要成分NO、NO2)脱硝。以N2为载气,将含一定量NO、NH3及O2的模拟烟气以一定流速通过装有催化剂CeO2的反应管,研究温度、SO2(g)、H2O(g)对脱硝反应的影响。
①如图1所示,温度高于350 ℃时,NO转化率下降,推测原因是________________________________________________________________________。
图1
温度升高,催化剂的活性下降;NH3和O2反应生成NO;还原剂NH3的量减少
②如图2所示,温度高于350 ℃时,和不含水蒸气的烟气相比,含10%水蒸气的烟气的NO转化率更高,其原因是____________________ ____________________________________________________________________________________________________。
图2
在350 ℃以上含10%水蒸气的烟气中,水蒸气的存在抑制了NH3和O2生成NO的反应,更多的NH3和NO反应,提高NO转化率
③实验证明,烟气中含SO2会导致催化剂不可逆的中毒(Ce4+氧化SO2生成SO覆盖在生成的Ce3+表面,阻止了O2氧化Ce3+)。而添加CuO后抗硫能力显著增强,请结合图3机理,说明抗硫能力增强的原因:____________________________________________________________________________。
图3
核 心 串 讲
核心1 影响化学平衡的外界因素分析
条件的改变(其他条件不变) 化学平衡的移动
浓度 增大反应物浓度或减小生成物浓度 向正反应方向移动
减小反应物浓度或增大生成物浓度 向逆反应方向移动
压强(对有气体存在的反应) 反应前后气体分子数改变 增大压强 向气体分子数减小的方向移动
减小压强 向气体分子数增大的方向移动
反应前后气体分子数不变 改变压强 平衡不移动
条件的改变(其他条件不变) 化学平衡的移动
温度 升高温度 向吸热反应方向移动
降低温度 向放热反应方向移动
催化剂 使用催化剂 平衡不移动
(1) 恒压条件下充入“惰性气体”,同等程度地改变反应混合物中各气体物质的浓度时(如稀释),视为减小压强。
(2) 同时改变反应物和产物,则需要通过浓度商(Q)和平衡常数K比较判断。
平衡正向移动:Q<K;达到平衡状态:Q=K;平衡逆向移动:Q>K。
核心2 温度、催化剂等反应条件之间竞争,对转化率等产生影响
1 pH的改变对反应物转化率的影响
溶液中pH的变化直接影响溶液中H+和OH-浓度的变化,然后通过具体反应影响反应速率和平衡,如弱酸的酸根离子与H+反应,金属离子与OH-反应等。
①pH越大,溶液中H+浓度________(填“减小”或“增大”,下同),OH-浓度________。
②由溶液中H+浓度和OH-浓度变化引发的反应,根据情境推断变化:
a. 纳米FeS颗粒表面带正电荷,OH-浓度增大会竞争吸附,导致含铬微粒吸附量变少。
减小
增大
低于
③综合分析完成答案:______________________________________ _____________________________________________________________________________________________。
FeS溶解量变少,
溶液中Fe2+和HS-浓度降低
2 温度、浓度对去除率的影响
例2 在恒压、NO和O2的起始浓度一定的
条件下,催化反应相同时间,测得不同温度下
NO转化为NO2的转化率如图中实线所示(图中
虚线表示相同条件下NO的平衡转化率随温度
的变化)。
250 ℃前NO的转化率随温度升高而升高的原因是________________ _____________________________________________________________。
250 ℃后NO的转化率随温度升高而降低的原因是________________ ____________________________________________________________。
250 ℃时反应为非平衡状态,则从反应速率角度理解,即250 ℃前NO的转化率随温度升高而升高的原因:催化剂活性随温度升高增大与温度升高共同使反应速率增大;250 ℃后,两条曲线没有立即重叠,故既要讨论非平衡点又要讨论平衡点,则250 ℃后NO的转化率随温度升高而降低的原因:催化剂活性下降,反应速率减小;反应的ΔH<0,温度升高使NOx的平衡转化率降低(或温度升高使反应正向进行程度减小)。
总结 ①条件变化对反应物转化率的影响,需弄清:是讨论反应速率还是讨论平衡;
②转化率(或去除率)受多个因素影响;
③先分析每个因素对转化率的影响(一般是相反的影响);
④再根据结论推断哪个因素对反应起决定作用,还是共同作用。
核心3 有关多重平衡及选择性的问题
在多重平衡中,几个可逆反应是相互影响的。
(1) 若主反应的生成物又与主反应的某一反应物发生另一个可逆反应,则该反应物的平衡转化率就会增大。
(2) 在一定温度下,特定的混合体系,多重平衡选择性为定值,催化剂不能提高某一物质的平衡转化率,也不能提高某一物质的平衡选择性。
(3) 若在同一条件下,两种物质同时可以发生几个可逆反应,则温度、浓度、催化剂等的选用就可以通过改变某一个反应的速率,从而使该反应的选择性提高或降低。
(4) 多重平衡体系中,若两种物质的选择性之和等于100%,则二者的选择性变化曲线呈镜像对称,反之亦成立。
①上图实际是两个图的叠加。图中纵坐标的转化率不是平衡转化率。NH3与O2作用分别生成N2、NO、N2O的三个反应均为放热反应。达到平衡之前,升高温度,NH3的转化率增大。当达到平衡之后,升高温度,反应正向进行的程度减小,NH3的平衡转化率减小。
②由图可知,其他条件不变,在175~300 ℃内,随温度的升高,N2的选择性减小。
③由图可知,低温下NH3的转化率较低,N2的选择性较高。若要高效除去尾气中的NH3,则需研发低温下NH3转化率高和N2选择性高的催化剂。
检 测 反 馈
2
4
1
3
1 [2024盐城、南京期末]乙醇-水催化重整可获得H2。其主要反应如下:
①C2H5OH(g)+3H2O(g)===2CO2(g)+6H2(g)
ΔH1=+173.3 kJ/mol
②CO2(g)+H2(g)===CO(g)+H2O(g)
ΔH2=+41.2 kJ/mol
③CO2(g)+4H2(g)===CH4(g)+2H2O(g)
ΔH3=-164.7 kJ/mol
2
4
1
3
2
4
1
3
下列说法正确的是( )
D
2
4
1
3
2
4
1
3
2 [2023苏锡常镇二调]用H3COOCCOOCH3(草酸二甲酯)和氢气为原料制备乙二醇的反应原理如下:
2
4
1
3
A.曲线Ⅰ表示乙二醇的选择性随温度的变化
B.其他条件不变,增大压强或升高温度,草酸二甲酯的平衡转化率均增大
C.其他条件不变,在190~195 ℃内,随着温度升高,出口处乙醇酸甲酯的量不断减小
D
2
4
1
3
2
4
3
1
2
4
3
1
在913 K、100 kPa下,将质量比为1∶1.3的水蒸气和乙苯在催化剂作用下反应,测得乙苯的转化率和苯乙烯、苯、甲苯的选择性与时间的关系如图所示。
2
4
3
1
下列说法不正确的是( )
A.曲线a表示乙苯的转化率
B.t1~t4时,所得H2的物质的量逐渐减少
C.其他条件不变,增大水蒸气与乙苯的质量比,可以提高乙苯的平衡转化率
D.t1~t4时,苯乙烯选择性下降的原因之一是反应Ⅰ生成的H2促进了反应Ⅲ的进行
B
2
4
3
【解析】 苯乙烯是主反应产物,选择性最大,随着反应的进行,主反应生成的氢气促使副反应Ⅲ正向移动,使得甲苯的选择性增大,乙苯转化率增大,曲线a表示乙苯的转化率,b为甲苯选择性,A正确;反应Ⅰ生成氢气,反应Ⅲ消耗氢气,反应Ⅰ生成的氢气用于反应Ⅲ,氢气的物质的量应先增大,而不是一直减小,B错误;增大水蒸气和乙苯的质量比,充入的水蒸气更多,由于是恒压体系,相当于减小了乙苯的分压,有利于反应Ⅰ、Ⅱ正向进行,可以提高乙苯的平衡转化率,C正确;反应Ⅰ生成的氢气促进了反应Ⅲ正向进行,从而降低了苯乙烯的选择性,D正确。
1
2
4
3
1
4 [2024南通如皋适应性考试二]沸石分子筛的结构为相邻的硅氧四面体和铝氧四面体相互连接形成的笼状结构,沸石分子筛的结构示意图及部分平面结构分别如图1、2所示。沸石分子筛中存在一定大小的空隙,其中的Na+可与其他阳离子发生交换。
图1
图2
图3
2
4
3
1
沸石分子筛对Cu2+去除率随溶液pH的关系如图3所示。pH越大,Cu2+去除率越高的原因是________________________________________ __________________________________________________________________________________________________________________________。
H+与Cu2+均可与沸石分子筛中的Na+进行交换,pH较小时,H+浓度较高,与Na+交换的Cu2+变少;随着pH升高,溶液中的Cu2+会生成Cu(OH)2沉淀,Cu2+去除率增大
谢谢观看
Thank you for watching
主题3
反应原理与规律
微主题5 化学反应速率与化学平衡
内容索引
核心串讲
体系建构
名卷优选
基础回归
检测反馈
基 础 回 归
1 H2O2分解速率受多种因素影响。实验测得70 ℃时不同条件下H2O2浓度随时间的变化如图所示。下列说法正确的是( )
A. 图甲表明,其他条件相同时,H2O2浓度越小,其分解速率越快
B. 图乙表明,其他条件相同时,溶液pH越小,H2O2分解速率越快
C. 图丙表明,少量Mn 2+存在时,溶液碱性越强,H2O2分解速率越快
D. 图丙和图丁表明,碱性溶液中,Mn2+对H2O2分解速率的影响大
甲
乙
丙
丁
D
【解析】 图甲表明,其他条件相同时,H2O2浓度越大,其分解速率越快,A错误;图乙表明,其他条件相同时,氢氧化钠的浓度越大,即溶液的pH越大,H2O2分解速率越快,B错误;图丙表明,少量Mn2+存在时,在0.1 mol/L氢氧化钠溶液作用下,H2O2分解速率最快,C错误;图丙和图丁表明,碱性溶液中,Mn2+对H2O2分解速率的影响大,D正确。
2 已知反应6H2(g)+2CO2(g)===CH2===CH2(g)+4H2O(g),一定条件下,温度对CO2平衡转化率和CO2实际转化率的影响关系如图所示。
(1) 相同温度下,CO2实际转化率为什么小于平衡转化率?CO2实际转化率受哪些因素影响?
________________________________________________________________________________________________________________________________________________________________________________
一定温度下,反应没有达到平衡,故实际转化率小于平衡转化率 实际转化率主要由反应快慢和反应时间决定,即实际转化率受温度、浓度、催化剂等影响反应速率的因素影响,也和时间长短有关
(2) 250 ℃时,CO2实际转化率达到最高,反应______(填“已”或“未”)达到平衡。
(3) CO2实际转化率随温度升高先升高后降低的原因是____________ ____________________________________________________________________________________________________________________。
(4) 反应为________(填“吸热”或“放热”)反应。
(5) M、N点反应的K:KM______(填“>”“<”或“=”)KN;100 ℃时,使该反应CO2转化率达到X点可以采用的方法有________________ _________________________________________________________(任写一种)。
未
前期转化率增大是因为温度升高和催化剂活性增强共同作用使反应速率增大;后期由于催化剂失活导致反应速率下降,使CO2转化率降低
放热
>
延长反应时间或适当增大H2的量或缩小容器容积或使用催化效率更高的催化剂
体 系 建 构
名 卷 优 选
考向1 化学反应速率与反应过程中的转化率、选择性
温度高于70 ℃时,NaHCO3受热分解,HCO浓度降低;氢气溶解度减小;催化剂活性降低
【解析】 影响产品产率下降的因素有反应速率、副反应等。影响反应速率的因素有温度、浓度、催化剂等。
2 [2023江苏卷]V2O5-WO3/TiO2催化剂能催化NH3
脱除烟气中NO,反应为4NH3(g)+O2(g)+4NO(g)===
4N2(g)+6H2O(g) ΔH=-1 632.4 kJ/mol。
(1) 催化剂的应用。将一定物质的量浓度的NO、
O2、NH3(其余为N2)气体匀速通过装有V2O5-WO3/TiO2
催化剂的反应器,测得NO的转化率随温度的变化如图所示。反应温度在320~360 ℃内,NO转化率随温度变化不明显的原因是_______________ _____________________________________________________________________________________________________________;反应温度高于380 ℃,NO转化率下降,除因为进入反应器的NO被还原的量减少外,还有
_________________________________ (用化学方程式表示)。
在该温度范围内,催化剂的活性变化不大,消耗NO的反应速率与生成NO的反应速率随温度升高而增大,对NO转化率的影响相互抵消
(2) 废催化剂的回收。回收 V2O5-WO3/TiO2废催化剂并制备NH4VO3的过程可表示如图:
酸浸时,加料完成后,以一定速率搅拌反应。提高钒元素浸出率的方法还有______________________________。
提高反应温度,延长浸出时间
【解析】 (1) 将气体匀速通过装有催化剂的反应器,应该从反应速率角度思考问题。开始随温度升高催化剂活性增强,反应速率加快;反应一段时间,催化剂的活性基本不再变化,但温度继续升高,主反应速率仍然增大,此时NO转化率变化不明显,故应考虑生成的NO和消耗的NO量基本相等,反应的逆反应或副反应均可以生成NO,所以得出消耗NO的反应速率与生成NO的反应速率随温度升高而增大,对NO转化率的影响相互抵消。根据题意得出发生副反应使NO量增大,NH3和N2均可以与O2反应生成NO,但NH3与O2更容易反应,注意反应条件。(2) 提高浸出率的方法一般是指实际条件下(非平衡状态),此题是有限定条件的,限定了反应物和搅拌,故可通过升高温度加快反应速率提高浸取率,同时还要特别注意时间因素,即延长浸取时间可以增大反应的量,提高浸出率。
温度升高反应速率增
大,温度升高催化剂的活性增强
考向2 多重平衡体系分析
5 [2022江苏卷]乙醇-水催化重整可获得H2。其主要反应如下:
C2H5OH(g)+3H2O(g)===2CO2(g)+6H2(g)
ΔH=+173.3 kJ/mol
CO2(g)+H2(g)===CO(g)+H2O(g)
ΔH=+41.2 kJ/mol
在1.0×105 Pa、n始(C2H5OH)∶n始(H2O)=
1∶3时,若仅考虑上述反应,平衡时CO2和CO
的选择性及H2的产率随温度的变化如图所示。
B
【解析】 根据选择性定义,结合图像易知①③是CO或CO2平衡的选择性,②代表H2的平衡产率。300 ℃前,随温度升高,H2的产率增大,说明主要以反应①为主,含碳主要产物是CO2,所以①代表CO2的选择性,300 ℃后,氢气的产率降低,说明主要以反应②为主,消耗的氢气增大更多,氢气的产率减小,生成CO增多明显,所以③代表CO的选择性。由分析可知,A错误;根据分析,升高温度,平衡时CO的选择性增大,B正确;两种物质参加反应,增大一种物质的浓度,会降低该物质的平衡转化率,C错误;温度一定选用高效催化剂不能改变平衡,即不能改变平衡时H2产率,D错误。
6 [2020江苏卷改编]CH4与CO2重整生成H2和CO的过程中主要发生下列反应:
CH4(g)+CO2(g)===2H2(g)+2CO(g)
ΔH=+247.1 kJ/mol
H2(g)+CO2(g)===H2O(g)+CO(g)
ΔH=+41.2 kJ/mol
在恒压、反应物起始物质的量比n(CH4)∶
n(CO2)=1∶1条件下,CH4和CO2的平衡转化率
随温度变化的曲线如图所示。
下列有关说法正确的是( )
A.升高温度、增大压强均有利于提高CH4的平衡转化率
B.曲线A表示CH4的平衡转化率随温度的变化
C.相同条件下,改用高效催化剂能使曲线A和曲线B相重叠
D.恒压、800 K、n(CH4)∶n(CO2)=1∶1条件下,反应至CH4转化率达到X点的值,改变除温度外的特定条件继续反应,CH4转化率能达到Y点的值
D
【解析】 甲烷和二氧化碳反应是吸热反应,升高温度,平衡向吸热反应方向(即正向)移动,甲烷转化率增大,甲烷和二氧化碳反应是体积增大的反应,增大压强,平衡逆向移动,甲烷转化率减小,A错误;加入的CH4与CO2的物质的量相等,CO2消耗量大于CH4,因此CO2的平衡转化率大于CH4,曲线B表示CH4的平衡转化率随温度的变化,B错误;使用高效催化剂,只能提高反应速率,但不能改变平衡转化率,C错误;800 K时,甲烷的转化率为X点的值,可以通过增大二氧化碳的量继续反应,甲烷的转化率能达到Y点的值,D正确。
考向3 化学平衡和反应速率叠加
7 [2024江苏卷]二氧化碳加氢制甲醇的过程中的主要反应(忽略其他副反应)如下:
①CO2(g)+H2(g)===CO(g)+H2O(g) ΔH1=+41.2 kJ/mol
②CO(g)+2H2(g)===CH3OH(g) ΔH2
225 ℃、8×106 Pa下,将一定比例CO2、H2混合气匀速通过装有催化剂的绝热反应管。装置及L1、L2、L3…位点处(相邻位点距离相同)的气体温度、CO和CH3OH的体积分数如图所示。
(容器内与外界没有热量交换)
下列说法正确的是( )
A. L4处与L5处反应①的平衡常数K相等
B.反应②的焓变ΔH2>0
C. L6处的H2O的体积分数大于L5处
D.混合气从起始到通过L1处,CO的生成速率小于CH3OH的生成速率
C
【解析】 L4处与L5处的温度不同,故反应①的平衡常数K不相等,A错误;反应初始温度是225 ℃,由图可知,绝热装置中气体温度高于225 ℃,说明反应过程中有热量放出,已知反应①是吸热反应,故反应②为放热反应,ΔH2<0,B错误;由图可知,L6处的CH3OH的体积分数大于L5处,但CO体积分数没有明显变化,说明L5~L6反应①②均正向进行,n(H2O)增大,n总(气体)减小,故L6处的 H2O的体积分数大于L5处,C正确;由图可知,L1处CO 的体积分数大于 CH3OH,说明n(CO)>n(CH3OH),则CO的生成速率大于CH3OH的生成速率,D错误。
8 [2023江苏卷]二氧化碳加氢制甲烷过程
中的主要反应如下:
CO2(g)+4H2(g)===CH4(g)+2H2O(g)
ΔH=-164.7 kJ/mol
CO2(g)+H2(g)===CO(g)+H2O(g)
ΔH=+41.2 kJ/mol
下列说法正确的是( )
D
【解析】 根据盖斯定律,上式-下式×2即该反应,焓变应为 -247.1 kJ/mol,A错误;随温度升高,生成甲烷的反应正向进行程度减小,生成CO的反应正向进行程度增大,故CH4的平衡选择性随温度升高而减小,B错误;由于甲烷平衡选择性随温度升高而减小,适宜较低温度,结合CO2实际转化率分析,生成甲烷的适宜温度为350~400 ℃,C错误;450 ℃时,改变投料比或改变压强,平衡转化率可超过原平衡点而达到X点的值,D正确。
①含铁滤渣的主要成分为____________
(填化学式)。
②浸出初期Fe浸出率先上升后下降的原
因是__________________________________ ______________________________________
______________________________________。
考向4 化学反应速率与化学平衡综合
9 [2024江苏卷]回收磁性合金钕铁硼(Nd2Fe14B)可制备半导体材料铁酸铋和光学材料氧化钕。
Fe2O3
浸出初期,c(H+)较大,铁的浸出率较大,约5 min后,溶液酸性减弱,Fe3+水解生成Fe(OH)3进入滤渣
10 [2023江苏卷]合成尿素[CO(NH2)2]是利用CO2的途径之一。尿素合成主要通过下列反应实现:
反应Ⅰ:2NH3(g)+CO2(g)===NH2COONH4(l)
反应Ⅱ:NH2COONH4(l)===CO(NH2)2(l)+H2O(l)
(1) 密闭体系中反应Ⅰ的平衡常数K与温度的关系如图,反应Ⅰ的ΔH______(填“=”“>”或“<”)0。
<
(2) 反应体系中除发生反应Ⅰ、反应Ⅱ外,还发生尿素水解、尿素缩合生成缩二脲[(NH2CO)2NH]和尿素转化为氰酸铵(NH4OCN)等副反应。尿素生产中实际投入NH3和CO2的物质的量之比为n(NH3)∶n(CO2)=4∶1,其实际投料比值远大于理论值的原因是_______________________ ________________________________________。
抑制尿素水解,抑制尿
素缩合生成缩二脲,提高CO2的转化率
【解析】 (1) 由图可知,随着温度的升高,反应Ⅰ的lgK减小,即K随着温度的升高而减小,说明反应Ⅰ是放热反应,ΔH<0。(2) 尿素水解的化学方程式为CO(NH2)2+H2O===CO2↑+2NH3↑,尿素缩合生成缩二脲的化学方程式为2CO(NH2)2===(NH2CO)2NH+NH3↑,尿素转化为氰酸铵(NH4OCN)的化学方程式为CO(NH2)2===NH4OCN,前2个副反应中均生成NH3,尿素生产中实际投入的n(NH3)∶n(CO2)=4∶1,实际投料比值远大于理论值的原因是抑制尿素水解,抑制尿素缩合生成缩二脲,提高CO(NH2)2的产率,氨气与二氧化碳的投料比越大,二氧化碳的转化率越高。
11 [2021江苏卷]甲烷是重要的资源,通过下列过程可实现由甲烷到氢气的转化。
(1) 500 ℃时,CH4与H2O重整主要发生下列反应:
CH4(g)+H2O(g)===CO(g)+3H2(g)
CO(g)+H2O(g)===H2(g)+CO2(g)
已知:CaO(s)+CO2(g)===CaCO3(s) ΔH=-178.8 kJ/mol。
向重整反应体系中加入适量多孔CaO,其优点是________________ ________________________。
吸收CO2,提高
H2的产率,提供热量
(2) CH4与CO2重整的主要反应如下:
反应Ⅰ:CH4(g)+CO2(g)===2CO(g)+2H2(g)
ΔH1=+246.5 kJ/mol
反应Ⅱ:H2(g)+CO2(g)===CO(g)+H2O(g)
ΔH2=+41.2 kJ/mol
反应Ⅲ:2CO(g)===CO2(g)+C(s)
ΔH3=-172.5 kJ/mol
反应Ⅰ和反应Ⅱ的ΔH>0,高温下反应的平衡常数大(反应正向进行程度大),CO2的消耗量多,反应Ⅲ的ΔH<0,高温下反应的平衡常数小(反应正向进行程度小),CO2的生成量少
考向1 化学反应速率与反应过程中的转化率、选择性
1 (1) [2024苏州学业质量调研]尿素在结晶过程中主要副反应是尿素发生脱氨反应。其反应历程如下:
反应1:CO(NH2)2(l)===HNCO(g)+NH3(g)(快反应)
反应2:HNCO(g)+CO(NH2)2(l)===(H2NCO)2NH(l)(慢反应)
在尿素结晶过程中,反应1可视为处于平衡状态。实验表明,在合成尿素的体系中,NH3的浓度越高,缩二脲生成速率越慢,其原因是________________________________________________________________________________________________。
反应1处于平衡状态,NH3浓度越高,则HNCO浓度越低,反应2速率减慢,故生成缩二脲速率越慢
(2) [2024南通、泰州等八市三模] 将废旧锂离子电池(外壳为铁,电芯含铝)置于不同浓度的Na2S和NaCl溶液中使电池充分放电是电池回收工艺的首要步骤。电池在不同溶液中放电的残余电压随时间的变化如图1所示。对浸泡液中沉淀物热处理后,得到XRD示意图谱如图2所示。
图1
图2
①电池在5% Na2S溶液中比在5%NaCl溶液中放电速率更大,其原因是___________________________________________________________ ________________________________。
②与Na2S溶液相比,NaCl溶液的溶质质量分数由5%增大至10%时,电池残余电压降低速率更快。依据图2 XRD图谱,分析其主要原因:___________________________________________________________ _____________。
等质量分数的Na2S溶液中离子浓度更大、离子所带电荷更多; S2-、HS-还原性比Cl-强
NaCl质量分数由5%增大为10%时,对电池外壳和电芯的腐蚀速率加快
【解析】 (2) ①废旧锂离子电池的外壳为铁,电芯含铝,分别置于不同浓度的Na2S和NaCl溶液中使电池充分放电,由图1知,同种电解质溶液的物质的量浓度越大,电池放电速率快,说明电池放电快慢与离子浓度大小有关,与NaCl溶液相比,相同质量分数的Na2S溶液的离子浓度更大,离子所带电荷数更多,电池放电速率快;由图2知,放电过程中,Na2S溶液中有S生成,也会加快铁、铝放电,故电池放电速率更快的原因还应包括:S2-、HS-的还原性比Cl-的强。②图2所示的XRD(X射线衍射)图谱中,显示含有Fe2O3、Al2O3,而废旧锂离子电池的外壳为铁,电芯含铝,故猜测NaCl溶质质量分数由5%增大为10%时,电池残余电压降低速率更快的主要原因是电池外壳和电芯发生腐蚀速率加快。
2 [2024南京调研]“碳达峰、碳中和”是我国社会发展重大战略之一。CH4与CO2经催化重整可制得CO和H2,相关反应如下:
主反应:CH4(g)+CO2(g)===2CO(g)+2H2(g) ΔH
副反应:
Ⅰ. H2(g)+CO2(g)===H2O(g)+CO(g) ΔH1
Ⅱ. 2CO(g)===CO2(g)+C(s) ΔH2
Ⅲ. CH4(g)===C(s)+2H2(g) ΔH3
Ⅳ. CO(g)+H2(g)===C(s)+H2O(g) ΔH4
其中,副反应Ⅱ、Ⅲ、Ⅳ形成的积碳易导致催化剂活性降低。
图1
①CH4的转化率在800 ℃时远大于400
℃时的原因是_________________________ _____________________________________。
②400~600 ℃时,R值的变化情况为
______________________。
③1 000 ℃时R值为__________(写出计算过程)。
升高温度,化学反应速率加快;催化剂活性增强;发生副反应Ⅲ
R随温度升高而减小
1.8
(2) CH4在Pt-Ni合金或Sn-Ni合金催化下脱氢反应历程与相对能量关系如图2所示(*表示吸附在催化剂表面的物质)。从化学反应速率角度分析,脱氢反应选择的催化剂为________________(填“Pt-Ni 合金”或“Sn-Ni合金”),理由是______________________________________ ________________________________________。
图2
Pt-Ni合金
Pt-Ni合金作催化剂时,反应历程中基元反应的活化能都较小,化学反应速率更快
【解析】 (1) ①首先要明确该实验测得数据时的反应均未达到平衡状态,故CH4的转化率在800 ℃时远大于400 ℃时的原因是800 ℃时CH4的平均反应速率更大,具体原因可能是800 ℃时温度高,促进活化分子有效碰撞、催化剂活性增强、发生副反应Ⅲ。②由图1可知,温度低于600 ℃时,随温度升高,CH4的转化率增幅比CO2的大,故此温度范围内R值减小。(2) 化学反应的决速步骤是基元反应活化能最高的一步。由图2知,Pt-Ni合金作催化剂时,基元反应活化能普遍偏低,反应速率较快。
考向2 多重平衡体系分析
3 [2024盐城考前模拟]CO2催化加氢合成
CH3OH能实现碳的循环利用。一定压强下,1
mol CO2与3 mol H2在密闭容器中发生的主要
反应如下:
反应Ⅰ:CO2(g)+3H2(g)===CH3OH(g)+
H2O(g) ΔH1
反应Ⅱ:CO2(g)+H2(g)===CO(g)+H2O(g) ΔH2
下列说法不正确的是( )
A.该测定实验体系未达到化学平衡状态
B.相同条件下,压缩容器容积能提高CO2转化率的实验值
C.相同温度下,CH3OH选择性的实验值大于平衡值,说明反应Ⅰ的速率大于反应Ⅱ
D.260~280 ℃,CO2转化率平衡值随温度升高而增大,说明随温度升高反应Ⅰ平衡正向移动的程度大于反应Ⅱ平衡逆向移动的程度
D
【解析】 平衡值与实验值不重合,显然该测定实验体系未达到化学平衡状态,A正确;相同条件下,压缩容器容积能加快CO2的反应速率,CO2转化率的实验值增大,B正确;相同温度下,不考虑其他副反应,反应时间足够长,CH3OH选择性的实验值应等于平衡值,但CH3OH选择性的实验值大于平衡值,说明反应Ⅰ的速率大于反应Ⅱ,C正确;260~280 ℃内,CH3OH的平衡选择性降低,说明反应Ⅰ的进行程度减小,反应Ⅱ的进行程度增大,故CO2转化率平衡值随温度升高而增大,说明随温度升高反应Ⅱ平衡正向移动的程度大于反应Ⅰ平衡逆向移动的程度,D错误。
4 [2024盐城考前模拟]二氧化碳加氢制甲烷过程中的主要反应如下:
下列说法正确的是( )
D
【解析】 依据盖斯定律,反应Ⅰ-2×反应Ⅱ可得目标热化学方程式,ΔH=(-164.7-2×41.2)kJ/mol=-247.1 kJ/mol,A错误;300 ℃以前,CO的体积分数为0,即只发生反应Ⅰ,CO2和H2按物质的量之比为1∶1投料,平衡时CH4的体积分数小于CO2,故曲线①表示平衡时CO2的体积分数随温度的变化,曲线②表示平衡时CH4的体积分数随温度的变化,B错误;其他条件不变,使用高效催化剂不能提高平衡时甲烷的产率,C错误;温度在200~300 ℃时,只发生反应Ⅰ,设CO2、H2的物质的量均为1 mol,平衡时CO2转化了x mol,列三段式:
考向3 化学平衡和反应速率叠加
5 [2024南通、泰州等八市三模] CH3OH是一种液体燃料。利用CO2和H2合成CH3OH的主要反应为
反应Ⅰ:CO2(g)+3H2(g)===CH3OH
(g)+H2O(g) ΔH1=-58 kJ/mol
反应Ⅱ:CO2(g)+H2(g)===CO(g)
+H2O(g) ΔH2=+41 kJ/mol
在密闭容器中,1.01×105 Pa,n起始(CO2)∶n起始(H2)=1∶2 时,CO2平衡转化率、在催化剂作用下反应t min所测得的CO2实际转化率及CH3OH的选择性随温度的变化如图所示。
B
【解析】 由图可知,0~t min内,CH3OH的选择性:240 ℃> 280 ℃,CO2的实际转化率:240 ℃>280 ℃,故反应Ⅰ的速率:240 ℃>280 ℃,A正确;根据化学方程式知,CO2平衡转化率与H2O的平衡产率变化趋势基本一致,故从220~280 ℃,H2O的平衡产率先减小后缓慢增大,B错误;由图可知,280 ℃时CO2平衡转化率为40%,若在此基础上增大压强,则反应Ⅰ的平衡会正向移动,反应Ⅱ受反应Ⅰ影响会逆向移动,反应Ⅰ消耗CO2,反应Ⅱ产生CO2,两个反应进行的程度未知,故CO2的转化率有可能大于40%,C正确;反应Ⅰ是放热反应,高温不利于反应Ⅰ正向进行,CH3OH的产率低,虽然低温下反应正向进行程度大,但是反应速率慢,故需研发低温下CO2转化率高和CH3OH选择性高的催化剂,D正确。
6 [2024南京二模]利用管状透氧膜反应器实现乙醇-水重整制氢,具有无需额外热源、氧气可协助消除积碳等优点。其主要反应如下:
反应Ⅰ:C2H5OH(g)+H2O(g)===2CO(g)+4H2(g) ΔH1=+256 kJ/mol
反应Ⅱ:2C2H5OH(g)+3O2(g)===4CO2(g)+6H2(g) ΔH2=-1 107 kJ/mol
反应Ⅲ:CO(g)+H2O(g)===CO2(g)+H2(g) ΔH3=-41 kJ/mol
反应Ⅳ:2H2(g)+O2(g)===2H2O(g) ΔH4
B
考向4 化学反应速率与化学平衡综合
7 [2024苏锡常镇二调]丙烷脱氢制丙烯是较为理想的丙烯生产渠道。
(1) 丙烷直接催化脱氢
在Pd-C2N催化剂作用下,丙烷直接脱氢制丙烯反应历程中的相对能量变化如图1所示(*表示催化剂表面吸附位点,如*C3H8表示吸附在催化剂表面的C3H8)。
图1
①丙烷直接催化脱氢制丙烯反应C3H8(g)===C3H6(g)+H2(g)的ΔH=___________kJ/mol。
②该反应历程共分五步,其中速率控制步骤为第______________步。
③研究表明,实际生产中除使用Pd-C2N催化剂外,还需控制反应温度在480 ℃。选择温度为480 ℃的原因是_________________________ ____________________________________。
+123.21
四(或4)
该温度下催化剂的活性较
高,反应速率较快,丙烯的产率较高
图2
①随着反应的进行,4 h前A组分原料气中C3H8转化率和C3H6选择性均有所提升,且在反应床出口检测到CO。研究表明,CO2氧化丙烷脱氢经历了以下两个反应:
8 [2024盐城考前模拟]氢能是应用前景广阔的新能源。
(2) 释氢。MgH2可通过热分解和水解两种方法制得H2。相较于热分解,从物质转化和能量利用的角度分析,MgH2水解释氢方法的优点有_____________________________________________________________。
提高N2在合成气中的比例,增大N2在催化剂表面的吸附活化总量,加快反应速率;有利于提高H2的转化率,同时提高储氢率
等量的MgH2水解比热分解产生的氢气多,同时不需要消耗大量热能
(3) 储氢物质NH3的运用。NH3常用于烟气(主要成分NO、NO2)脱硝。以N2为载气,将含一定量NO、NH3及O2的模拟烟气以一定流速通过装有催化剂CeO2的反应管,研究温度、SO2(g)、H2O(g)对脱硝反应的影响。
①如图1所示,温度高于350 ℃时,NO转化率下降,推测原因是________________________________________________________________________。
图1
温度升高,催化剂的活性下降;NH3和O2反应生成NO;还原剂NH3的量减少
②如图2所示,温度高于350 ℃时,和不含水蒸气的烟气相比,含10%水蒸气的烟气的NO转化率更高,其原因是____________________ ____________________________________________________________________________________________________。
图2
在350 ℃以上含10%水蒸气的烟气中,水蒸气的存在抑制了NH3和O2生成NO的反应,更多的NH3和NO反应,提高NO转化率
③实验证明,烟气中含SO2会导致催化剂不可逆的中毒(Ce4+氧化SO2生成SO覆盖在生成的Ce3+表面,阻止了O2氧化Ce3+)。而添加CuO后抗硫能力显著增强,请结合图3机理,说明抗硫能力增强的原因:____________________________________________________________________________。
图3
核 心 串 讲
核心1 影响化学平衡的外界因素分析
条件的改变(其他条件不变) 化学平衡的移动
浓度 增大反应物浓度或减小生成物浓度 向正反应方向移动
减小反应物浓度或增大生成物浓度 向逆反应方向移动
压强(对有气体存在的反应) 反应前后气体分子数改变 增大压强 向气体分子数减小的方向移动
减小压强 向气体分子数增大的方向移动
反应前后气体分子数不变 改变压强 平衡不移动
条件的改变(其他条件不变) 化学平衡的移动
温度 升高温度 向吸热反应方向移动
降低温度 向放热反应方向移动
催化剂 使用催化剂 平衡不移动
(1) 恒压条件下充入“惰性气体”,同等程度地改变反应混合物中各气体物质的浓度时(如稀释),视为减小压强。
(2) 同时改变反应物和产物,则需要通过浓度商(Q)和平衡常数K比较判断。
平衡正向移动:Q<K;达到平衡状态:Q=K;平衡逆向移动:Q>K。
核心2 温度、催化剂等反应条件之间竞争,对转化率等产生影响
1 pH的改变对反应物转化率的影响
溶液中pH的变化直接影响溶液中H+和OH-浓度的变化,然后通过具体反应影响反应速率和平衡,如弱酸的酸根离子与H+反应,金属离子与OH-反应等。
①pH越大,溶液中H+浓度________(填“减小”或“增大”,下同),OH-浓度________。
②由溶液中H+浓度和OH-浓度变化引发的反应,根据情境推断变化:
a. 纳米FeS颗粒表面带正电荷,OH-浓度增大会竞争吸附,导致含铬微粒吸附量变少。
减小
增大
低于
③综合分析完成答案:______________________________________ _____________________________________________________________________________________________。
FeS溶解量变少,
溶液中Fe2+和HS-浓度降低
2 温度、浓度对去除率的影响
例2 在恒压、NO和O2的起始浓度一定的
条件下,催化反应相同时间,测得不同温度下
NO转化为NO2的转化率如图中实线所示(图中
虚线表示相同条件下NO的平衡转化率随温度
的变化)。
250 ℃前NO的转化率随温度升高而升高的原因是________________ _____________________________________________________________。
250 ℃后NO的转化率随温度升高而降低的原因是________________ ____________________________________________________________。
250 ℃时反应为非平衡状态,则从反应速率角度理解,即250 ℃前NO的转化率随温度升高而升高的原因:催化剂活性随温度升高增大与温度升高共同使反应速率增大;250 ℃后,两条曲线没有立即重叠,故既要讨论非平衡点又要讨论平衡点,则250 ℃后NO的转化率随温度升高而降低的原因:催化剂活性下降,反应速率减小;反应的ΔH<0,温度升高使NOx的平衡转化率降低(或温度升高使反应正向进行程度减小)。
总结 ①条件变化对反应物转化率的影响,需弄清:是讨论反应速率还是讨论平衡;
②转化率(或去除率)受多个因素影响;
③先分析每个因素对转化率的影响(一般是相反的影响);
④再根据结论推断哪个因素对反应起决定作用,还是共同作用。
核心3 有关多重平衡及选择性的问题
在多重平衡中,几个可逆反应是相互影响的。
(1) 若主反应的生成物又与主反应的某一反应物发生另一个可逆反应,则该反应物的平衡转化率就会增大。
(2) 在一定温度下,特定的混合体系,多重平衡选择性为定值,催化剂不能提高某一物质的平衡转化率,也不能提高某一物质的平衡选择性。
(3) 若在同一条件下,两种物质同时可以发生几个可逆反应,则温度、浓度、催化剂等的选用就可以通过改变某一个反应的速率,从而使该反应的选择性提高或降低。
(4) 多重平衡体系中,若两种物质的选择性之和等于100%,则二者的选择性变化曲线呈镜像对称,反之亦成立。
①上图实际是两个图的叠加。图中纵坐标的转化率不是平衡转化率。NH3与O2作用分别生成N2、NO、N2O的三个反应均为放热反应。达到平衡之前,升高温度,NH3的转化率增大。当达到平衡之后,升高温度,反应正向进行的程度减小,NH3的平衡转化率减小。
②由图可知,其他条件不变,在175~300 ℃内,随温度的升高,N2的选择性减小。
③由图可知,低温下NH3的转化率较低,N2的选择性较高。若要高效除去尾气中的NH3,则需研发低温下NH3转化率高和N2选择性高的催化剂。
检 测 反 馈
2
4
1
3
1 [2024盐城、南京期末]乙醇-水催化重整可获得H2。其主要反应如下:
①C2H5OH(g)+3H2O(g)===2CO2(g)+6H2(g)
ΔH1=+173.3 kJ/mol
②CO2(g)+H2(g)===CO(g)+H2O(g)
ΔH2=+41.2 kJ/mol
③CO2(g)+4H2(g)===CH4(g)+2H2O(g)
ΔH3=-164.7 kJ/mol
2
4
1
3
2
4
1
3
下列说法正确的是( )
D
2
4
1
3
2
4
1
3
2 [2023苏锡常镇二调]用H3COOCCOOCH3(草酸二甲酯)和氢气为原料制备乙二醇的反应原理如下:
2
4
1
3
A.曲线Ⅰ表示乙二醇的选择性随温度的变化
B.其他条件不变,增大压强或升高温度,草酸二甲酯的平衡转化率均增大
C.其他条件不变,在190~195 ℃内,随着温度升高,出口处乙醇酸甲酯的量不断减小
D
2
4
1
3
2
4
3
1
2
4
3
1
在913 K、100 kPa下,将质量比为1∶1.3的水蒸气和乙苯在催化剂作用下反应,测得乙苯的转化率和苯乙烯、苯、甲苯的选择性与时间的关系如图所示。
2
4
3
1
下列说法不正确的是( )
A.曲线a表示乙苯的转化率
B.t1~t4时,所得H2的物质的量逐渐减少
C.其他条件不变,增大水蒸气与乙苯的质量比,可以提高乙苯的平衡转化率
D.t1~t4时,苯乙烯选择性下降的原因之一是反应Ⅰ生成的H2促进了反应Ⅲ的进行
B
2
4
3
【解析】 苯乙烯是主反应产物,选择性最大,随着反应的进行,主反应生成的氢气促使副反应Ⅲ正向移动,使得甲苯的选择性增大,乙苯转化率增大,曲线a表示乙苯的转化率,b为甲苯选择性,A正确;反应Ⅰ生成氢气,反应Ⅲ消耗氢气,反应Ⅰ生成的氢气用于反应Ⅲ,氢气的物质的量应先增大,而不是一直减小,B错误;增大水蒸气和乙苯的质量比,充入的水蒸气更多,由于是恒压体系,相当于减小了乙苯的分压,有利于反应Ⅰ、Ⅱ正向进行,可以提高乙苯的平衡转化率,C正确;反应Ⅰ生成的氢气促进了反应Ⅲ正向进行,从而降低了苯乙烯的选择性,D正确。
1
2
4
3
1
4 [2024南通如皋适应性考试二]沸石分子筛的结构为相邻的硅氧四面体和铝氧四面体相互连接形成的笼状结构,沸石分子筛的结构示意图及部分平面结构分别如图1、2所示。沸石分子筛中存在一定大小的空隙,其中的Na+可与其他阳离子发生交换。
图1
图2
图3
2
4
3
1
沸石分子筛对Cu2+去除率随溶液pH的关系如图3所示。pH越大,Cu2+去除率越高的原因是________________________________________ __________________________________________________________________________________________________________________________。
H+与Cu2+均可与沸石分子筛中的Na+进行交换,pH较小时,H+浓度较高,与Na+交换的Cu2+变少;随着pH升高,溶液中的Cu2+会生成Cu(OH)2沉淀,Cu2+去除率增大
谢谢观看
Thank you for watching
同课章节目录
