微主题6 电离平衡与盐类水解 课件(共87张PPT) 2025届高考化学二轮复习
文档属性
| 名称 | 微主题6 电离平衡与盐类水解 课件(共87张PPT) 2025届高考化学二轮复习 |

|
|
| 格式 | pptx | ||
| 文件大小 | 3.5MB | ||
| 资源类型 | 教案 | ||
| 版本资源 | 通用版 | ||
| 科目 | 化学 | ||
| 更新时间 | 2025-02-22 00:00:00 | ||
图片预览










文档简介
(共87张PPT)
主题3
反应原理与规律
微主题6 电离平衡与盐类水解
内容索引
核心串讲
体系建构
名卷优选
基础回归
检测反馈
基 础 回 归
1 室温下,下列说法不能说明CH3COOH的酸性弱于盐酸的是( )
A.相同浓度的CH3COOH和盐酸,前者pH大
B.相同pH的CH3COOH和盐酸,导电能力后者强
C.相同浓度的CH3COONa溶液和NaCl溶液,前者pH大
D.pH=2的CH3COOH和盐酸,加水稀释100倍,前者变化小于后者
B
B
3 铁矿石用稀硫酸溶解时,稀硫酸要过量的原因是______________ _____________________________。
4 工业中常用Na2CO3溶液浸泡金属,从而去除金属表面的油污。
(1) Na2CO3溶液除油污是由于其溶液呈碱性,呈碱性的原因是__________________________________(用方程式表示)。
提高矿石中铁
元素浸取率;抑制Fe3+水解
<
Na2CO3溶
液的碱性强,易产生Fe(OH)2和Fe(OH)3沉淀
向FeSO4溶液中缓慢加入NaHCO3溶液
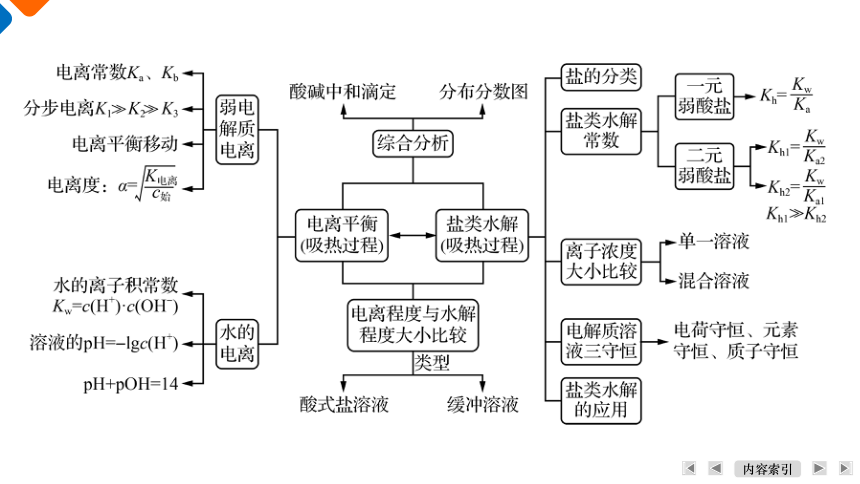
体 系 建 构
名 卷 优 选
考向1 溶液中粒子浓度大小分析
题型1 固定成分溶液中粒子浓度大小分析
1 判断下列说法是否正确。
√
×
×
√
×
题型2 反应过程中粒子浓度大小分析
[工业流程中粒子浓度大小关系]
2 判断下列粒子浓度关系是否正确。
(1) [2023江苏卷]室温下,用含少量Mg2+的MnSO4溶液制备MnCO3的过程如图所示。已知:Ksp(MgF2)=5.2×10-11,Ka(HF)=6.3×10-4。
×
×
√
[实验过程中粒子浓度分析]
3 [2024江苏卷]室温下,通过下列实验探究SO2的性质。已知Ka1(H2SO3)=1.3×10-2,Ka2(H2SO3)=6.2×10-8。
实验1:将SO2气体通入水中,测得溶液pH=3。
实验2:将SO2气体通入0.1 mol/L NaOH溶液中,当溶液pH=4时停止通气。
实验3:将SO2气体通入0.1 mol/L酸性KMnO4溶液中,当溶液恰好褪色时停止通气。
D
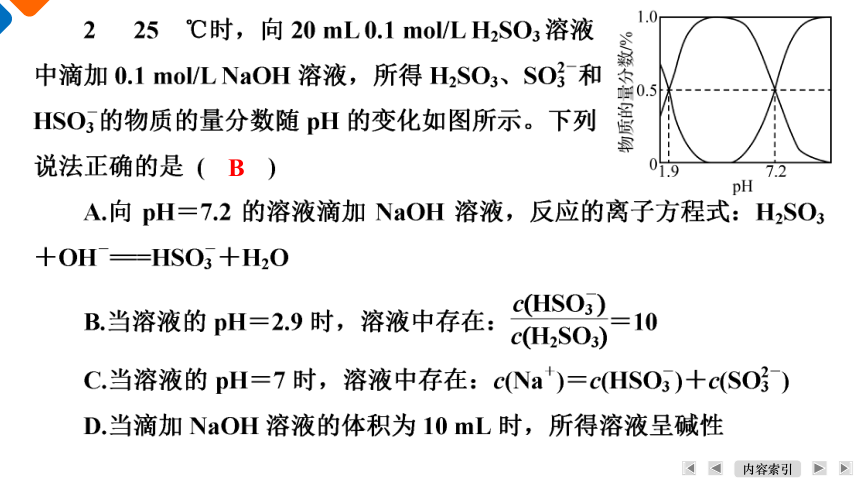
考向2 酸碱滴定过程和分布曲线中粒子浓度分析
D
B
考向3 盐类水解的综合应用
6 判断下列说法是否正确。
(1) [2023江苏卷]向2 mL FeSO4溶液中滴加2~3滴酚酞试液,观察溶液颜色变化判断Fe2+是否水解( )
×
×
√
不引入杂质
离子Na+(或制得的催化剂不含Na+)
考向1 溶液中粒子浓度大小分析
题型1 固定成分溶液中粒子浓度大小分析
1 判断下列说法是否正确。
×
×
×
×
题型2 反应过程中粒子浓度大小分析
[工业流程中粒子浓度大小关系]
2 判断下列情境下粒子浓度关系式是否正确。
(1) [2024无锡期末]室温下,用含有少量Mg2+的Li2SO4溶液(模拟盐湖水)制备Li2CO3的过程如图所示。
×
(2) [2024南通、泰州等六市一调] 室温下,用含有少量Mn2+的ZnSO4溶液制备ZnCO3的过程如下:
√
[实验过程中粒子浓度分析]
3 [2023泰州期末]室温下,某兴趣小组通过下列实验制备少量NaHCO3并探究其性质。
实验1:测得100 mL 14 mol/L氨水的pH约为12;
实验2:向上述氨水中加NaCl粉末至饱和,通入足量CO2后析出晶体;
实验3:将所得混合物静置后过滤、洗涤、干燥,得到NaHCO3;
实验4:配制100 mL一定浓度的NaHCO3溶液,测得pH为8.0。
D
4 [2023扬州一模]合成环氧氯丙烷时产生了盐酸和醋酸(HAc)的混合液,为研究混合溶液的定量分析方法,进行以下实验。
实验1:向20 mL 0.1 mol/L HCl溶液中滴加0.1 mol/L NaOH溶液;
实验2:向20 mL 0.1 mol/L HAc溶液中滴加0.1 mol/L NaOH溶液;
实验3:向20 mL某浓度HCl与HAc混合溶液中滴加0.1 mol/L NaOH溶液。
测得实验1、2中溶液pH的变化如图所示。
下列说法正确的是( )
C
考向2 酸碱滴定过程和分布曲线中粒子浓度分析
下列说法正确的是( )
B
守恒,溶液中存在:c(H2A)+c(HA-)+c(A2-)=0.1 mol/L,当加入酸或碱,增大了溶液体积,所以c(H2A)+c(HA-)+c(A2-)<0.1 mol/L,C错误;NH4HA溶液显酸性,主要发生HA-的电离,所以向NH4HA溶液中滴加少量NaOH溶液,优先反应的离子方程式为HA-+OH-===A2-+H2O,D错误。
D
考向3 盐类水解的综合应用
7 判断下列说法是否正确。
√
×
(3) [2024盐城、南京期末]用干燥、洁净的玻璃棒蘸取0.1 mol/L NaHCO3溶液,点在干燥的pH试纸上,测出溶液的pH,由此判 HCO是否发生水解( )
(4) [2024南通、泰州等六市一调]Na2SO3溶液呈碱性的原因实验设计:向Na2SO3溶液中先滴加酚酞,再滴加BaCl2溶液至过量,观察溶液颜色变化( )
√
√
8 [2024苏州期末]已知:TiO2++2H2O===TiO(OH)2↓+2H+。其他条件不变,初始溶液pH对含Fe3+的TiO2+溶液水解率的影响如图所示,pH在1.7~1.8内,随着pH增大,TiO2+水解率下降的原因是_______ _________________________________________。
Fe3+水
解产生的H+抑制了TiO2+的水解
【解析】 初始pH在1.7~1.8内,由图可知,随着pH的增大,Fe3+水解程度增大,产生的H+对TiO2+的水解有抑制作用,从而导致TiO2+的水解率下降。
9 [2024无锡期末]以FeSO4·7H2O为原料制备FeCO3的实验流程如图所示。沉淀剂使用尿素[CO(NH2)2],不使用Na2CO3的原因是_________________________________________________________________________________________。
Na2CO3溶液为碱性,易生成Fe(OH)2,碱性条件下,Fe(OH)2易被氧化产生Fe(OH)3沉淀等杂质
酸
酸
核 心 串 讲
核心1 电离平衡常数(K电离)、水的离子积常数(Kw)与盐类水解常数(Kh)
1 电离平衡常数
(1) 常见的弱电解质有弱酸、弱碱和水,弱电解质在溶液中存在电离平衡。弱电解质的电离是吸热过程,升高温度,可促进其电离;常用弱电解质Ka比较酸性强弱、粒子或粒子浓度比的变化及粒子浓度的大小比较。
①Ka越小,酸性________。
②醋酸Ka=1.75×10-5,pH=5时c(CH3COO-)______(填“>”“<”或“=”)c(CH3COOH)。
越弱
>
(2) 多元弱酸(或弱碱)的电离是分步进行的,一般K1 K2 K3。因此计算多元弱酸溶液的c(H+)或比较多元弱酸酸性相对强弱时,通常只考虑第一步电离。
①可以通过比较弱酸一级电离平衡常数的大小来比较它们电离程度的大小,也可比较酸性强弱。如酸性:H2C2O4>H3PO4>CH3COOH>H2CO3。
增大
CO2
2 水的电离[25 ℃时,水的离子积常数Kw=
c(H+)·c(OH-)=10-14]。
图中曲线表示不同温度下,水溶液中c(H+)
与c(OH-)的关系。由于水的电离是吸热过程,
升高温度可促进水电离,水的离子积常数增大,
曲线cd对应的温度高于25 ℃,故T>25。
一定温度下,水溶液中c(H+)与c(OH-)的关系是一个定值,但水的电离程度不一定相同。在酸或碱溶液中,水的电离受到________;电离程度________。
抑制
变小
3 盐类水解常数(Kh)
4 综合应用(没有特殊说明时,使用的数据均在室温下)
(1) 证明弱电解质的方法
以CH3COOH为例:
①测定0.1 mol/L CH3COOH溶液的pH,pH______(填“>”或“<”,下同)1,说明CH3COOH为弱电解质。
大
大
>
②测定CH3COONa溶液的pH,pH______7,说明CH3COOH为弱电解质。
③相同温度、相同浓度的盐酸的导电性______醋酸的导电性,说明CH3COOH是弱电解质。
④取pH=3的CH3COOH溶液1 mL,用水稀释到100 mL,pH______5,说明CH3COOH为弱电解质。
⑤向0.1 mol/L CH3COOH溶液中加入少量CH3COONH4(水溶液呈中性)固体(溶液体积变化忽略不计),pH__________(填“变大”或“变小”),说明CH3COOH为弱电解质。
>
>
<
变大
碱
小于
大于
酸
>
核心2 电解质溶液中“三个守恒和一个比较”
1 电荷守恒
电解质溶液中,无论存在多少种离子,溶液都呈电中性,即电解质溶液中阳离子所带的电荷总数与________________________相等,如Na2S溶液中:c(Na+)+c(H+)=2c(S2-)+c(HS-)+c(OH-)。
2 元素守恒
在电解质溶液中,由于某些离子发生水解或电离,离子的存在形式发生了变化,变成了其他离子或分子,使离子的种类增多,但却不能使离子或分子中某种特定元素原子的数目发生变化,其质量在反应前后是守恒的,始终遵循原子守恒,如Na2S溶液中:c(Na+)=2c(S2-)+ 2c(HS-)+2c(H2S)。
阴离子所带的电荷总数
3 质子守恒
以Na2S溶液为例:
(1) 方法1:可以由电荷守恒与元素守恒推导出来,c(H+)+2c(H2S)+c(HS-)=c(OH-)。
(2) 方法2:可利用下图进行快速书写。
质子守恒: c(H+)+2c(H2S)+c(HS-)=c(OH-)。
核心3 酸碱滴定反应图像
1 强碱滴定一元强酸、一元弱酸
氢氧化钠滴定等浓度等体积的盐酸、醋酸的滴定曲线
①曲线起点不同:强碱滴定强酸、弱酸的曲线中,强酸起点低
②突跃点变化范围不同:强碱与强酸反应的突跃点变化范围大于强碱与弱酸反应
③室温下pH=7不一定是终点:强碱与强酸反应时,终点的pH=7;强碱与弱酸反应时,终点的pH≠7,而是pH>7
2 强酸滴定一元强碱、一元弱碱
盐酸滴定等浓度等体积的氢氧化钠溶液、氨水的滴定曲线
①曲线起点不同:强酸滴定强碱、弱碱的曲线,强碱起点高
②突跃点变化范围不同:强酸与强碱反应的突跃点变化范围大于强酸与弱碱反应
③室温下pH=7时不一定是终点:强酸与强碱反应时,终点的pH=7;强酸与弱碱反应时,终点的pH≠7,而是pH<7
3★ 滴定曲线上特殊点的分析
常温下,用0.100 0 mol/L NaOH溶液滴定20.00 mL 0.100 0 mol/L CH3COOH溶液,所得滴定曲线如图所示。
(1) pH-V图像中各特殊点对水电离程度的影响(表中HAc为CH3COOH)。
点 溶质 水的电离情况
A __________ ________
B ____________________ ________
C ____________________ ____________
D ____________ ________
E ____________________ ________
F ____________________ ________
HAc
抑制
HAc、NaAc(1∶1)
抑制
HAc、NaAc
正常电离
NaAc
促进
NaAc、NaOH
抑制
NaAc、NaOH(1∶1)
抑制
根据图中pH数据,图中A、B、C、D、E、F各点对应的溶液中水的电离程度大小顺序如图所示。
(2) pH-V图像中各特殊点离子浓度大小比较及变化趋势。
点 溶质 离子浓度大小比较
A HAc c(H+)>c(Ac-)>c(OH-)
B(1∶1) HAc、NaAc c(Ac-)>c(Na+)>c(H+)>c(OH-)
C(pH=7) HAc、NaAc c(Ac-)=c(Na+)>c(H+)=c(OH-)
D NaAc c(Na+)>c(Ac-)>c(OH-)>c(H+)
E(2∶1) NaAc、NaOH c(Na+)>c(Ac-)>c(OH-)>c(H+)
F(1∶1) NaAc、NaOH c(Na+)>c(OH-)>c(Ac-)>c(H+)
核心4 弱电解质分布分数图
分布分数图是指以pH为横坐标、分布分数(即组分的平衡浓度占总浓度的分数)为纵坐标的关系图。
★分布分数图及分析
一元弱酸(以CH3COOH为例) 二元酸(以草酸H2C2O4为例)
注:pKa为电离常数的负对数
书写一定pH条件下的离子方程式时,要判断溶液中存在的主要微粒。
如H2C2O4,向溶液中滴加NaOH使溶液pH由3到6时的离子方程式为______________________________________;
pH=1.2时,溶液中加入KMnO4发生反应的离子方程式为____________________________________________________________
检 测 反 馈
2
1
3
1 [2024南京二模] 以磷石膏(含CaSO4和少量SiO2等)为原料制备轻质CaCO3的部分流程如图所示。室温下,Ka1(H2CO3)=4.5×10-7,Ka2(H2CO3)=4.7×10-11,Kb(NH3·H2O)=1.8×10-5。
C
2
1
3
2
1
3
2
1
3
2
1
3
向10.00 mL 0.01 mol/L N2H4的水溶液中逐滴滴加0.005 mol/L稀硫酸,下列说法正确的是( )
B
2
1
3
2
3
1
3 [2024盐城考前模拟](1) 氯化亚铜(CuCl)是一种白色固体,难溶于乙醇,微溶于水,易水解,在空气中易被氧化。实验室利用NaCl粉末、CuSO4溶液、Na2SO3溶液反应制取CuCl晶体。反应完成时溶液pH对CuCl产率的影响如图所示。当pH大于3.5时,随溶液pH升高,CuCl产率降低的原因是____________________________________________。
pH升高,CuCl水解程度增大,产率降低
2
3
1
(2) 向MnSO4溶液中滴加NH4HCO3溶液至沉淀完全,过滤、洗涤、干燥,得MnCO3固体。不使用Na2CO3溶液作沉淀剂的原因是______________________________________________________________________________________________________________。
等浓度的Na2CO3溶液的碱性比NH4HCO3溶液的强,用Na2CO3溶液作沉淀剂,会生成较多的Mn(OH)2,影响产品的纯度
谢谢观看
Thank you for watching
主题3
反应原理与规律
微主题6 电离平衡与盐类水解
内容索引
核心串讲
体系建构
名卷优选
基础回归
检测反馈
基 础 回 归
1 室温下,下列说法不能说明CH3COOH的酸性弱于盐酸的是( )
A.相同浓度的CH3COOH和盐酸,前者pH大
B.相同pH的CH3COOH和盐酸,导电能力后者强
C.相同浓度的CH3COONa溶液和NaCl溶液,前者pH大
D.pH=2的CH3COOH和盐酸,加水稀释100倍,前者变化小于后者
B
B
3 铁矿石用稀硫酸溶解时,稀硫酸要过量的原因是______________ _____________________________。
4 工业中常用Na2CO3溶液浸泡金属,从而去除金属表面的油污。
(1) Na2CO3溶液除油污是由于其溶液呈碱性,呈碱性的原因是__________________________________(用方程式表示)。
提高矿石中铁
元素浸取率;抑制Fe3+水解
<
Na2CO3溶
液的碱性强,易产生Fe(OH)2和Fe(OH)3沉淀
向FeSO4溶液中缓慢加入NaHCO3溶液
体 系 建 构
名 卷 优 选
考向1 溶液中粒子浓度大小分析
题型1 固定成分溶液中粒子浓度大小分析
1 判断下列说法是否正确。
√
×
×
√
×
题型2 反应过程中粒子浓度大小分析
[工业流程中粒子浓度大小关系]
2 判断下列粒子浓度关系是否正确。
(1) [2023江苏卷]室温下,用含少量Mg2+的MnSO4溶液制备MnCO3的过程如图所示。已知:Ksp(MgF2)=5.2×10-11,Ka(HF)=6.3×10-4。
×
×
√
[实验过程中粒子浓度分析]
3 [2024江苏卷]室温下,通过下列实验探究SO2的性质。已知Ka1(H2SO3)=1.3×10-2,Ka2(H2SO3)=6.2×10-8。
实验1:将SO2气体通入水中,测得溶液pH=3。
实验2:将SO2气体通入0.1 mol/L NaOH溶液中,当溶液pH=4时停止通气。
实验3:将SO2气体通入0.1 mol/L酸性KMnO4溶液中,当溶液恰好褪色时停止通气。
D
考向2 酸碱滴定过程和分布曲线中粒子浓度分析
D
B
考向3 盐类水解的综合应用
6 判断下列说法是否正确。
(1) [2023江苏卷]向2 mL FeSO4溶液中滴加2~3滴酚酞试液,观察溶液颜色变化判断Fe2+是否水解( )
×
×
√
不引入杂质
离子Na+(或制得的催化剂不含Na+)
考向1 溶液中粒子浓度大小分析
题型1 固定成分溶液中粒子浓度大小分析
1 判断下列说法是否正确。
×
×
×
×
题型2 反应过程中粒子浓度大小分析
[工业流程中粒子浓度大小关系]
2 判断下列情境下粒子浓度关系式是否正确。
(1) [2024无锡期末]室温下,用含有少量Mg2+的Li2SO4溶液(模拟盐湖水)制备Li2CO3的过程如图所示。
×
(2) [2024南通、泰州等六市一调] 室温下,用含有少量Mn2+的ZnSO4溶液制备ZnCO3的过程如下:
√
[实验过程中粒子浓度分析]
3 [2023泰州期末]室温下,某兴趣小组通过下列实验制备少量NaHCO3并探究其性质。
实验1:测得100 mL 14 mol/L氨水的pH约为12;
实验2:向上述氨水中加NaCl粉末至饱和,通入足量CO2后析出晶体;
实验3:将所得混合物静置后过滤、洗涤、干燥,得到NaHCO3;
实验4:配制100 mL一定浓度的NaHCO3溶液,测得pH为8.0。
D
4 [2023扬州一模]合成环氧氯丙烷时产生了盐酸和醋酸(HAc)的混合液,为研究混合溶液的定量分析方法,进行以下实验。
实验1:向20 mL 0.1 mol/L HCl溶液中滴加0.1 mol/L NaOH溶液;
实验2:向20 mL 0.1 mol/L HAc溶液中滴加0.1 mol/L NaOH溶液;
实验3:向20 mL某浓度HCl与HAc混合溶液中滴加0.1 mol/L NaOH溶液。
测得实验1、2中溶液pH的变化如图所示。
下列说法正确的是( )
C
考向2 酸碱滴定过程和分布曲线中粒子浓度分析
下列说法正确的是( )
B
守恒,溶液中存在:c(H2A)+c(HA-)+c(A2-)=0.1 mol/L,当加入酸或碱,增大了溶液体积,所以c(H2A)+c(HA-)+c(A2-)<0.1 mol/L,C错误;NH4HA溶液显酸性,主要发生HA-的电离,所以向NH4HA溶液中滴加少量NaOH溶液,优先反应的离子方程式为HA-+OH-===A2-+H2O,D错误。
D
考向3 盐类水解的综合应用
7 判断下列说法是否正确。
√
×
(3) [2024盐城、南京期末]用干燥、洁净的玻璃棒蘸取0.1 mol/L NaHCO3溶液,点在干燥的pH试纸上,测出溶液的pH,由此判 HCO是否发生水解( )
(4) [2024南通、泰州等六市一调]Na2SO3溶液呈碱性的原因实验设计:向Na2SO3溶液中先滴加酚酞,再滴加BaCl2溶液至过量,观察溶液颜色变化( )
√
√
8 [2024苏州期末]已知:TiO2++2H2O===TiO(OH)2↓+2H+。其他条件不变,初始溶液pH对含Fe3+的TiO2+溶液水解率的影响如图所示,pH在1.7~1.8内,随着pH增大,TiO2+水解率下降的原因是_______ _________________________________________。
Fe3+水
解产生的H+抑制了TiO2+的水解
【解析】 初始pH在1.7~1.8内,由图可知,随着pH的增大,Fe3+水解程度增大,产生的H+对TiO2+的水解有抑制作用,从而导致TiO2+的水解率下降。
9 [2024无锡期末]以FeSO4·7H2O为原料制备FeCO3的实验流程如图所示。沉淀剂使用尿素[CO(NH2)2],不使用Na2CO3的原因是_________________________________________________________________________________________。
Na2CO3溶液为碱性,易生成Fe(OH)2,碱性条件下,Fe(OH)2易被氧化产生Fe(OH)3沉淀等杂质
酸
酸
核 心 串 讲
核心1 电离平衡常数(K电离)、水的离子积常数(Kw)与盐类水解常数(Kh)
1 电离平衡常数
(1) 常见的弱电解质有弱酸、弱碱和水,弱电解质在溶液中存在电离平衡。弱电解质的电离是吸热过程,升高温度,可促进其电离;常用弱电解质Ka比较酸性强弱、粒子或粒子浓度比的变化及粒子浓度的大小比较。
①Ka越小,酸性________。
②醋酸Ka=1.75×10-5,pH=5时c(CH3COO-)______(填“>”“<”或“=”)c(CH3COOH)。
越弱
>
(2) 多元弱酸(或弱碱)的电离是分步进行的,一般K1 K2 K3。因此计算多元弱酸溶液的c(H+)或比较多元弱酸酸性相对强弱时,通常只考虑第一步电离。
①可以通过比较弱酸一级电离平衡常数的大小来比较它们电离程度的大小,也可比较酸性强弱。如酸性:H2C2O4>H3PO4>CH3COOH>H2CO3。
增大
CO2
2 水的电离[25 ℃时,水的离子积常数Kw=
c(H+)·c(OH-)=10-14]。
图中曲线表示不同温度下,水溶液中c(H+)
与c(OH-)的关系。由于水的电离是吸热过程,
升高温度可促进水电离,水的离子积常数增大,
曲线cd对应的温度高于25 ℃,故T>25。
一定温度下,水溶液中c(H+)与c(OH-)的关系是一个定值,但水的电离程度不一定相同。在酸或碱溶液中,水的电离受到________;电离程度________。
抑制
变小
3 盐类水解常数(Kh)
4 综合应用(没有特殊说明时,使用的数据均在室温下)
(1) 证明弱电解质的方法
以CH3COOH为例:
①测定0.1 mol/L CH3COOH溶液的pH,pH______(填“>”或“<”,下同)1,说明CH3COOH为弱电解质。
大
大
>
②测定CH3COONa溶液的pH,pH______7,说明CH3COOH为弱电解质。
③相同温度、相同浓度的盐酸的导电性______醋酸的导电性,说明CH3COOH是弱电解质。
④取pH=3的CH3COOH溶液1 mL,用水稀释到100 mL,pH______5,说明CH3COOH为弱电解质。
⑤向0.1 mol/L CH3COOH溶液中加入少量CH3COONH4(水溶液呈中性)固体(溶液体积变化忽略不计),pH__________(填“变大”或“变小”),说明CH3COOH为弱电解质。
>
>
<
变大
碱
小于
大于
酸
>
核心2 电解质溶液中“三个守恒和一个比较”
1 电荷守恒
电解质溶液中,无论存在多少种离子,溶液都呈电中性,即电解质溶液中阳离子所带的电荷总数与________________________相等,如Na2S溶液中:c(Na+)+c(H+)=2c(S2-)+c(HS-)+c(OH-)。
2 元素守恒
在电解质溶液中,由于某些离子发生水解或电离,离子的存在形式发生了变化,变成了其他离子或分子,使离子的种类增多,但却不能使离子或分子中某种特定元素原子的数目发生变化,其质量在反应前后是守恒的,始终遵循原子守恒,如Na2S溶液中:c(Na+)=2c(S2-)+ 2c(HS-)+2c(H2S)。
阴离子所带的电荷总数
3 质子守恒
以Na2S溶液为例:
(1) 方法1:可以由电荷守恒与元素守恒推导出来,c(H+)+2c(H2S)+c(HS-)=c(OH-)。
(2) 方法2:可利用下图进行快速书写。
质子守恒: c(H+)+2c(H2S)+c(HS-)=c(OH-)。
核心3 酸碱滴定反应图像
1 强碱滴定一元强酸、一元弱酸
氢氧化钠滴定等浓度等体积的盐酸、醋酸的滴定曲线
①曲线起点不同:强碱滴定强酸、弱酸的曲线中,强酸起点低
②突跃点变化范围不同:强碱与强酸反应的突跃点变化范围大于强碱与弱酸反应
③室温下pH=7不一定是终点:强碱与强酸反应时,终点的pH=7;强碱与弱酸反应时,终点的pH≠7,而是pH>7
2 强酸滴定一元强碱、一元弱碱
盐酸滴定等浓度等体积的氢氧化钠溶液、氨水的滴定曲线
①曲线起点不同:强酸滴定强碱、弱碱的曲线,强碱起点高
②突跃点变化范围不同:强酸与强碱反应的突跃点变化范围大于强酸与弱碱反应
③室温下pH=7时不一定是终点:强酸与强碱反应时,终点的pH=7;强酸与弱碱反应时,终点的pH≠7,而是pH<7
3★ 滴定曲线上特殊点的分析
常温下,用0.100 0 mol/L NaOH溶液滴定20.00 mL 0.100 0 mol/L CH3COOH溶液,所得滴定曲线如图所示。
(1) pH-V图像中各特殊点对水电离程度的影响(表中HAc为CH3COOH)。
点 溶质 水的电离情况
A __________ ________
B ____________________ ________
C ____________________ ____________
D ____________ ________
E ____________________ ________
F ____________________ ________
HAc
抑制
HAc、NaAc(1∶1)
抑制
HAc、NaAc
正常电离
NaAc
促进
NaAc、NaOH
抑制
NaAc、NaOH(1∶1)
抑制
根据图中pH数据,图中A、B、C、D、E、F各点对应的溶液中水的电离程度大小顺序如图所示。
(2) pH-V图像中各特殊点离子浓度大小比较及变化趋势。
点 溶质 离子浓度大小比较
A HAc c(H+)>c(Ac-)>c(OH-)
B(1∶1) HAc、NaAc c(Ac-)>c(Na+)>c(H+)>c(OH-)
C(pH=7) HAc、NaAc c(Ac-)=c(Na+)>c(H+)=c(OH-)
D NaAc c(Na+)>c(Ac-)>c(OH-)>c(H+)
E(2∶1) NaAc、NaOH c(Na+)>c(Ac-)>c(OH-)>c(H+)
F(1∶1) NaAc、NaOH c(Na+)>c(OH-)>c(Ac-)>c(H+)
核心4 弱电解质分布分数图
分布分数图是指以pH为横坐标、分布分数(即组分的平衡浓度占总浓度的分数)为纵坐标的关系图。
★分布分数图及分析
一元弱酸(以CH3COOH为例) 二元酸(以草酸H2C2O4为例)
注:pKa为电离常数的负对数
书写一定pH条件下的离子方程式时,要判断溶液中存在的主要微粒。
如H2C2O4,向溶液中滴加NaOH使溶液pH由3到6时的离子方程式为______________________________________;
pH=1.2时,溶液中加入KMnO4发生反应的离子方程式为____________________________________________________________
检 测 反 馈
2
1
3
1 [2024南京二模] 以磷石膏(含CaSO4和少量SiO2等)为原料制备轻质CaCO3的部分流程如图所示。室温下,Ka1(H2CO3)=4.5×10-7,Ka2(H2CO3)=4.7×10-11,Kb(NH3·H2O)=1.8×10-5。
C
2
1
3
2
1
3
2
1
3
2
1
3
向10.00 mL 0.01 mol/L N2H4的水溶液中逐滴滴加0.005 mol/L稀硫酸,下列说法正确的是( )
B
2
1
3
2
3
1
3 [2024盐城考前模拟](1) 氯化亚铜(CuCl)是一种白色固体,难溶于乙醇,微溶于水,易水解,在空气中易被氧化。实验室利用NaCl粉末、CuSO4溶液、Na2SO3溶液反应制取CuCl晶体。反应完成时溶液pH对CuCl产率的影响如图所示。当pH大于3.5时,随溶液pH升高,CuCl产率降低的原因是____________________________________________。
pH升高,CuCl水解程度增大,产率降低
2
3
1
(2) 向MnSO4溶液中滴加NH4HCO3溶液至沉淀完全,过滤、洗涤、干燥,得MnCO3固体。不使用Na2CO3溶液作沉淀剂的原因是______________________________________________________________________________________________________________。
等浓度的Na2CO3溶液的碱性比NH4HCO3溶液的强,用Na2CO3溶液作沉淀剂,会生成较多的Mn(OH)2,影响产品的纯度
谢谢观看
Thank you for watching
同课章节目录
